ELEKTROLIT DAN NON ELEKTROLIT A Pengertian Larutan Elektrolit














- Slides: 21

ELEKTROLIT DAN NON ELEKTROLIT

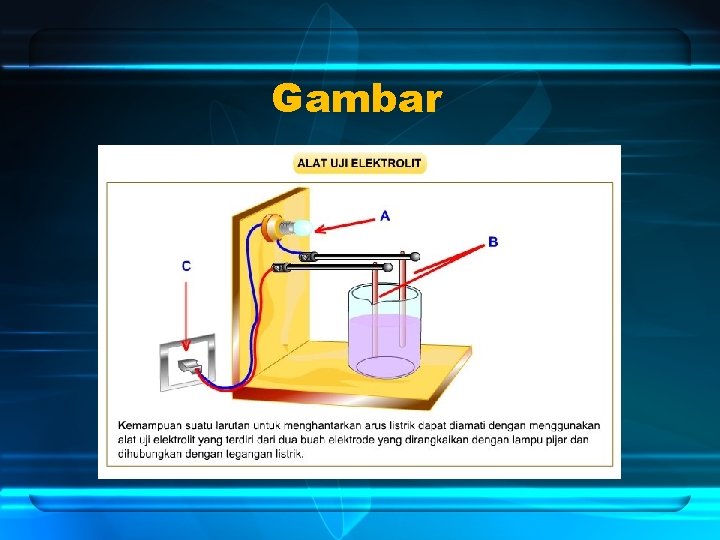
A. Pengertian Larutan Elektrolit dan Non elektrolit a. Larutan Elektrolit : larutan yang dapat menghantarkan arus listrik b. Larutan non elektrolit: larutan yang tidak dapat menghantarkan arus listrik

B. Teori Ion Svante Arrhenius Menurut Arrhenius, larutan elektrolit dapat menghantarkan arus listrik karena mengandung ion-ion yang dapat bergerak bebas

Gambar

Larutan Elektrolit asam basa garam

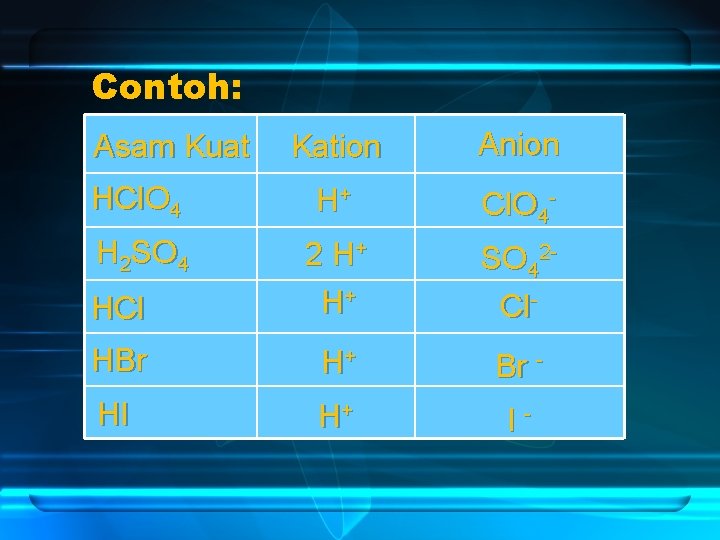
1. Larutan Asam ( H+) a. Asam Kuat Larutan asam kuat akan terionisasi Sempurna menjadi ion H+ dan sisa asam X-

Contoh: Kation Anion HCl. O 4 H+ Cl. O 4 - H 2 SO 4 HCl 2 H+ H+ SO 42 Cl- HBr H+ Br - HI H+ I- Asam Kuat

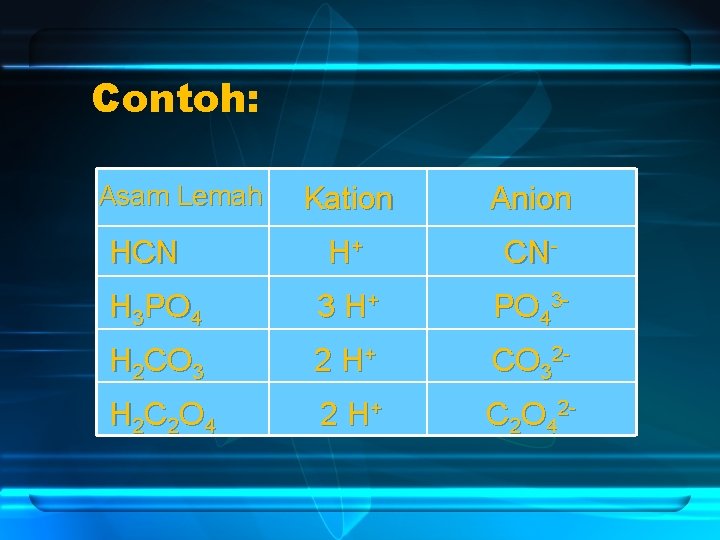
b. Asam lemah tidak terionisasi sempurna seperti asam kuat sehingga uji elektrolit hanya terlihat gelembung-gelembung gas pada elektroda.

Contoh: Asam Lemah Kation Anion H+ CN- H 3 PO 4 3 H+ PO 43 - H 2 CO 3 2 H+ CO 32 - H 2 C 2 O 4 2 H+ C 2 O 42 - HCN

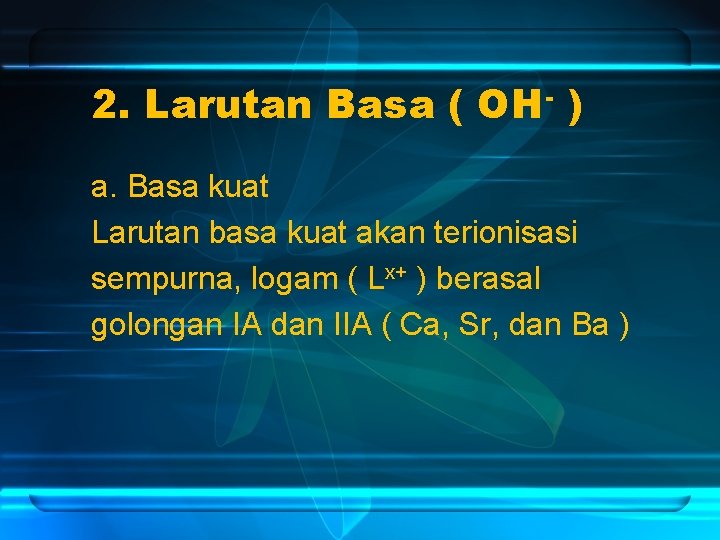
2. Larutan Basa ( OH- ) a. Basa kuat Larutan basa kuat akan terionisasi sempurna, logam ( Lx+ ) berasal golongan IA dan IIA ( Ca, Sr, dan Ba )

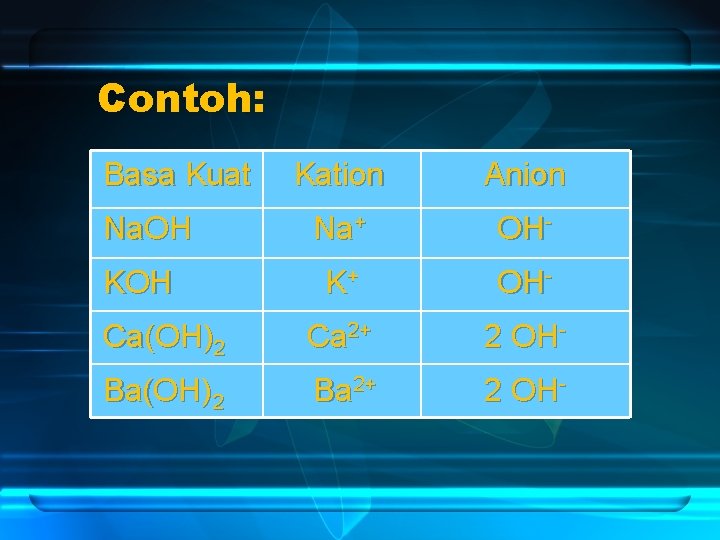
Contoh: Basa Kuat Kation Anion Na+ OH- K+ OH- Ca(OH)2 Ca 2+ 2 OH- Ba(OH)2 Ba 2+ 2 OH- Na. OH KOH

b. Basa lemah Larutan basa lemah tidak terionisasi sempurna sama dengan asam lemah Contoh: Kation Anion Fe(OH)3 Fe 3+ 3 OH- Al(OH)3 Al 3+ 3 OH- Zn(OH)2 Zn 2+ 2 OH- Basa Lemah

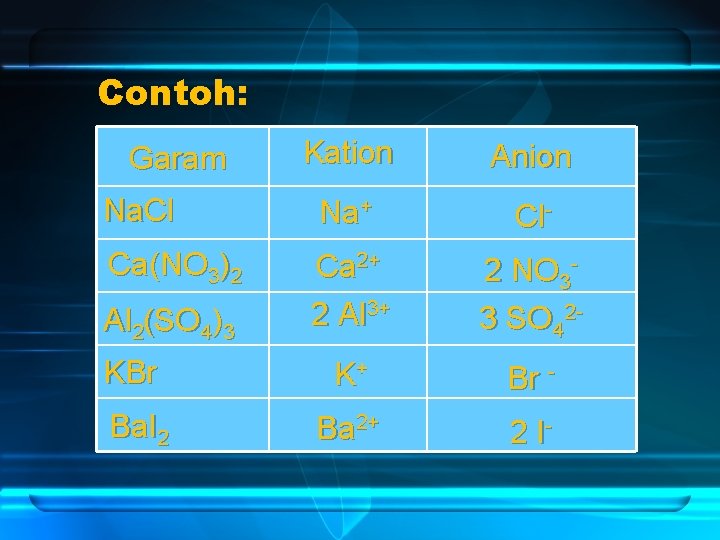
3. Larutan Garam Larutan garam umumnya larutan elektrolit kuat jadi akan terionisasi sempurna seperti asam kuat dan basa kuat. Contoh: Na. Cl, Ca(NO 3)2, Al 2(SO 4)3

Contoh: Kation Anion Na. Cl Na+ Cl- Ca(NO 3)2 Ca 2+ 2 Al 3+ 2 NO 33 SO 42 - KBr K+ Br - Ba. I 2 Ba 2+ 2 I- Garam Al 2(SO 4)3

Reaksi asam, basa, garam a. asam + basa b. Logam + asam c. Logam + garam d. Garam-1 + garam-2

Asam + Basa Garam + Air Contoh: HCl (aq) + Na. OH (aq) Na. Cl (aq) + H 2 O (l) Persamaan ion: H+(aq)+ Cl-(aq) + Na+(aq)+ OH-(aq) Na+ (aq) + Cl- (aq) + H 2 O (l) Persamaan ion Bersih: H+ (aq) + OH- (aq) H 2 O (l)

Logam + Asam Garam + H 2(g) 2 Al(s) + 3 H 2 SO 4(aq) Al 2(SO 4)3(aq) + 3 H 2(g) Persamaan ion 2 Al(s) + 6 H+(aq) + 3 SO 42 -(aq) 2 Al 3+(aq) + 3 SO 42 -(aq) + 3 H 2(g) Persamaan ion bersih 2 Al(s) + 6 H+(aq) 2 Al 3+(aq) +3 H 2(g)

Logam+Garam 3 Na(s) +Fe. Cl 3(aq) 3 Na. Cl(aq)+ Fe(s) Persamaan ion: 3 Na(s) +Fe 3+(aq) + 3 Cl- (aq) 3 Na+(aq) + 3 Cl-(aq) + Fe(s) Persamaan ion bersih: 3 Na(s) +Fe 3+ (aq) 3 Na+ (aq)+ Fe(s)

Garam 1+Garam 2 Garam 3+Garam 4 Pb(NO 3)2 (aq) + 2 KI (aq) Pb. I 2 (s) + 2 KNO 3(aq) Persamaan ion bersih: Pb (aq) + 2 I- (aq) Pb. I 2 (s)

