LARUTAN ELEKTROLIT DAN NON ELEKTROLIT PERTANYAAN Mengapa orang
















- Slides: 23

LARUTAN ELEKTROLIT DAN NON ELEKTROLIT

PERTANYAAN ? Mengapa orang mencari ikan disungai dengan strum/accu? Mengapa pada saat hujan tidak boleh berada dibawah pohon? Mengapa larutan garam dapat menghantarkan listrik sedangkan larutan gula tidak?

Misalnya ada larutan gula, larutan garam, larutan teh. Tapi bagaimana dengan air kopi? Apakah kita menganggapnya sebagai sebuah larutan? ? ?

Suatu campuran terdiri dari dua komponen utama, yaitu zat terlarut dan zat pelarut. Jika dari contoh di atas zat terlarutnya adalah, gula, garam, teh, dan kopi, sedangkan zat pelarutnya adalah air. Suatu zat dikatakan larutan jika campuran antara zat terlarut dan pelarutnya bersifat homogen. Artinya tidak terdapat batas antar komponennya, sehingga tidak dapat dibedakan lagi antara zat pelarut (air) dan terlarutnya (gula, kopi, maupun teh).

Suatu larutan dapat dikatakan sebagai larutan elektrolit jika zat tersebut mampu menghantarkan listrik. Mengapa zat elektrolit dapat menghantarkan listrik?

Suatu zat dapat menghantarkan listrik karena zat tersebut memiliki ion-ion yang bergerak bebas di dalam larutan tersebut. ion-ion inilah yang nantinya akan menjadi penghantar. Semakin banyak ion yang dihasilkan semakin baik pula larutan tersebut menghantarkan listrik.

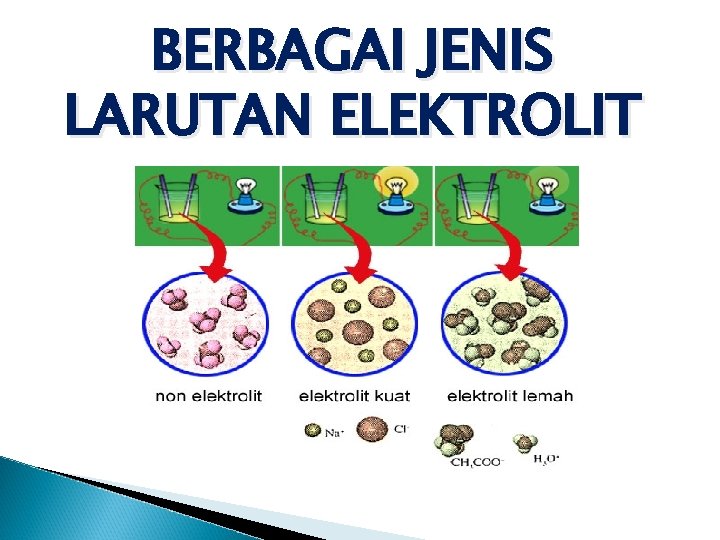
BERBAGAI JENIS LARUTAN ELEKTROLIT

Terdapat berbagai jenis larutan yang bisa menghantarkan listrik. Pembagian zat tersebut adalah sebagai berikut:

Berdasarkan jenis larutan Larutan asam (zat yang melepas ion H+ jika dilarutkan dalam air), contohnya adalah: Asam Asam klorida florida sulfat asetat/cuka sianida nitrat fospat : HCl : : : HF H 2 SO 4 CH 3 COOH HCN HNO 3 : H 3 PO 4

Larutan basa (zat yang melepas ion OH- jika dilarutkan dalam air), contohnya adalah: Natrium hidroksida Calcium hidroksida Litium hidroksida Kalium hidroksida Barium hidroksida Magnesium hidroksida Aluminium hidroksida Besi (II) hidroksida Besi (III) hidroksida Amonium hirdoksida : : : : Na. OH Ca(OH)2 Li. OH KOH Ba(OH)2 Mg(OH)2 Al(OH)3 : Fe(OH)2 : Fe(OH)3 : NH 4 OH

Larutan garam (zat yang terbentuk dari reaksi antara asam dan basa), contohnya adalah: Natrium klorida/garam dapur : Na. Cl Ammonium clorida : NH 4 Cl Ammonium sulfat : (NH 4)2 SO 4 Calcium diklorida : Ca. Cl 2

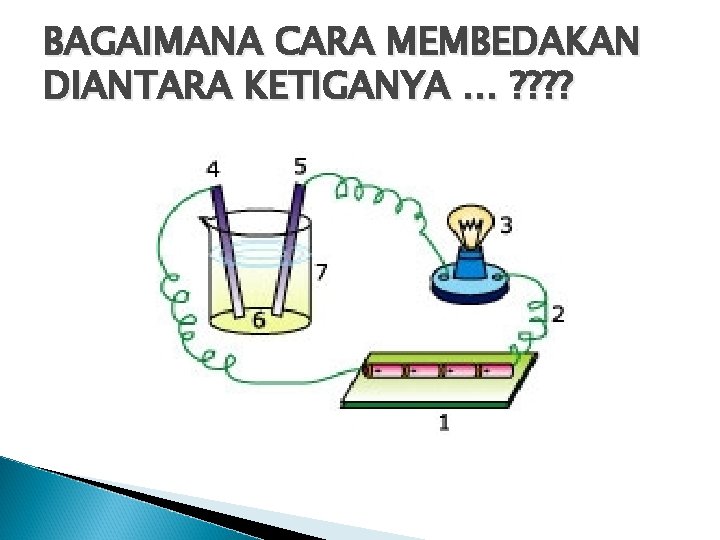
BAGAIMANA CARA MEMBEDAKAN DIANTARA KETIGANYA … ? ?

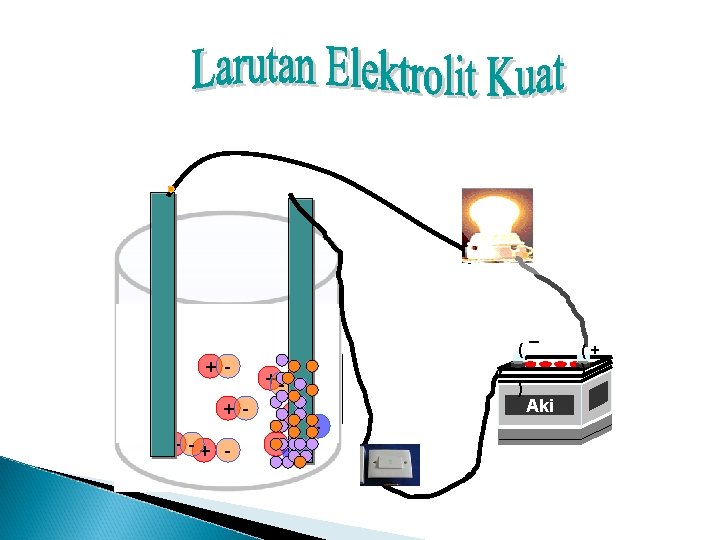
ELEKTROLIT KUAT. . . Elektrolit kuat, karakteristiknya adalah sebagai berikut: Menghasilkan banyak ion Molekul netral dalam larutan hanya sedikit/tidak ada sama sekali Terionisasi sempurna, atau sebagian besar terionisasi sempurna Jika dilakukan uji daya hantar listrik: gelembung gas yang dihasilkan banyak, lampu menyala Penghantar listrik yang baik Derajat ionisasi = 1, atau mendekati 1


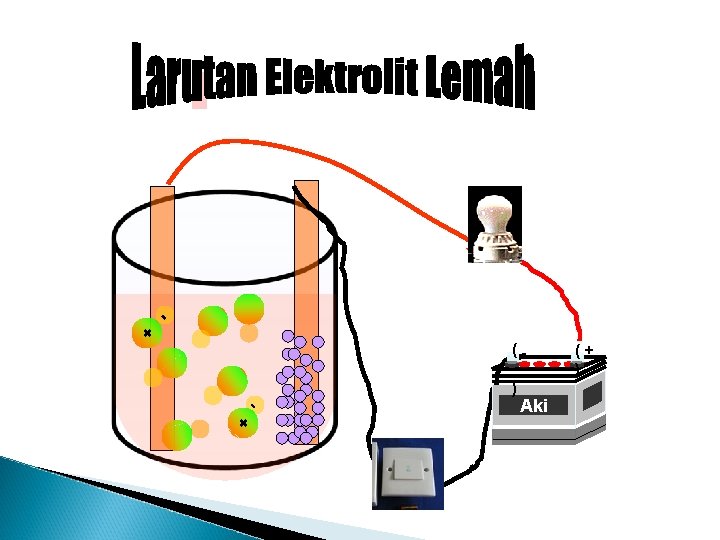
ELEKTROLIT LEMAH. . . Elektrolit lemah, karakteristiknya adalah sebagai berikut: Menghasilkan sedikit ion Molekul netral dalam larutan banyak Terionisasi hanya sebagian kecil Jika dilakukan uji daya hantar listrik: gelembung gas yang dihasilkan sedikit, lampu tidak menyala Penghantar listrik yang buruk Derajat ionisasi mendekati 0


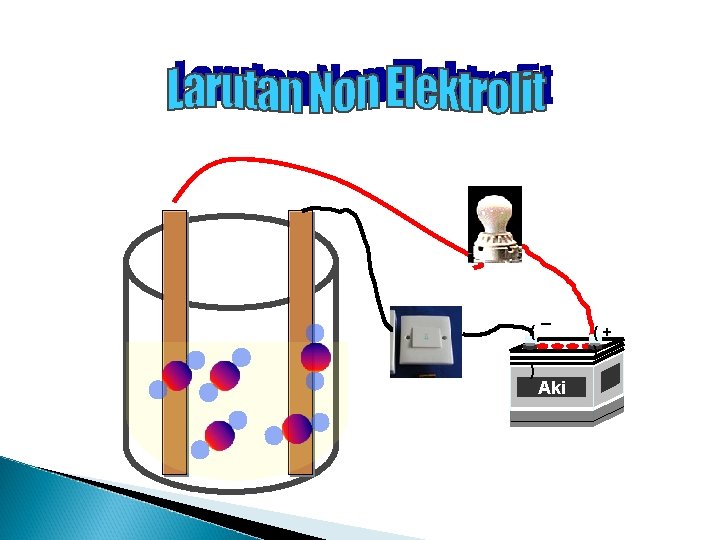
Non elektrolit. . . larutan non elektrolit memiliki karakteristik sebagai berikut: Tidak menghasilkan ion Semua dalam bentuk molekul netral dalam larutannya Tidak terionisasi Jika dilakukan uji daya hantar listrik: tidak menghasilkan gelembung, dan lampu tidak menyala


Berdasarkan Jenis Ikatan 1. Senyawa ion (senyawa yang terbentuk melalui ikatan ion), contohnya adalah: Na. Cl, Ca. Cl 2, Al. Cl 3, Mg. F 2, Li. F (sebagian besar berasal dari garam) 2. Senyawa kovalen polar (senyawa melalui ikatan kovalen yang bersifat polar/memiliki perbedaan keelektronegatifan yang besar antar atom), contohnya adalah: HCl, Na. OH, H 2 SO 4, H 3 PO 4, HNO 3, Ba(OH)2 (berasal dari asam dan basa)

KEKUATAN LARUTAN ELEKTROLIT

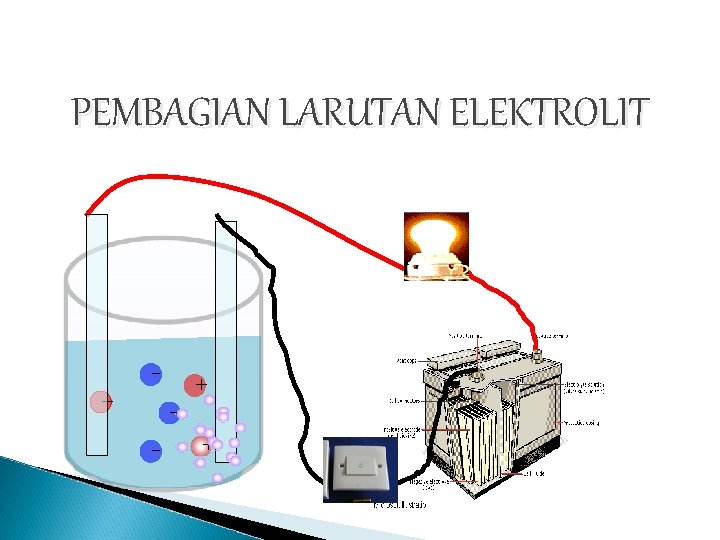
PEMBAGIAN LARUTAN ELEKTROLIT + - + +

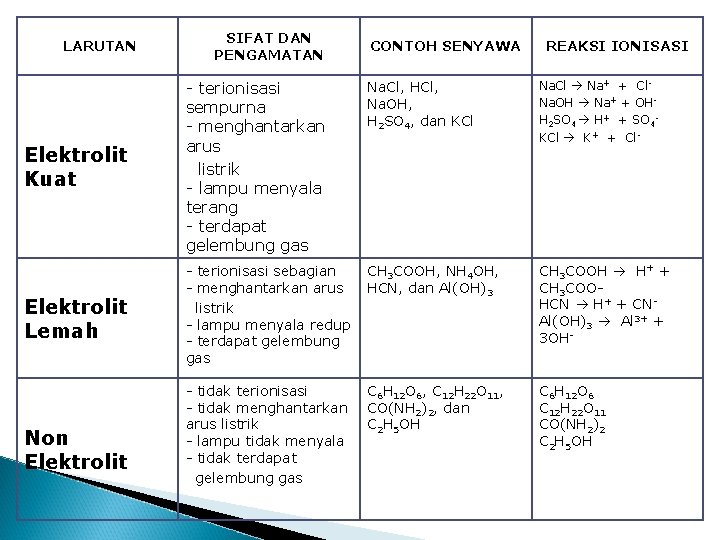
LARUTAN SIFAT DAN PENGAMATAN CONTOH SENYAWA REAKSI IONISASI Na. Cl, HCl, Na. OH, H 2 SO 4, dan KCl Elektrolit Kuat - terionisasi sempurna - menghantarkan arus listrik - lampu menyala terang - terdapat gelembung gas Na. Cl Na+ + Cl. Na. OH Na+ + OHH 2 SO 4 H+ + SO 4 KCl K+ + Cl- Elektrolit Lemah - terionisasi sebagian - menghantarkan arus listrik - lampu menyala redup - terdapat gelembung gas CH 3 COOH, NH 4 OH, HCN, dan Al(OH)3 CH 3 COOH H+ + CH 3 COOHCN H+ + CNAl(OH)3 Al 3+ + 3 OH- - tidak terionisasi - tidak menghantarkan arus listrik - lampu tidak menyala - tidak terdapat gelembung gas C 6 H 12 O 6, C 12 H 22 O 11, CO(NH 2)2, dan C 2 H 5 OH C 6 H 12 O 6 C 12 H 22 O 11 CO(NH 2)2 C 2 H 5 OH Non Elektrolit

TERIMA KASIH