exit ELECTROLYTE AND NONELECTROLYTE SOLUTIONS LARUTAN ELEKTROLIT LARUTAN





















- Slides: 24

exit ELECTROLYTE AND NONELECTROLYTE SOLUTIONS

LARUTAN ELEKTROLIT LARUTAN adalah campuran homogen dua zat atau lebih yang saling melarutkan dan masing-masing zat penyusunnya tidak dapat dibedakan lagi secara fisik. Larutan terdiri atas zat terlarut dan pelarut. Berdasarkan daya hantar listriknya (daya ionisasinya), larutan dibedakan dalam dua macam, yaitu : larutan elektrolit dan larutan non elektrolit. exit Larutan elektrolit adalah larutan yang dapat menghantarkan arus listrik.

1. ELEKTROLIT KUAT Larutan elektrolit kuat adalah larutan yang mempunyai daya hantar listrik yang kuat, karena zat terlarutnya didalam pelarut (umumnya air), seluruhnya berubah menjadi ion-ion (alpha = 1). Yang tergolong elektrolit kuat adalah: a. Asam-asam kuat, seperti : HCl, HCl 03, H 2 SO 4, HNO 3 dan lain-lain. b. Basa-basa kuat, yaitu basa-basa golongan alkali dan alkali tanah, seperti: Na. OH, KOH, Ca(OH)2, Ba(OH)2 dan lain-lain. c. Garam-garam yang mudah larut, seperti: Na. Cl, KI, exit Al 2(SO 4)3 dan lain-lain

2. ELEKTROLIT LEMAH Larutan elektrolit lemah adalah larutan yang daya hantar listriknya lemah dengan harga derajat ionisasi sebesar: O < alpha < 1. Yang tergolong elektrolit lemah: a. Asam-asam lemah, seperti : CH 3 COOH, HCN, H 2 CO 3, H 2 S dan lain b. Basa-basa lemah seperti : NH 4 OH, Ni(OH)2 dan lain-lain c. Garam-garam yang sukar larut, seperti : Ag. Cl, Ca. Cr. O 4, Pb. I 2 dan lain

Larutan non elektrolit adalah larutan yang tidak dapat menghantarkan arus listrik, karena zat terlarutnya di dalam pelarut tidak dapat menghasilkan ion-ion (tidak mengion). exit Tergolong ke dalam jenis ini misalnya: - Larutan urea - Larutan sukrosa - Larutan glukosa - Larutan alkohol dan lain-lain

exit Gambaran Bentuk Molekul Elektrolit Kuat dan Elektrolit Lemah

Larutan Non Elektrolit exit Larutan non-elektrolit adalah larutan yang tidak dapat menghantarkan arus listrik, hal ini disebabkan karena larutan tidak dapat menghasilkan ion-ion (tidak meng-ion).

exit termasuk dalam larutan non elektrolit antara lain : * Larutan urea * Larutan sukrosa * Larutan glukosa * Larutan alkohol dan lain-lain

exit Perbandingan sifat-sifat larutan elektrolit dan larutan non elektrolit

Menguji Larutan Elektrolit dan Non-elektrolit exit Dalam menguji suatu larutan elektrolit dan non-elektrolit, dalam dilakukan percobaan dengan beberapa larutan.

a. Alat dan bahan yang harus disediakan Alat dan bahan Gelas kimia Alat penguji elektrolit Baterai Air suling Larutan HCl Larutan asam cuka(CH 3 COOH) Larutan Na. OH Larutan ammonia (NH 3) Larutan gula – 50 m. L Larutan Na. Cl Etanol (alcohol) Air ledeng Air sumur Ukuran/satuan Jumlah 100 ml – 9 volt – 1 M 1 M – 1 M 70% – 10 1 set 1 50 m. L 50 m. L – exit Tabel 1. Alat dan bahan

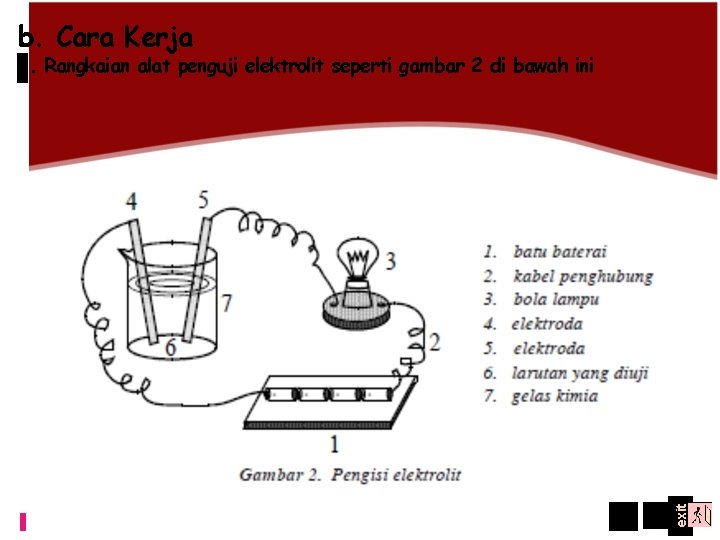
b. Cara Kerja exit 1. Rangkaian alat penguji elektrolit seperti gambar 2 di bawah ini

exit 2. Masukkan kira-kira 50 ml air kran ke dalam gelas kimia dan uji daya hantar listriknya. Catat apakah lampu menyala atau timbul pada elektroda. . Bersihkan elektroda dengan air dan keringkan, kemudian dengan cara yang sama uji daya hantar listrik larutan yang lain

Reaksi Ionisasi larutan elektrolit dapat menghantarkan arus listrik disebabkan penguraian zat menjadi ion-ion penyusunnya (proses ionisasi) dalam pelarut air. exit A. Reaksi Ionisasi Elektrolit Kuat dan Elektrolit Lemah Jenis dan konsentrasi (kepekatan) suatu larutan dapat berpengaruh terhadap daya hantar listriknya. Untuk menunjukkan kekuatan elektrolit digunakan derajat ionisasi. Makin besar harga α , makin kuat elektrolit tersebut.

1. Reaksi Ionisasi Elektrolit Kuat exit Larutan yang dapat memberikan lampu terang, gelembung gasnya banyak, maka larutan ini merupakan elektrolit kuat. Umumnya elektrolit kuat adalah larutan garam. Dalam proses ionisasinya, elektrolit kuat menghasilkan banyak ion maka a= 1 (terurai senyawa), pada persamaan reaksi ionisasi elektrolit kuat ditandai dengan anak panah satu arah ke kanan.

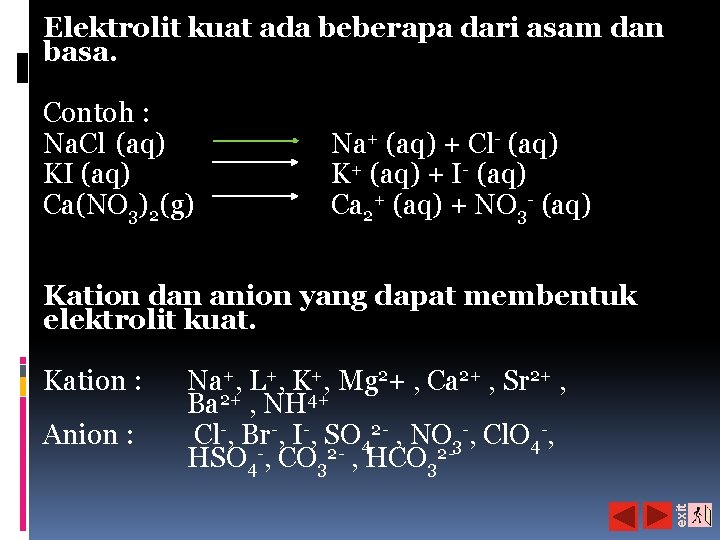
Elektrolit kuat ada beberapa dari asam dan basa. Contoh : Na. Cl (aq) KI (aq) Ca(NO 3)2(g) Na+ (aq) + Cl- (aq) K+ (aq) + I- (aq) Ca 2+ (aq) + NO 3 - (aq) Kation dan anion yang dapat membentuk elektrolit kuat. Anion : Na+, L+, K+, Mg 2+ , Ca 2+ , Sr 2+ , Ba 2+ , NH 4+ Cl-, Br-, I-, SO 42 - , NO 3 -, Cl. O 4 -, HSO 4 -, CO 32 - , HCO 32 exit Kation :

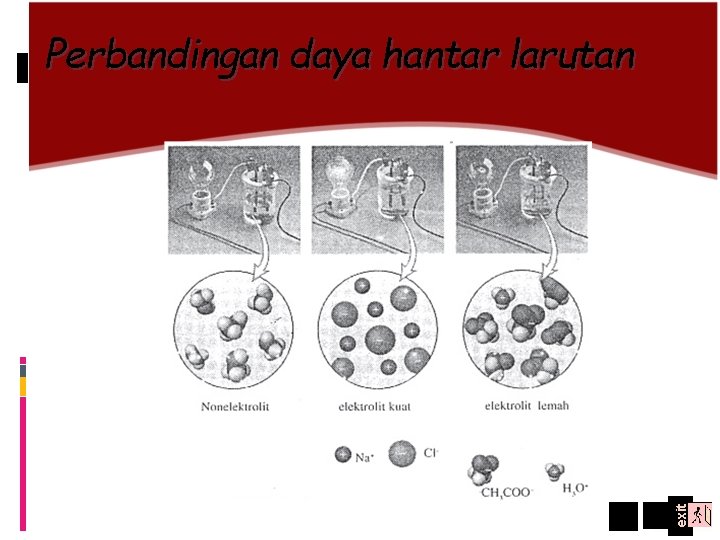
exit Perbandingan daya hantar larutan

Contoh : CH 3 COOH(aq) CH 3 COO- (aq) + H+ (aq) NH 4 OH(g) NH 4+ (aq) + OH- (aq) exit 2. Reaksi Ionisasi Elektrolit Lemah Larutan yang dapat memberikan nyala redup ataupun tidak menyala, tetapi masih terdapat gelembung gas pada elektrodanya maka larutan ini merupakan elekrtolit lemah. Daya hantarnya buruk dan memiliki á (derajat ionisasi) kecil, karena sedikit larutan yang terurai (terionisasi). Makin sedikit yang terionisasi, makin lemah elektrolit tersebut. Dalam persamaan reaksi ionisasi elektrolit lemah ditandai dengan panah dua arah (bolak-balik) artinya tidak semua molekul terurai (ionisasi tidak sempurna)

Derajat Ionisasi Banyak atau sedikitnya molekul zat yang terionisasi dinyatakan dalam derajat ionisasi. Derajat ionisasi ( α) merupakan perbandingan banyaknya molekul zat yang terurai dengan banyaknya molekul zat mula-mula. exit α = 1, elektrolit kuat 0 < α < 1, elektrolit lemah α = 0, non elektrolit

exit Derajat Ionisasi

exit Derajat Ionisasi

exit Derajat Ionisasi

exit Derajat Ionisasi

exit Thank you for your attention