CAT DNAANALYSE VIA FLOWCYTOMETRIE APR INGE THOELEN U



























- Slides: 40

CAT DNA-ANALYSE VIA FLOWCYTOMETRIE APR. INGE THOELEN U. Z. LEUVEN, 3 MEI 2005

WAT? • Analyse DNA-inhoud • DNA-aneuploïdie: – Diploïd: 46 chromosomen – Hyperdiploïd: > 46 chromosomen – Hypodiploïd: < 46 chromosomen • Maligne cellen: numerische en structurele chromosomale aberranties • DNA-analyse: enkel numerische aberranties! • ≠ fasen celcyclus: G 1, S, G 2 → %S-fase fractie (tumor-proliferatie)

HOE? • Staal: beenmerg, bloed, weefselbiopten • Isoleren en kleuren celkernen m. b. v. Cycle. TEST PLUS DNA reagens kit (BD): – – Lyseren RBC (RCLB, zelfbereid) Oplossing A: detergent, trypsine Oplossing B: trypsine inhibitor, RNase Oplossing C: propidium jodide (intercalator) • Vervolgens flowcytometrische analyse (FACSCalibur, BD) • Auto-analyse resulterende DNA-histogram met Mod. Fit LT® software

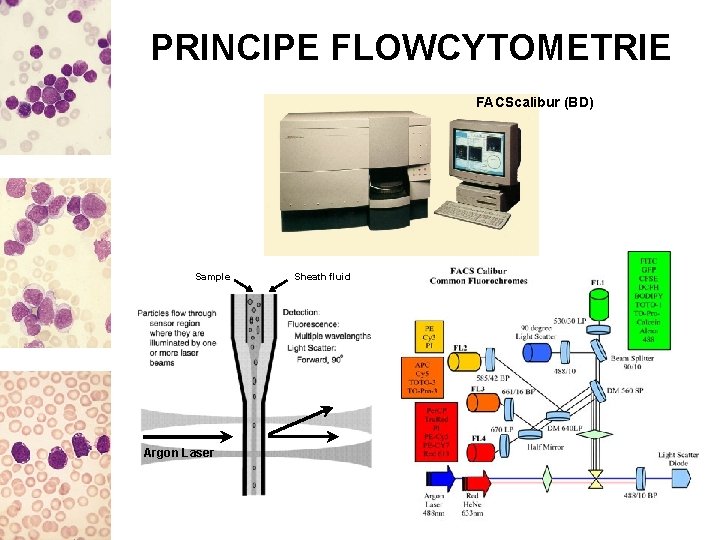
PRINCIPE FLOWCYTOMETRIE FACScalibur (BD) Sample Argon Laser Sheath fluid

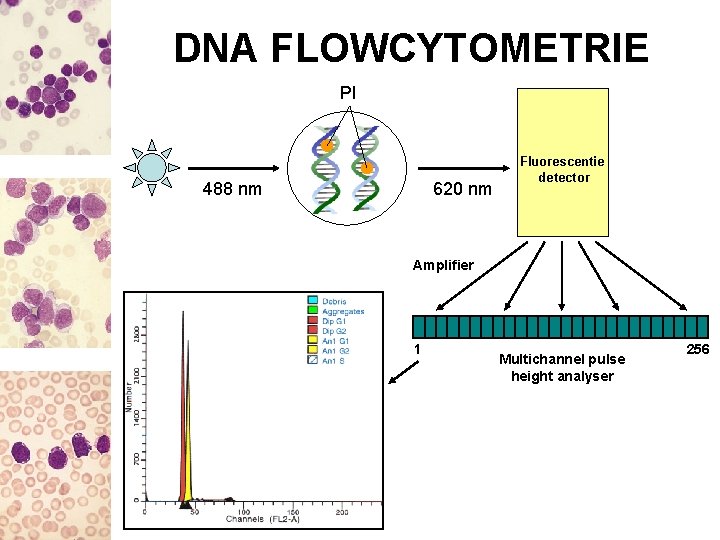
DNA FLOWCYTOMETRIE PI 488 nm 620 nm Fluorescentie detector Amplifier 1 Multichannel pulse height analyser 256

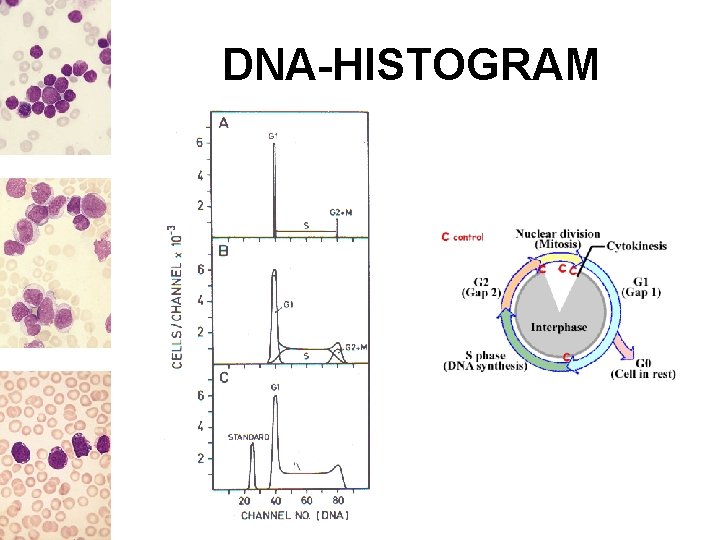
DNA-HISTOGRAM

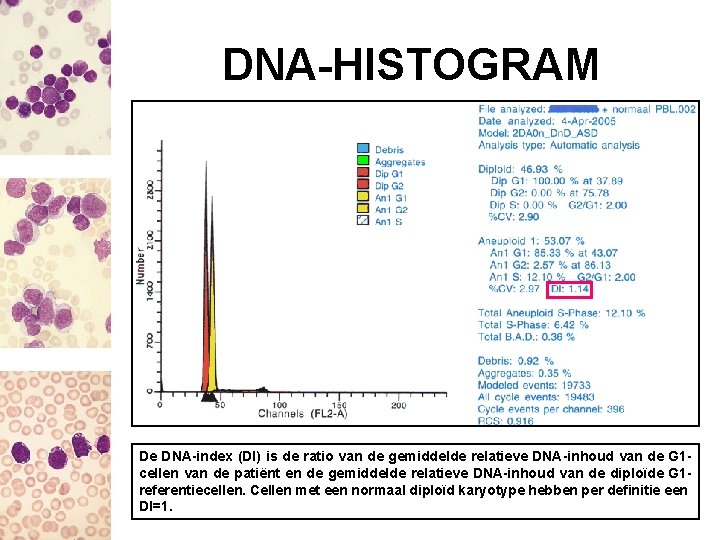
DNA-HISTOGRAM De DNA-index (DI) is de ratio van de gemiddelde relatieve DNA-inhoud van de G 1 cellen van de patiënt en de gemiddelde relatieve DNA-inhoud van de diploïde G 1 referentiecellen. Cellen met een normaal diploïd karyotype hebben per definitie een DI=1.

ANALYTISCHE PERFORMANTIE • • # events > 10. 000 CV diploïde piek ≤ 3% % B. A. D. (debris/aggregaten) < 20% (Reduced Chi-Square (RCS): goodness of fit) – 1, 0 tot 3, 0: goed – 3, 0 tot 5, 0: matig – > 5, 0: slecht Prout’s Neck DNA Cytometry Consensus Conference guidelines, USA 1992 (Shankey et al. , 1993)

WAAROM? • Ploïdie-status blasten is prognostische indicator in acute lymfoblastische leukemie (ALL) • DNA-index opgenomen in risico-classificatie criteria pediatrische ALL (< 18 jaar) • Behandeling verschillend naargelang risicogroep • Kinderen met zeer laag risico op recidief: minder intensieve en minder toxische therapieschema’s; zeer hoog risico-ALL: aangepaste en aggresievere therapie

ACUTE LYMFOBLASTISCHE LEUKEMIE • Systemische, neoplastische proliferatie van lymfoblasten • +/- 70% van de gevallen: patiënten < 17 jaar • ALL meest voorkomende vorm van kanker bij kinderen: +/- kwart van de kankerdiagnoses • Acute leukemie bij kinderen: ALL/AML → 5: 1 • Genezingskans pediatrische patiënten: 80% • Ongekende etiologie – Bestraling – Genetische factoren: Down syndroom

ACUTE LYMFOBLASTISCHE LEUKEMIE • Klinisch: bloed cytopenieën (bleek, vermoeid, bloedingen, koorts, infecties), extramedullaire leukemische infiltraten (CNS, lymfadenopathie, hepatosplenomegalie) • Origine blasten: – Precursor B-lymfocyten: 85% – Precursor T-lymfocyten: 15% • Classificatie morfologisch (FAB): L 1, L 2, L 3 (Burkitt) • Classificatie immunofenotypisch (EORTC): – Pro-B ALL, common B, pre-B, mature B – Pro-T ALL, pre-T, cortical T (common-T), mature T

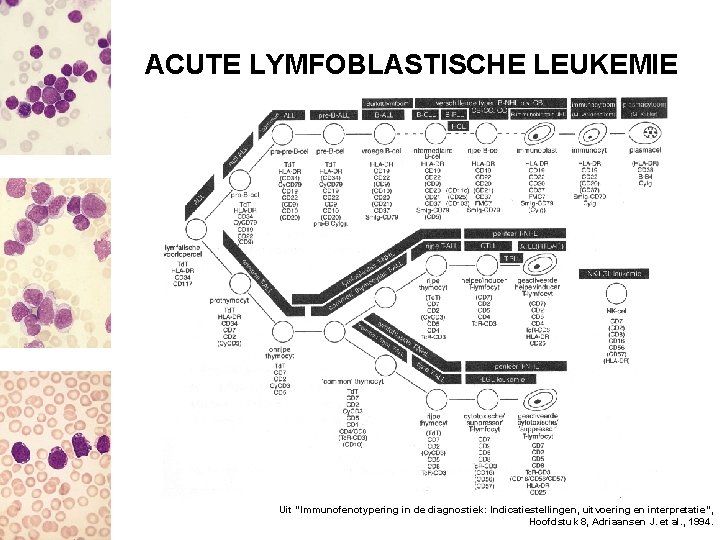
ACUTE LYMFOBLASTISCHE LEUKEMIE Uit “Immunofenotypering in de diagnostiek: Indicatiestellingen, uitvoering en interpretatie”, Hoofdstuk 8, Adriaansen J. et al. , 1994.

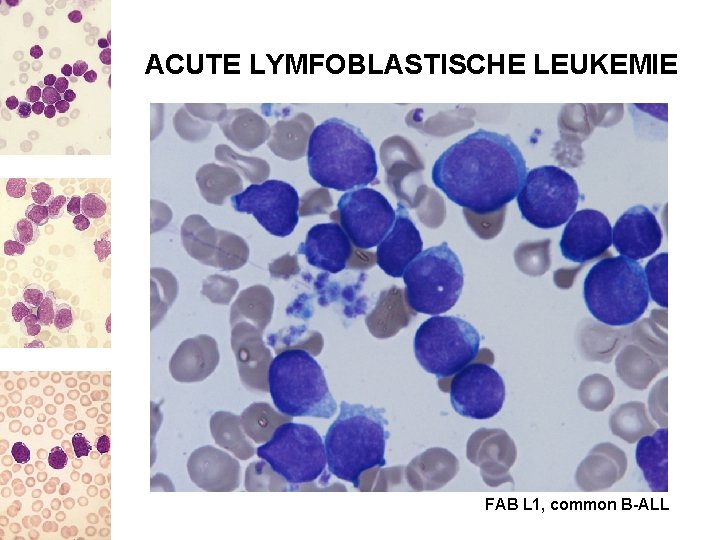
ACUTE LYMFOBLASTISCHE LEUKEMIE FAB L 1, common B-ALL

BEHANDELINGSSTRATEGIE • Grondige evaluatie van risico op recidief: voorkomen van over- of onderbehandeling • Meeste pediatrische hemato-oncologische centra: deelname aan klinische studies waardoor behandeling volgens gestandaardiseerde onderzoeksprotocols • Geen uniform risico-classificatiesysteem • Belangrijke risico-classificatie criteria: – – – Initieel WBC-aantal Leeftijd bij diagnose Cytogenetica en ploïdie Immunofenotype Respons op inductietherapie

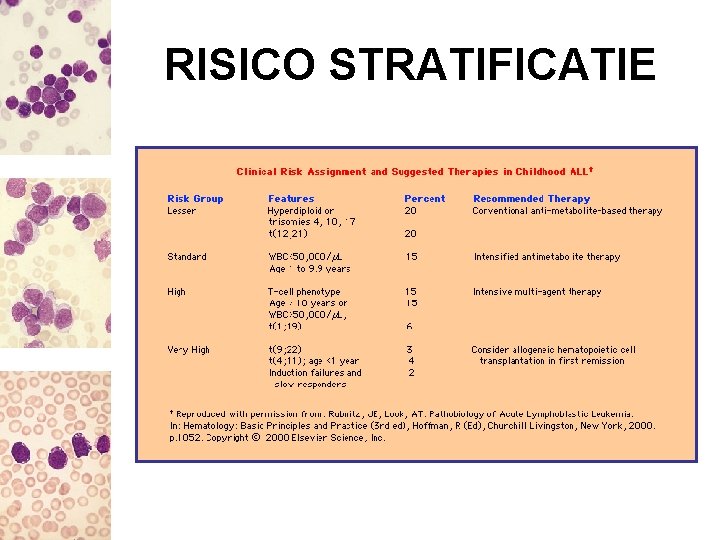
RISICO STRATIFICATIE

EORTC PROTOCOL 58951 “Dexamethasone vs prednisolone during induction and maintenance therapy, prolonged vs conventional duration of L-Asparaginase therapy during consolidation and late intensification, in ALL and NHL of childhood. A Randomised phase III. ” • EORTC: European Organisation for Research and Treatment of Cancer • CLCG (EORTC Children’s Leukemia Cooperative Study Group) trial 58951: België, Frankrijk, Portugal • Vier risicogroepen: – – Very low risk (VLR) Average risk 1 (AR 1) Average risk 2 (AR 2) Very high risk (VHR)

VLR CRITERIA • • ALL of B-cell lineage – WBC less than 10, 000/mm 3 – Must meet 1 of the following conditions: • DNA index greater than 1. 16 and less than 1. 50 and chromosome number 51 -66 or unknown • DNA index not assessed and chromosome number 51 -66 • DNA index greater than 1. 16 and less than 1. 50 and chromosome number is unknown – Good response to prephase therapy – Absence of t(9; 22) or BCR/ABL, t(4; 11)/MLL-AF 4, or 11 q 23/MLL rearrangement – No acute undifferentiated leukemia (AUL) – No CNS or gonadal involvement Precursor B-lymphoblastic NHL stage I or II

AR CRITERIA • • • Must meet 1 of the following criteria: – ALL with good response to prephase therapy who are neither VLR or very high risk (VHR) – VLR ALL with CNS involvement (CSF positive or negative) – Precursor B-lymphoblastic NHL stage III or IV without any VHR feature – Precursor T-lymphoblastic NHL AR patients substratified in: – AR 1: B-cell lineage ALL with WBC less than 100, 000/mm 3 • Surreptitious or hemorrhagic CSF becoming negative at D 4 of prephase therapy • Precursor B-lymphoblastic NHL stage III or IV • Precursor T-lymphoblastic NHL stage I or II – AR 2: B-cell lineage ALL with WBC at least 100, 000/mm 3 • T-cell lineage ALL regardless of the WBC • Overt or non-equivocal CNS involvement at D 0 or any CSF involvement at D 4 • Gonadal involvement • Precursor T-lymphoblastic NHL stage III or IV Newborn Down syndrome patients with AR 2 features are assigned to the AR 1 group

VHR CRITERIA • • • Must meet 1 of the following criteria: – ALL patients meeting 1 of the following conditions: • Poor response to prephase therapy (at least 1, 000/mm 3 blasts in peripheral blood after completion of prephase therapy) • t(9; 22) or BCR/ABL • t(4; 11)/MLL-AF 4 • 11 q 23/MLL rearrangement • Near haploidy (no more than 34 chromosomes or DNA index less than 0. 7) • Hypodiploid (35 -40 chromosomes or DNA index 0. 7 to 0. 8) • AUL • For B lineage ALL: failure to achieve complete response (CR) after completion of protocol IA • For T lineage ALL: failure to achieve CR or good partial response (GPR) after completion of protocol IA • Minimal-residual disease (greater than 1, 000 blasts/100, 000 mononuclear bone marrow cells) at evaluation of IA (day 35) – NHL patients who failed to achieve CR or GPR after completion of protocol IA All VHR patients are eligible for stem cell transplantation except those whose sole VHR criterion is a poor response to prephase therapy and who have none of the following features: – T-cell immunophenotype – Early B ALL (CD 10 negative) – WBC at least 100, 000/mm 3 Newborn Down syndrome patients with VHR features are assigned to AR 1 group

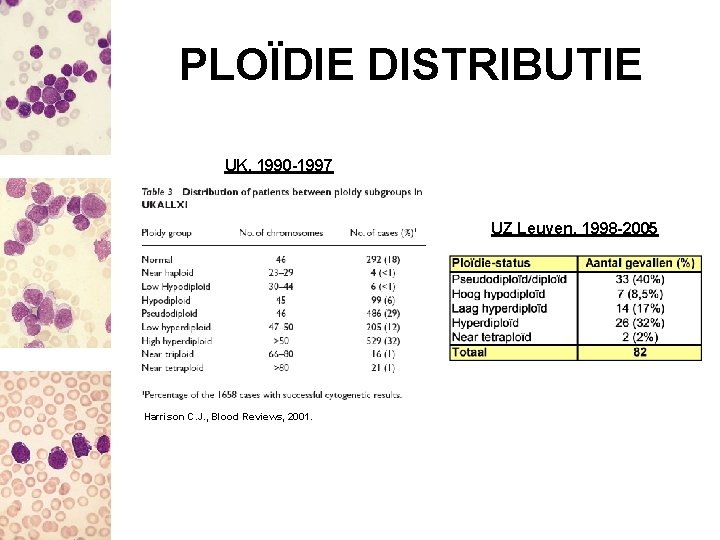
PLOÏDIE DISTRIBUTIE UK, 1990 -1997 UZ Leuven, 1998 -2005 Harrison C. J. , Blood Reviews, 2001.

DNA-analyse onder de loep…. 1. Doen we het goed? 2. Gaan we de analyse behouden?

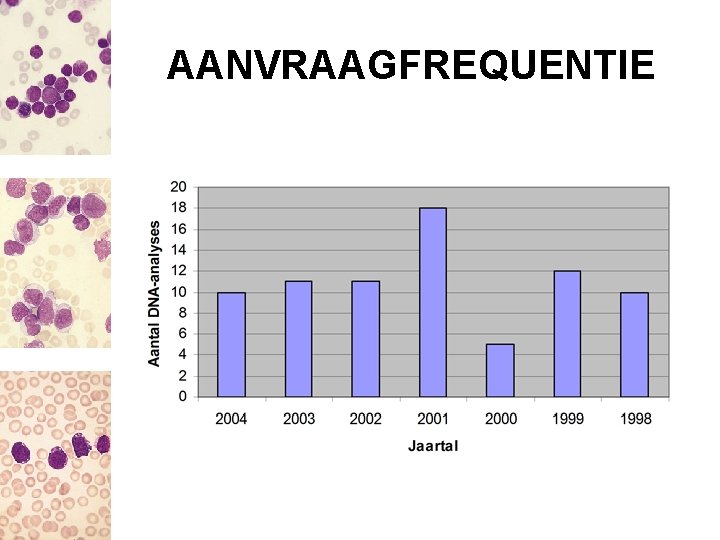
AANVRAAGFREQUENTIE

CYTOGENETICA • Cytogenetica: complementaire versus alternatieve methode • Karyotypering en FISH: numerische én structurele chromosomale abnormaliteiten • ALL: lage mitose-index, lage kwaliteit van de metafasen → karyotypering vaak bemoeilijkt – Doch slechts 1 x geen diagnose via karyotypering op een totaal van 82 stalen (1. 2%) door CME UZ Leuven – FISH tevens uitgevoerd indien geen definitieve conclusie via karyotype • Cytogenetische testen: langere antwoordtijden ( DNA-analyse: < 2 dagen) – Karyotypering: +/- 3 dagen – FISH: tot +/- 1 maand

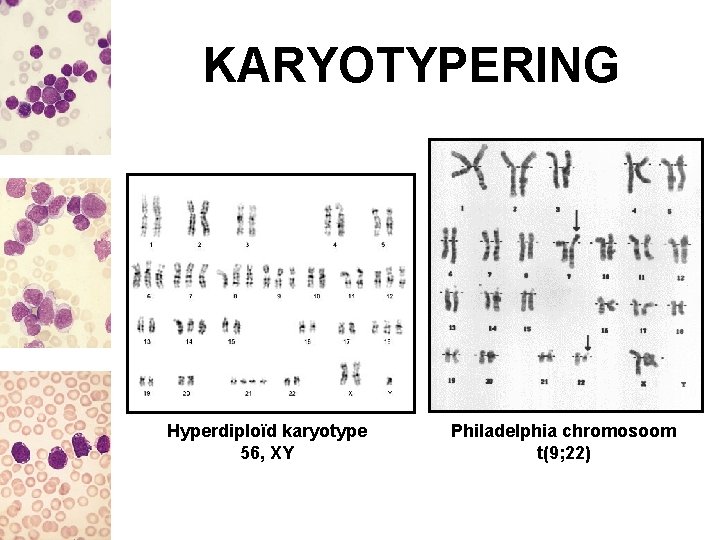
KARYOTYPERING Hyperdiploïd karyotype 56, XY Philadelphia chromosoom t(9; 22)

RETROSPECTIEVE ANALYSE: WAAROM? • Zeer lage uitvoerfrequentie: vervallen reagentia, matige expertise • Geen adequate interne controle (normaal perifeer bloed PBMC) • Geen interne kwaliteitscontrole met kippen erytrocyt nucleï (DNA QC Particles, BD) – Geen kalibratie flowcytometer – Geen controle lineariteit – Geen controle resolutie

RETROSPECTIEVE ANALYSE • Resultaten DNA-analyse vergelijken met de karyotypering • Slechts 82 stalen tussen januari 1998 – maart 2005 • DNA-analyse praktisch altijd op beenmerg uitgevoerd, slechts in 2 gevallen op perifeer bloed • Karyotypering: (vermoedelijk) altijd op beenmerg

RESULTATEN • 68%: goede correlatie tussen DNA FCM en karyotypering • Gebrekkige correlatie in 21 gevallen (26%): altijd slechts 1 -3 chromosomen afwijkend → te lage resolutie FCM – Look et al. (1985), Hiddemann et al. (1987), Perez-Vera et al. (2004) missen eveneens lage hyperdiploïdie/hoge hypodiploïdie met DNA FCM – Deze gebrekkige correlatie echter geen invloed op risico stratificatie (> 50 chromosomen: VLR, ≤ 40 chromosomen: VHR) • 5 (6%) belangrijke discordanties DNA FCM karyotypering

DISCORDANTIES • 3 gevallen met meerdere leukemische lijnen (patiënt 24, 48, 49) – Leukemische lijn met laagste ploïdie arbitrair als primaire lijn – Prognostisch minst gunstige lijn bepaalt het risico – Risico diploïdie lage hyperdiploïdie near tetraploïdie > risico hyperdiploïdie • 1 geval (patiënt 47) met correcte analyse (DI = 1, 14), echter foutief gerapporteerd • 1 geval (patiënt 46) foutief geanalyseerd als diploïd (histogram toont schouder!)

DNA FCM VS CYTOGENETICA • DNA-analyse na uitsluiten onoverkomelijke discordanties: 1 foutieve interpretatie op een totaal van 82 stalen (1, 2%) • Karyotypering: 1 x geen diagnose (1, 2%), FISH toont wel vermoeden van hyperdiploïdie • Deze twee gevallen telkens toch toegewezen aan de very low risk-groep op basis van het cytogenetische respectievelijk het DNA-analyse resultaat

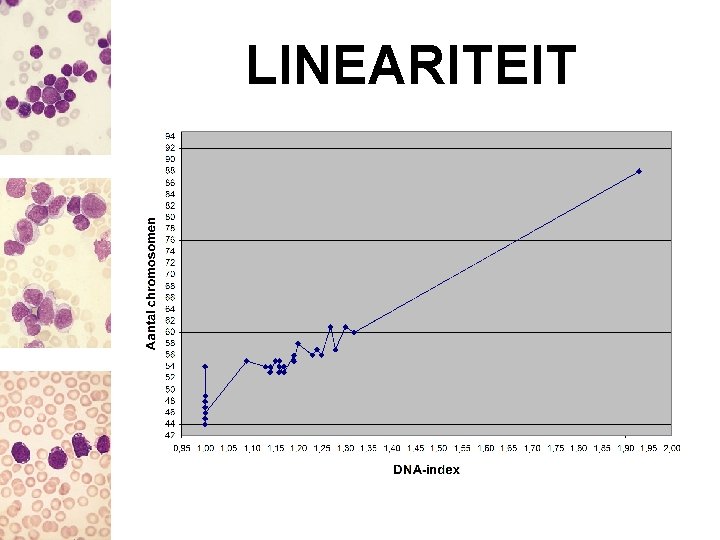
LINEARITEIT

LINEARITEIT Cut-off voor gunstige hyperdiploïdie: DI ≥ 1, 16 of > 50 chromosomen!

LINEARITEIT • Look et al. (Blood, 1985) – DI ≥ 1, 16 geassocieerd met ≥ 53 chromosomen – Uitzonderingen: individuele chromosomen kunnen tot 4, 5 -voud variëren in DNA-inhoud • Cut-off van 1, 16 dient met de grootste voorzichtigheid gehanteerd te worden • Matige lineariteit van DNA FCM in ons laboratorium voornamelijk te wijten aan slechte lineariteit flowcytometer (immers geen controle!)

DIAGNOSTISCHE PERFORMANTIE • DNA-index geen diagnostische maar prognostische waarde • Diagnose van very low risk-patiënten (DI ≥ 1, 16 en > 50 chromosomen) – Vals negatief resultaat: DI < 1, 16 en > 50 chromosomen → sensitiviteit = 17/24 = 71% – Vals positief resultaat: DI ≥ 1, 16 en < 50 chromosomen → specificiteit = 54/54 = 100% • Rekening gehouden met de matige lineariteit van de flowcytometer → vals negatief resultaat in ons labo definiëren als DI ≤ 1 en > 50 chromosomen sensitiviteit = 23/24 = 96% • Sensitiviteit/specificiteit DNA-analyse: moeilijk tot geen exacte cijfers terug te vinden in de literatuur – Enkele onderzoeksgroepen (Hiddemann et al. , Perez-Vera et al. ): sensitiviteit van 100% – Andere onderzoeksgroepen (Smets et al. , Look et al. ): near 100% retrieval van hyperdiploïdie d. m. v. DNA FCM

KOSTEN IMPACT • Bij elke aanvraag analyse steeds op drie verschillende celsuspensies uitgevoerd – Cellen patiënt + normale controle – Cellen normale controle • Totaalkost/test: 32, 28 € • Honoraria RIZIV voor ambulante patiënt en enkelvoudig voorschrift (B 450 -test): 23, 23 € • Nettokost/test: 9, 05 € • Prijs Cycle. TEST PLUS DNA reagens kit (BD; 40 testen): 233 € • Prijs DNA QC Particles kit (BD; 25 controles): 294 €

OVERGEBRUIK/ONDERGEBRUIK DNA-ANALYSE • UZ Leuven: enkel bij nieuwe diagnose pediatrische ALL • Andere mogelijke indicaties: – Multiple myeloma (hyperdiploïdie hier ook betere prognose) – Non-Hodgkin lymfomen (%S-fase fractie) – Vaste weefseltumoren (bijv. borsttumor: %S-fase fractie) • Andere ziekenhuizen: – UZ Gent: ALL, neuroblastoma (reagens kit Beckman Coulter) – AZ VUB: ALL (stalen worden doorgestuurd naar extern labo) – Virga Jesse Hasselt: multiple myeloma, lymfomen, weefseltumoren (reagens kit BD) – UZA: multiple myeloma (zelf-bereide reagentia) • DNA FCM en karyotypering gelijktijdig uitgevoerd om risico op vals negatieven te beperken, sequentiële strategieën echter meer kosten-efficiënt

Gaan we de DNA-analyse behouden of afschaffen in ons laboratorium?

PRO • • Snelle antwoordtijd (meestal binnen 24 uur) Pediaters voor behoud: DNA FCM en karyotypering als wederzijdse controle → keuze therapieschema CONTRA • • • Sensitiviteit in ons labo slechts 71% bij cut-off DI ≥ 1, 16 DI is géén vereiste voor risico stratificatie (ploïdie via karyotypering volstaat) Karyotypering en FISH superieur aan DNA FCM Analyse is verlieslatend Mogelijkheid van doorsturen naar extern labo (echter antwoordtijd )

KWALITEIT VERBETEREN? • Aliquots maken van de reagentia en bewaren op -18°C • Adequate interne controle: PBMC i. p. v. vol bloed • QC-kit of overeenkomst met BD voor (half)jaarlijkse controle en kalibratie zoals voor de overige flowcytometrische testen • Eventueel zelf-bereide reagentia i. p. v. commerciële kit (goedkoper, langere houdbaarheid) • Verhogen uitvoerfrequentie (M. Kahler, lymfomen, weefseltumoren)?

TO DO • Overleg met de pediaters: voor- en nadelen van de DNA-analyse goed tegen elkaar afwegen test al dan niet afschaffen • Indien de test behouden blijft, stappen ondernemen om de kwaliteit te verbeteren (aliquots, PBMC, afspraken BD, …) • Pediaters informeren over de matige lineariteit tussen DI en # chromosomen: voorzichtigheid geboden bij hanteren van de cut-off van 1, 16

THE END…