BRZINA KEMIJSKE REAKCIJE PONAVLJANJE I UTVRIVANJE GRADIVA NASTAVNI

BRZINA KEMIJSKE REAKCIJE PONAVLJANJE I UTVRĐIVANJE GRADIVA • NASTAVNI PREDMET: FIZIKALNA KEMIJA • NASTAVNI PLAN I PROGRAM/KURIKULUM: EKOLOŠKI TEHNIČAR • RAZRED: 2. • TRAJANJE: 2 SATA • AUTOR: TAMARA TKALEC -CAR

DRAGE UČENICE I DRAGI UČENICI! • Kako bismo vam olakšali učenje za vas smo pripremili materijale za samostalni rad. U ovoj prezentaciji su sadržaji koji se odnose na nastavni predmet : Fizikalna kemija. Prezentacija sadrži zadatke za ponavljanje i utvrđivanje gradiva vezanog uz brzinu kemijske reakcije uz detaljne korake rješavanja, ukoliko vam je potrebno. • Na kraju prezentacije je tablica za samovrednovanje, iz koje možete procijeniti svoje znanje. Vaši nastavnici će vam također pružati podršku u učenju na daljinu. Želimo vam uspješno učenje!

PONOVIMO • Brzinu reakcije možemo povećati: üPovećanjem koncentracije reaktanata üPovišenjem temperature üPovećanjem površine reaktanata (usitnjavanje) üDodavanjem katalizatora •

• U nastavku se nalazi 10 zadataka čijim rješavanjem možete procijeniti svoje znanje. • Nakon što je zadatak zadan pokušajte ga odmah samostalno riješiti. • Ukoliko zapnete u rješavanju i potrebna vam je pomoć, u nastavku zadatka se koraci za njegovo rješavanje i rješenja za provjeru točnosti riješenog zadatka.

1. Za reakciju koja se zbiva pri sobnoj temperaturi prema jednadžbi, navedi kako se mijenja brzina te reakcije: Fe(s) + H 2 SO 4(aq) Fe. SO 4 (aq) + H 2(g) Rješenja: a) Usitnjavanjem željeza ubrzava b) Dodavanjem vode usporava c) Dodavanjem katalizatora ubrzava d) Dokapavanjem koncentrirane H 2 SO 4 ubrzava

2. Koje su od slijedećih tvrdnji točne za katalizatore? Rješenja: a) Mogu ubrzati samo one reakcije koje teku bez katalizatora b) Mogu potaknuti reakciju među tvarima koje inače ne reagiraju c) Sudjeluju u kemijskoj reakciji i na kraju reakcije ostaju nepromijenjeni d) Djeluju samo u količini mjerodavnog reaktanta e) Djeluje u malim količinama

3. Za prikazanu reakciju napiši izraz za brzinu na temelju promjene koncentracije svih reaktanata i produkata. 2 NO(g) + O 2(g) 2 NO 2(g) •

4. Za reakciju prikazanu u općem obliku: 2 A + B C + 3 D a) Izračunaj srednju brzinu reakcije u vremenu t= 2 min do t=8 min, ako se koncentracija reaktanta A u tom vremenu smanjila od 6, 69 mol/l do 2, 00 mol/l. b) Izračunaj brzinu promjene koncentracije samo reaktanta A. c) Izračunaj brzinu promjene koncentracije produkta D

a) izračunaj srednju brzinu reakcije u vremenu t= 2 min do t=8 min, ako se koncentracija reaktanta A u tom vremenu smanjila od 6, 69 mol/l do 2, 00 mol/l. •
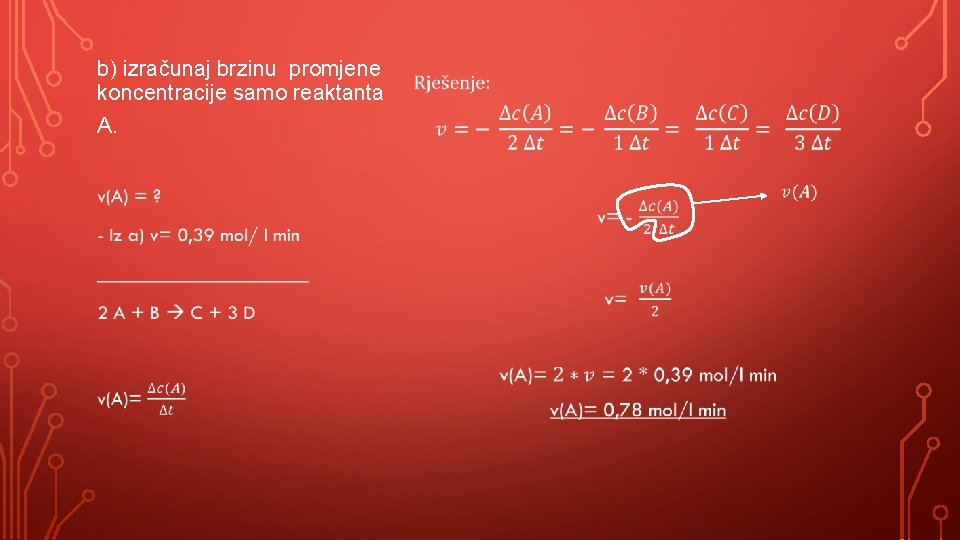
b) izračunaj brzinu promjene koncentracije samo reaktanta A. •

c) izračunaj brzinu promjene koncentracije produkta D 2 A + B C + 3 D - Iz a) v=0, 39 mol/l min - Iz b) v(A)= 0, 78 mol/l min __________ v(D)= ? Rješenje: •

5. Termički raspad didušikovog pentoksida pri 45 oc teče prema jednadžbi: 2 N 2 O 5(g) 4 NO 2 (g) + O 2(g) Ako srednja brzina te reakcije u prvih 20 minuta iznosi 2, 8 x 10 -4 mol l 1 min-1 kolika je promjena koncentracije N O u prvih 20 minuta? 2 5 t= 20 min v=2, 8 x 10 -4 mol l-1 min 1 ________ v(N 2 O 5)= ? •
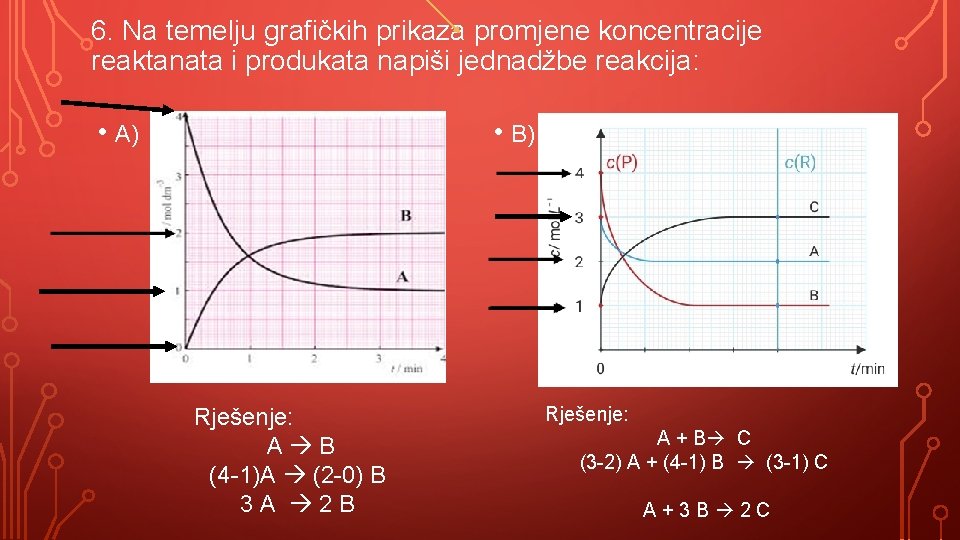
6. Na temelju grafičkih prikaza promjene koncentracije reaktanata i produkata napiši jednadžbe reakcija: • A) • B) Rješenje: A B (4 -1)A (2 -0) B 3 A 2 B Rješenje: A + B C (3 -2) A + (4 -1) B (3 -1) C A + 3 B 2 C
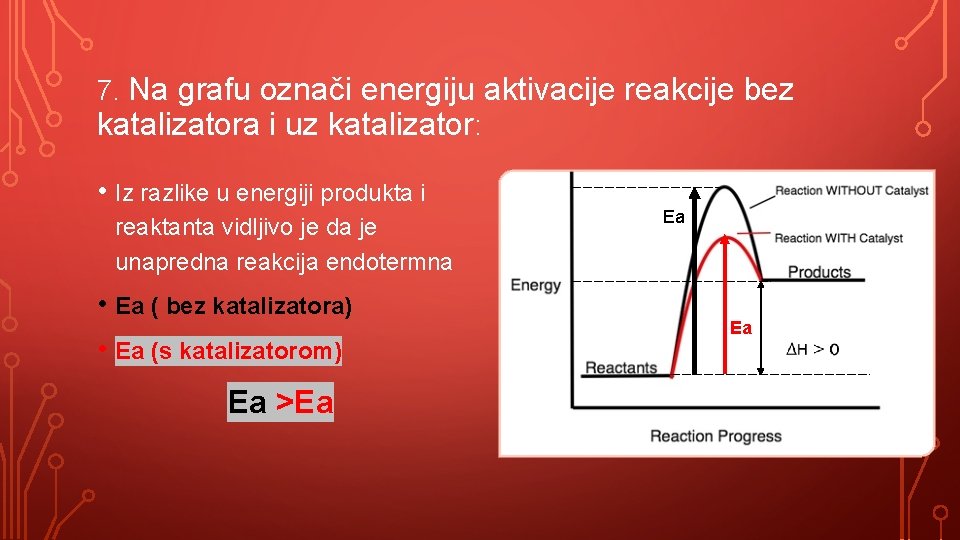
7. Na grafu označi energiju aktivacije reakcije bez katalizatora i uz katalizator: • Iz razlike u energiji produkta i reaktanta vidljivo je da je unapredna reakcija endotermna • Ea ( bez katalizatora) • Ea (s katalizatorom) Ea >Ea Ea Ea

8. Na gafičkim prikazima označi energiju aktivacije unapredne i unazadne reakcije: Ea Ea Ea Unapredna reakcija: reaktanti produkti Unazadna reakcija: produkti

9. Na temelju ZAKONA O BRZINI napiši izraz za brzinu za slijedeće jednadžbe reakcija 2 NO(g) + O 2(g) 2 NO 2(g) Rješenje: v= k [NO]2 * [O 2] 2 H 2 O (l) 2 H 2(g) + O 2(g) Rješenje: v= k [H 2 O]2

10. Za navedenu reakciju odredi kako će se promijeniti brzina ako se koncentracija dušika poveća 2 puta u odnosu na početnu koncentraciju, a koncentracija vodika ostane ista? 2 N 2(g) + 3 H 2(g) 2 NH 3(g) Rješenje: Izraz za brzinu prema zakonu o brzini: v(početna)= k [N 2]2 [H 2]3 [N 2](druga) = 2 [N 2](početna) V(druga) = k (2[N 2])2 [H 2]3 = k 4 [N ]2 [H ]3 2 2 Odnosno : v(druga) = 4 v(početna) Brzina će se povećati 4 puta u odnosu na početnu

TABLICA ZA SAMOVREDNOVANJE U stanju sam/mogu: Navesti/nabrojati: sve utjecaje na brzinu reakcije, objasniti promjene u brzini reakcije s obzirom na promjenu pojedinog parametra Razlikovati na grafičkom prikazu: reaktante i produkte, energiju aktivacije reakcije s i bez katalizatora, unaprednu i unazadnu reakciju te pripadajuće energije aktivacije. Pomoću podataka s grafičkog prikazu odrediti jednadžbu reakcije Riješiti zadatak: napisati izraz za brzinu bilo koje reakcije pomoću promjene koncentracija reaktanata i produkata. Napisat izraz za brzinu na temelju zakona o brzini. Izračunati brzinu iz zadanih vrijednost. Dobro (samostalno, bez pogreške) Uglavnom dobro (uz manje pogreške) Ne baš, trebam dodatnu pomoć

HVALA NA PAŽNJI I SRETNO U RJEŠAVANJU NOVIH ZADATAKA
- Slides: 19


































