BRZINA KEMIJSKE REAKCIJE NASTAVNI PREDMET FIZIKALNA KEMIJA EKOLOKI

BRZINA KEMIJSKE REAKCIJE NASTAVNI PREDMET: FIZIKALNA KEMIJA EKOLOŠKI TEHNIČAR/KEMIJSKI TEHNIČAR TRAJANJE: 2 SATA/3 SATA PREZENTACIJU PRIPREMILA: NADA PITINAC

DRAGI UČENICI I DRAGE UČENICE, KAKO BISMO VAM OLAKŠALI UČENJE ZA VAS SMO PRIPREMILI MATERIJALE ZA SAMOSTALNI RAD. U OVOJ PREZENTACIJI SU SADRŽAJI KOJI SE ODNOSE NA NASTAVNI PREDMET: FIZIKALNA KEMIJA NA KRAJU PREZENTACIJE NALAZE SE ZADACI ZA VJEŽBU TE PITANJA ZA PONAVLJANJE GRADIVA. VAŠI NASTAVNICI ĆE VAM TAKOĐER PRUŽATI PODRŠKU U UČENJU NA DALJINU. 2 ŽELIMO VAM SRETNO I UGODNO UČENJE.

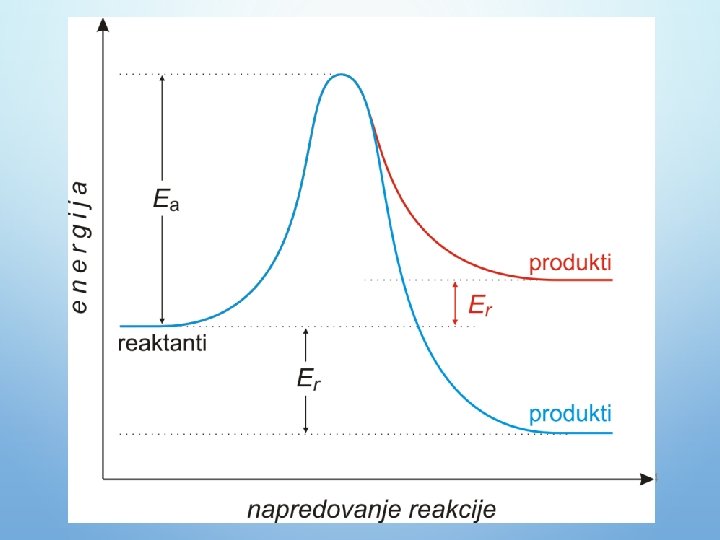
• KEMIJSKA KINETIKA? • KAKO NASTAJE KEMIJSKA REAKCIJA? • ENERGIJA AKTIVACIJE? • PRIMJERI BRZIH I SPORIH KEMIJSKIH REAKCIJA? 3
4

ŠTO JE BRZINA • U SVAKODNEVNOM ŽIVOTU? • PROMJENA PUTA, VOLUMENA ILI KOLIČINE PODATAKA U ODREĐENOM VREMENU. 5

ŠTO JE BRZINA • U KEMIJI? • PRIRAST MNOŽINSKE KONCENTRACIJE JEDNOG SASTOJKA REAKCIJSKOG SUSTAVA U ODREĐENOM VREMENU. prirast koncentracije od A V(A)= vrijeme u kojem je nastala promatrana promjena Brzina prirasta koncentracije sastojka A 6
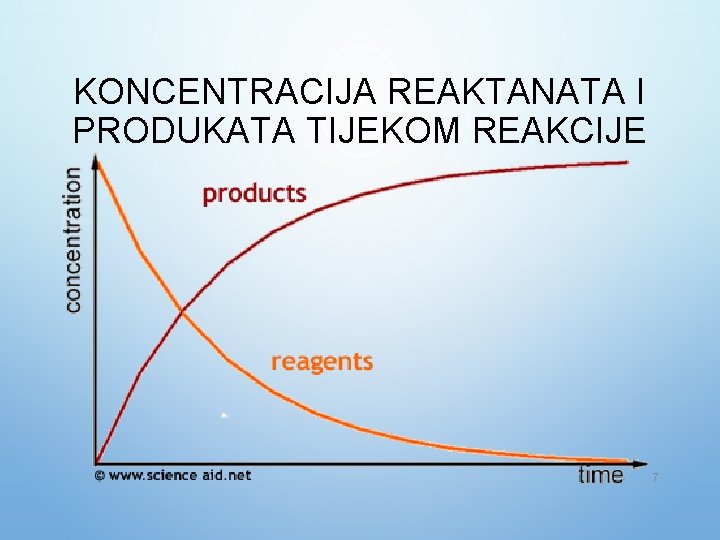
KONCENTRACIJA REAKTANATA I PRODUKATA TIJEKOM REAKCIJE 7

• BRZINA PRIRASTA KONCENTRACIJE REAKTANATA JE NEGATIVNA VRIJEDNOST JER SE NJIHOVA KONCENTRACIJA NAPREDOVANJEM REAKCIJE SMANJUJE. • ΔC= C 2 - C 1 • BRZINA PRIRASTA PRODUKTA JE POZITIVNA VRIJEDNOST JER NJEGOVA KONCENTRACIJA NAPREDOVANJEM REAKCIJE RASTE. 8
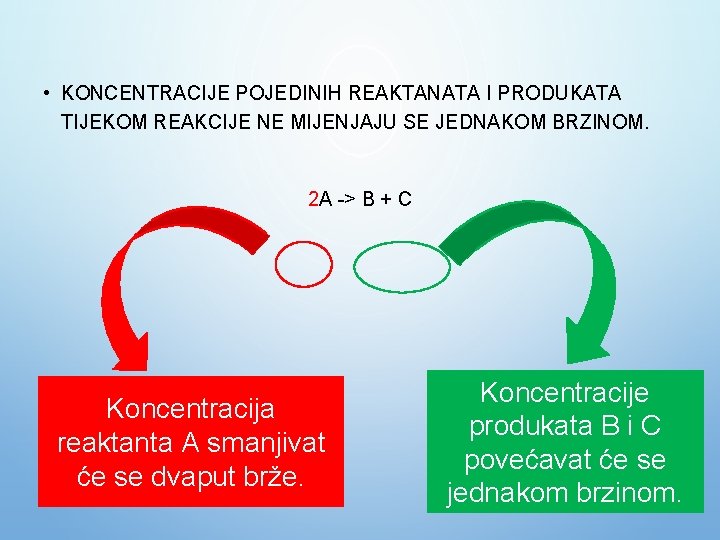
• KONCENTRACIJE POJEDINIH REAKTANATA I PRODUKATA TIJEKOM REAKCIJE NE MIJENJAJU SE JEDNAKOM BRZINOM. 2 A -> B + C Koncentracija reaktanta A smanjivat će se dvaput brže. Koncentracije produkata B i C povećavat će se 9 jednakom brzinom.

• ZA KEMIJSKE REAKCIJE PRI KOJIMA JE VOLUMEN STALAN BRZINA REAKCIJE R IZRAŽAVA SE KAO BRZINA PRIRASTA KONCENTRACIJE SASTOJKA PODIJELJENOG NJEGOVIM STEHIOMETRIJSKIM BROJEM (NEGATIVAN ZA REAKTANTE, POZITIVAN ZA PRODUKTE). 2 A -> 1 B + 1 C 10
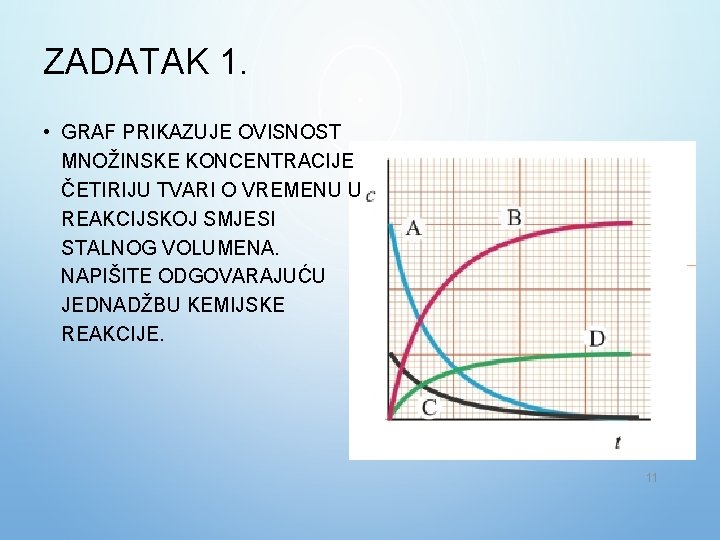
ZADATAK 1. • GRAF PRIKAZUJE OVISNOST MNOŽINSKE KONCENTRACIJE ČETIRIJU TVARI O VREMENU U REAKCIJSKOJ SMJESI STALNOG VOLUMENA. NAPIŠITE ODGOVARAJUĆU JEDNADŽBU KEMIJSKE REAKCIJE. 11
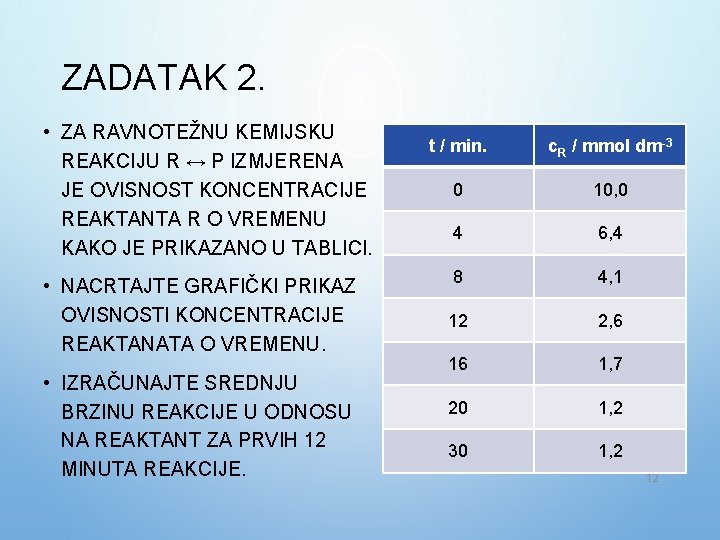
ZADATAK 2. • ZA RAVNOTEŽNU KEMIJSKU REAKCIJU R ↔ P IZMJERENA JE OVISNOST KONCENTRACIJE REAKTANTA R O VREMENU KAKO JE PRIKAZANO U TABLICI. • NACRTAJTE GRAFIČKI PRIKAZ OVISNOSTI KONCENTRACIJE REAKTANATA O VREMENU. • IZRAČUNAJTE SREDNJU BRZINU REAKCIJE U ODNOSU NA REAKTANT ZA PRVIH 12 MINUTA REAKCIJE. t / min. c. R / mmol dm-3 0 10, 0 4 6, 4 8 4, 1 12 2, 6 16 1, 7 20 1, 2 30 1, 2 12

HVALA NA POZORNOSTI! 13
- Slides: 13























