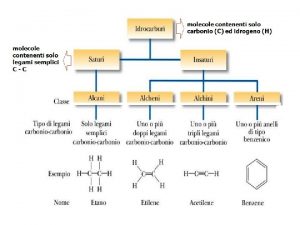
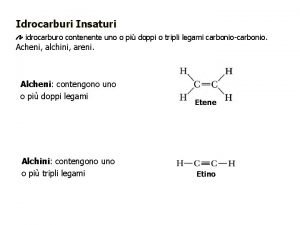
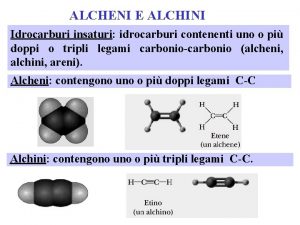
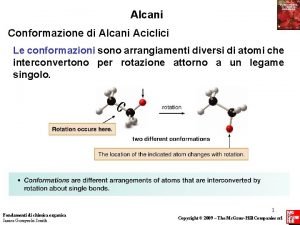
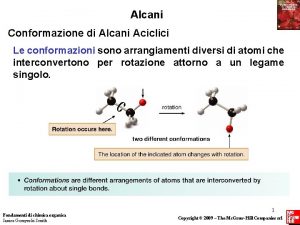
ALCANI Alcani idrocarburi saturi contenenti solo legami semplici

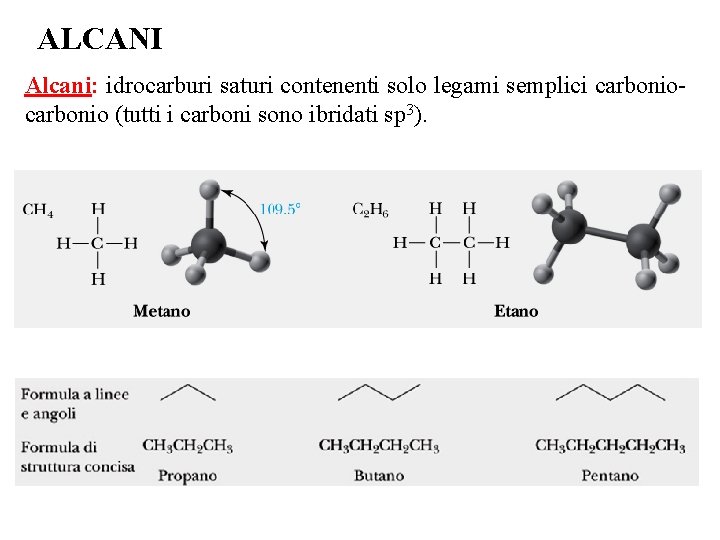
ALCANI Alcani: idrocarburi saturi contenenti solo legami semplici carbonio (tutti i carboni sono ibridati sp 3).
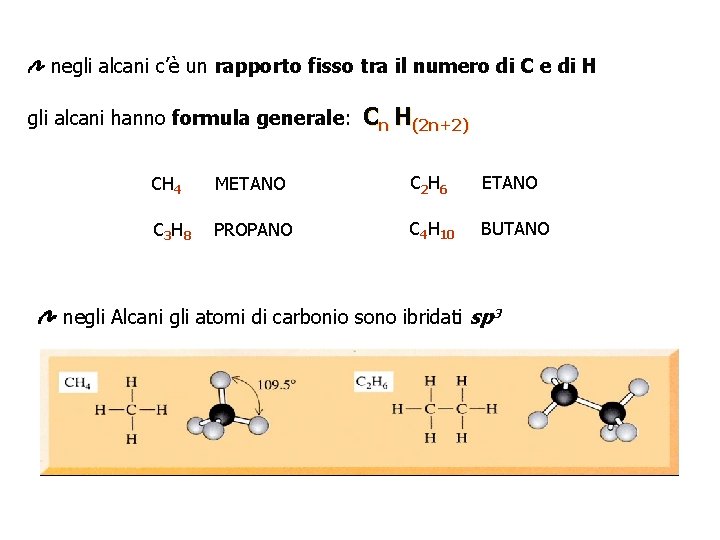
negli alcani c’è un rapporto fisso tra il numero di C e di H gli alcani hanno formula generale: Cn H(2 n+2) CH 4 METANO C 2 H 6 ETANO C 3 H 8 PROPANO C 4 H 10 BUTANO negli Alcani gli atomi di carbonio sono ibridati sp 3
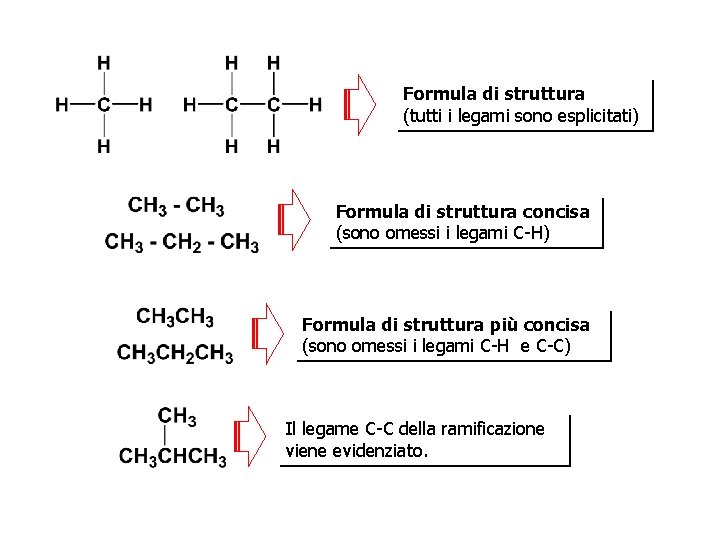
Formula di struttura (tutti i legami sono esplicitati) Formula di struttura concisa (sono omessi i legami C-H) Formula di struttura più concisa (sono omessi i legami C-H e C-C) Il legame C-C della ramificazione viene evidenziato.
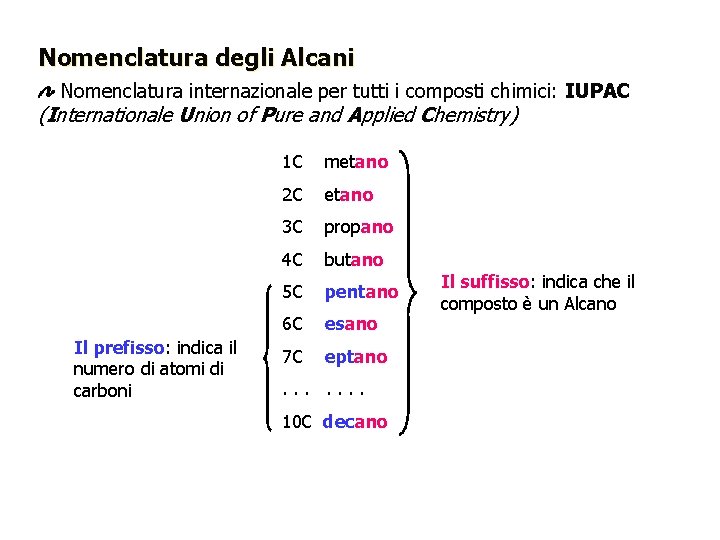
Nomenclatura degli Alcani Nomenclatura internazionale per tutti i composti chimici: IUPAC (Internationale Union of Pure and Applied Chemistry) Il prefisso: indica il numero di atomi di carboni 1 C metano 2 C etano 3 C propano 4 C butano 5 C pentano 6 C esano 7 C eptano . . . . 10 C decano Il suffisso: indica che il composto è un Alcano
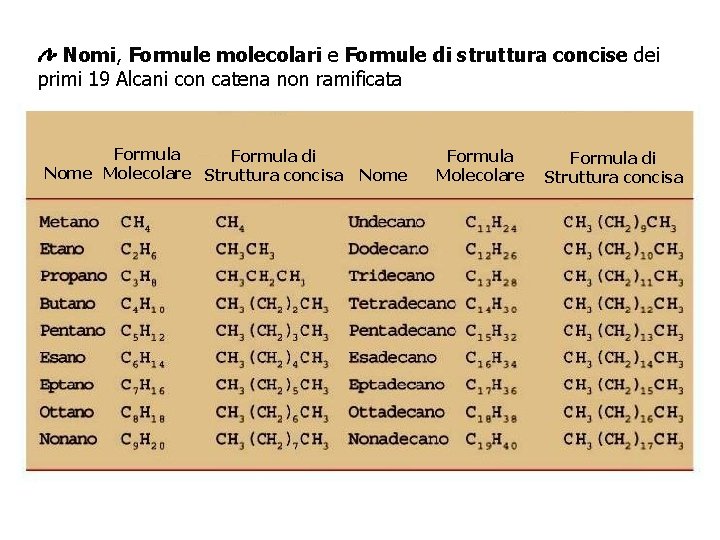
Nomi, Formule molecolari e Formule di struttura concise dei primi 19 Alcani con catena non ramificata Formula di Nome Molecolare Struttura concisa Nome Formula Molecolare Formula di Struttura concisa
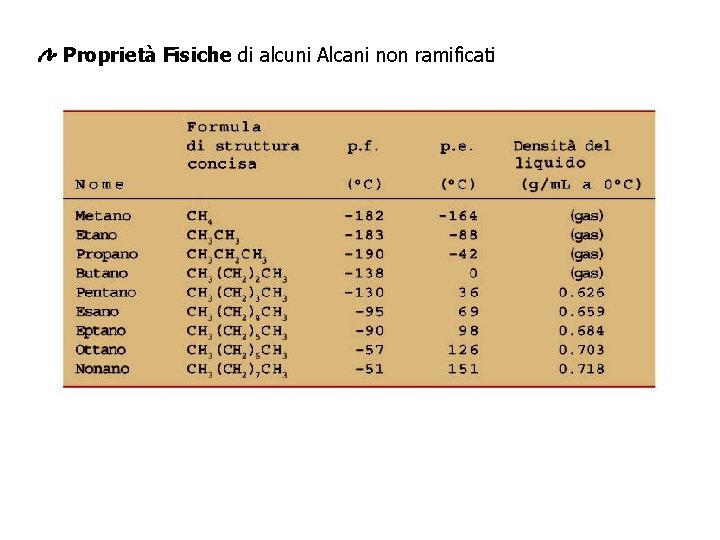
Proprietà Fisiche di alcuni Alcani non ramificati
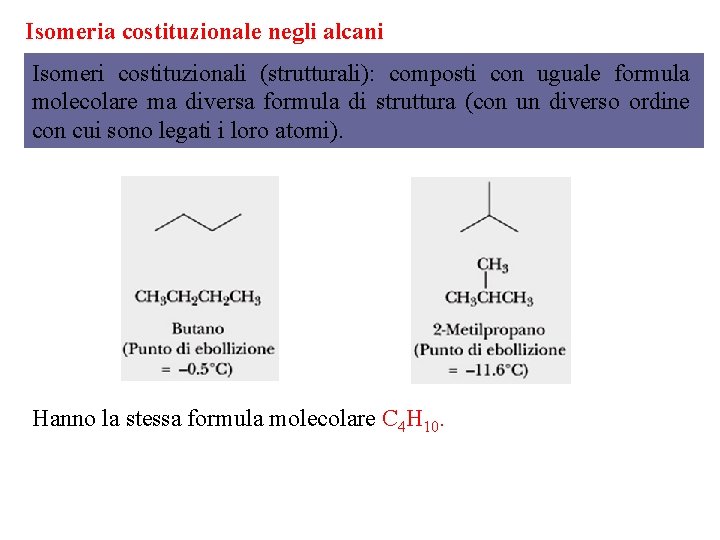
Isomeria costituzionale negli alcani Isomeri costituzionali (strutturali): composti con uguale formula molecolare ma diversa formula di struttura (con un diverso ordine con cui sono legati i loro atomi). Hanno la stessa formula molecolare C 4 H 10.

Numero di isomeri costituzionali Atomi di carbonio Isomeri costituzionali 1 5 6 10 15 25 0 3 5 75 4. 347 36. 797. 588
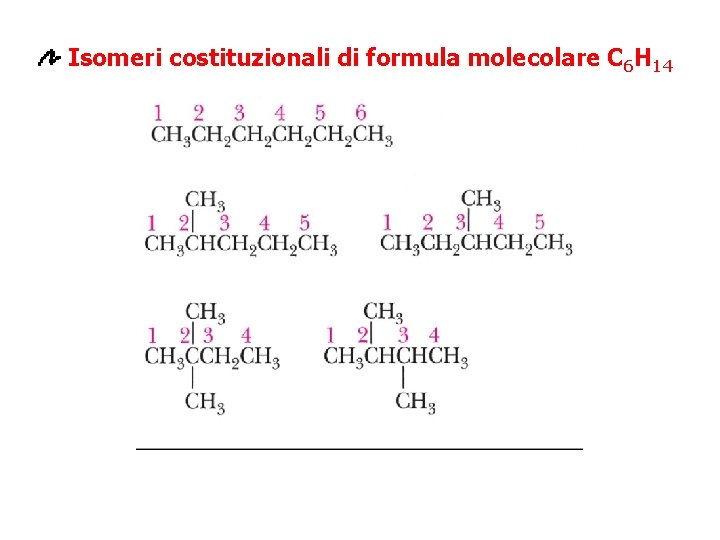
Isomeri costituzionali di formula molecolare C 6 H 14
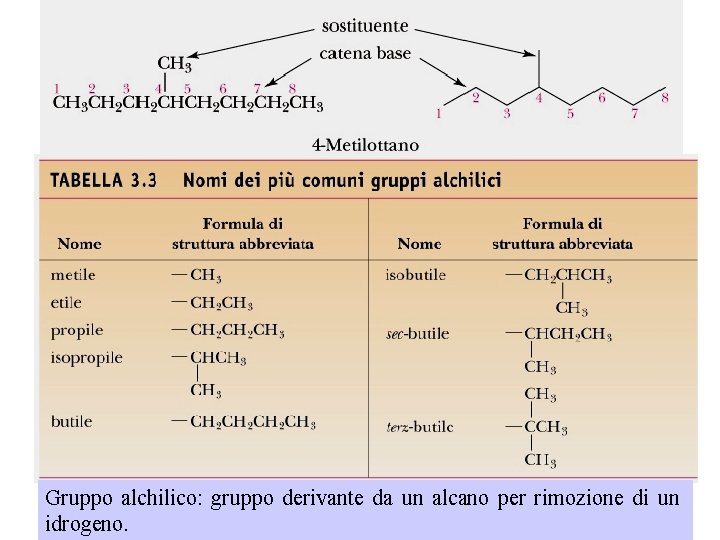
Gruppo alchilico: gruppo derivante da un alcano per rimozione di un idrogeno.
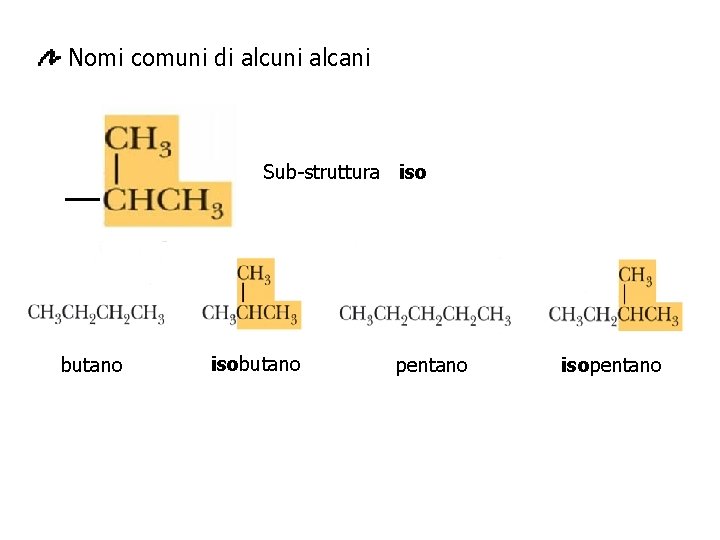
Nomi comuni di alcuni alcani Sub-struttura iso butano isobutano pentano isopentano

Come assegnare il nome IUPAC ad un Alcano Regole IUPAC – Criteri generali 1. Trovare nel composto la catena di atomi di carbonio più lunga 2. Attribuire il nome ad ogni ramificazione 3. Mettere le ramificazioni in ordine alfabetico (I prefissi iso, ciclo e neo contano come parte del nome del radicale ai fini dell’ordine alfabetico) 4. Numerare la catena principale a partire da un estremità in modo da attribuire al primo sostituente il numero più piccolo 5. Assegnare ad ogni ramificazione il numero che corrisponde al suo punto di attacco alla catena principale
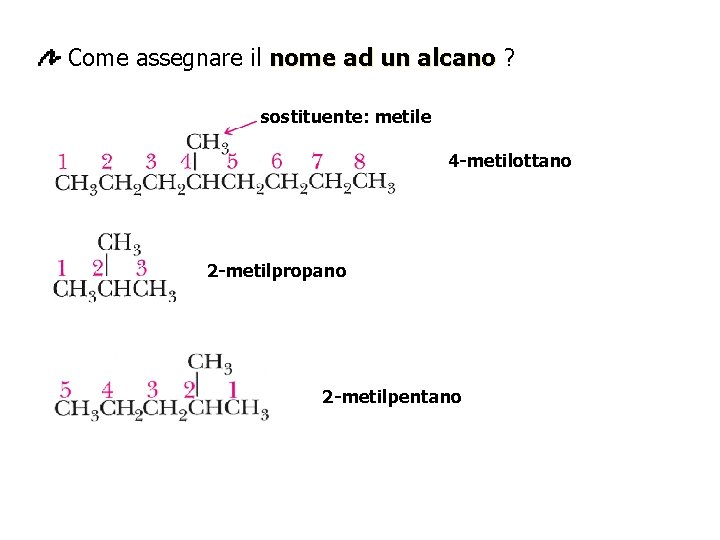
Come assegnare il nome ad un alcano ? sostituente: metile 4 -metilottano 2 -metilpropano 2 -metilpentano
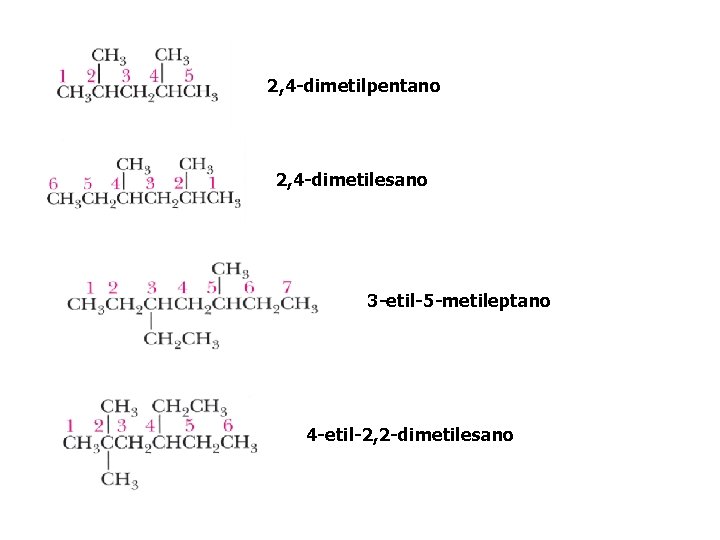
2, 4 -dimetilpentano 2, 4 -dimetilesano 3 -etil-5 -metileptano 4 -etil-2, 2 -dimetilesano
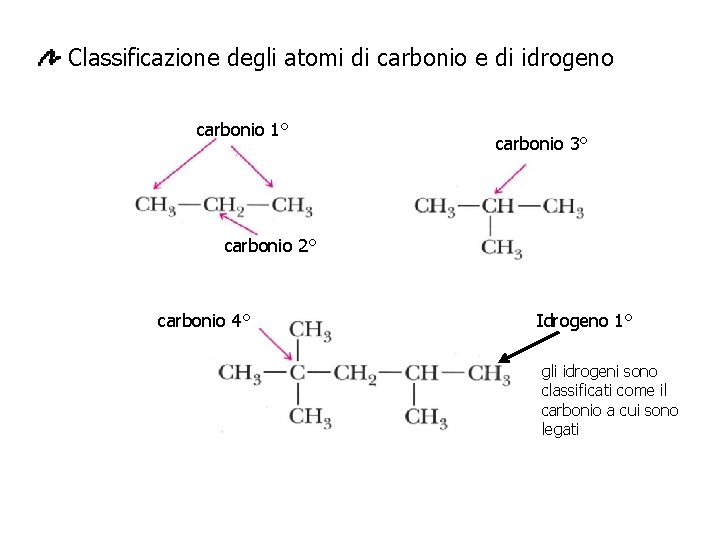
Classificazione degli atomi di carbonio e di idrogeno carbonio 1° carbonio 3° carbonio 2° carbonio 4° Idrogeno 1° gli idrogeni sono classificati come il carbonio a cui sono legati
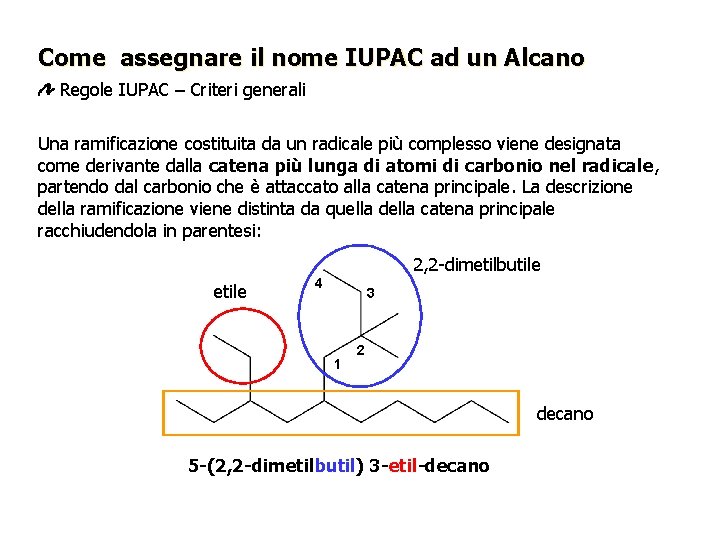
Come assegnare il nome IUPAC ad un Alcano Regole IUPAC – Criteri generali Una ramificazione costituita da un radicale più complesso viene designata come derivante dalla catena più lunga di atomi di carbonio nel radicale, partendo dal carbonio che è attaccato alla catena principale. La descrizione della ramificazione viene distinta da quella della catena principale racchiudendola in parentesi: 2, 2 -dimetilbutile etile 4 3 1 2 decano 5 -(2, 2 -dimetilbutil) 3 -etil-decano
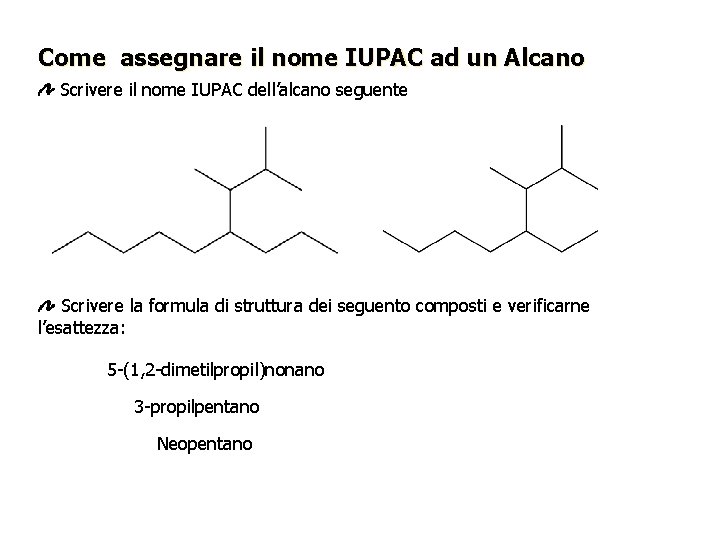
Come assegnare il nome IUPAC ad un Alcano Scrivere il nome IUPAC dell’alcano seguente Scrivere la formula di struttura dei seguento composti e verificarne l’esattezza: 5 -(1, 2 -dimetilpropil)nonano 3 -propilpentano Neopentano
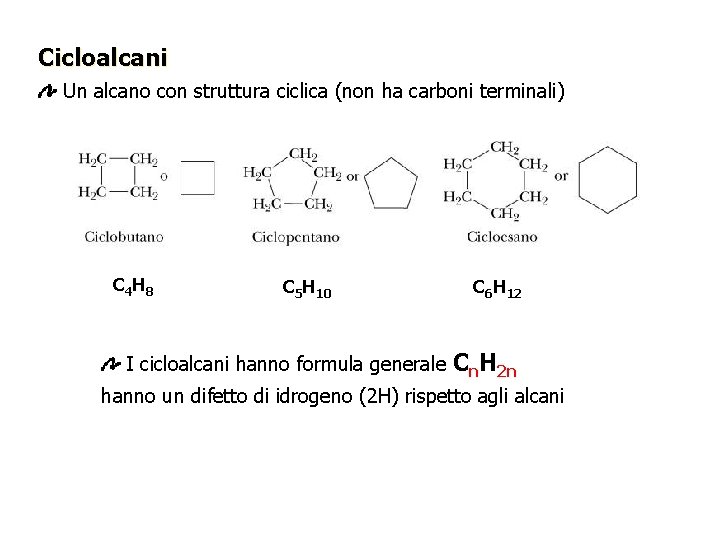
Cicloalcani Un alcano con struttura ciclica (non ha carboni terminali) C 4 H 8 C 5 H 10 I cicloalcani hanno formula generale C 6 H 12 Cn. H 2 n hanno un difetto di idrogeno (2 H) rispetto agli alcani
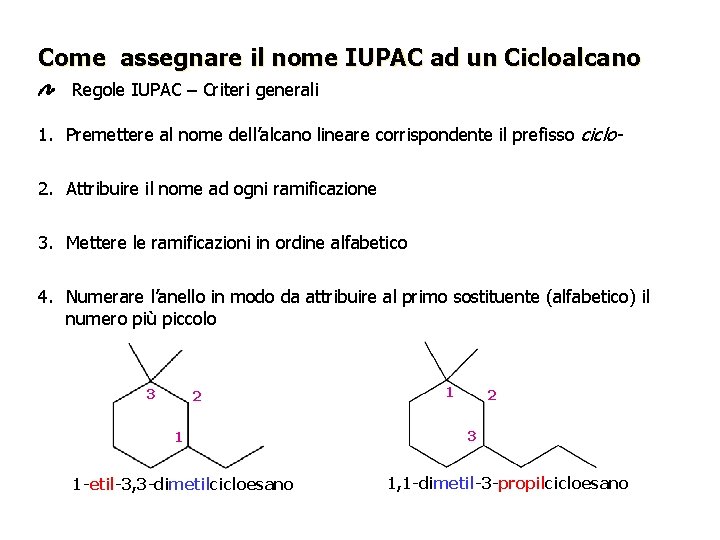
Come assegnare il nome IUPAC ad un Cicloalcano Regole IUPAC – Criteri generali 1. Premettere al nome dell’alcano lineare corrispondente il prefisso ciclo 2. Attribuire il nome ad ogni ramificazione 3. Mettere le ramificazioni in ordine alfabetico 4. Numerare l’anello in modo da attribuire al primo sostituente (alfabetico) il numero più piccolo 3 2 1 1 -etil-3, 3 -dimetilcicloesano 1 2 3 1, 1 -dimetil-3 -propilcicloesano
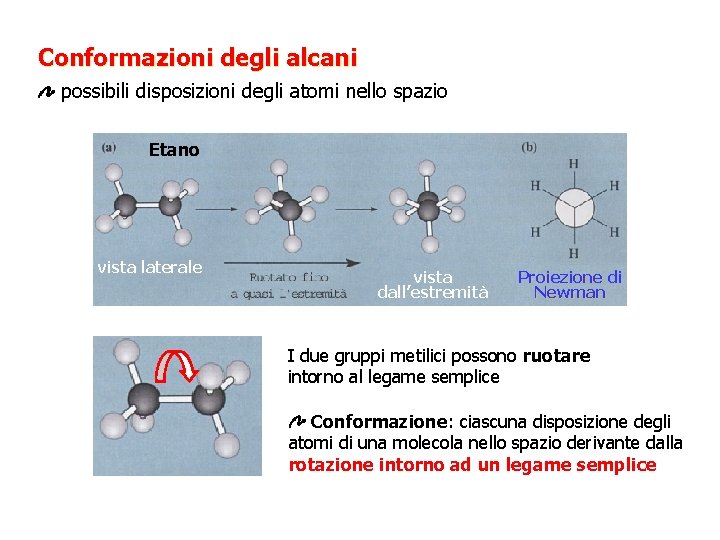
Conformazioni degli alcani possibili disposizioni degli atomi nello spazio Etano vista laterale vista dall’estremità Proiezione di Newman I due gruppi metilici possono ruotare intorno al legame semplice Conformazione: ciascuna disposizione degli atomi di una molecola nello spazio derivante dalla rotazione intorno ad un legame semplice
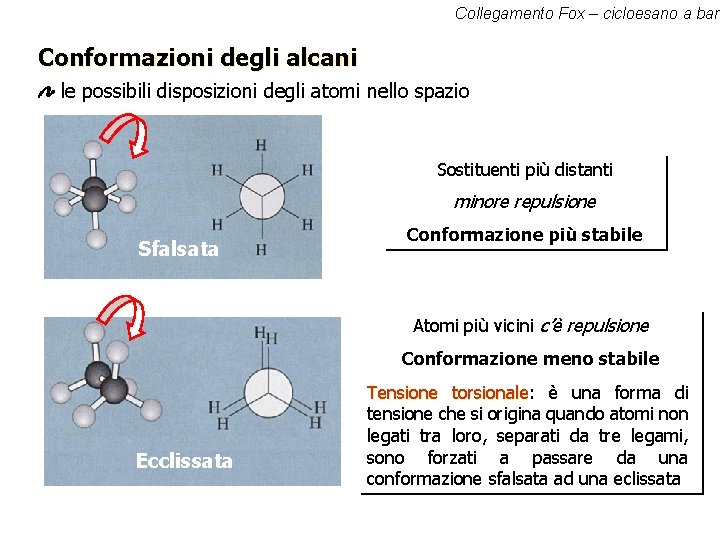
Collegamento Fox – cicloesano a barc Conformazioni degli alcani le possibili disposizioni degli atomi nello spazio Sostituenti più distanti minore repulsione Sfalsata Conformazione più stabile Atomi più vicini c’è repulsione Conformazione meno stabile Ecclissata Tensione torsionale: torsionale è una forma di tensione che si origina quando atomi non legati tra loro, separati da tre legami, sono forzati a passare da una conformazione sfalsata ad una eclissata
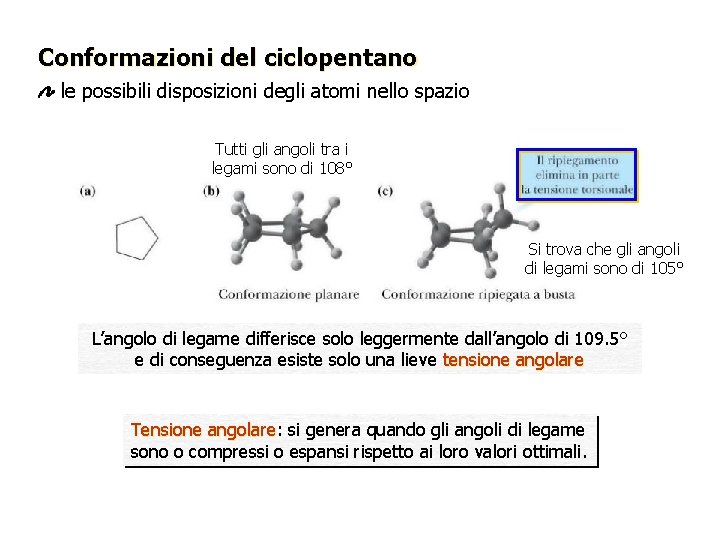
Conformazioni del ciclopentano le possibili disposizioni degli atomi nello spazio Tutti gli angoli tra i legami sono di 108° Si trova che gli angoli di legami sono di 105° L’angolo di legame differisce solo leggermente dall’angolo di 109. 5° e di conseguenza esiste solo una lieve tensione angolare Tensione angolare: angolare si genera quando gli angoli di legame sono o compressi o espansi rispetto ai loro valori ottimali.
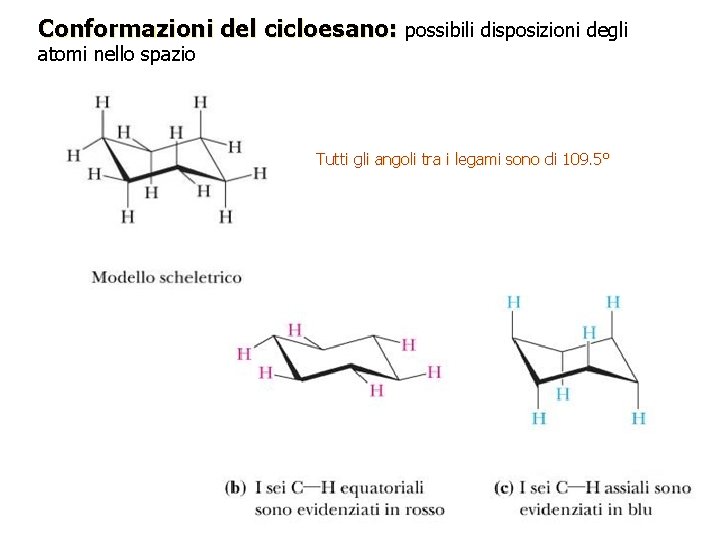
Conformazioni del cicloesano: possibili disposizioni degli atomi nello spazio Tutti gli angoli tra i legami sono di 109. 5°
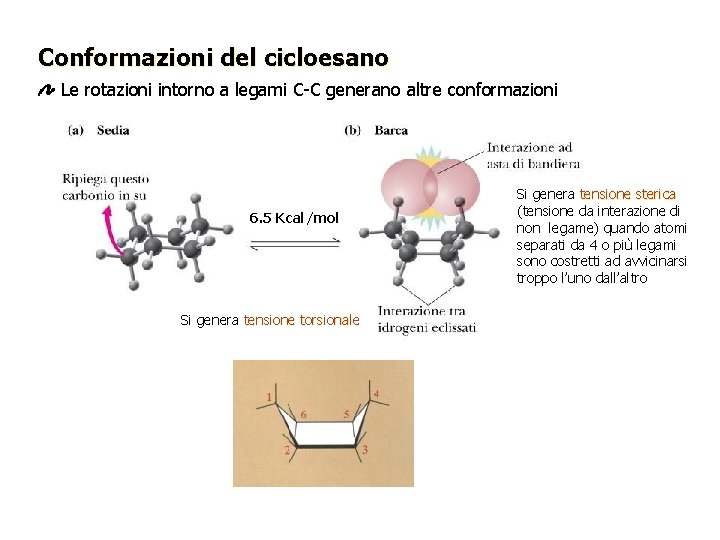
Conformazioni del cicloesano Le rotazioni intorno a legami C-C generano altre conformazioni 6. 5 Kcal/mol Si genera tensione torsionale Si genera tensione sterica (tensione da interazione di non legame) quando atomi separati da 4 o più legami sono costretti ad avvicinarsi troppo l’uno dall’altro
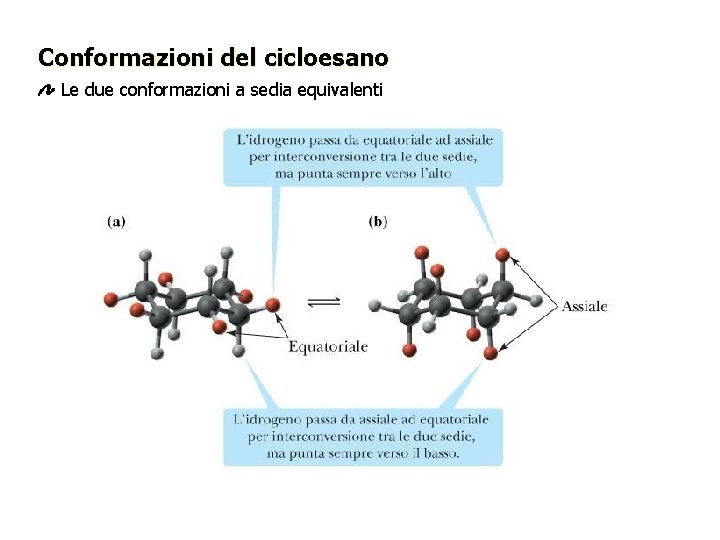
Conformazioni del cicloesano Le due conformazioni a sedia equivalenti
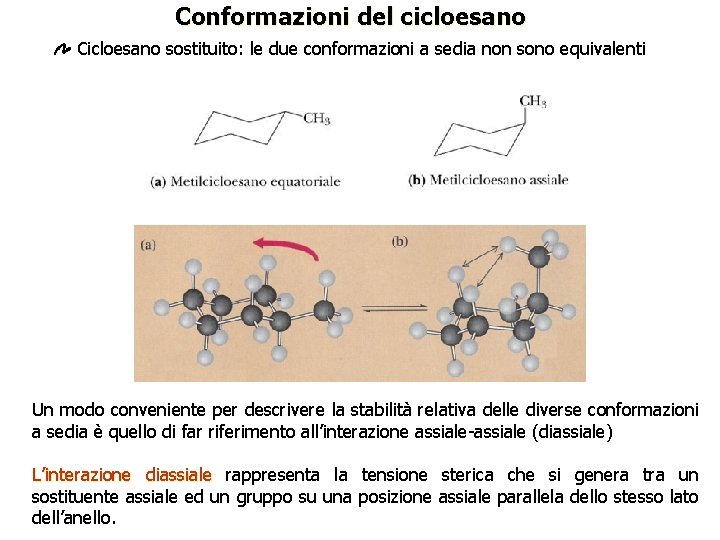
Conformazioni del cicloesano Cicloesano sostituito: le due conformazioni a sedia non sono equivalenti Un modo conveniente per descrivere la stabilità relativa delle diverse conformazioni a sedia è quello di far riferimento all’interazione assiale-assiale (diassiale) L’interazione diassiale rappresenta la tensione sterica che si genera tra un sostituente assiale ed un gruppo su una posizione assiale parallela dello stesso lato dell’anello.
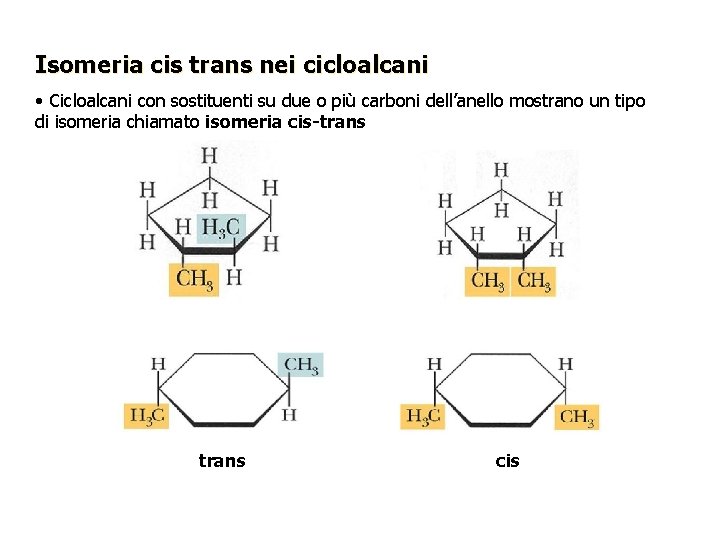
Isomeria cis trans nei cicloalcani • Cicloalcani con sostituenti su due o più carboni dell’anello mostrano un tipo di isomeria chiamato isomeria cis-trans cis
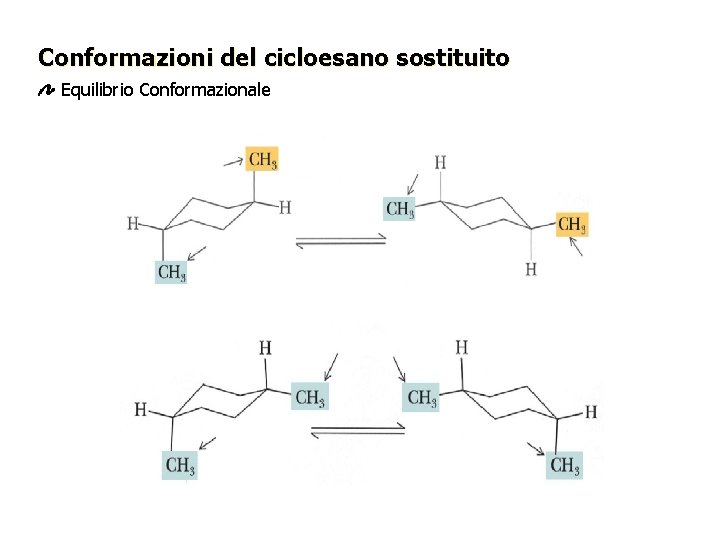
Conformazioni del cicloesano sostituito Equilibrio Conformazionale

Reazioni degli Alcani Combustione – Calori di combustione Combustione (Ossidazione): è una reazione con l’ossigeno ed è utilizzata come fonte di energia CH 4 + O 2 → CO 2 + 2 H 2 O DH° = -212 Kcal/mol CH 3 CH 2 CH 3 + 5 O 2 → 3 CO 2 + 4 H 2 O DH° = -530 Kcal/mol Quando una mole di un dato alcano è completamente bruciato ad anidride carbonica ed acqua, si libera una quantità caratteristica di calore: Il Calore di combustione standard
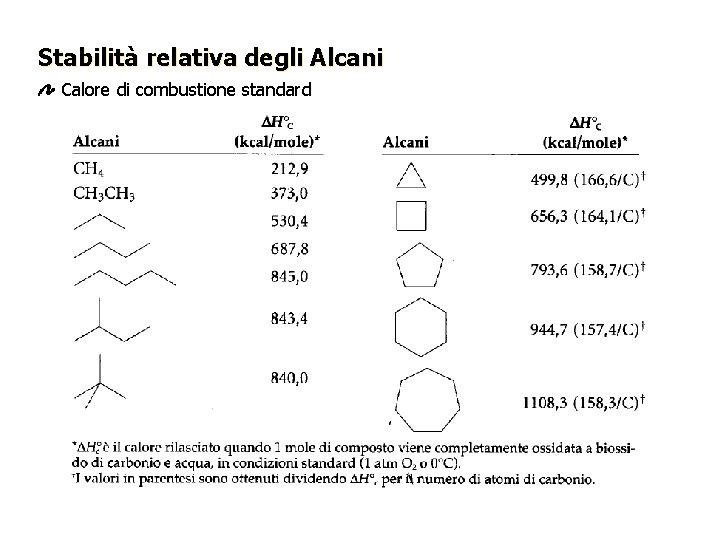
Stabilità relativa degli Alcani Calore di combustione standard
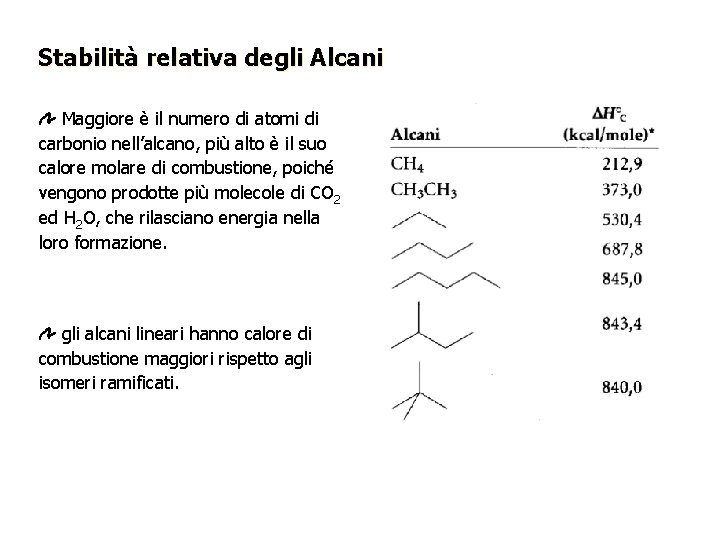
Stabilità relativa degli Alcani Maggiore è il numero di atomi di carbonio nell’alcano, più alto è il suo calore molare di combustione, poiché vengono prodotte più molecole di CO 2 ed H 2 O, che rilasciano energia nella loro formazione. gli alcani lineari hanno calore di combustione maggiori rispetto agli isomeri ramificati.
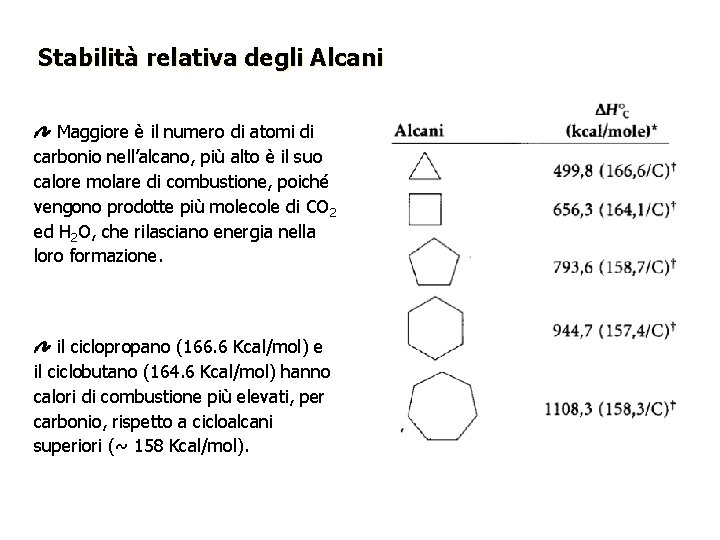
Stabilità relativa degli Alcani Maggiore è il numero di atomi di carbonio nell’alcano, più alto è il suo calore molare di combustione, poiché vengono prodotte più molecole di CO 2 ed H 2 O, che rilasciano energia nella loro formazione. il ciclopropano (166. 6 Kcal/mol) e il ciclobutano (164. 6 Kcal/mol) hanno calori di combustione più elevati, per carbonio, rispetto a cicloalcani superiori (~ 158 Kcal/mol).
- Slides: 33