Dalle soluzioni alla chimica del carbonio Capitolo 14

Dalle soluzioni alla chimica del carbonio

Capitolo 14 Gli idrocarburi Unità 46 Idrocarburi alifatici 14. 1 Classificazione degli idrocarburi 14. 2 Alcani 14. 3 La reattività degli alcani 14. 4 Cicloalcani 14. 5 Alcheni 14. 6 Alchini Unità 47 Idrocarburi aromatici ed eterociclici 14. 7 Idrocarburi aromatici 14. 8 Idrocarburi policiclici aromatici 14. 9 Idrocarburi eteroliciclici 14. 10 Alcaloidi Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 2
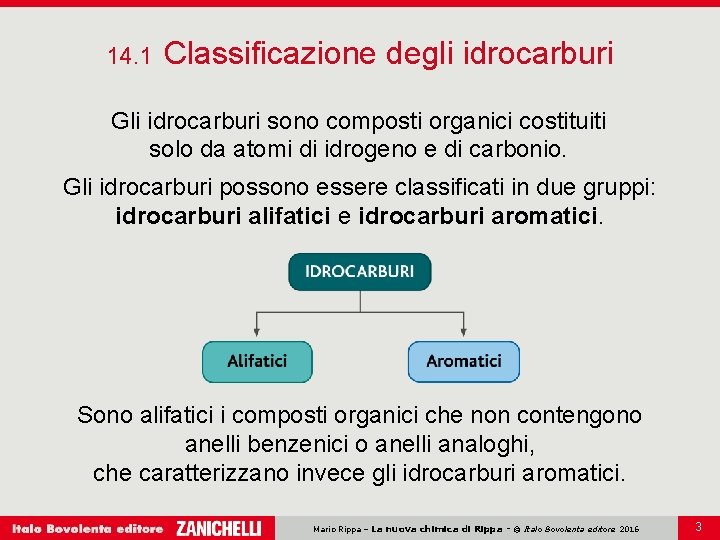
14. 1 Classificazione degli idrocarburi Gli idrocarburi sono composti organici costituiti solo da atomi di idrogeno e di carbonio. Gli idrocarburi possono essere classificati in due gruppi: idrocarburi alifatici e idrocarburi aromatici. Sono alifatici i composti organici che non contengono anelli benzenici o anelli analoghi, che caratterizzano invece gli idrocarburi aromatici. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 3

14. 1 Classificazione degli idrocarburi Gli idrocarburi alifatici sono a loro volta suddivisi in saturi e insaturi. Gli idrocarburi saturi sono gli alcani e i cicloalcani, gli insaturi gli alcheni e gli alchini con i correlati composti ciclici. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 4

14. 2 Alcani Gli alcani sono idrocarburi a catena aperta caratterizzati dalla formula generale Cn. H 2 n + 2 e dall’assenza di doppi o tripli legami. Gli atomi di carbonio degli alcani hanno ibridazione sp 3. Il nome degli alcani si ottiene aggiungendo alla radice il suffisso -ano. La radice del nome si ricava dal numero di atomi di carbonio presenti nella molecola. Un radicale alchilico è un alcano a cui si è tolto un atomo di idrogeno. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 5
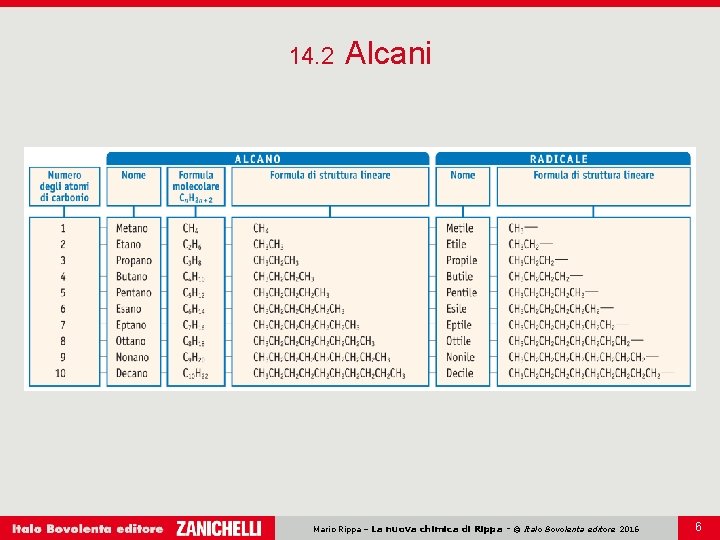
14. 2 Alcani Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 6

14. 2 Alcani Gli alcani non sono solubili in acqua, a temperatura ambiente i primi quattro alcani sono allo stato aeriforme, dal quinto al sedicesimo sono allo stato liquido, dal diciassettesimo in poi sono allo stato solido. Il principale uso degli alcani è la produzione di energia. Le due principali fonti di alcani sono il gas naturale e il petrolio. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 7

14. 3 La reattività degli alcani Gli alcani sono composti molto stabili e quindi poco reattivi. Gli alcani sono interessati da due tipi di reazione: le reazioni di sostituzione dove un atomo di idrogeno viene sostituito da un altro atomo. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 8

14. 3 La reattività degli alcani le reazioni di combustione, che portano alla formazione di acqua e diossido di carbonio: Ad alte temperature possono dare reazioni di eliminazione, come la deidrogenazione: o il cracking: Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 9

14. 4 Cicloalcani I cicloalcani sono alcani in cui la catena carboniosa forma un anello di atomi di carbonio. I cicloalcani hanno formula generale Cn. H 2 n. Nei nomi dei cicloalcani si premette il prefisso cicloal nome dell’alcano corrispondente. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 10
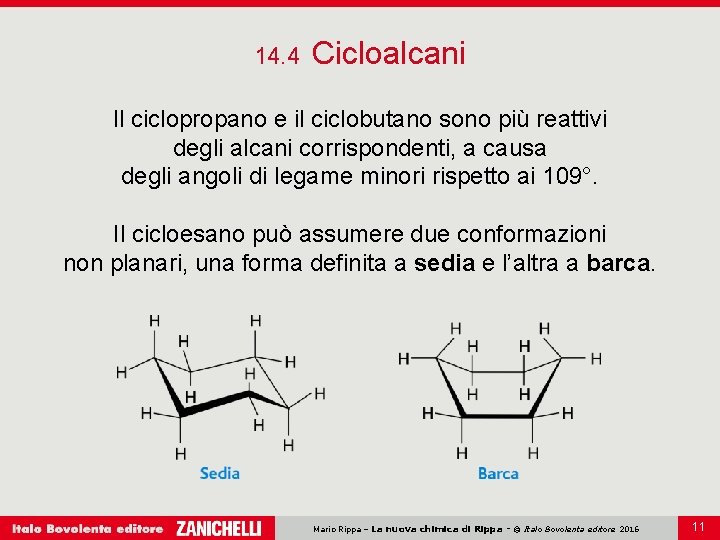
14. 4 Cicloalcani Il ciclopropano e il ciclobutano sono più reattivi degli alcani corrispondenti, a causa degli angoli di legame minori rispetto ai 109°. Il cicloesano può assumere due conformazioni non planari, una forma definita a sedia e l’altra a barca. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 11

14. 4 Cicloalcani Nella forma a sedia gli atomi di idrogeno tendono a disporsi il più possibile lontani gli uni dagli altri. Sei atomi di idrogeno, detti idrogeni equatoriali, sono più o meno sullo stesso piano degli atomi di carbonio. Gli altri sei idrogeni sono sotto o sopra al piano dell’anello e sono chiamati idrogeni assiali. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 12

14. 5 Alcheni Gli alcheni sono idrocarburi insaturi a catena aperta, con formula generale Cn. H 2 n in cui vi è almeno una coppia di atomi di carbonio legati da un doppio legame. Gli atomi di carbonio impegnati nei doppi legami hanno ibridazione sp 2. Il loro nome termina con il suffisso -ene. Se una molecola di alchene contiene due doppi legami, il nome del composto termina col suffisso -diene. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 13
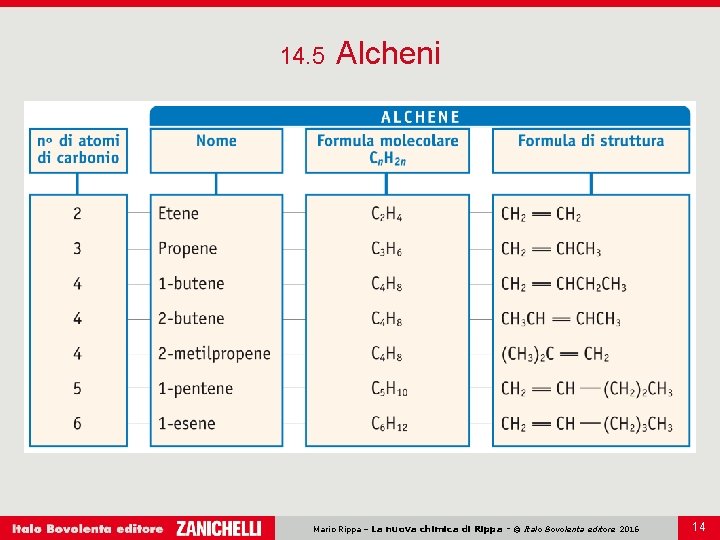
14. 5 Alcheni Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 14

14. 5 Alcheni Negli alcheni, oltre all’isomeria di conformazione e l’isomeria di catena, vi sono l’isomeria di posizione del doppio legame e l’isomeria cis-trans. Se gli atomi diversi dall’idrogeno sono dalla stessa parte del doppio legame si ha l’isomero cis, se sono dalla parte opposta si ha l’isomero trans. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 15

14. 5 Alcheni Gli alcheni, per la presenza del doppio legame, sono molto più reattivi dei corrispondenti alcani. Oltre alla reazione di combustione danno reazione di addizione: Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 16

14. 5 Alcheni e reazioni di polimerizzazione, dove più molecole di alchene si legano tra loro per formare un polimero. I polimeri sono macromolecole formate da unità uguali tra loro, chiamate monomeri. Gli alcheni si ottengono tramite cracking del petrolio o per deidratazione di un alcool: Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 17
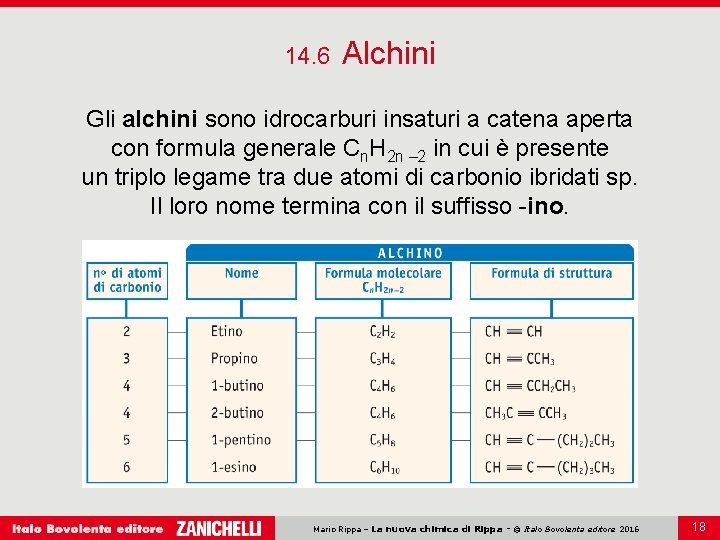
14. 6 Alchini Gli alchini sono idrocarburi insaturi a catena aperta con formula generale Cn. H 2 n – 2 in cui è presente un triplo legame tra due atomi di carbonio ibridati sp. Il loro nome termina con il suffisso -ino. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 18

14. 6 Alchini Gli alchini sono molto reattivi e addizionano idrogeno, alogeni e acidi; con acqua formano le aldeidi: Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 19

14. 7 Idrocarburi aromatici Gli idrocarburi aromatici sono idrocarburi a catena chiusa in cui gli elettroni di legame sono delocalizzati, cioè possono spostarsi tra più atomi. Il benzene è l’idrocarburo aromatico di riferimento la cui formula bruta è C 6 H 6. Nel benzene i sei atomi di carbonio si trovano ai vertici di un esagono regolare. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 20
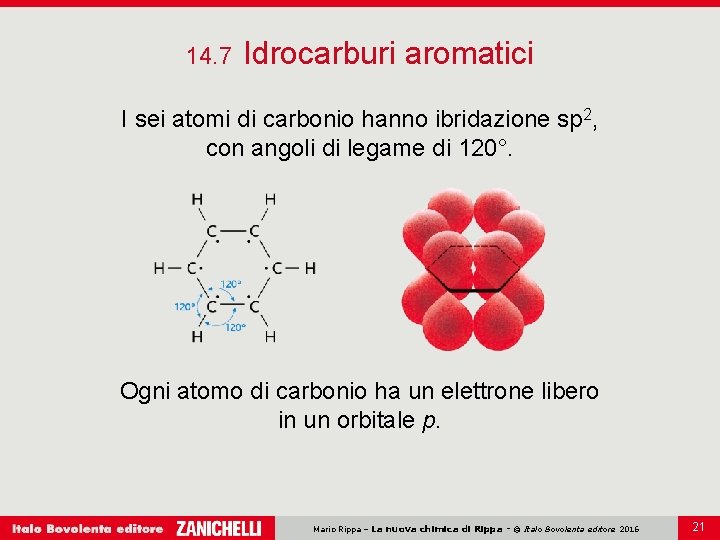
14. 7 Idrocarburi aromatici I sei atomi di carbonio hanno ibridazione sp 2, con angoli di legame di 120°. Ogni atomo di carbonio ha un elettrone libero in un orbitale p. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 21

14. 7 Idrocarburi aromatici I sei orbitali p si fondono per dare un solo orbitale, dove i sei elettroni possono muoversi. La delocalizzazione elettronica si rappresenta con un cerchio inserito nell’anello del benzene. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 22

14. 7 Idrocarburi aromatici I sei atomi di carbonio sono uniti da un legame singolo e da un legame a elettroni delocalizzati. La delocalizzazione rende i composti poco reattivi e molto stabili. La maggior parte delle reazioni del benzene sono reazioni di sostituzione, in cui un atomo di idrogeno è sostituito da altri gruppi. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 23
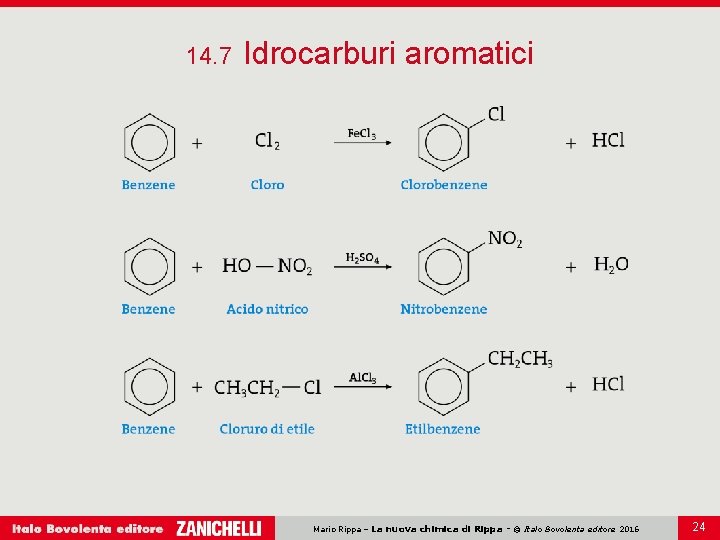
14. 7 Idrocarburi aromatici Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 24
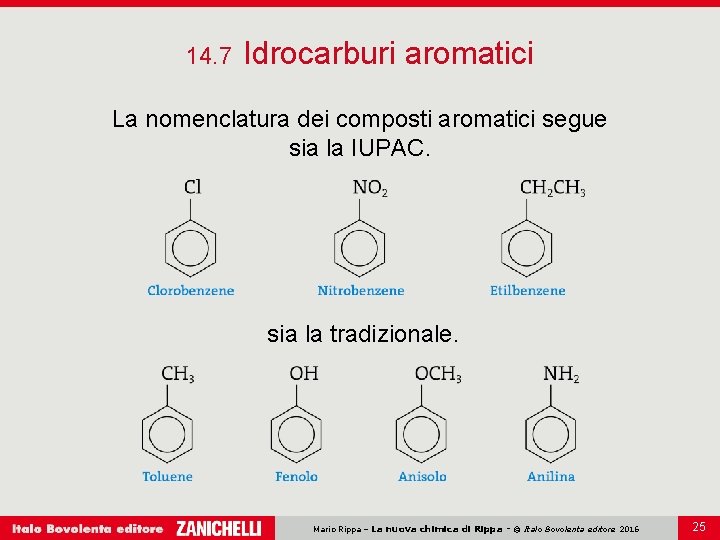
14. 7 Idrocarburi aromatici La nomenclatura dei composti aromatici segue sia la IUPAC. sia la tradizionale. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 25
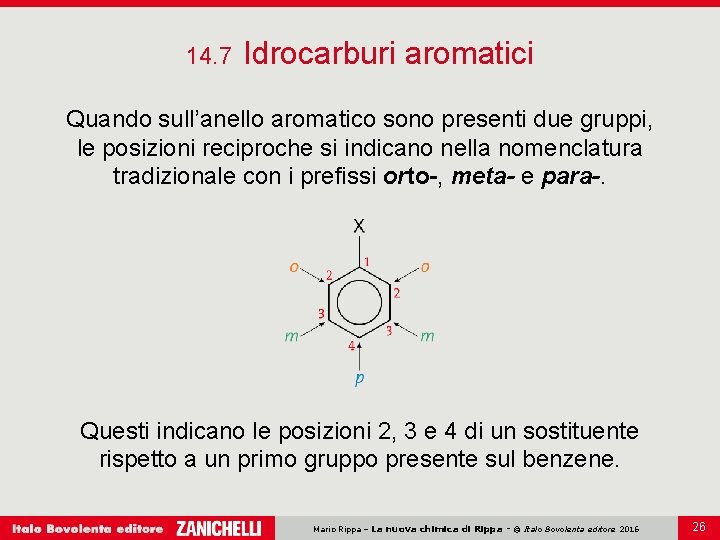
14. 7 Idrocarburi aromatici Quando sull’anello aromatico sono presenti due gruppi, le posizioni reciproche si indicano nella nomenclatura tradizionale con i prefissi orto-, meta- e para-. Questi indicano le posizioni 2, 3 e 4 di un sostituente rispetto a un primo gruppo presente sul benzene. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 26
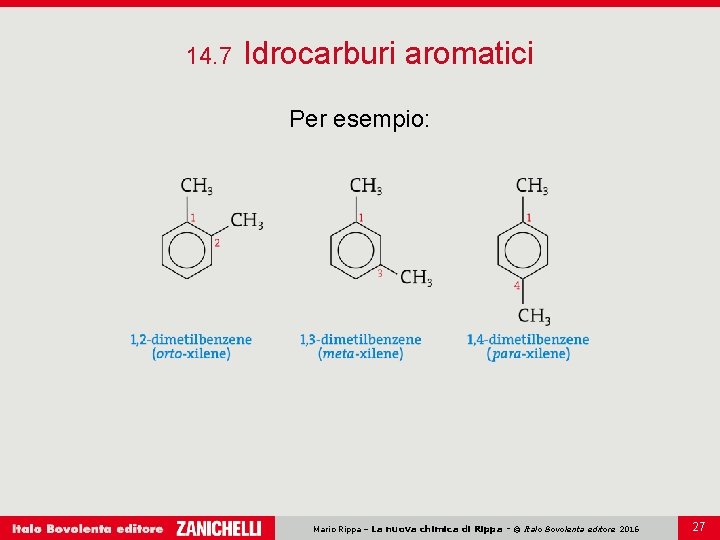
14. 7 Idrocarburi aromatici Per esempio: Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 27

14. 7 Idrocarburi aromatici Come classe di composti, gli idrocarburi aromatici prendono il nome di areni. Negli areni per indicare un generico radicale arilico o gruppo arile si usa il simbolo Ar. Nella nomenclatura IUPAC il gruppo C 6 H 5 —, ottenuto rimuovendo un idrogeno dal benzene, è detto gruppo fenile o fenilico e si indica con Ph. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 28
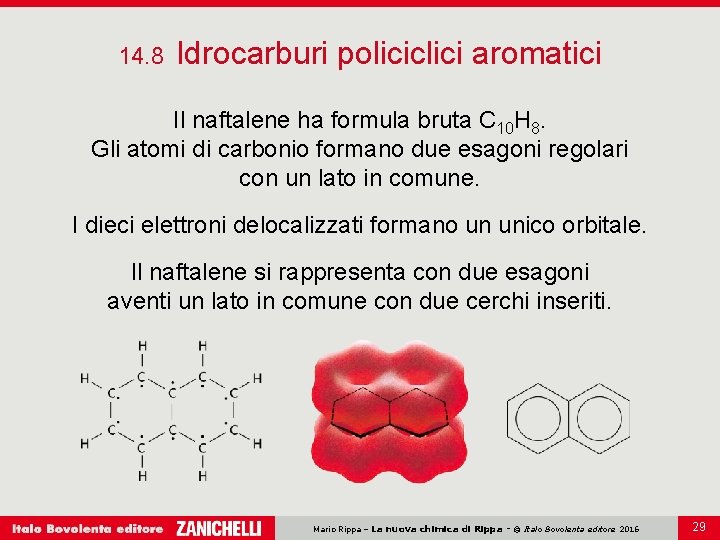
14. 8 Idrocarburi policiclici aromatici Il naftalene ha formula bruta C 10 H 8. Gli atomi di carbonio formano due esagoni regolari con un lato in comune. I dieci elettroni delocalizzati formano un unico orbitale. Il naftalene si rappresenta con due esagoni aventi un lato in comune con due cerchi inseriti. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 29

14. 8 Idrocarburi policiclici aromatici Gli idrocarburi policiclici aromatici (IPA) sono presenti tra i composti naturali. Molti IPA sono tossici e spesso cancerogeni. Gli IPA si formano per combustione in carenza di ossigeno in derivati del petrolio e sono presenti nel fumo delle sigarette. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 30

14. 9 Idrocarburi eterociclici I composti eterociclici sono composti insaturi a catena carboniosa chiusa che contengono nell’anello uno o più atomi diversi dal carbonio, gli eteroatomi. Gli eteroatomi possono essere l’ossigeno, l’azoto e lo zolfo. I composti eterociclici possono essere aromatici o non aromatici e, a seconda che l’anello sia formato da 5 o da 6 atomi, si classificano in pentatomici o esatomici. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 31
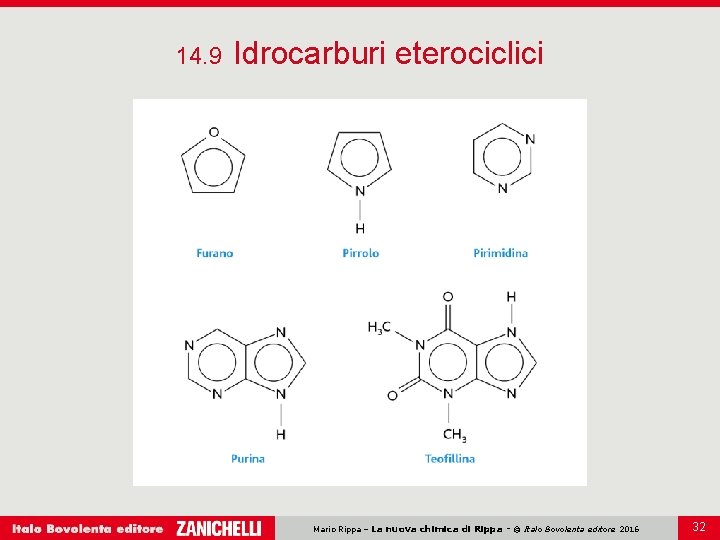
14. 9 Idrocarburi eterociclici Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 32

14. 10 Alcaloidi Gli alcaloidi sono composti eterociclici contenenti uno o più atomi di azoto. Sono sostanze alcaline, da qui il nome. La nicotina, presente nel tabacco, e la caffeina, presente nel caffè, hanno un effetto stimolante sul sistema nervoso centrale. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 33

14. 10 Alcaloidi Molti alcaloidi sono usati come medicinali, come l’atropina e il chinino. Altri, derivati dall’oppio estratto dalle piante di papavero, sono potenti antidolorifici, come la codeina e la morfina. La morfina, modificata chimicamente, produce eroina, una potente droga che crea dipendenza. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 34
- Slides: 34