Idrocarburi saturi Alcani I composti di questa classe
Idrocarburi saturi: Alcani
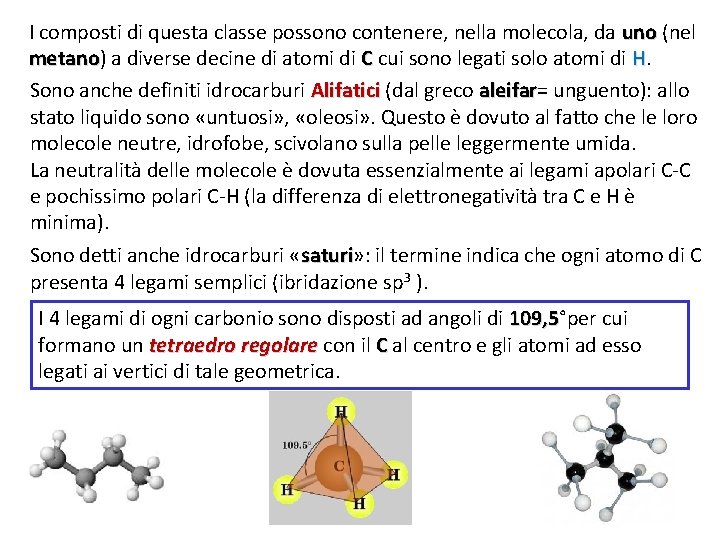
I composti di questa classe possono contenere, nella molecola, da uno (nel metano) metano a diverse decine di atomi di C cui sono legati solo atomi di H. Sono anche definiti idrocarburi Alifatici (dal greco aleifar= aleifar unguento): allo stato liquido sono «untuosi» , «oleosi» . Questo è dovuto al fatto che le loro molecole neutre, idrofobe, scivolano sulla pelle leggermente umida. La neutralità delle molecole è dovuta essenzialmente ai legami apolari C-C e pochissimo polari C-H (la differenza di elettronegatività tra C e H è minima). Sono detti anche idrocarburi «saturi» : saturi il termine indica che ogni atomo di C presenta 4 legami semplici (ibridazione sp 3 ). I 4 legami di ogni carbonio sono disposti ad angoli di 109, 5°per cui 109, 5 formano un tetraedro regolare con il C al centro e gli atomi ad esso legati ai vertici di tale geometrica.
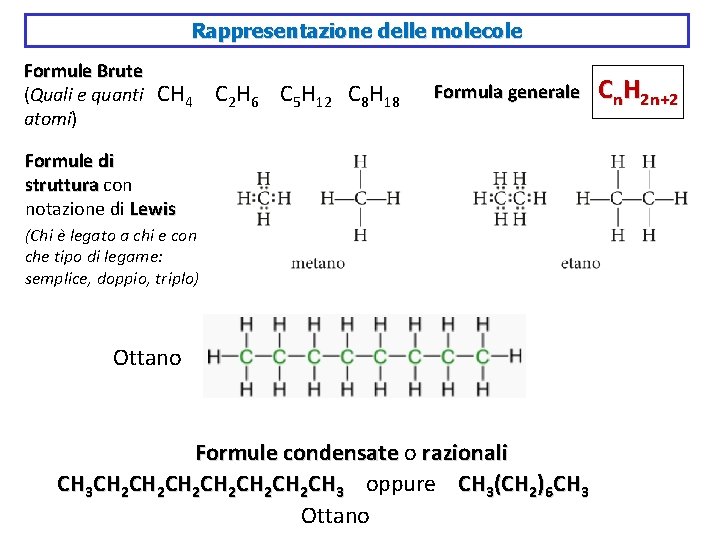
Rappresentazione delle molecole Formule Brute (Quali e quanti atomi) CH 4 C 2 H 6 C 5 H 12 C 8 H 18 Formula generale Formule di struttura con notazione di Lewis (Chi è legato a chi e con che tipo di legame: semplice, doppio, triplo) Ottano Formule condensate o razionali CH 3 CH 2 CH 2 CH 2 CH 3 oppure CH 3(CH 2)6 CH 3 Ottano Cn. H 2 n+2
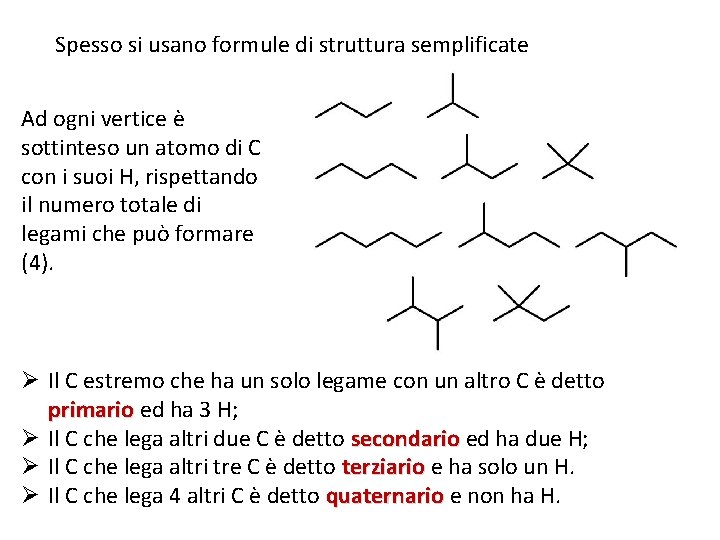
Spesso si usano formule di struttura semplificate Ad ogni vertice è sottinteso un atomo di C con i suoi H, rispettando il numero totale di legami che può formare (4). Ø Il C estremo che ha un solo legame con un altro C è detto primario ed ha 3 H; Ø Il C che lega altri due C è detto secondario ed ha due H; Ø Il C che lega altri tre C è detto terziario e ha solo un H. Ø Il C che lega 4 altri C è detto quaternario e non ha H. 13/11/11
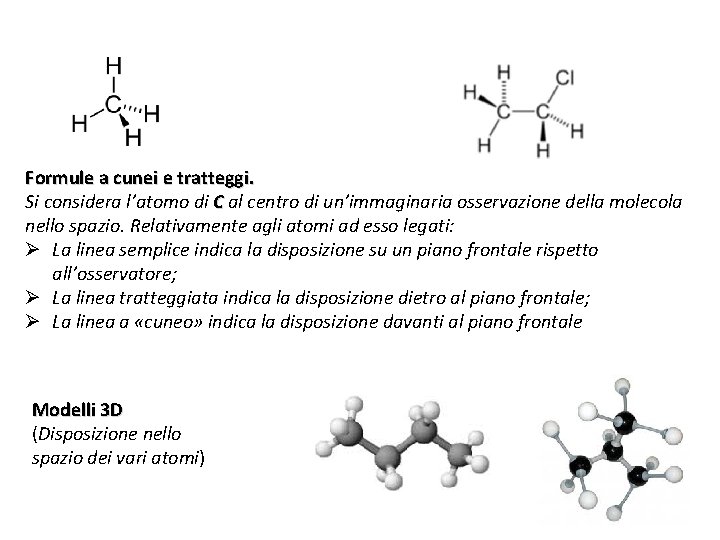
Formule a cunei e tratteggi. Si considera l’atomo di C al centro di un’immaginaria osservazione della molecola nello spazio. Relativamente agli atomi ad esso legati: Ø La linea semplice indica la disposizione su un piano frontale rispetto all’osservatore; Ø La linea tratteggiata indica la disposizione dietro al piano frontale; Ø La linea a «cuneo» indica la disposizione davanti al piano frontale Modelli 3 D (Disposizione nello spazio dei vari atomi)
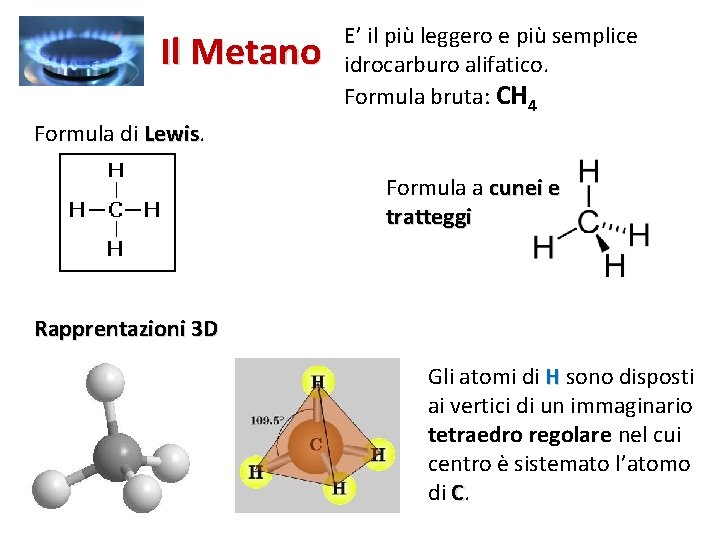
Il Metano E’ il più leggero e più semplice idrocarburo alifatico. Formula bruta: CH 4 Formula di Lewis Formula a cunei e tratteggi Rapprentazioni 3 D Gli atomi di H sono disposti ai vertici di un immaginario tetraedro regolare nel cui centro è sistemato l’atomo di C.
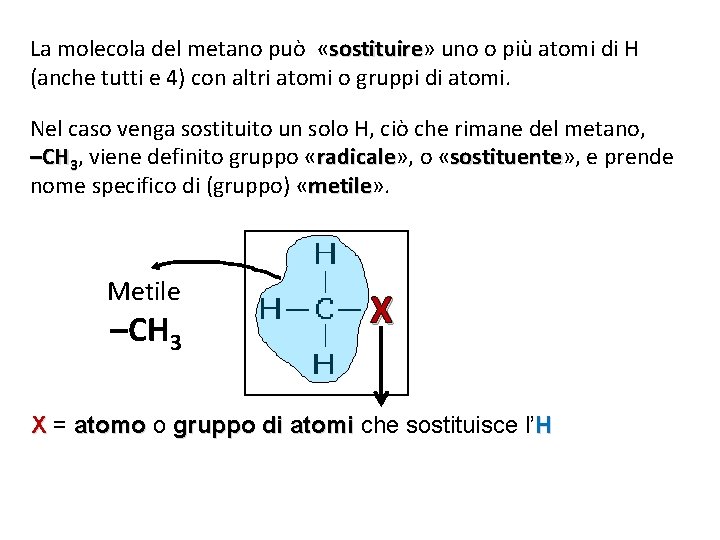
La molecola del metano può «sostituire» sostituire uno o più atomi di H (anche tutti e 4) con altri atomi o gruppi di atomi. Nel caso venga sostituito un solo H, ciò che rimane del metano, –CH 3, viene definito gruppo «radicale» , radicale o «sostituente» , sostituente e prende nome specifico di (gruppo) «metile» . metile Metile –CH 3 X X = atomo o gruppo di atomi che sostituisce l’H
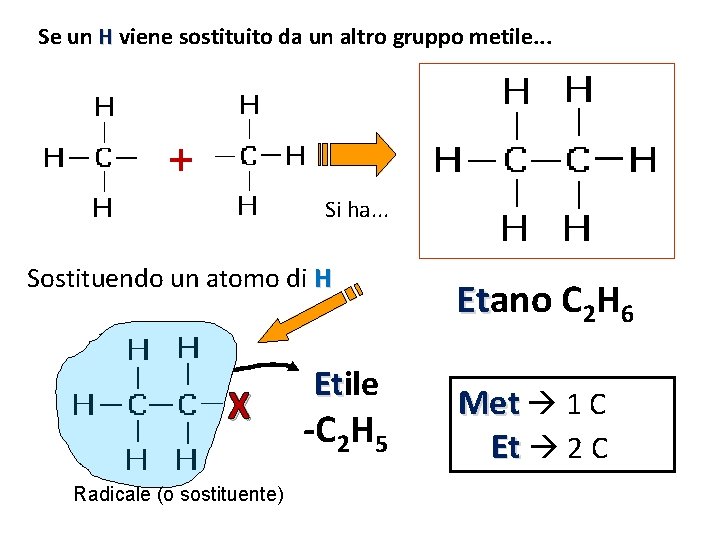
Se un H viene sostituito da un altro gruppo metile. . . + Si ha. . . Sostituendo un atomo di H X Radicale (o sostituente) Etile Et -C 2 H 5 Etano C 2 H 6 Et Met 1 C Et 2 C
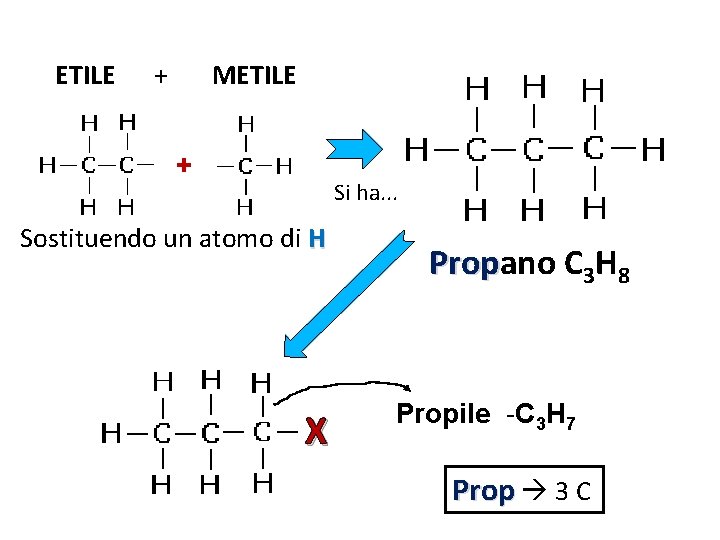
ETILE + METILE + Si ha. . . Sostituendo un atomo di H X Propano C 3 H 8 Propile -C 3 H 7 Prop 3 C
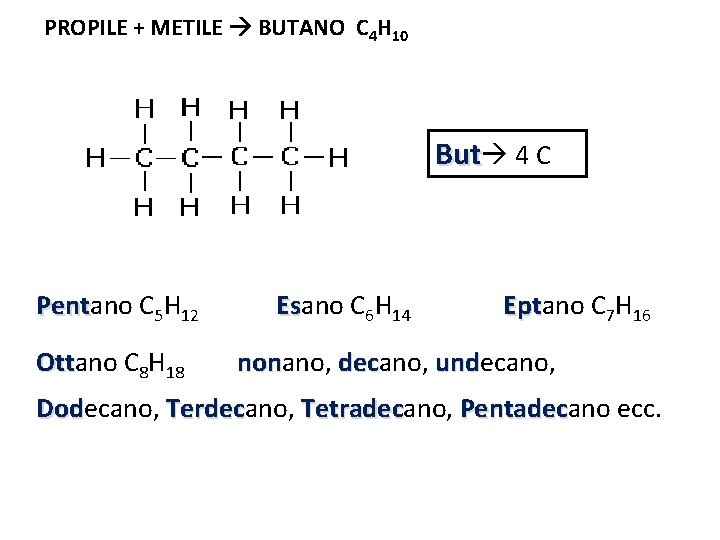
PROPILE + METILE BUTANO C 4 H 10 But 4 C Pentano C 5 H 12 Pent Ottano C 8 H 18 Ott Esano C 6 H 14 Es Eptano C 7 H 16 Ept nonano, decano, undecano, non dec und Dodecano, Terdecano, Tetradecano, Pentadecano ecc. Dod Terdec Tetradec Pentadec
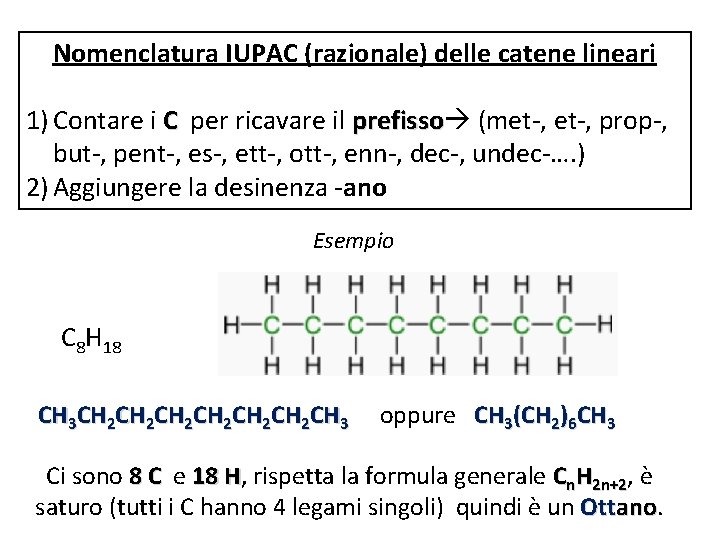
Nomenclatura IUPAC (razionale) delle catene lineari 1) Contare i C per ricavare il prefisso (met-, prop-, but-, pent-, es-, ett-, ott-, enn-, dec-, undec-…. ) 2) Aggiungere la desinenza -ano Esempio C 8 H 18 CH 3 CH 2 CH 2 CH 2 CH 3 oppure CH 3(CH 2)6 CH 3 Ci sono 8 C e 18 H, H rispetta la formula generale Cn. H 2 n+2, è saturo (tutti i C hanno 4 legami singoli) quindi è un Ottano. ano
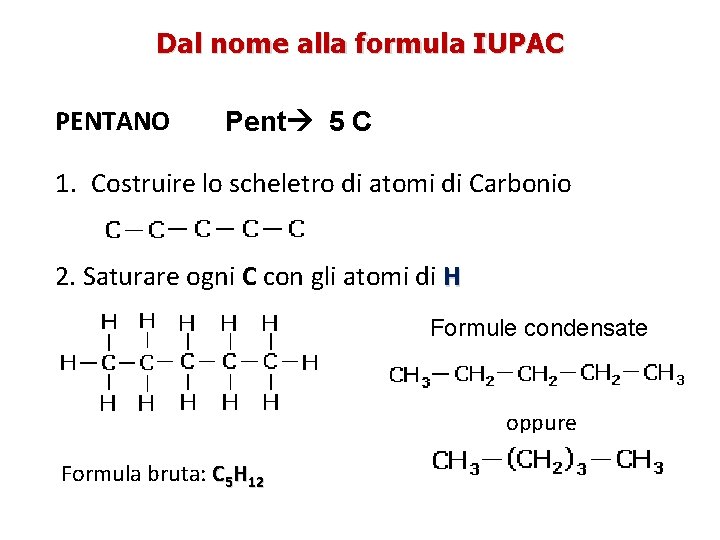
Dal nome alla formula IUPAC PENTANO Pent 5 C 1. Costruire lo scheletro di atomi di Carbonio 2. Saturare ogni C con gli atomi di H Formule condensate oppure Formula bruta: C 5 H 12
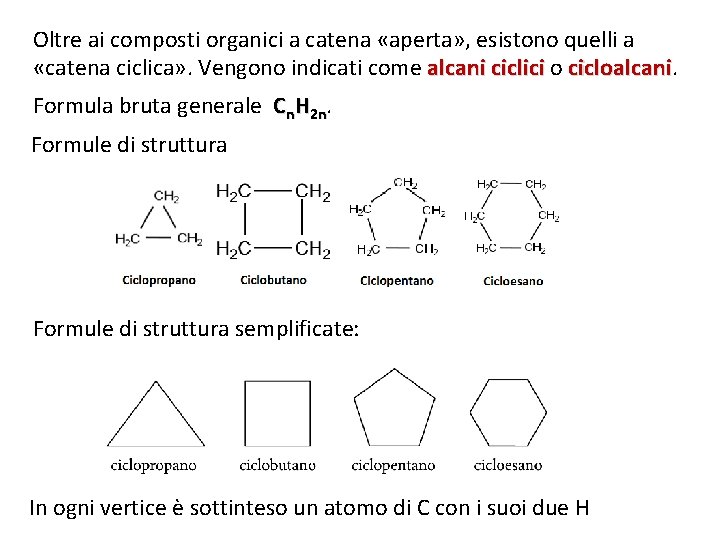
Oltre ai composti organici a catena «aperta» , esistono quelli a «catena ciclica» . Vengono indicati come alcani ciclici o cicloalcani Formula bruta generale Cn. H 2 n. Formule di struttura semplificate: In 13/11/11 ogni vertice è sottinteso un atomo di C con i suoi due H

Alcune puntualizzazioni Ø Dato che la differenza tra i vari alcani consiste sostanzialmente nel numero di gruppi -CH 2, si dice che gli alcani costituiscono una serie omologa di composti. Ø A volte gli alcani sono anche indicati con il termine paraffine (poco affine): indica la proprietà di essere refrattari alle reazioni chimiche. Ø Il gruppo di atomi ottenuto privando di un H la molecola di un alcano si definisce genericamente gruppo alchililco o radicale alchilico o, semplicemente, alchile (metile, propile, butile ecc. ). Ø I radicali alchilici non costituiscono molecole, ma solo parti di esse. Tuttavia è possibile che, in seguito a reazioni chimiche o ad esposizione a fonti energetiche particolari (radiazioni), alcuni di essi si stacchino dalla molecola formando «radicali liberi» liberi estremamente reattivi.
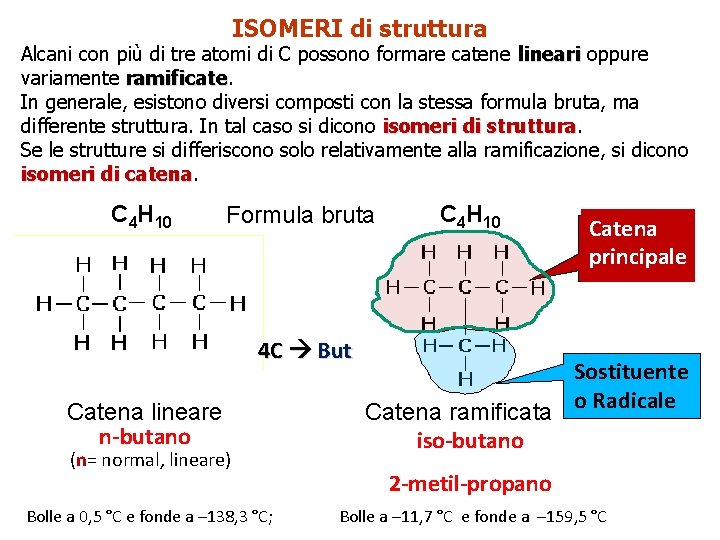
ISOMERI di struttura Alcani con più di tre atomi di C possono formare catene lineari oppure variamente ramificate In generale, esistono diversi composti con la stessa formula bruta, ma differente struttura. In tal caso si dicono isomeri di struttura Se le strutture si differiscono solo relativamente alla ramificazione, si dicono isomeri di catena C 4 H 10 Formula bruta 4 C But Catena lineare n-butano (n= normal, lineare) Bolle a 0, 5 °C e fonde a – 138, 3 °C; C 4 H 10 Catena principale Sostituente Catena ramificata o Radicale iso-butano 2 -metil-propano Bolle a – 11, 7 °C e fonde a – 159, 5 °C
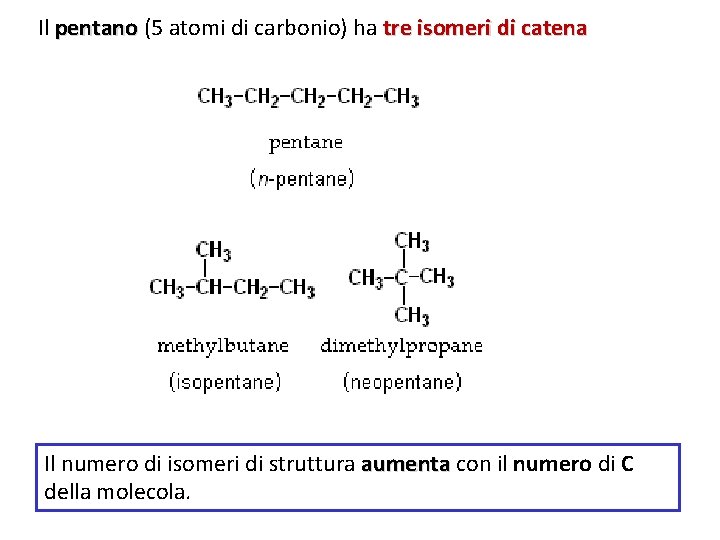
Il pentano (5 atomi di carbonio) ha tre isomeri di catena Il numero di isomeri di struttura aumenta con il numero di C della molecola.

Se le strutture si differenziano solo per la posizione di uno o più radicali (sostituenti) si definiscono isomeri di posizione C 6 H 14
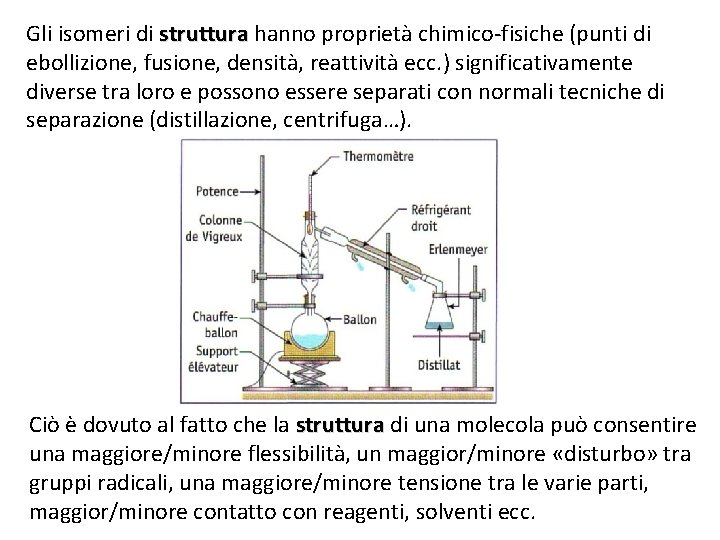
Gli isomeri di struttura hanno proprietà chimico-fisiche (punti di ebollizione, fusione, densità, reattività ecc. ) significativamente diverse tra loro e possono essere separati con normali tecniche di separazione (distillazione, centrifuga…). Ciò è dovuto al fatto che la struttura di una molecola può consentire una maggiore/minore flessibilità, un maggior/minore «disturbo» tra gruppi radicali, una maggiore/minore tensione tra le varie parti, maggior/minore contatto con reagenti, solventi ecc.

Nomenclatura IUPAC per gli isomeri di struttura e di posizione 13/11/11
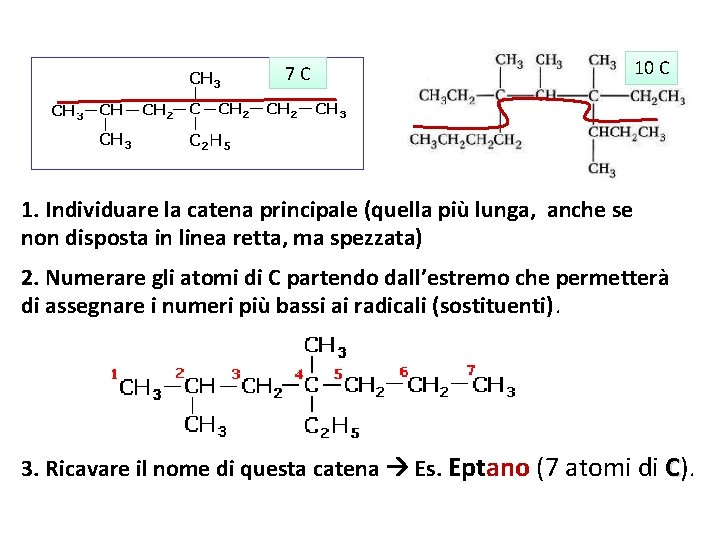
7 C 10 C 1. Individuare la catena principale (quella più lunga, anche se non disposta in linea retta, ma spezzata) 2. Numerare gli atomi di C partendo dall’estremo che permetterà di assegnare i numeri più bassi ai radicali (sostituenti). 3. Ricavare il nome di questa catena Es. Eptano (7 atomi di C).
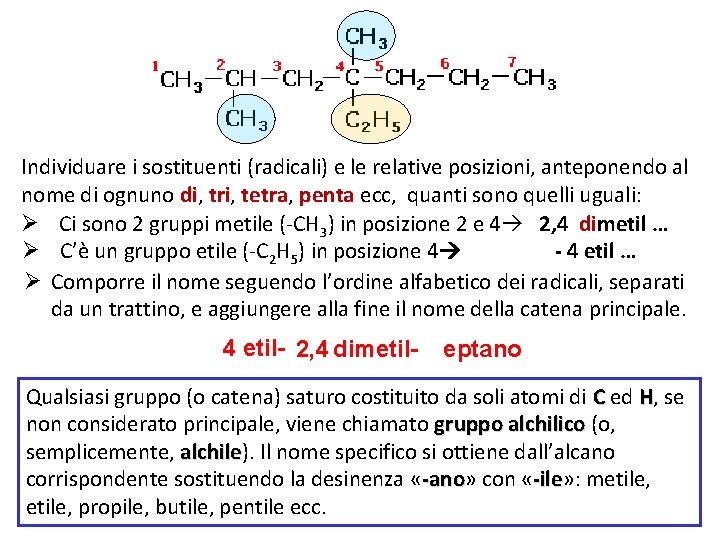
Individuare i sostituenti (radicali) e le relative posizioni, anteponendo al nome di ognuno di, tri, tetra, penta ecc, quanti sono quelli uguali: Ø Ci sono 2 gruppi metile (-CH 3) in posizione 2 e 4 2, 4 dimetil … Ø C’è un gruppo etile (-C 2 H 5) in posizione 4 - 4 etil … Ø Comporre il nome seguendo l’ordine alfabetico dei radicali, separati da un trattino, e aggiungere alla fine il nome della catena principale. 4 etil- 2, 4 dimetil- eptano Qualsiasi gruppo (o catena) saturo costituito da soli atomi di C ed H, se non considerato principale, viene chiamato gruppo alchilico (o, semplicemente, alchile). alchile Il nome specifico si ottiene dall’alcano corrispondente sostituendo la desinenza «-ano» -ano con «-ile» : -ile metile, propile, butile, pentile ecc.
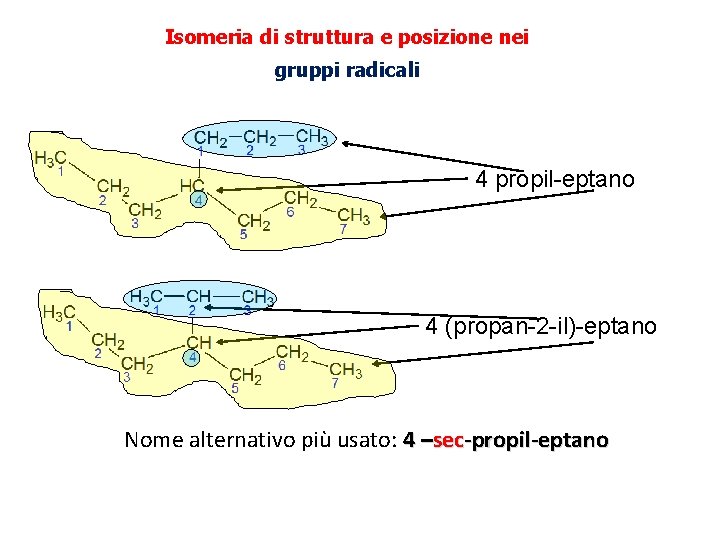
Isomeria di struttura e posizione nei gruppi radicali 4 propil-eptano 4 (propan-2 -il)-eptano Nome alternativo più usato: 4 –sec-propil-eptano

Nomenclatura in caso di isomeria dei radicali X X Entrambi questi radicali sono propili, propili ma le sostanze non hanno lo stesso comportamento chimico-fisico. 1. Il primo viene indicato come propile primario, primario o npropile 2. Il secondo viene indicato come propile secondario (abbreviato: sec-propile) sec-propile o iso-propile Butile primario (n-butile) X Butile secondario (sec-butile) X X Butile terziario (terz-butile) Regola generale: Se il carbonio legato alla catena principale (X) è legato 1. Ad un altro solo C n 2. Ad altri 2 C sec 3. Ad altri 3 C terz.

Alcani: Proprietà chimiche Gli alcani sono considerati poco reattivi, in quanto posseggono solo legami covalenti forti (carbonio-carbonio e carbonio-idrogeno). In condizioni normali, infatti, non danno alcuna reazione: né con acidi, né con basi, né con agenti ossidanti (ossigeno, clorati, cloriti, permanganati, nitrati ecc. ) Per tale ragione gli idrocarburi, soprattutto quelli pesanti (a catene più lunghe), vengono anche indicati con il nome di paraffine (dal latino parum affinis poco affine alle reazioni) Le reazioni tipiche degli idrocarburi saturi sono, comunque: • La combustione (ossidazione) ossidazione • La sostituzione (in particolare alogenazione) alogenazione

Reazione di combustione (ossidazione) In particolari condizioni (scintilla o fuoco) sono soggetti a reazione di Combustione : CH 4 + 2 O 2 → CO 2 + 2 H 2 O La combustione a H 2 O e CO 2 (CO in caso di carenza di ossigeno, come negli ambienti chiusi) è una proprietà caratteristica di tutti i composti organici; viene spesso usata proprio per la determinazione del contenuto di C e H in una sostanza organica. l'ossidazione per combustione dei composti organici è fortemente esotermica La combustione del metano, ad esempio, ha un potere calorifero di circa 50 MJ/Kg contro i 33 MJ/Kg del carbone e i 17 MJ/Kg di legna secca e zucchero. Per la loro forte esotermia e buona velocità di reazione, gli alcani di peso molecolare leggeromedio, sono usati come carburanti (le benzine sono miscele di alcani da C 6 H 14 a C 12 H 26 )

Reazione di alogenazione (sostituzione) In presenza di luce o alte temperature (250 -400°C) gli alcani reagiscono con gli alogeni (Cl 2, F 2, Br 2, I 2) e i loro acidi, producendo gli alogeno-derivati mono, di, tri, tetrasostituiti (1, 2, 3, 4 idrogeni H sostituiti con atomi dello stesso o di diversi alogeni) Dalla reazione del metano con il cloro, cloro ad esempio, si ottiene una miscela di cloruro di metile, metile dicloruro di metile, metile tricloruro di metile e tetracloruro di carbonio (cloroformio). cloroformio CH 4 + Cl 2 CH 3 Cl + HCl cloruro di metile o cloro metano CH Cl 3 + Cl 2 CCl 4 + HCl Tetracloro metano (Cloroformio) Prodotti analoghi si ottengono con i vari alcani e con altri alogeni (gli HFC idrofluorocarburi o, in combinazione mista, i CFC clorofluorocarburi). Per gli idrocarburi in genere, più sono le sostituzioni, maggiore è la loro stabilità. Sono usati, o stati usati, come solventi, solventi smacchianti (Es. Trielina C 2 HCl 3), propellenti (spray), refrigeranti (macchine frigorifere), insetticidi (Es. DDT).

Alcani: Fonti industriali Il Petrolio : (dal latino petrus–roccia e oleum–olio), –olio detto anche oro nero, è un liquido infiammabile, denso, di colore marrone scuro o verdognolo, che si trova in alcuni punti negli strati superiori della crosta terrestre. È composto da una mistura di vari idrocarburi, idrocarburi in prevalenza alcani Gas naturale : Il gas naturale è un gas prodotto dalla decomposizione anaerobica di materiale organico (archea o archibatteri) Solitamente si trova insieme al petrolio e in giacimenti di gas naturale, naturale ma si genera anche in paludi (in questo caso viene chiamato anche gas di palude), in discariche, discariche e durante la digestione negli animali E’ costituito principalmente da metano. Viene utilizzato come combustibile e carburante Gas di petrolio liquefatti (GPL) : Contiene idrocarburi gassosi più pesanti del gas naturale, come etano (C 2 H 6), propano (C 3 H 8) e butano (C 4 H 10), e altri gas, in varie quantità. Viene usato come alternativa meno inquinante ad altri carburanti per automobili
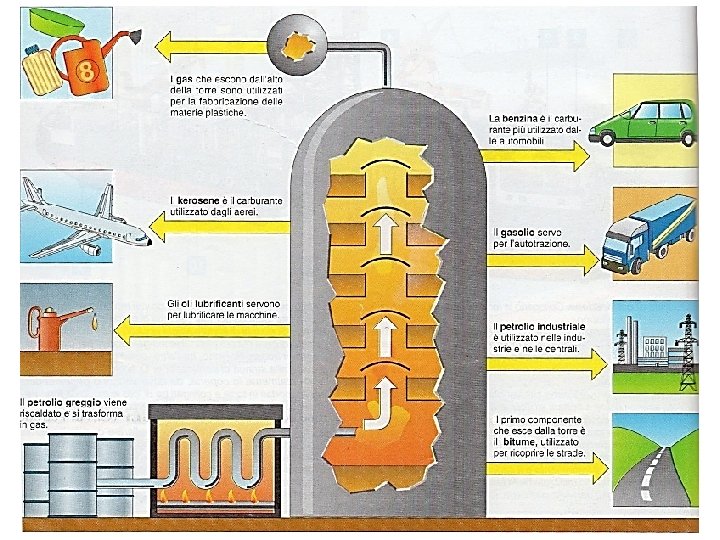
13/11/11

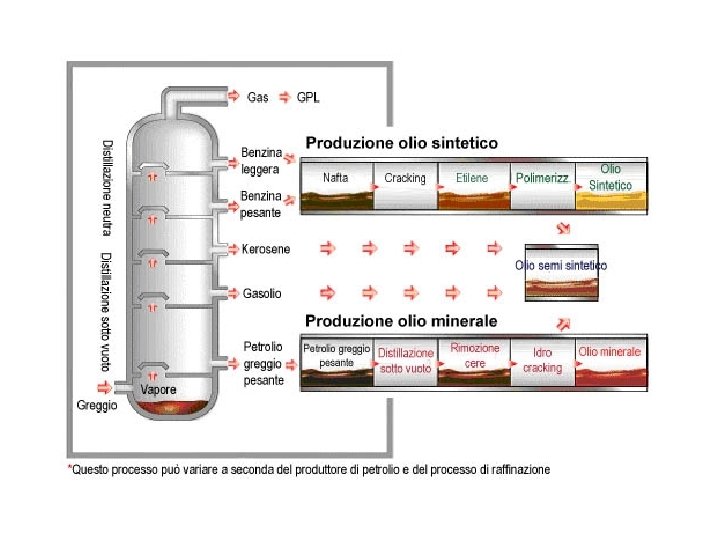
Prodotti della distillazione Dalla distillazione del greggio si ottengono varie frazioni: I primi 4 sono gassosi a t° ambiente, il loro uso è esclusivamente combustibili e carburanti o asfalti Pentano ed esano sono liquidi a t° amb. ; vengono usati, per lo più, come solventi (per grassi, colle) e smacchianti (es. n-esano). Dall’eptano all’undecano, all’undecano liquidi, liquidi in miscela (di vari isomeri) costituiscono le benzine Importantissimi sono gli isoottani per il loro maggior potere antidetonante. Miscela di alcani in prevalenza con 12 -15 atomi di C costituiscono il Kerosene, Kerosene Miscela di alcani in prevalenza con 13 -20 atomi di C costituiscono il Gasolio, Gasolio Miscele di alcani in prevalenza con n° di C Tra i 20 e i 30 costituiscono le paraffine, paraffine Per la loro insolubilità in acqua e la resistenza agli agenti chimici, trova impiego nella fabbricazione di imballaggi impermeabili, di cere per pavimenti e per mobili, di cosmetici, ecc. , oltre che nella fabbricazione dei cerini, nell'industria tessile e in farmacia. Miscele di alcani con maggior n° di atomi di C, C insieme a vari altri composti, per le loro proprietà collanti e impermeabili formano i catrami o bitumi o asfalti
Alcani: Raffinazione Una quota della distillazione viene ulteriormente elaborata tramite: Isomerizzazione. Attraverso uso di opportuni catalizzatori (Al. Br 3 o Al. Cl 3 ecc. ) i composti lineari vengo trasformati in isomeri ramificati (es. isoottani). Cracking. Ad altissime temperature, in assenza di ossigeno, lunghe catene vengono «frammentate» frammentate in molecole più piccole, più ramificate. Si ottengono anche molecole insature (con doppi legami). Alchilazione. Ad alte temperature, in presenza di opportuni catalizzatori, piccole molecole vengono legate insieme per formare catene più lunghe e ramificate. Reforming catalitico. Ad alte temperature e pressioni, gli alcani vengono fatti passare su un catalizzatore di platino facendo ottenere composti pregiati come idrocarburi aromatici (benzene, toluene) o benzine ad alto numero di isottani.
13/11/11
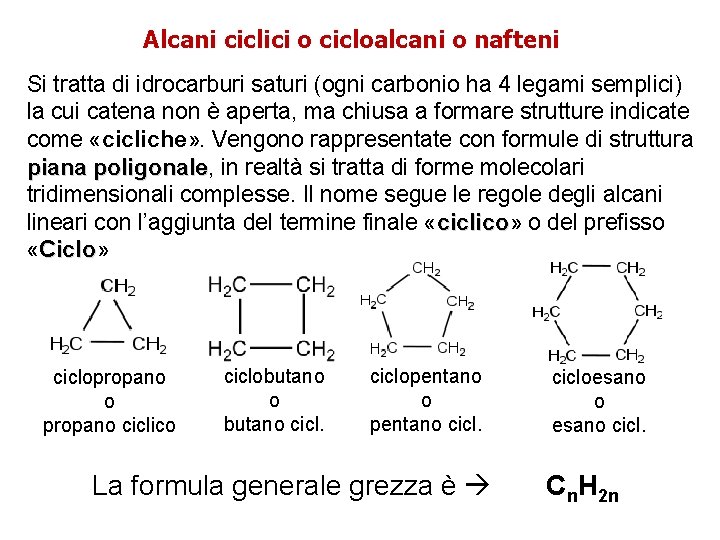
Alcani ciclici o cicloalcani o nafteni Si tratta di idrocarburi saturi (ogni carbonio ha 4 legami semplici) la cui catena non è aperta, ma chiusa a formare strutture indicate come «cicliche» . Vengono rappresentate con formule di struttura piana poligonale, poligonale in realtà si tratta di forme molecolari tridimensionali complesse. Il nome segue le regole degli alcani lineari con l’aggiunta del termine finale «ciclico» ciclico o del prefisso «Ciclo» Ciclo ciclopropano o propano ciclico ciclobutano o butano ciclopentano o pentano cicl. La formula generale grezza è cicloesano o esano cicl. Cn. H 2 n
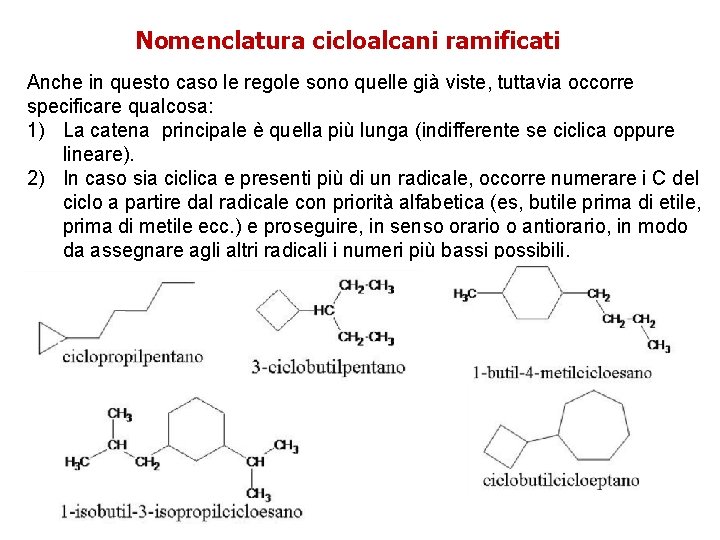
Nomenclatura cicloalcani ramificati Anche in questo caso le regole sono quelle già viste, tuttavia occorre specificare qualcosa: 1) La catena principale è quella più lunga (indifferente se ciclica oppure lineare). 2) In caso sia ciclica e presenti più di un radicale, occorre numerare i C del ciclo a partire dal radicale con priorità alfabetica (es, butile prima di etile, prima di metile ecc. ) e proseguire, in senso orario o antiorario, in modo da assegnare agli altri radicali i numeri più bassi possibili.

Cicloalcani: Caratteristiche, Produzione e Usi Hanno caratteristiche simili agli alcani, ma sono mediamente più reattivi. In particolare i cicloalcani con meno di 6 atomi di C hanno angoli di legame tra i C inferiori a 109, 5°. Questo crea una certa tensione che facilita la rottura del ciclo stesso. Il ciclopropano, ciclopropano infatti, è stato utilizzato come base per esplosivi. Dal cicloesano in poi, gli angoli di legami sono abbastanza ampi per cui la tensione dovuta all’anello è minima, se non trascurabile: le caratteristiche, come gli usi, sono comuni a quelli degli alcani lineari. Attualmente il cicloesano viene utilizzato anche come base per la produzione del nylon. I cicloalcani si ritrovano insieme agli alcani, soprattutto negli olii combustibili, combustibili ma possono essere sintetizzati per addizione di H al benzene e altri composti aromatici. Oltre che combustibili e carburanti (sono presenti in quantità ridotte nelle benzine e nel gas naturale), possono essere usati come solventi e smacchianti. Alcuni di essi, un tempo, erano usati come refrigeranti (n-ciclopentano)
- Slides: 35