Termodinmica Tema 9 segunda parte Limitaciones de la

















- Slides: 24

Termodinámica Tema 9 (segunda parte)

Limitaciones de la 1 ra. ley de la termodinámica Procesos espontáneos o irreversibles • Una cascada corre cuesta abajo • Un terrón de azúcar se disuelve en una taza de café • El agua se congela a 1 atm, por debajo de 0 °C y el hielo se funde por encima de 0 °C • El calor fluye de un objeto más caliente a un objeto más frío • Un gas se expande en una bombilla al vacío • El hierro expuesto al oxígeno y al agua forma herrumbre espontáneo no espontáneo 9. 1

Procesos espontáneos 9. 2

¿Una disminución en la entalpía significa que una reacción procede espontáneamente? Reacciones espontáneas CH 4 (g) + 2 O 2 (g) CO 2 (g) + 2 H 2 O (l) H 0 = -890. 4 k. J H+ (ac) + OH- (ac) H 2 O (l) H 0 = -56. 2 k. J H 2 O (s) NH 4 NO 3 (s) H 2 O (l) H 0 = 6. 01 k. J H 2 O NH 4+(ac) + NO 3 - (ac) H 0 = 25 k. J 9. 3

Entropía (S) → función de estado La entropía se relaciona con el desorden Segunda ley de la termodinámica La entropía del universo aumenta en un proceso espontáneo y permanece inalterada en un proceso en equilibrio Proceso espontáneo o irreversible Proceso en equilibrio o reversible Suniverso = Ssistema + Sambiente > 0 Suniverso = Ssistema + Sambiente = 0 Proceso que NO se produce Suniverso < 0 9. 4

La entropía (S) es una medida del desorden o aleatoriedad de un sistema S = k. B ln (desorden) S desorden ≈ donde: k. B = constante de Boltzman desorden número de microestados o estados microscópicos S = k. B ln monóxido de carbono CO > > S > desorden 9. 5

Variación de la entropía ( S) S = Sf - Si Cuando el estado final es más desordenado que el estado inicial, se cumple: Sf > S i S > 0 Para cualquier sustancia, el estado sólido es más ordenado que el estado líquido y el estado líquido es más ordenado que el estado gaseoso líquido Ssólido< Slíquido<< Sgas H 2 O (s) H 2 O (l) S > 0 H 2 O (l) H 2 O (s) S < 0 sólido 9. 6

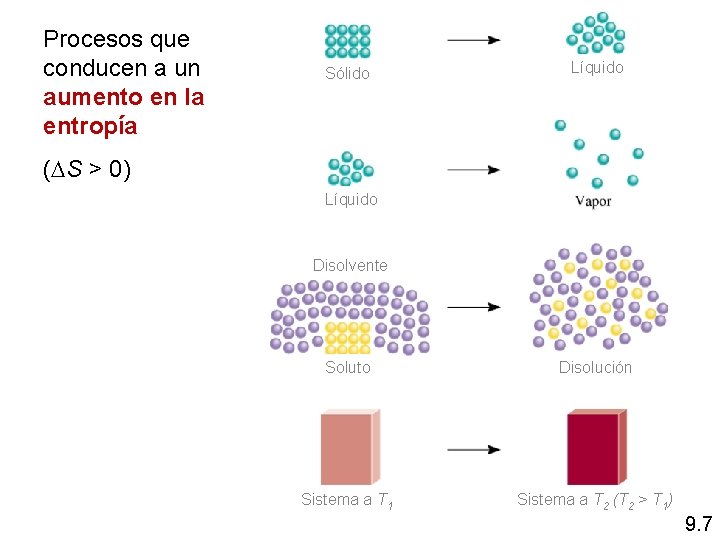
Procesos que conducen a un aumento en la entropía Sólido Líquido ( S > 0) Líquido Disolvente Soluto Disolución Sistema a T 1 Sistema a T 2 (T 2 > T 1) 9. 7

¿Cómo cambia la entropía del sistema para cada uno de los procesos siguientes? (a) condensación de vapor de agua el desorden disminuye la entropía disminuye ( S → < 0) (b) formación de cristales de sacarosa de una disolución sobresaturada el desorden disminuye → la entropía disminuye ( S < 0) (c) calentamiento de hidrógeno gaseoso desde 600 C a 800 C el desorden aumenta → la entropía aumenta ( S > 0) (d) sublimación del hielo seco el desorden aumenta → la entropía aumenta ( S > 0) 9. 8

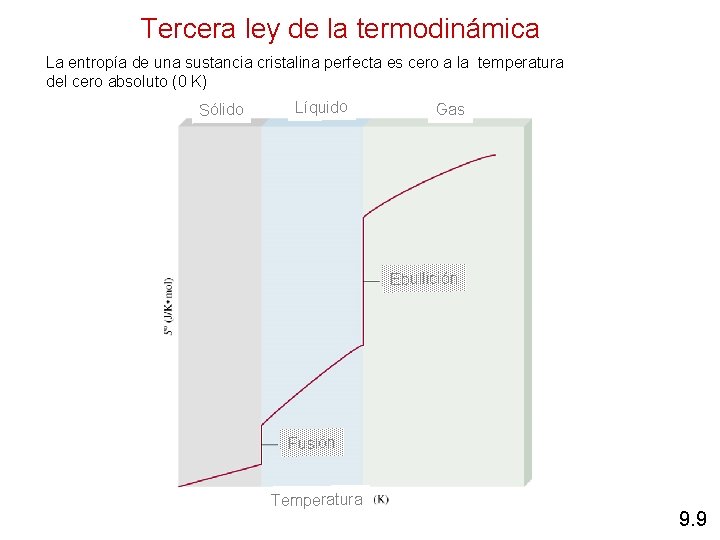
Tercera ley de la termodinámica La entropía de una sustancia cristalina perfecta es cero a la temperatura del cero absoluto (0 K) Sólido Líquido Gas Ebullición Fusión Temperatura 9. 9

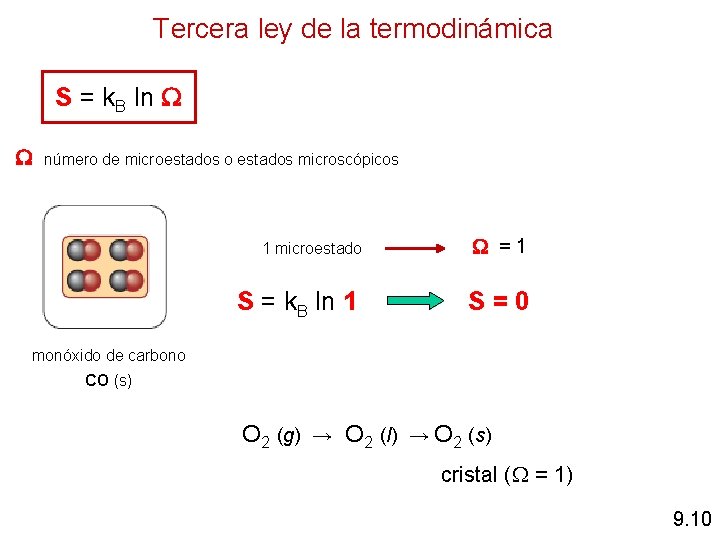
Tercera ley de la termodinámica S = k. B ln número de microestados o estados microscópicos 1 microestado S = k. B ln 1 =1 S=0 monóxido de carbono CO (s) O 2 (g) → O 2 (l) → O 2 (s) cristal ( = 1) 9. 10

Tercera ley de la termodinámica S = Sf - Si cuando Si = 0 S = Sf se denomina entropía absoluta es un valor verdadero y no un valor obtenido utilizando alguna referencia arbitraria La tercera ley de la termodinámica permite determinar la entropía absoluta de las sustancias 9. 11

Variación de la entropía en una reacción química ( S 0 R) La entropía estándar de una reacción ( S 0 R) es el cambio de la entropía para una reacción a 1 atm de presión S 0 R = S n S 0 (productos) - S n S 0 (reactivos) a. A + b. B c. C + d. D S 0 R = [c. S 0(C) + d. S 0(D) ] - [ a. S 0(A) + b. S 0(B)] ¿Cuál es el cambio en la entropía estándar en la siguiente reacción a 250 C? 2 CO (g) + O 2 (g) S 0(CO) = 197. 9 J/K • mol 2 CO 2 (g) S 0(CO 2) = 213. 6 J/K • mol S 0(O 2) = 205. 0 J/K • mol S 0 R = 2 x S 0(CO 2) – [2 x S 0(CO) + S 0 (O 2)] S 0 R = 427. 2 – [395. 8 + 205. 0] = -173. 6 J/K • mol 9. 12

Signo de S 0 R en una reacción química Cuando los gases son producidos (o consumidos) • Si una reacción produce más moléculas de gas que las que consume → S 0 > 0 • Si el número total de moléculas de gas disminuye → S 0 < 0 • Si no hay cambio neto en el número total de moléculas de gas , entonces S 0 puede ser positivo o negativo PERO será un número pequeño ¿Cuál es el signo de la variación de entropía para la reacción siguiente? 2 Zn (s) + O 2 (g) 2 Zn. O (s) El número total de moléculas de gas disminuye → S es negativo 9. 13

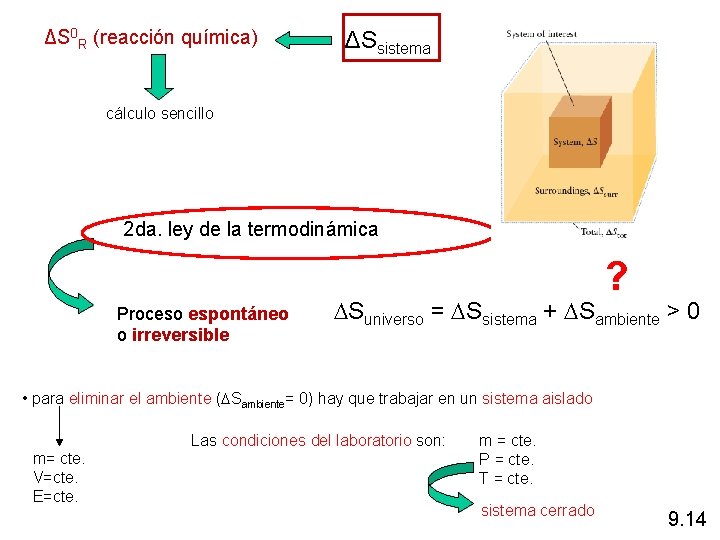
ΔS 0 R (reacción química) ΔSsistema cálculo sencillo 2 da. ley de la termodinámica ? Proceso espontáneo o irreversible Suniverso = Ssistema + Sambiente > 0 • para eliminar el ambiente ( Sambiente= 0) hay que trabajar en un sistema aislado Las condiciones del laboratorio son: m= cte. V=cte. E=cte. m = cte. P = cte. T = cte. sistema cerrado 9. 14

Energía libre de Gibbs (G) → función de estado La energía libre de Gibbs permite predecir la espontaneidad de una reacción química en base a propiedades exclusivamente del sistema (sin tener en cuenta el ambiente) y nos permite trabajar en las condiciones del laboratorio G = H–TS def. G = H – (TS) G = H – T S - S T cuando T = cte. Josiah Willard Gibbs (1839– 1903) G = H – T S para un proceso a temperatura constante 9. 15

Energía libre de Gibbs Para una reacción a T = constante G = H – T S Criterio de espontaneidad G < 0 la reacción es espontánea de reactivos a productos R → P G > 0 la reacción es espontánea de productos a reactivos P → R G = 0 la reacción está en equilibrio R P 9. 16

Cálculo de la variación de la energía libre estándar (ΔG 0) La energía libre estándar de reacción ( G 0 R ) es el cambio de energía libre para una reacción a 1 atm de presión G 0 R = S n ΔG 0 f (productos) - S n ΔG 0 f (reactivos) donde: G 0 f es la energía libre estándar de formación La energía libre estándar de formación (ΔG 0 f) representa la variación de energía libre estándar puesta en juego cuando se forma un mol de sustancia a partir de sus elementos en su estado más estable a una presión de 1 atm y a una temperatura dada La energía libre estándar de formación ( G 0 f) de los elementos en su forma más estable por convención es cero (a cualquier temperatura) Ejemplos: G 0 f (O 2, gas) = 0 G 0 f (C, grafito) = 0 9. 17

¿Cuál es la variación de la energía libre estándar (DG 0 R) para la siguiente reacción a 25 0 C? 2 C 6 H 6 (l) + 15 O 2 (g) 12 CO 2 (g) + 6 H 2 O (l) G 0 R = S n ΔG 0 f (productos) - S n ΔG 0 f (reactivos) G 0 R = [12 G 0 f (CO 2) + 6 G 0 f (H 2 O)] - [ 2 G 0 f (C 6 H 6)] G 0 R = [ 12 x– 394. 4 + 6 x– 237. 2 ] – [ 2 x 124. 5 ] = -6405 k. J ¿Es la reacción espontánea a 25 0 C? G 0 = -6405 k. J < 0 SI es espontánea 9. 18

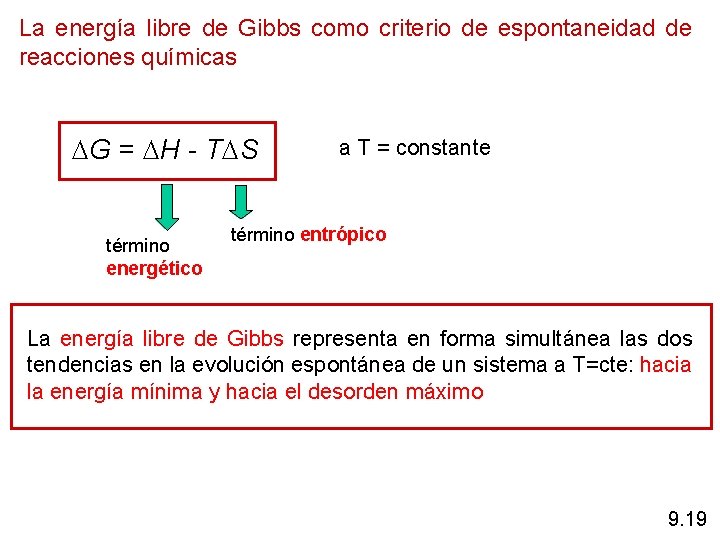
La energía libre de Gibbs como criterio de espontaneidad de reacciones químicas G = H - T S término energético a T = constante término entrópico La energía libre de Gibbs representa en forma simultánea las dos tendencias en la evolución espontánea de un sistema a T=cte: hacia la energía mínima y hacia el desorden máximo 9. 19

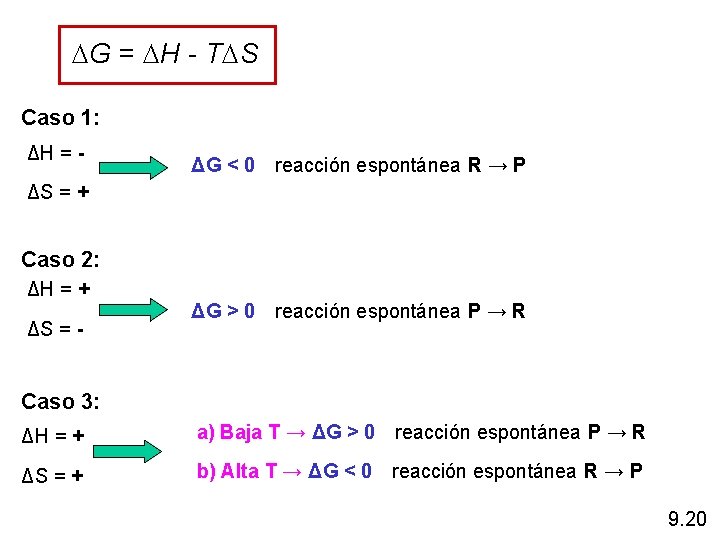
G = H - T S Caso 1: ΔH = - ΔG < 0 reacción espontánea R → P ΔG > 0 reacción espontánea P → R ΔS = + Caso 2: ΔH = + ΔS = - Caso 3: ΔH = + a) Baja T → ΔG > 0 reacción espontánea P → R ΔS = + b) Alta T → ΔG < 0 reacción espontánea R → P 9. 20

Qué es una temperatura baja o alta? Temperatura de equilibrio Teq G = H - T S En el equilibrio se cumple: ΔG = 0 Teq = H / S 0 = H - T S Por ejemplo Teq= 500 K bajas T significa T < 500 K altas temperaturas indica T > 500 K T=500 K indica reacción en equilibrio Caso 4: ΔH = - a) Baja T → ΔG < 0 reacción espontánea R → P ΔS = - b) Alta T → ΔG > 0 reacción espontánea P → R 9. 21

9. 22

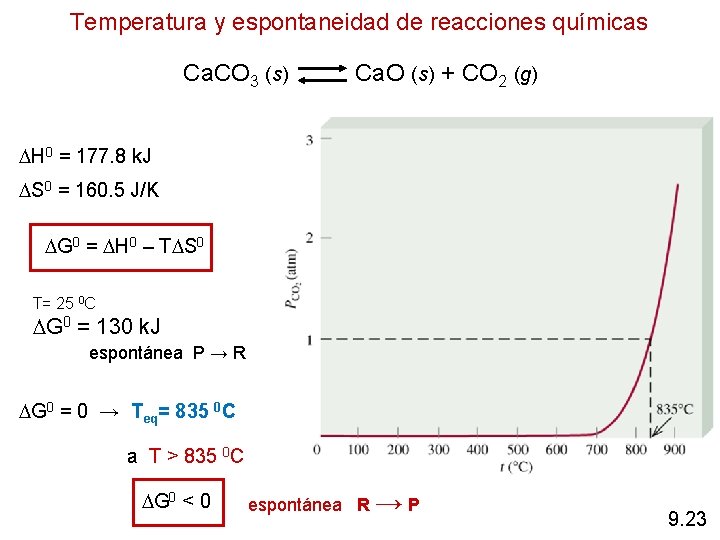
Temperatura y espontaneidad de reacciones químicas Ca. CO 3 (s) Ca. O (s) + CO 2 (g) H 0 = 177. 8 k. J S 0 = 160. 5 J/K G 0 = H 0 – T S 0 T= 25 0 C G 0 = 130 k. J espontánea P → R G 0 = 0 → Teq= 835 0 C a T > 835 0 C G 0 < 0 espontánea R → P 9. 23