CLASE 7 ESTRUCTURAS DE LEWIS Y LA REGLA


![En la formación de compuestos IONICOS Li + F Li+ + [ F ]- En la formación de compuestos IONICOS Li + F Li+ + [ F ]-](https://slidetodoc.com/presentation_image_h/be60b53287e4623062e1ce18f61f5bbc/image-4.jpg)





- Slides: 13

CLASE 7

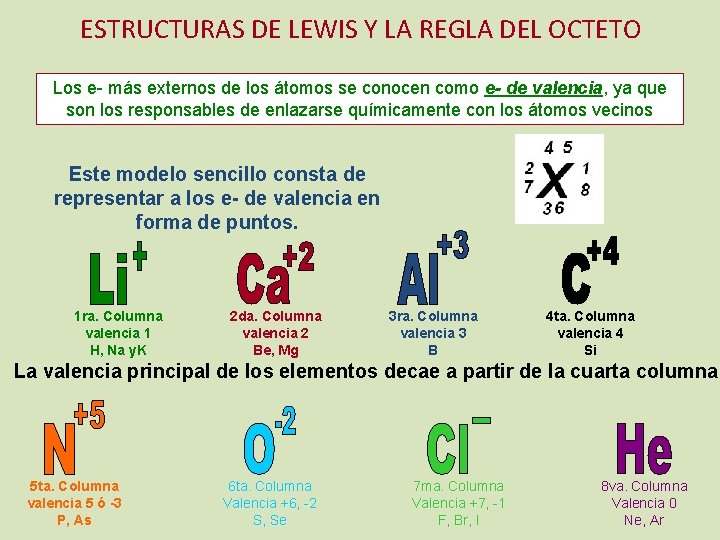
ESTRUCTURAS DE LEWIS Y LA REGLA DEL OCTETO Los e- más externos de los átomos se conocen como e- de valencia, ya que son los responsables de enlazarse químicamente con los átomos vecinos Este modelo sencillo consta de representar a los e- de valencia en forma de puntos. 1 ra. Columna valencia 1 H, Na y. K 2 da. Columna valencia 2 Be, Mg 3 ra. Columna valencia 3 B 4 ta. Columna valencia 4 Si La valencia principal de los elementos decae a partir de la cuarta columna 5 ta. Columna valencia 5 ó -3 P, As 6 ta. Columna Valencia +6, -2 S, Se 7 ma. Columna Valencia +7, -1 F, Br, I 8 va. Columna Valencia 0 Ne, Ar

¿Por qué la valencia decae a partir de la 4 ta columna? La estructura de Lewis consta de: Kernel: representado por el símbolo del elemento. Contiene tanto al núcleo como a los e- internos Puntos: representan a los e- de valencia, que se colocan alrededor del símbolo. El # de puntos ó e- de valencia coincide con la columna en la que se encuentra el elemento en la tabla periodica. Este modelo propone que al combinarse los átomos, tienden a terminar con el mismo número de e- de valencia que los gases nobles (8 e-) y a esto se le conoce como la “regla del octeto”
![En la formación de compuestos IONICOS Li F Li F En la formación de compuestos IONICOS Li + F Li+ + [ F ]-](https://slidetodoc.com/presentation_image_h/be60b53287e4623062e1ce18f61f5bbc/image-4.jpg)
En la formación de compuestos IONICOS Li + F Li+ + [ F ]- Li+ [ F ]- El e- del Li se transfiere al F quedando el kernel del Li cargado positivamente y el F con su octeto completo También para representar enlaces COVALENTES H + H H H Los 2 e- están asociados o compartidos entre ambos núcleos. En este caso, cada átomo de H tiene el mismo # de e- que el helio, por lo que se cumple la regla de Lewis. Cuando 2 átomos de F se aproximan, los eno apareados son compartidos por los 2 núcleos y se forma un enlace covalente formando la molécula F 2. Ambos átomos tienen 8 e- de valencia y se cumple la regla del octeto. F + F F F Escribir con estructuras de Lewis la reacción de formación del Fluoruro de magnesio

ACTIVIDAD 1. - Escribe las estructuras de Lewis de los siguientes elementos a partir de su posición en la tabla periódica: a) b) c) d) e) f) Bromo Xenón Fósforo Rubidio Aluminio Calcio 2. - Utiliza estructuras de puntos para representar la reacción de formación de los siguientes compuestos iónicos, con sus fórmulas correctas: a) Floruro de rubidio b) Cloruro de aluminio c) Bromuro de calcio

Para escribir las estructuras de puntos de un compuesto más complicado, se pueden seguir las siguientes reglas: • Observa el tipo y # de átomos del compuesto a partir de su fórmula química. • Determina el # de e- de valencia que tiene c/átomo utilizando su posición en la tabla periódica y también conoces el # total de e- de valencia que vas a utilizar para construir la estructura de puntos. • Dibuja 1 propuesta de esqueleto para el compuesto. Une los átomos entre sí con líneas rectas, puede resultar dificil, pero puedes asumir que en moléculas sencillas que tienen 1 átomo de 1 elemento y varios átomos de otro, el átomo único está en el centro. • Coloca los puntos alrededor de los átomos, de tal manera que c/1 tenga 8 e- ( para cumplir con la regla del octeto). El H es una excepción, tan solo tiene 2 e-. • Verifica que el # total de e- de valencia esté plasmado en tu estructura. Si no es el caso, posiblemente se trate de 1 compuesto que no satisface la regla del octeto. Ejemplo: Molécula Tipo y # de E- de valencia átomos de c/átomo # total de ede valencia Estructura del esqueleto CHCl 3 C =1 x 4 = 4 H=1 x 1=1 Cl= 3 x 7 = 21 TOTAL = 26 H H Cl Cl Cl C=1 H=1 Cl =3 C=4 H=1 Cl =7 Arreglo de los puntos Porque crees que se decidió colocar al C como átomo central y no al H?

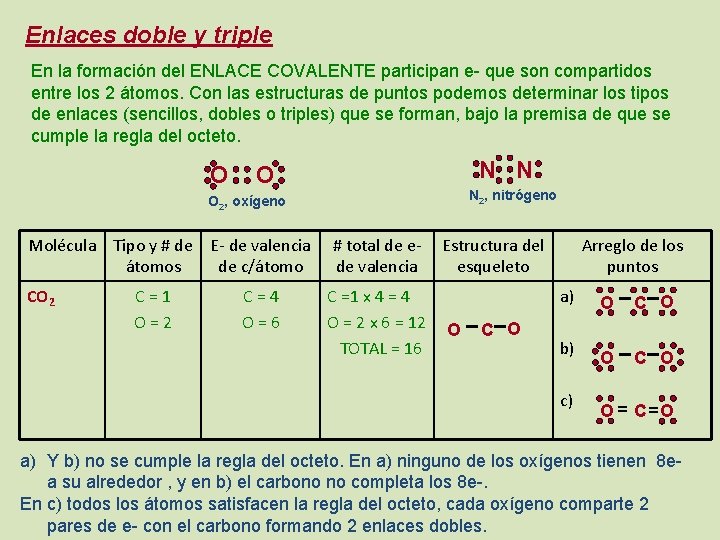
Enlaces doble y triple En la formación del ENLACE COVALENTE participan e- que son compartidos entre los 2 átomos. Con las estructuras de puntos podemos determinar los tipos de enlaces (sencillos, dobles o triples) que se forman, bajo la premisa de que se cumple la regla del octeto. O N N O N 2, nitrógeno O 2, oxígeno Molécula Tipo y # de E- de valencia átomos de c/átomo # total de ede valencia CO 2 C =1 x 4 = 4 O = 2 x 6 = 12 TOTAL = 16 C=1 O=2 C=4 O=6 Estructura del esqueleto Arreglo de los puntos a) O C O b) c) O C O O = C=O a) Y b) no se cumple la regla del octeto. En a) ninguno de los oxígenos tienen 8 ea su alrededor , y en b) el carbono no completa los 8 e-. En c) todos los átomos satisfacen la regla del octeto, cada oxígeno comparte 2 pares de e- con el carbono formando 2 enlaces dobles.

Los enlaces se representan por líneas rectas, un enlace sencillo con 1 línea, uno doble con 2 líneas y uno triple con 3 líneas. Estas fórmulas se conocen como fórmulas desarrolladas 1 enlace covalente en el que se comparte 1 par de e- es un enlace sencillo, si se comparten 2 pares de ees un enlace doble y si se comparten 3 pares de e- es un enlace triple.

Distancia de enlace En los enlaces triples hay mas e- compartidos que en los dobles, y en éstos que en los sencillos, la distancia que separa los 2 núcleos es diferente en cada caso. Enlace N-N N=N N N C-C C=C C C O-O O=O Distancia (A) 1. 45 1. 23 1. 09 1. 54 1. 34 1. 20 1. 48 1. 21 Los enlaces SENCILLOS son más largos que los DOBLES y éstos que los TRIPLES. actividad

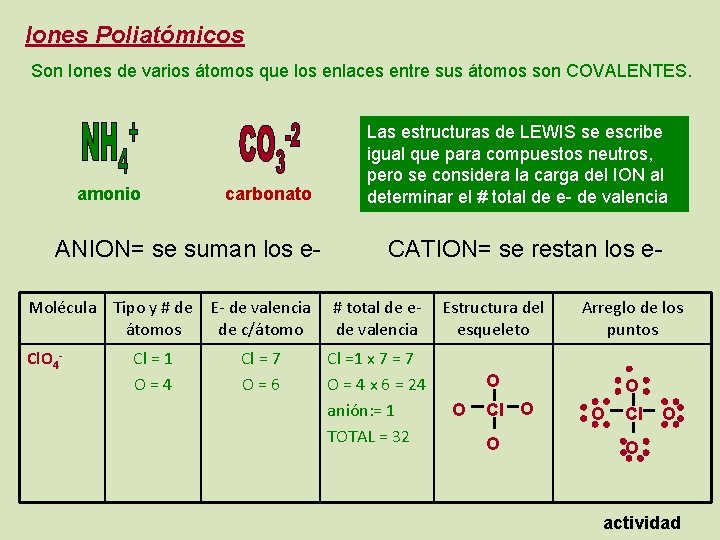
Iones Poliatómicos Son Iones de varios átomos que los enlaces entre sus átomos son COVALENTES. amonio carbonato ANION= se suman los e- Las estructuras de LEWIS se escribe igual que para compuestos neutros, pero se considera la carga del ION al determinar el # total de e- de valencia CATION= se restan los e- Molécula Tipo y # de E- de valencia átomos de c/átomo # total de ede valencia Cl. O 4 - Cl =1 x 7 = 7 O = 4 x 6 = 24 anión: = 1 TOTAL = 32 Cl = 1 O=4 Cl = 7 O=6 Estructura del esqueleto Arreglo de los puntos O O O Cl O O actividad

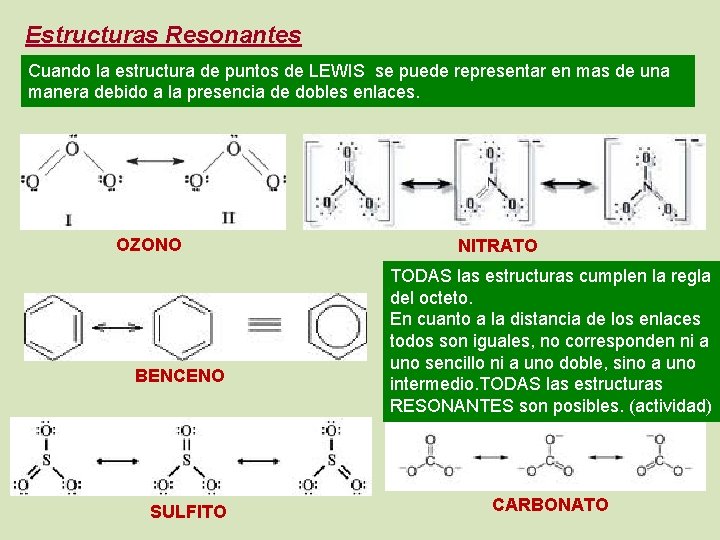
Estructuras Resonantes Cuando la estructura de puntos de LEWIS se puede representar en mas de una manera debido a la presencia de dobles enlaces. OZONO BENCENO SULFITO NITRATO TODAS las estructuras cumplen la regla del octeto. En cuanto a la distancia de los enlaces todos son iguales, no corresponden ni a uno sencillo ni a uno doble, sino a uno intermedio. TODAS las estructuras RESONANTES son posibles. (actividad) CARBONATO

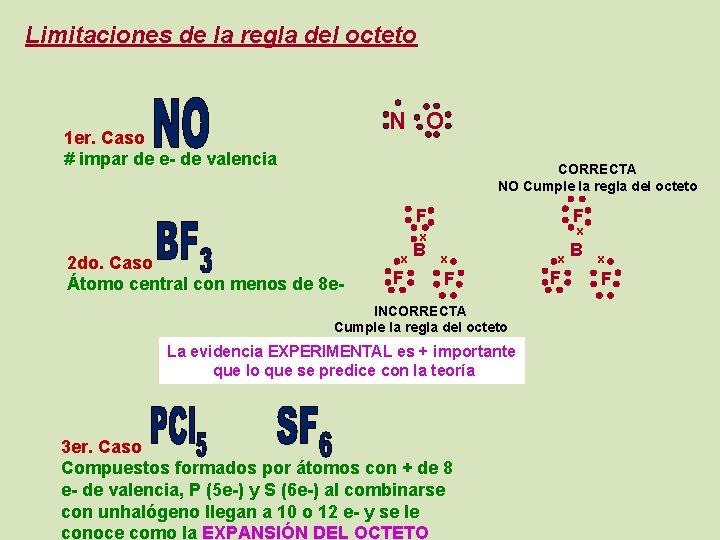
Limitaciones de la regla del octeto N O 1 er. Caso # impar de e- de valencia CORRECTA NO Cumple la regla del octeto F F x x 2 do. Caso Átomo central con menos de 8 e- x F B x F INCORRECTA Cumple la regla del octeto La evidencia EXPERIMENTAL es + importante que lo que se predice con la teoría 3 er. Caso Compuestos formados por átomos con + de 8 e- de valencia, P (5 e-) y S (6 e-) al combinarse con unhalógeno llegan a 10 o 12 e- y se le conoce como la EXPANSIÓN DEL OCTETO x F B x F

TAREA 1. -Escribe las estructuras de puntos de los siguientes compuestos: a) HCN b) H 2 O c)CHCl 3 d)CO e) SO 4 -2 2. - Escribe las estructuras de puntos de los siguiente compuestos y explica porque no cumplen con la regla del octeto. a) Be. Cl 2 b)NO 2 c)SF 4 3. - Escribe con estructura de puntos una estructura resonante.