Szerkezetvizsglati mdszerek a biofizikban 2020 tavaszi flv Czirk

Szerkezetvizsgálati módszerek a biofizikában 2020 tavaszi félév Czirók András, Szabó Bálint Elérhetőség: 3. 146 -os szoba, balintszabo 1@gmail. com

Félévi tematika I. (Szabó Bálint) 1. Optikai spektroszkópia. Kétsugaras abszorpciós spektrofotométer, fluoreszcens spektroszkópia, ultragyors lézerspektroszkópia, cirkuláris dikroizmus (CD) spektroszkópia, Förster típusú energiatranszfer (FRET) spektroszkópia. 2. Membránvizsgálati technikák és elektorfiziológia. Langmuir-Blodgett (LB), black lipid membrane (BLM) és patch-clamp. 3. Mikrofluidika. Az ún. lab-on-a-chip koncepció alkalmazása a biológiában. Alapvető fizikai határok és technikai problémák: felületi erők, lamináris áramlás, adszorpció. Kétfázisú, nagy áteresztőképességű csepp alapú mikrofluidikák. 4. Optikai mikroszkópok I. Konjugált síkok a modern mikroszkópokban. Inverz, fáziskontraszt, epifluoreszcens mikroszkópok. Fluoreszcens fehérjék és optogenetika. 5. Optikai mikroszkópok II. Konfokális és két-foton mikroszkópok. A pont szétterülési függvény (point spread function: PSF), diffrakciós limit és szuperfelbontású technikák. Teljes visszaverődésen alapuló TIRF mikroszkóp. 6. Pásztázószondás módszerek. Atomi erőmikroszkóp (AFM): felépítés, üzemmódok, vizsgálható struktúrák és jelenségek.

Félévi tematika II. (Czirók András) • Röntgen krisztallográfia. • Tömegspektrometria. • NMR spektroszkópia. • Szeparációs technikák II. • Molekuladinamika.

Vizsga • Szóbeli. • Beadandó feladatok Andrásnál.

Irodalom a felkészüléshez • http: //balintszabo. web. elte. hu/Szerk. Vizsg. Biofiz • Damjanovich et al. : Orvosi biofizika tankönyv • http: //microscopyu. com

I. előadás: Optikai spektroszkópia 1. 2. 3. 4. 5. 6. Kétsugaras abszorpciós spektrofotométer Fluoreszcens spektroszkópia Förster típusú energiatranszfer (FRET) spektroszkópia Cirkuláris dikroizmus (CD) spektroszkópia Optikai hullámvezető spektroszkópia Raman spektroszkópia
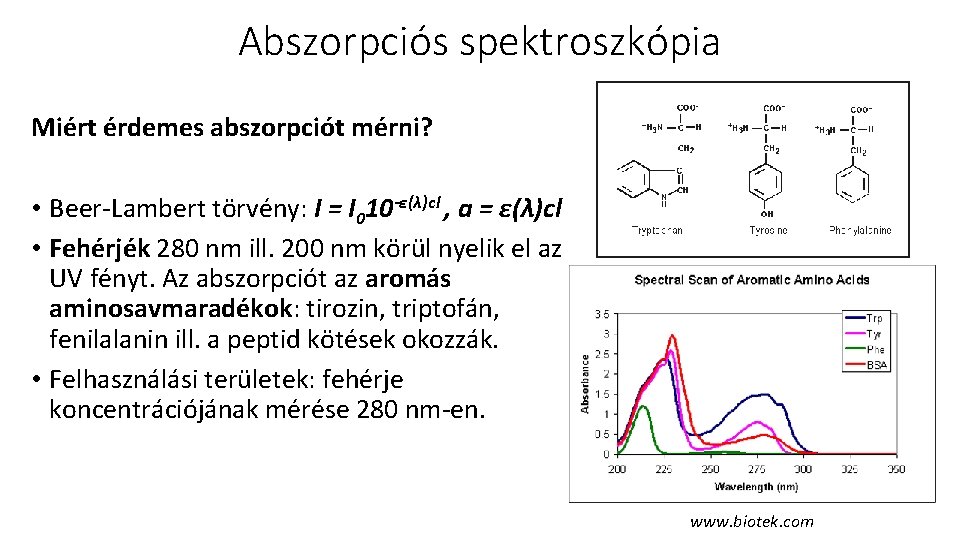
Abszorpciós spektroszkópia Miért érdemes abszorpciót mérni? • Beer-Lambert törvény: I = I 010 -ε(λ)cl , a = ε(λ)cl • Fehérjék 280 nm ill. 200 nm körül nyelik el az UV fényt. Az abszorpciót az aromás aminosavmaradékok: tirozin, triptofán, fenilalanin ill. a peptid kötések okozzák. • Felhasználási területek: fehérje koncentrációjának mérése 280 nm-en. www. biotek. com
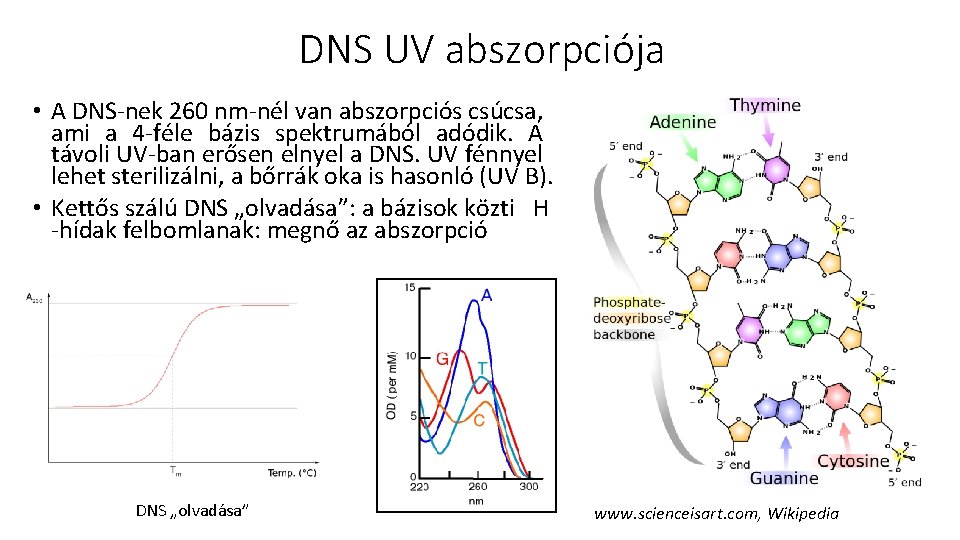
DNS UV abszorpciója • A DNS-nek 260 nm-nél van abszorpciós csúcsa, ami a 4 -féle bázis spektrumából adódik. A távoli UV-ban erősen elnyel a DNS. UV fénnyel lehet sterilizálni, a bőrrák oka is hasonló (UV B). • Kettős szálú DNS „olvadása”: a bázisok közti H -hídak felbomlanak: megnő az abszorpció DNS „olvadása” www. scienceisart. com, Wikipedia
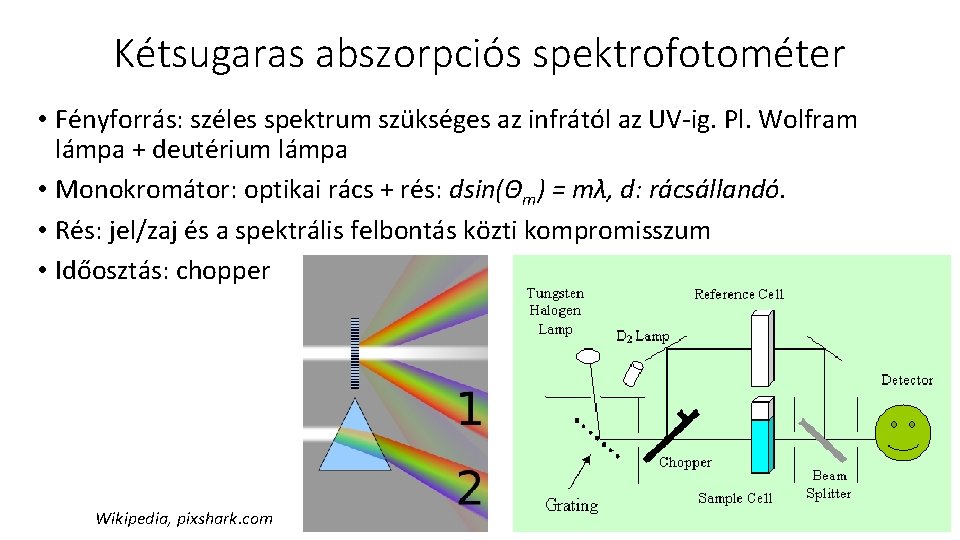
Kétsugaras abszorpciós spektrofotométer • Fényforrás: széles spektrum szükséges az infrától az UV-ig. Pl. Wolfram lámpa + deutérium lámpa • Monokromátor: optikai rács + rés: dsin(Θm) = mλ, d: rácsállandó. • Rés: jel/zaj és a spektrális felbontás közti kompromisszum • Időosztás: chopper Wikipedia, pixshark. com
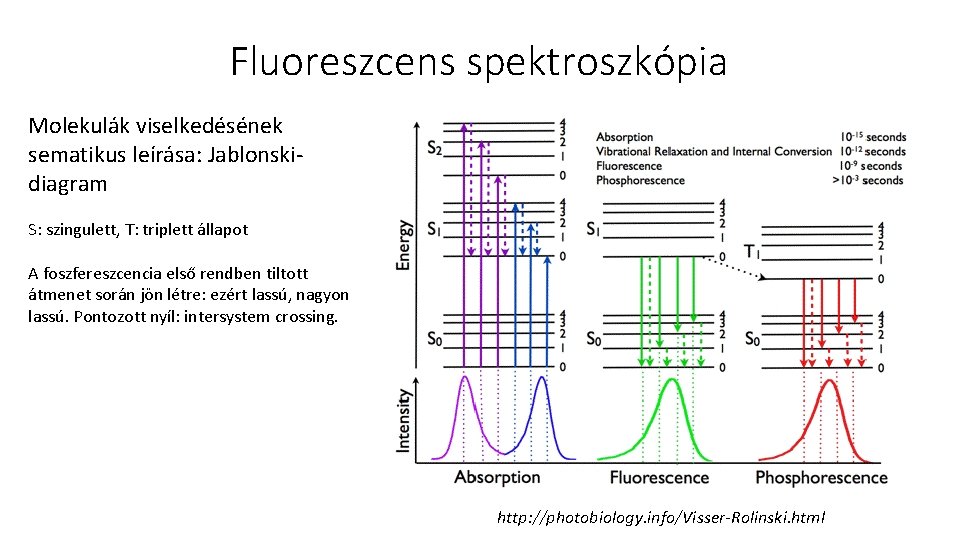
Fluoreszcens spektroszkópia Molekulák viselkedésének sematikus leírása: Jablonskidiagram S: szingulett, T: triplett állapot A foszfereszcencia első rendben tiltott átmenet során jön létre: ezért lassú, nagyon lassú. Pontozott nyíl: intersystem crossing. http: //photobiology. info/Visser-Rolinski. html

Fehérjék és DNS fluoreszcens vizsgálata Természetes és mesterséges fluoreszcencia Természetes: fluoreszcens aminosavak: tirozin, triptofán, fenilalanin. DNS autofluoreszcencia. Alkalmazások: molekuláris kölcsönhatások dinamikájának vizsgálata Mesterséges: • DNS: interkalálódó DNS festékek (etidium-bromid, propidiumjodid). Ezek hatásfoka 5%-ról közel 100%-ra nő, amikor a DNS kettős hélix nagy árkaiba kötődnek. • Fluoreszcens festékek, quantum-dots. Ezek specifitását általában immun antitest adja. • Fluoreszcens fehérjék: GFP és rokonai. Génsebészeti jelölés. Ábrák forrása: www. microscopyu. com
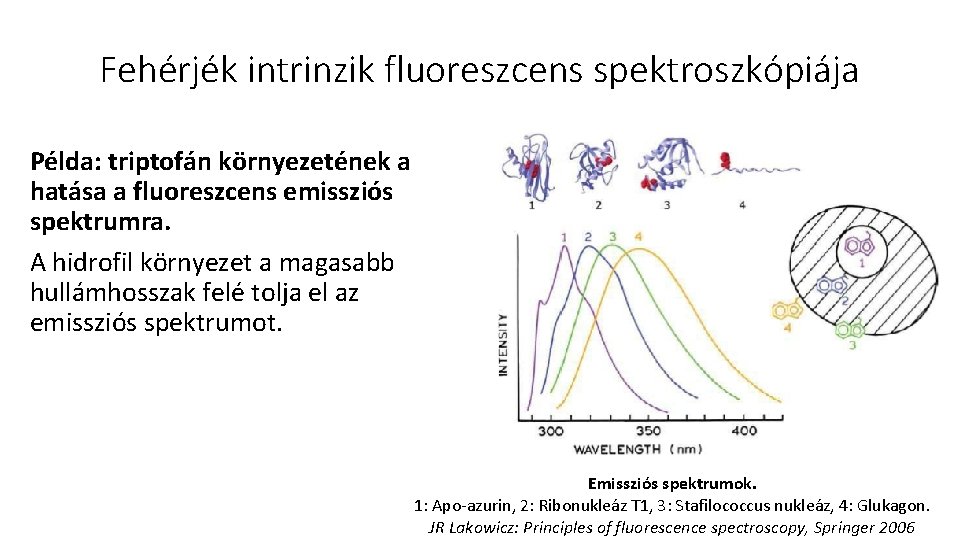
Fehérjék intrinzik fluoreszcens spektroszkópiája Példa: triptofán környezetének a hatása a fluoreszcens emissziós spektrumra. A hidrofil környezet a magasabb hullámhosszak felé tolja el az emissziós spektrumot. Emissziós spektrumok. 1: Apo-azurin, 2: Ribonukleáz T 1, 3: Stafilococcus nukleáz, 4: Glukagon. JR Lakowicz: Principles of fluorescence spectroscopy, Springer 2006
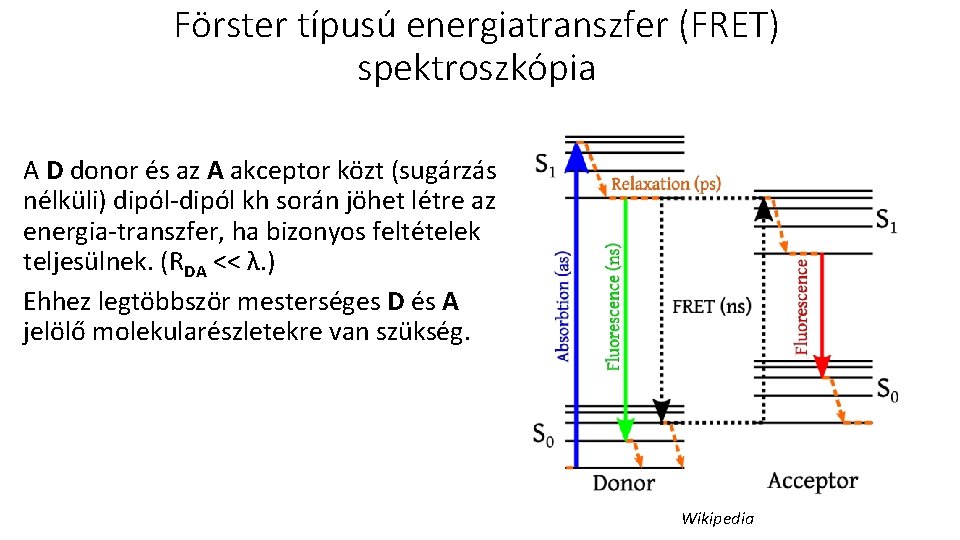
Förster típusú energiatranszfer (FRET) spektroszkópia A D donor és az A akceptor közt (sugárzás nélküli) dipól-dipól kh során jöhet létre az energia-transzfer, ha bizonyos feltételek teljesülnek. (RDA << λ. ) Ehhez legtöbbször mesterséges D és A jelölő molekularészletekre van szükség. Wikipedia
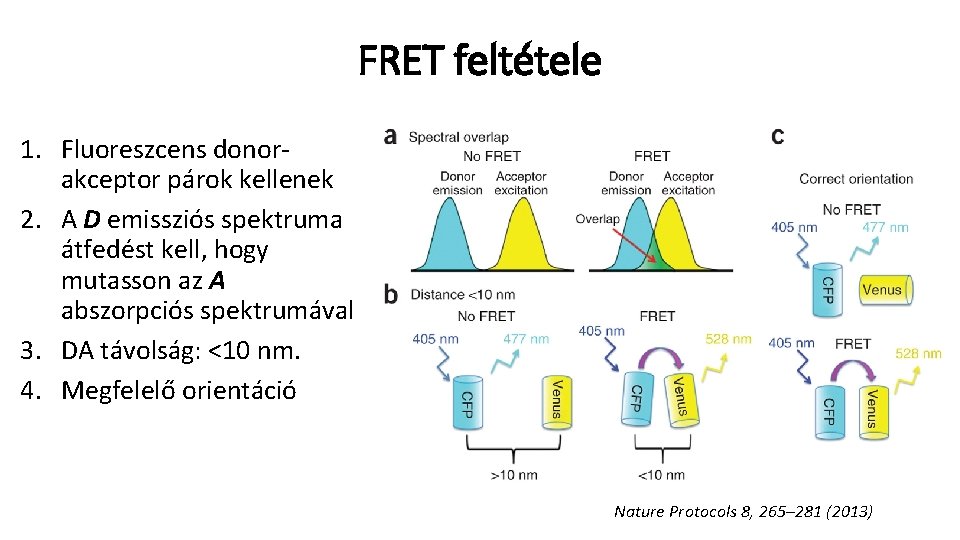
FRET feltétele 1. Fluoreszcens donorakceptor párok kellenek 2. A D emissziós spektruma átfedést kell, hogy mutasson az A abszorpciós spektrumával 3. DA távolság: <10 nm. 4. Megfelelő orientáció Nature Protocols 8, 265– 281 (2013)
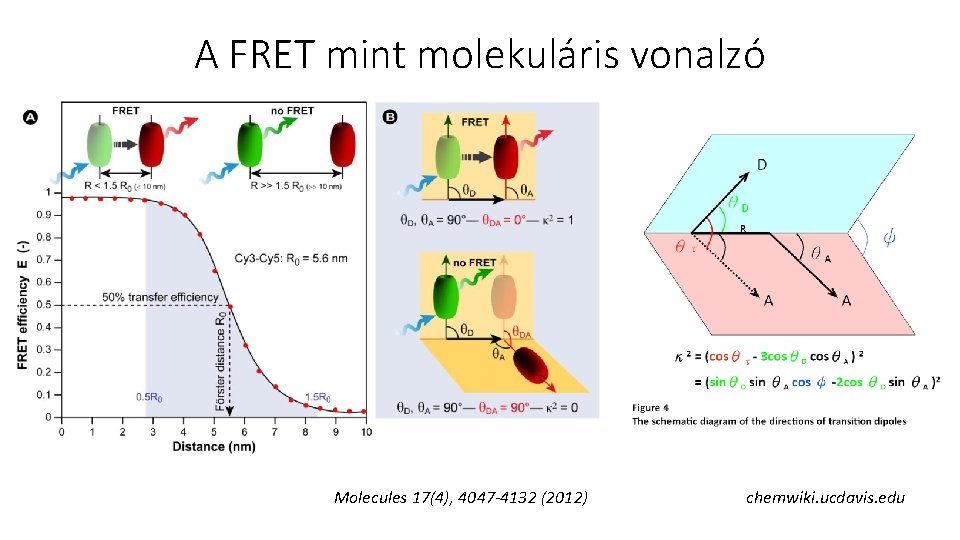
A FRET mint molekuláris vonalzó Molecules 17(4), 4047 -4132 (2012) chemwiki. ucdavis. edu

FRET: formulák •
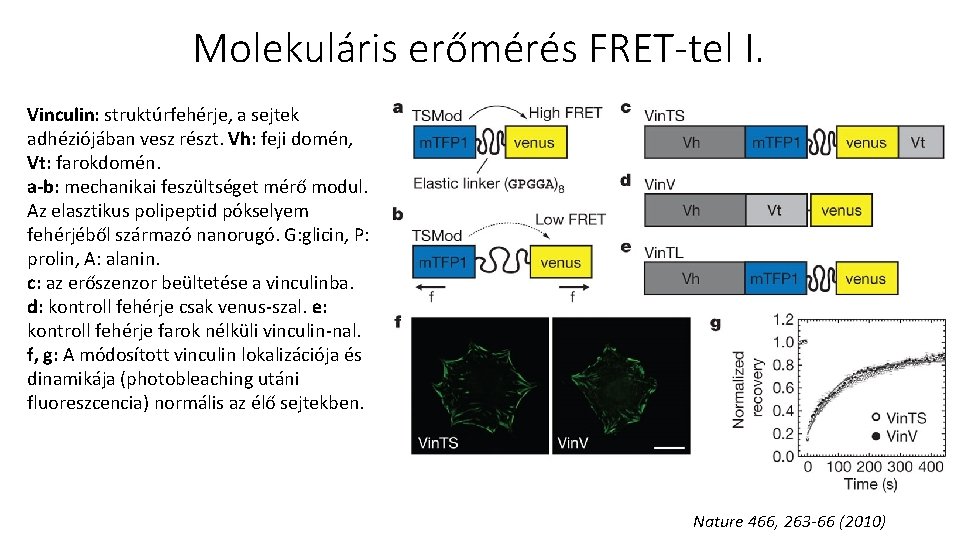
Molekuláris erőmérés FRET-tel I. Vinculin: struktúrfehérje, a sejtek adhéziójában vesz részt. Vh: feji domén, Vt: farokdomén. a-b: mechanikai feszültséget mérő modul. Az elasztikus polipeptid pókselyem fehérjéből származó nanorugó. G: glicin, P: prolin, A: alanin. c: az erőszenzor beültetése a vinculinba. d: kontroll fehérje csak venus-szal. e: kontroll fehérje farok nélküli vinculin-nal. f, g: A módosított vinculin lokalizációja és dinamikája (photobleaching utáni fluoreszcencia) normális az élő sejtekben. Nature 466, 263 -66 (2010)
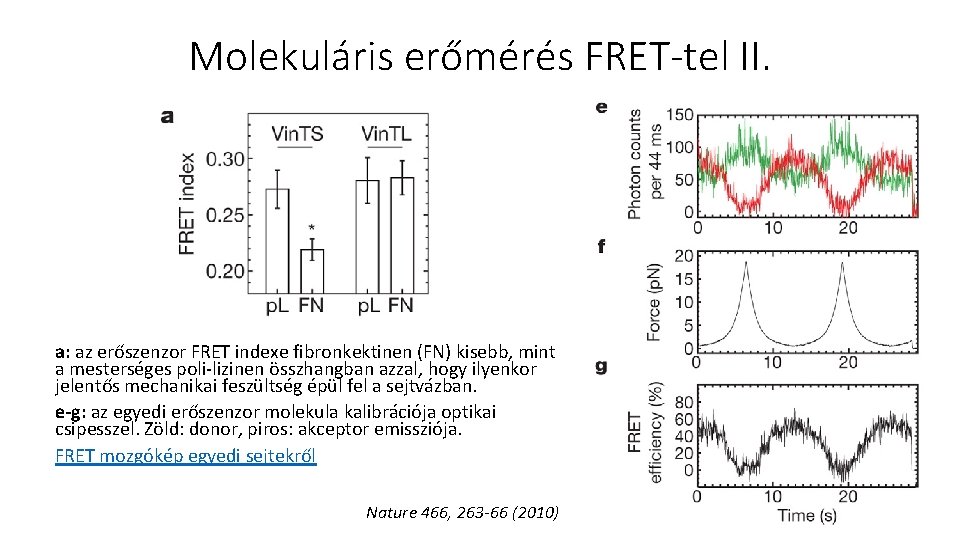
Molekuláris erőmérés FRET-tel II. a: az erőszenzor FRET indexe fibronkektinen (FN) kisebb, mint a mesterséges poli-lizinen összhangban azzal, hogy ilyenkor jelentős mechanikai feszültség épül fel a sejtvázban. e-g: az egyedi erőszenzor molekula kalibrációja optikai csipesszel. Zöld: donor, piros: akceptor emissziója. FRET mozgókép egyedi sejtekről Nature 466, 263 -66 (2010)

BRET: Biolumineszcens rezonancia energia transzfer • Biolumineszcens donor, fluoreszcens akceptor: nincs szükség külső gerjesztő fényre. A donor általában a luciferáz (szentjánosbogárból) • A luciferáz a következő reakciót katalizálja: 1. luciferin + ATP → luciferil adenilát + PPi 2. luciferil adenilát + O 2 → oxyluciferin + AMP + fény Szentjánosbogár, www. termeszettar. hu • Előnyei FRET-hez képest: kisebb háttér zaj és csökkent „photobleaching”, in vivo vizsgálatokra is alkalmas • Fehérje-fehérje kh vizsgálatához Renilla reniformis, polip kolónia, Wikipedia
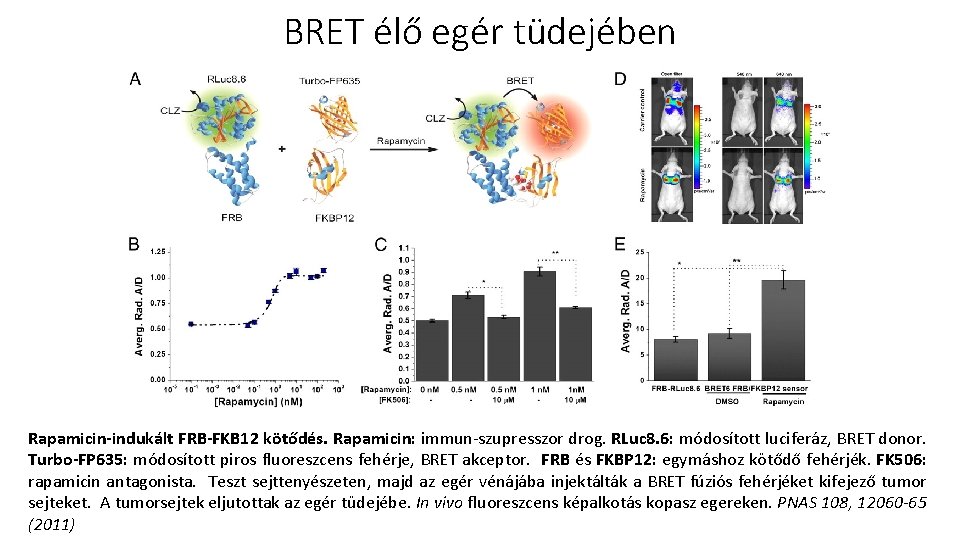
BRET élő egér tüdejében Rapamicin-indukált FRB-FKB 12 kötődés. Rapamicin: immun-szupresszor drog. RLuc 8. 6: módosított luciferáz, BRET donor. Turbo-FP 635: módosított piros fluoreszcens fehérje, BRET akceptor. FRB és FKBP 12: egymáshoz kötődő fehérjék. FK 506: rapamicin antagonista. Teszt sejttenyészeten, majd az egér vénájába injektálták a BRET fúziós fehérjéket kifejező tumor sejteket. A tumorsejtek eljutottak az egér tüdejébe. In vivo fluoreszcens képalkotás kopasz egereken. PNAS 108, 12060 -65 (2011)

Biomolekulák kiralitása • Királis molekulák: szinte minden biomolekula jobb-bal aszimmetriát mutat. • A kiralitás jelentősége a molekulák funkciójában: pl. L-glükóz édes, de nem emészthető a D-glükózzal (szőlőcukorral) szemben! • Fehérjeszerkezetben különösen fontos a kiralitás: pl. alfa-hélix vs. béta redő. Neptunea angulata és Neptunea despecta. Wikipedia

Kiralitás mérése: CD spektroszkópia • A Röntgen krisztallográfia nagy felbontású szerkezeti adatokat ad, de ehhez kristályosítani kell, ami sokszor nehéz vagy szinte lehetetlen. • Az NMR oldatban is működik, de csak kisebb fehérjék szerkezetének a megfejtésére. • A fentiekhez kiegészítő technika a CD spektroszkópia. Előnyei a következők: 1. Jelölésmentes. 2. Nem igényel kristályosítást: vizes fázisban dinamikai adatok is kimérhetők. 3. Egyszerű, költséghatékony, nem invazív technika. 4. Funkcionális vizsgálatra is alkalmas: ligand bekötése, denaturáció, oligomerizáció időbeli követése, különböző szerkezeti állapotok azonosítása. 5. Elméleti térszerkezeti jóslatok ellenőrzése, pontosítása.

Fény polarizációs tulajdonságainak változása anyagon áthaladva A cirkuláris dikroizmus és a cirkuláris kettőstörés két különböző effektus. 1. Cirkuláris kettőstörés: törésmutatóbeli eltérés: Δn = nbal -njobb Ezt a hullámhossz fv-ében mérve: optikai rotációs diszperzió (ORD) 2. Cirkuláris dikroizmus: abszorpcióbeli (pontosabban extinkciós koefficiensbeli) különbség: Δε = εbal – εjobb • Mozgóképes demonstráció

Matematikai összefüggések a CD spektroszkópiához • Cirkuláris dikroizmus: abszorpcióbeli (pontosabban extinkciós koefficiensbeli) különbség: Δε = εbal – εjobb • Ellipticitás: Θ = arct tg (b/a), ahol b és a az elliptikusan polarizált fény ellipszisének kis és nagy tengelye. Moláris ellipticitás [Θ] = 100 Θ/lc • [Θ] = 3298. 2 Δε [deg*cm 2/dmol]
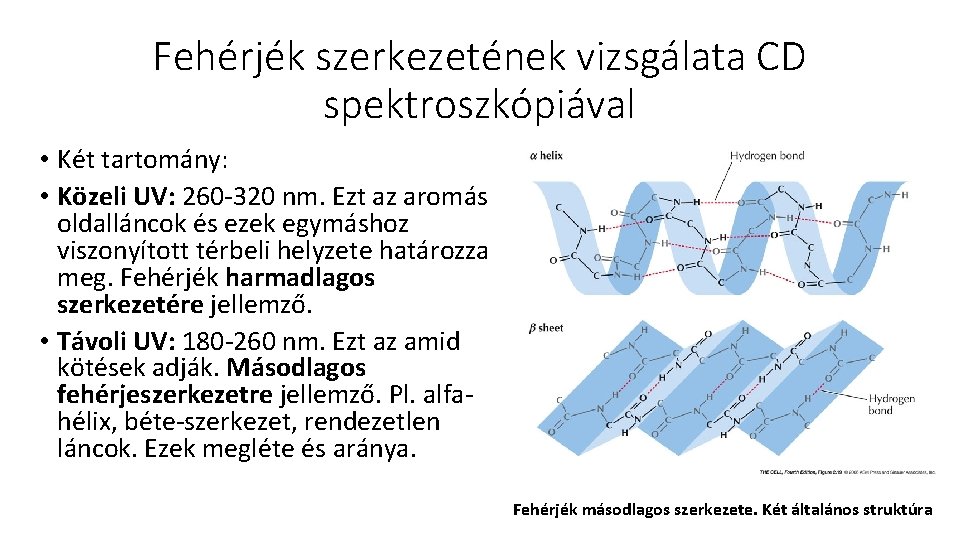
Fehérjék szerkezetének vizsgálata CD spektroszkópiával • Két tartomány: • Közeli UV: 260 -320 nm. Ezt az aromás oldalláncok és ezek egymáshoz viszonyított térbeli helyzete határozza meg. Fehérjék harmadlagos szerkezetére jellemző. • Távoli UV: 180 -260 nm. Ezt az amid kötések adják. Másodlagos fehérjeszerkezetre jellemző. Pl. alfahélix, béte-szerkezet, rendezetlen láncok. Ezek megléte és aránya. Fehérjék másodlagos szerkezete. Két általános struktúra
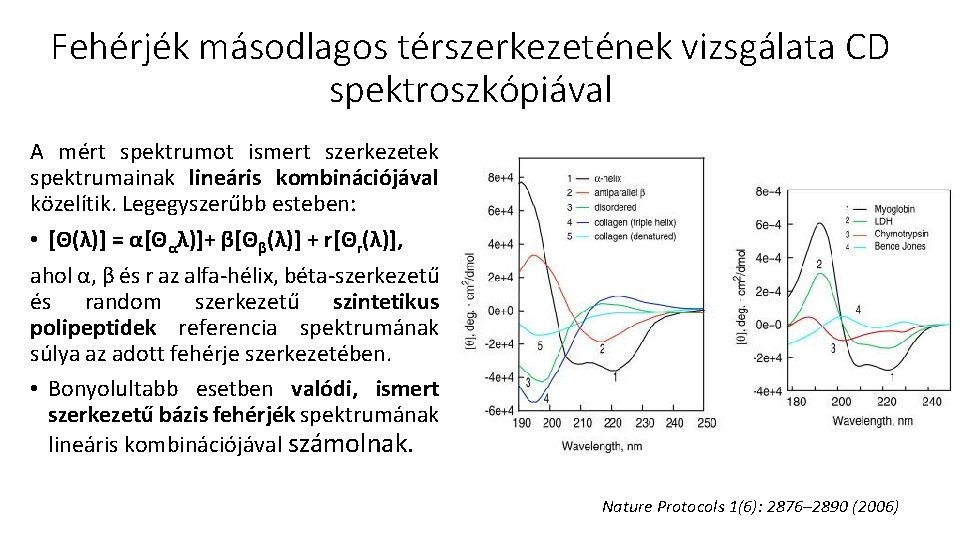
Fehérjék másodlagos térszerkezetének vizsgálata CD spektroszkópiával A mért spektrumot ismert szerkezetek spektrumainak lineáris kombinációjával közelítik. Legegyszerűbb esteben: • [Θ(λ)] = α[Θαλ)]+ β[Θβ(λ)] + r[Θr(λ)], ahol α, β és r az alfa-hélix, béta-szerkezetű és random szerkezetű szintetikus polipeptidek referencia spektrumának súlya az adott fehérje szerkezetében. • Bonyolultabb esetben valódi, ismert szerkezetű bázis fehérjék spektrumának lineáris kombinációjával számolnak. Nature Protocols 1(6): 2876– 2890 (2006)

Optikai hullámvezető spektroszkópia 1. A hullámvezetőben teljes visszaverődésekkel terjedhet a fény. 2. Csak diszkrét módusok tudnak terjedni, melyek diszkrét becsatolási szögek mellett jönnek létre. 3. A kisebb törésmutatójú térrészbe evaneszcens fény hatol be. 4. A becsatolás szöge nagyon érzékeny a fedő réteg törésmutatójára. Analyst 136, 227 -236 (2011)
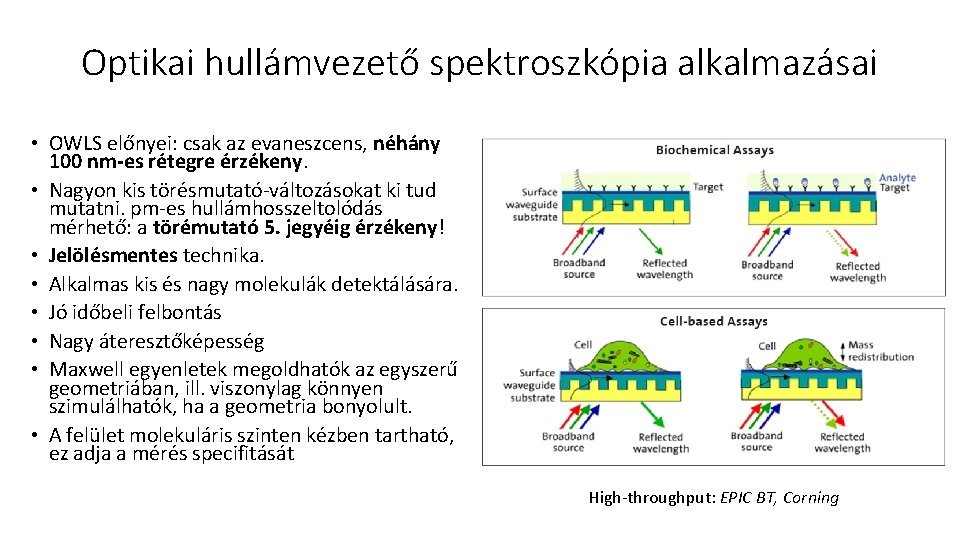
Optikai hullámvezető spektroszkópia alkalmazásai • OWLS előnyei: csak az evaneszcens, néhány 100 nm-es rétegre érzékeny. • Nagyon kis törésmutató-változásokat ki tud mutatni. pm-es hullámhosszeltolódás mérhető: a törémutató 5. jegyéig érzékeny! • Jelölésmentes technika. • Alkalmas kis és nagy molekulák detektálására. • Jó időbeli felbontás • Nagy áteresztőképesség • Maxwell egyenletek megoldhatók az egyszerű geometriában, ill. viszonylag könnyen szimulálhatók, ha a geometria bonyolult. • A felület molekuláris szinten kézben tartható, ez adja a mérés specifitását High-throughput: EPIC BT, Corning

Raman spektroszkópia • Fizikai háttér: a fény rugalmatlan szóródása. Alkalmas molekulák vibrációs és rotációs gerjesztések vizsgálatára. • Technikai nehézség: direkt nyaláb kiszűrése: „band-stop” („notch”) filter szükséges. Ezek destruktív interferencián alapulnak. Wikipedia
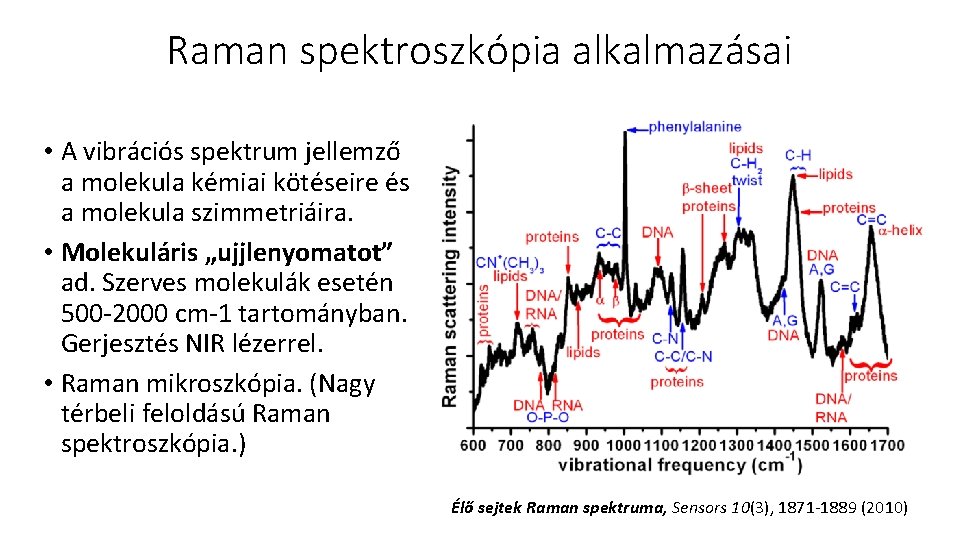
Raman spektroszkópia alkalmazásai • A vibrációs spektrum jellemző a molekula kémiai kötéseire és a molekula szimmetriáira. • Molekuláris „ujjlenyomatot” ad. Szerves molekulák esetén 500 -2000 cm-1 tartományban. Gerjesztés NIR lézerrel. • Raman mikroszkópia. (Nagy térbeli feloldású Raman spektroszkópia. ) Élő sejtek Raman spektruma, Sensors 10(3), 1871 -1889 (2010)
- Slides: 30






















































