SMA zmiany w zakresie opieki z perspektywy klinicznej


















- Slides: 27

SMA – zmiany w zakresie opieki z perspektywy klinicznej Katarzyna Kotulska 15 th International EBHC Symposium October 5 th-7 th, 2020 | ONLINE

Rdzeniowy zanik mięśni - definicja • Przewlekła postępujaca choroba o podłożu genetycznym • Dziedziczona autosomalnie recesywnie, • monogenowa • Degeneracja motoneuronów rdzenia kręgowego • Podstawowe objawy: hypotonia, osłabienie i zanik mięśni • Czestość 1 na 10, 000 żywych urodzeń • Jedna z najczęstszych przyczyn zgonów niemowląt (najczęstsza genetyczna) 1. Lunn MR, Wang CH. Lancet. 2008; 371(9630): 2120 -2133; 2. Farrar MA, et al. J Pediatr. 2013; 162(1): 155 -159; 3. Monani UR, et al. Hum Mol Genet. 2000; 9: 333 -339; 4. Prior TW, Finanger EF. Gene Reviews ®. https: //www. ncbi. nlm. nih. gov/books/NBK 1352/. Accessed April 8, 2019.

Typy SMA (podział wg Munsat, 1992) • 0 – u płodu/noworodka • 1 – najczęstszy, ciężki, rozwija się u dzieci przez 6 mż: nigdy nie siadają samodzielnie; nieleczone kończy się śmiercią większości dzieci przed 2 rż • 2 – początek między 7 a 12 mż, nigdy nie chodzą (około 70% przeżywa do 25 rż) • 3 – zaczynają chodzić samodzielnie, potem tracą tę umiejętność (ponad połowa nie chodzi w wieku 14 lat) • 4 - dorosły

Objawy SMA wtórne do zaniku mięśni • Nieprawidłowy rozwój kośćca • deformacje klatki piersiowej, stóp, skolioza, • zaburzenia karmienia (zwykle niedobór masy ciała u młodszych dzieci, dość często nadwaga u pacjentów starszych • zaburzenia oddychania (w typie 1, rzadziej w drugim – konieczne wspomaganie oddechu respiratorem) • wzmożone pocenie się Rozwój psychiczny/intelektualny pacjentów jest prawidłowy, a w typie 1 i 2 często powyżej przeciętnej

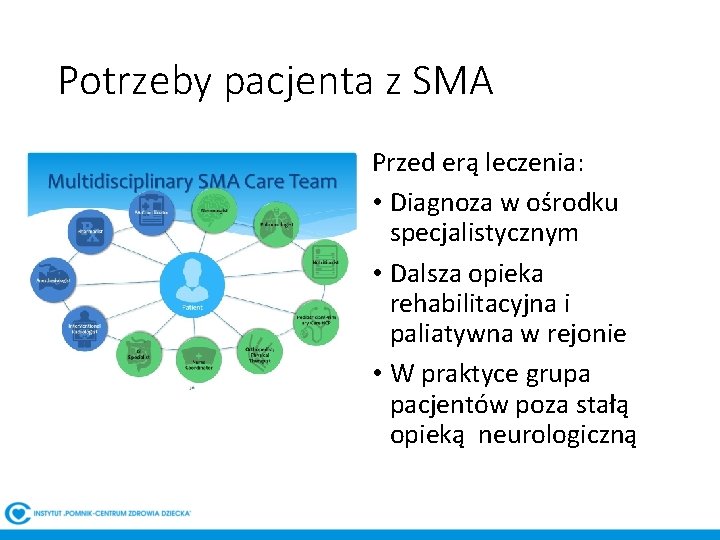
Potrzeby pacjenta z SMA Przed erą leczenia: • Diagnoza w ośrodku specjalistycznym • Dalsza opieka rehabilitacyjna i paliatywna w rejonie • W praktyce grupa pacjentów poza stałą opieką neurologiczną

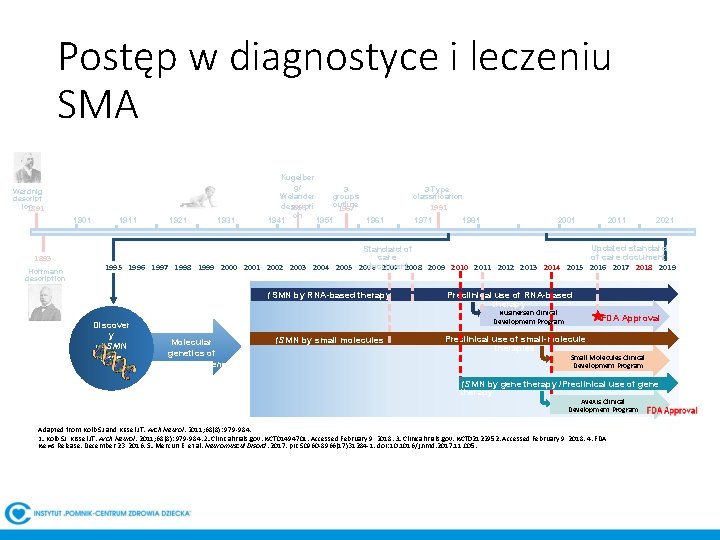
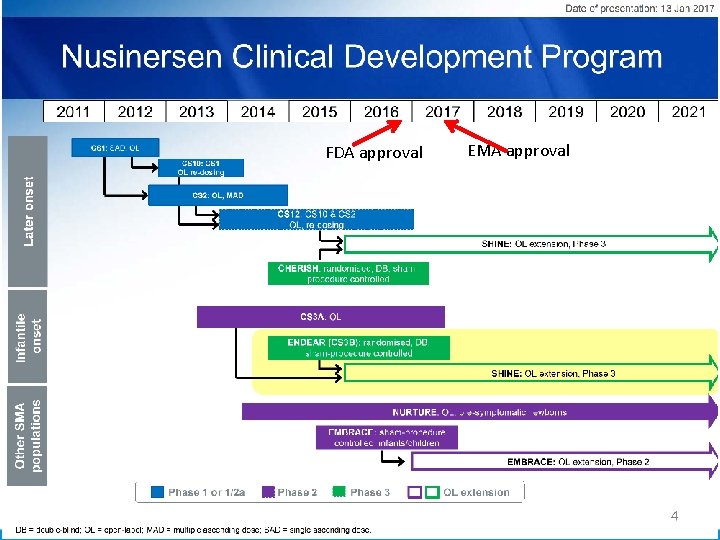
Postęp w diagnostyce i leczeniu SMA Werdnig descript ion 1891 1901 1893 Hoffmann description 1911 1921 1931 Kugelber g/ 3 Welander groups outline descripti 1956 1967 on 1941 1951 1961 3 Type classification 1991 1971 1981 2001 2011 2021 Updated standard Standard of of care document 1995 1996 1997 1998 1999 2000 2001 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011 2012 2013 2014 2015 2016 2017 2018 2019 ↑SMN by RNA-based therapy Discover y of SMN gene Preclinical use of RNA-based therapy Nusinersen Clinical Development Program Molecular genetics of SMN/SMN 2 gene ↑SMN by small molecules FDA Approval Preclinical use of small-molecule therapies Small Molecules Clinical Development Program ↑SMN by gene therapy /Preclinical use of gene therapy Ave. Xis Clinical Development Program Adapted from Kolb SJ and Kissel JT. Arch Neurol. 2011; 68(8): 979 -984. 1. Kolb SJ, Kissel JT. Arch Neurol. 2011; 68(8): 979 -984. 2. Clinicaltrials. gov. NCT 01494701. Accessed February 9, 2018. 3. Clinicaltrials. gov. NCT 02122952. Accessed February 9, 2018. 4. FDA News Release. December 23, 2016. 5. Mercuri E, et al. Neuromuscul Disord. 2017. pii: S 0960 -8966(17)31284 -1. doi: 10. 1016/j. nmd. 2017. 11. 005.

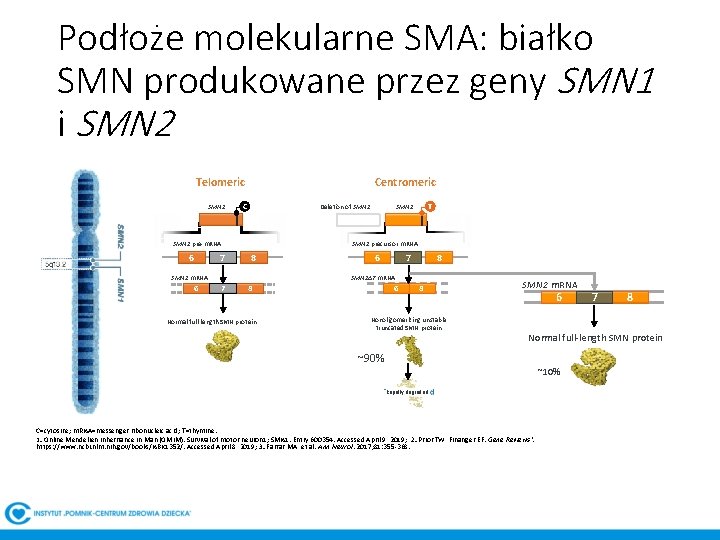
Podłoże molekularne SMA: białko SMN produkowane przez geny SMN 1 i SMN 2 Centromeric Telomeric SMN 1 C Deletion of SMN 1 pre-m. RNA 6 7 SMN 2 precursor m. RNA 8 6 7 8 SMN 2Δ 7 m. RNA SMN 1 m. RNA 6 T SMN 2 7 8 Normal full-length SMN protein 6 8 Nonoligomerizing unstable truncated SMN protein SMN 2 m. RNA 6 7 8 Normal full-length SMN protein ~90% ~10% Rapidly degraded C=cytosine; m. RNA=messenger ribonucleic acid; T=thymine. 1. Online Mendelien Inheritance in Man (OMIM). Survival of motor neuron 1; SMN 1. Entry 600354. Accessed April 9, 2019; 2. Prior TW, Finanger EF. Gene Reviews ®. https: //www. ncbi. nlm. nih. gov/books/NBK 1352/. Accessed April 8, 2019; 3. Farrar MA, et al. Ann Neurol. 2017; 81: 355 -368.

Diagnostyka SMA • Przed erą genetyczną: objawy kliniczne + EMG • Po wprowadzeniu dgn genetycznej: objawy kliniczne + analiza mutacji • Obecnie: analiza mutacji (niezależnie od objawów klinicznych lub ich braku) • Przyszłość: skrining noworodkowy

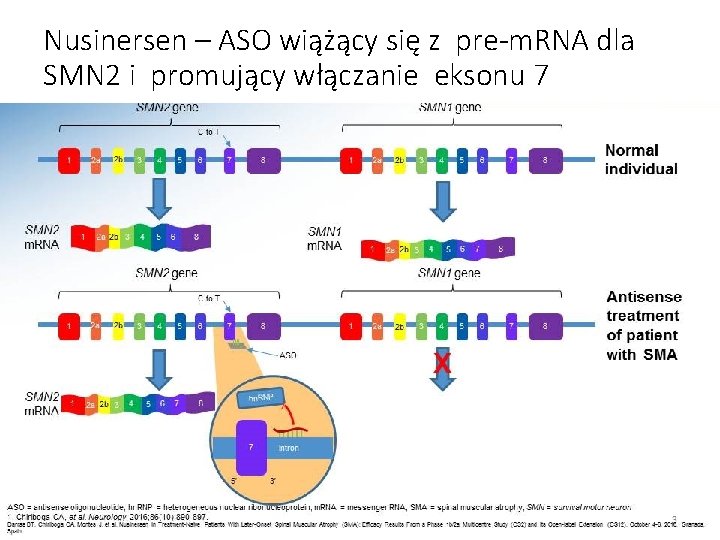
Nusinersen – ASO wiążący się z pre-m. RNA dla SMN 2 i promujący włączanie eksonu 7

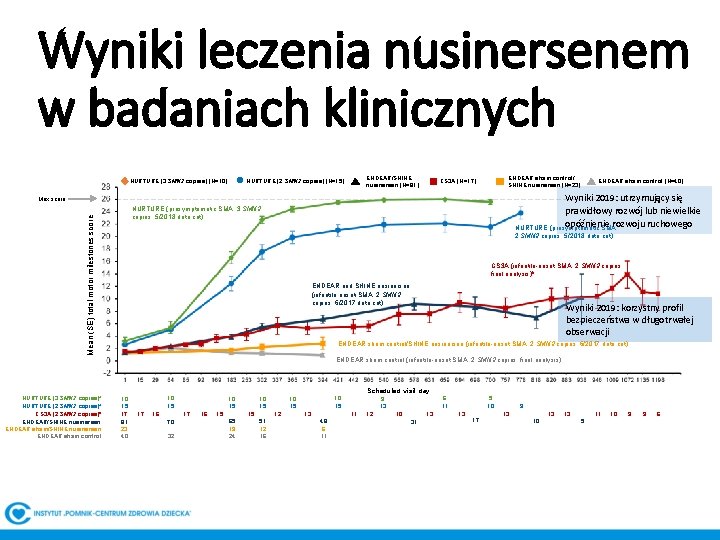
Wyniki leczenia nusinersenem w badaniach klinicznych NURTURE (3 SMN 2 copies) (N=10) ENDEAR/SHINE nusinersen (N=81) NURTURE (2 SMN 2 copies) (N=15) ENDEAR sham control/ SHINE nusinersen (N=23) CS 3 A (N=17) Wyniki 2019: utrzymujący się prawidłowy rozwój lub niewielkie opóźnienie rozwoju ruchowego NURTURE (presymptomatic SMA; Max score NURTURE (presymptomatic SMA; 3 SMN 2 copies; 5/2018 data cut) Mean (SE) total motor milestones score ENDEAR sham control (N=40) 2 SMN 2 copies; 5/2018 data cut) CS 3 A (infantile-onset SMA; 2 SMN 2 copies; final analysis)b ENDEAR and SHINE nusinersen (infantile onset-SMA; 2 SMN 2 copies; 6/2017 data cut) Wyniki 2019: korzystny profil bezpieczeństwa w długotrwałej obserwacji ENDEAR sham control/SHINE nusinersen (infantile-onset SMA; 2 SMN 2 copies; 6/2017 data cut) ENDEAR sham control (infantile-onset SMA; 2 SMN 2 copies; final analysis) Scheduled visit day NURTURE (3 SMN 2 copies)a NURTURE (2 SMN 2 copies)a CS 3 A (2 SMN 2 copies)b ENDEAR/SHINE nusinersen ENDEAR sham control 10 15 17 81 23 40 10 15 17 16 17 70 32 10 15 16 15 15 65 19 24 12 51 12 16 10 15 13 11 48 6 11 12 5 10 6 11 9 13 10 13 31 13 9 13 17 13 10 13 11 10 9 9 6 5 NURTURE study interim analysis data cutoff date: May 15, 2018; ENDEAR-SHINE integrated analysis data cutoff date: June 30, 2017. a. HINE Section 2 was assessed in NURTURE participants up until the Day 778 study visit. b. CS 3 A end-ofstudy data for the cohort of infants with 2 SMN 2 copies. ENDEAR participants with 2 SMN 2 copies in the intention-to-treat population. ENDEAR data were windowed into intervals based on time from baseline. For each study, n≥ 5 are plotted.

Dostęp do nusinersenu w Polsce • Program wczesnego dostępu • Program lekowy

FDA approval EMA approval

Program lekowy NFZ – od marca 2019

Program lekowy a program opieki koordynowanej • Program lekowy w SMA nie wyklucza żadnego niemal pacjenta • Obejmuje niektóre niezbędne badana, konsultacje, plan rehabilitacyjny • Wymusza koordynowaną opiekę, ale w ograniczonym zakresie • Wymusza opiekę w ośrodku specjalistycznym (odciąża opiekę w rejonie, obciąża pacjenta i rodzinę) • Braki w PL: opieka w rejonie, genetyka (poradnictwo), zabiegi ortopedyczne, transport medyczny • Bardzo niska wycena!

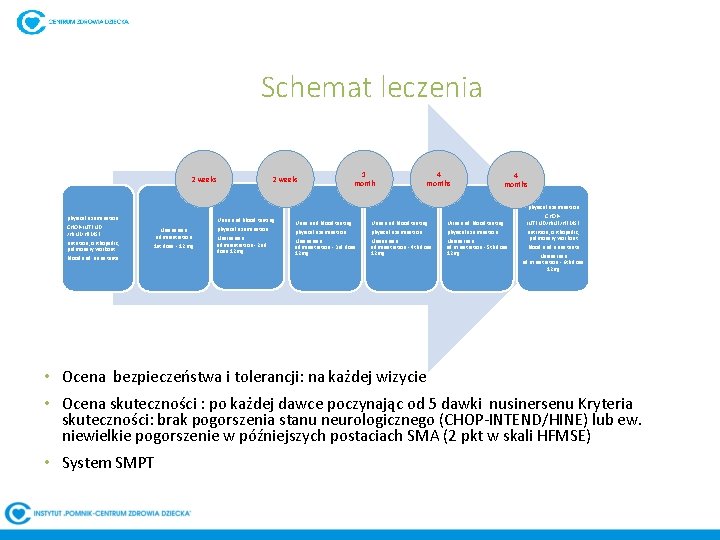
Schemat leczenia 2 weeks physical examination CHOP-INTEND /HINE/HFMSE nutrition, orthopedic, pulmonary workout Nusinersen administration 1 st dose - 12 mg blood and urine tests 2 weeks Urine and blood testing physical examination Nusinersen administration - 2 nd dose 12 mg 1 month Urine and blood testing physical examination Nusinersen administration - 3 rd dose 12 mg 4 months Urine and blood testing physical examination Nusinersen administration - 4 th dose 12 mg 4 months Urine and blood testing physical examination Nusinersen administration - 5 th dose 12 mg physical examination CHOPINTEND/HINE/HFMSE nutrition, orthopedic, pulmonary workout blood and urine tests Nusinersen administration - 6 th dose 12 mg • Ocena bezpieczeństwa i tolerancji: na każdej wizycie • Ocena skuteczności : po każdej dawce poczynając od 5 dawki nusinersenu Kryteria skuteczności: brak pogorszenia stanu neurologicznego (CHOP-INTEND/HINE) lub ew. niewielkie pogorszenie w późniejszych postaciach SMA (2 pkt w skali HFMSE) • System SMPT

Leczenie nusinersenem w Polsce w liczbach • Koordynowany przez Zespół powołany przez Prezesa NFZ • Ponad 750 wniosków • 24 ośrodki • Obecnie leczonych 646 pacjentów • 20 wyłączonych z programu; żaden z powodu nieskuteczności leczenia (gł. skolioza, rezygnacja – inne terapie)

Nusinersen w IPCZD w liczbach • 83 pacjentów zakwalifikowanych • 76 pacjentów obecnie leczonych • 1 zmarł • 2 zakończyło program • 5 przekazanych do innych ośrodków • Ponad 650 podanych dawek

Nusinersen w IPCZD w liczbach • 8 pacjentów: podanie pod kontrolą radiologiczną • 6 pacjentów: znieczulenie ogólne • Pozostali: znieczulenie miejscowe i sedacja

Podanie leku Dzień 1. • Przyjęcie do Oddziału • Ocena w kierunku ew. przeciwwskazań • Zamówienie leku • Ocena funkcjonalna • Zabezpieczenie żywieniowe, pulmonologiczne itp. wg potrzeb Dzień 2. • Podanie leku • Kontrola miejsca wkłucia • Wypis po co najmniej 12 godzinach

Problemy przy podaniu leku • Skolioza • Stan po zabiegu ortopedycznym • Wyciek płynu m-r (z lekiem? ) – 5 razy • Obserwowane działania niepożądane: wzrost transaminaz (wydaje się, że bez związku z lekiem, przemijający, tylko u młodszych dzieci), zanik nn. II

Organizacja podań leków • 2 punkcje dziennie • Lek zamawiany dzień wcześniej po potwierdzeniu przyjęcia pacjenta • Transport leku – na najwcześniejsze ranne godziny • Problemy związane z obecną sytuacją epidemiologiczną: rozliczanie opakowań, pobrania wirusologiczne

Opieka wielospecjalistyczna • Na miejscu: genetyk, stomatolog, anestezjolog, pulmonolog, dietetyk, logopeda, gastrolog, neurochirurg, fizjoterapeuta, neurolog, immunolog • Zewnętrznie: ortopeda

Zmiany systemowe wprowadzone w związku z nową terapią w SMA • Nowa grupa pacjentów (obecnie ponad 700) w ośrodkach specjalistycznych • Częste (do 7 w pierwszym roku, 3 w każdym kolejnym) hospitalizacje, często problematyczne, wymagające wielospecjalistycznej opieki, często ze wsparciem oddechu • Konieczność szkoleń personelu w zakresie skal funkcjonalnych, wytycznych, itp.

Potrzeby/braki systemowe w związku z nową terapią • Niedobór kadry specjalistycznej wyszkolonej w opiece nad pacjentami z SMA (lekarze, rehabilitanci) • Niedobór pielęgniarek • Niedobór łóżek szpitalnych • Nierozwiązanie kwestii transportu medycznego • Późne rozpoznanie=gorsze wyniki leczenia

Wyniki leczenia nusinersenem w IPCZD • W grupie pacjentów leczonych co najmniej rok z SMA 1: średnia poprawa o 7, 8 pkt w skali CHOPINTEND (zakres 1 -22) • U żadnego pacjenta nie zaobserwowano pogorszenia • U jednego stan neurologiczny się nie zmienił.

Przyszłość terapii SMA • Nowe leki zarejestrowane: Zolgensma (EU i USA), risdiplam (USA) • Nowe leki w trakcie badań: np. branaplam • Terapia zindywidualizowana? • Łączenie terapii? • Koszty leczenia? Wszystkie badania wskazują na zależność wyniku leczenia od momentu rozpoczęcia terapii – możliwe jest nawet uzyskanie „fenotypu zdrowego”

Podsumowanie • Wprowadzenie leków zmieniających naturalny przebieg choroby spowodowało powstanie zupełnie nowej grupy pacjentów • Grupa ta stanowi wyzwanie dla systemu opieki zdrowotnej oraz dla decydentów • Wprowadzenie programu przesiewu noworodkowego umożliwi uzyskanie największych korzyści z leczenia
 Rodzaje perspektyw
Rodzaje perspektyw Model bismarcka opieki zdrowotnej
Model bismarcka opieki zdrowotnej Rozwój technologii informacyjnej
Rozwój technologii informacyjnej Rodzaje perspektywy
Rodzaje perspektywy Dzienny dom opieki medycznej ministerstwo zdrowia
Dzienny dom opieki medycznej ministerstwo zdrowia Mnożenie w zakresie 10
Mnożenie w zakresie 10 Wytyczne w zakresie kwalifikowalnosci wydatków
Wytyczne w zakresie kwalifikowalnosci wydatków Teoria endosymbiozy zakłada że mitochondria i plastydy
Teoria endosymbiozy zakłada że mitochondria i plastydy Zmiany stanu skupienia
Zmiany stanu skupienia Epikryza
Epikryza Nieodwracalne zmiany w mózgu po dopalaczach
Nieodwracalne zmiany w mózgu po dopalaczach 4 fazy zmiany kottera
4 fazy zmiany kottera Przykładowe uzasadnienie zmiany nazwiska
Przykładowe uzasadnienie zmiany nazwiska Dopalacze do palenia
Dopalacze do palenia Pre kontemplacja
Pre kontemplacja Niechęć ciała do zmiany stanu ruchu
Niechęć ciała do zmiany stanu ruchu Geografia zmiany na mapie politycznej świata
Geografia zmiany na mapie politycznej świata Zmiany w przyrodzie wiosną
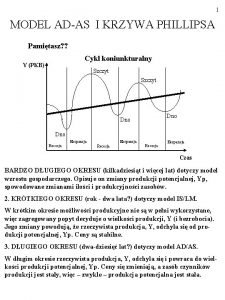
Zmiany w przyrodzie wiosną Model adas
Model adas Matematika kelas xi semester 2
Matematika kelas xi semester 2 Sebutkan 7k dalam wiyata mandala
Sebutkan 7k dalam wiyata mandala Tujuan tata krama
Tujuan tata krama Peta konsep 3d
Peta konsep 3d Seorang ibu membagikan coklat kepada 5 orang anaknya
Seorang ibu membagikan coklat kepada 5 orang anaknya Sma 3 tenggarong
Sma 3 tenggarong Kartu peserta ujian praktek
Kartu peserta ujian praktek Amperage can be described as
Amperage can be described as Sman 99 jakarta
Sman 99 jakarta