Protindorov imunita transplantace Martin Lika Imunologie onkologickch onemocnn





























- Slides: 30

Protinádorová imunita, transplantace Martin Liška

Imunologie onkologických onemocnění

Protinádorová imunita • Selhání mechanismů regulace buněčného dělení a/nebo regulace sociálního chování buněk → maligní transformace buňky → nádorové bujení • Poruchy obvykle vyvolány mutacemi v onkogenech (→ abnormálně konstitutivně ↑ aktivita) nebo antionkogenech (→ abnormálně konstitutivně ↓ aktivita) • Nádorové bb. se buď liší od normálních jen málo (→ ignorovány imunitním systémem) nebo využívají mechanismy, jimiž paralyzují prostředky imunitního systému

Nádorové antigeny Antigeny specifické pro nádory (TSA) = nevyskytují se na normálních bb. • Komplexy MHC gp. I s abnormálními fragmenty buněčných proteinů – typické např. pro chemicky indukované nádory nebo některé leukémie asociované s chromozomálními translokacemi (např. Bcr-Abl vznikající přepisem fúzního genu na filadelfském chromozómu (vzniká translokací mezi chromozómy 9 a 22)) • Komplexy MHC gp. s fragmenty proteinů onkogenních virů (např. EBV, Polyomavirus) • Idiotypy myelomů a lymfomů – na povrchu klonotypické BCR, resp. TCR

Nádorové antigeny Antigeny asociované s nádory (TAA) = nacházejí se i na normálních bb. x odlišná kvantita exprese nebo abnormální časová nebo místní exprese • Onkofetální antigeny – normálně v embryonálních bb. , postnatálně na nádorových bb. – např. AFP (hepatomy), CEA (CA tl. střeva) • Melanomové antigeny – v menších množstvích na normálních melanocytech, silně na melanomových bb. např. MAGE-1 • Antigen HER 2/neu – v malém množství na normálních epiteliích, silně exprimován u některých CA prsu • PSA – zvýšeně exprimován u CA prostaty • Diferenciační antigeny leukemických bb. – normálně exprimovány na některých diferenciačních stádiích leukocytů, zvýšeně leukémie - např. CALLA

Protinádorové imunitní mechanismy • Hypotéza imunitní editace (teorie 3 E) – vzájemná interakce nádoru a imunitního systému • Eliminace – složky imunitního systému rozpoznávají a ničí nádorové bb. (imunogenní smrt nádorových bb. → exprimují molekuly, které signalizují přítomnost nebezpečí (DAMPs) → rozpoznání nádorových bb. imunitním systémem → aktivace plnohodnotné imunitní reakce → nespecifická odpověď (neutrofily, makrofágy, NK bb. ) + specifická odpověď (protilátky aktivující komplement, ADCC, Th 17, Tc)

Protinádorové imunitní mechanismy • Rovnováha (ekvilibrium) – v nádorových bb. mohou probíhat další mutace → varianty, které jsou odolnější vůči imunitnímu systému → imunitní systém dokáže kontrolovat růst nádoru, ale nedokáže jej zcela eliminovat → 3 možné scénáře: a/ kompletní eliminace nádoru b/ dlouhodobá dynamická rovnováha • c/ Únik (escape) – nádorové bb. uniknou kontrole imunitního systému → rozvoj onemocnění

Mechanismy odolnosti nádorů vůči imunitnímu systému • Variabilita – vznik mutantních forem, které nemají původní nádorové antigeny • Nízká hustota exprese nádorových antigenů → ignorace imunitním systémem • Nádorové bb. nefungují jako profesionální APC → prekurzory Tc a Th jsou utlumeny • Nádorové bb. neexprimují dostatečné množství DAMPs • Produkce látek s imunosupresivním účinkem faktory inaktivující T-lymfocyty, blokující faktory (TGF-b, IL-10, rozpustné formy nádorových antigenů)

Mechanismy odolnosti nádorů vůči imunitnímu systému • Exprese Fas. L → indukce apoptózy protinádorových bb. • Inhibice funkce nebo životnosti dendritických bb. – produkce NO, IL-10, TGF-b • Působení Treg – chrání nádory podobně jako normální tkáně před (auto)imunitními mechanismy • Podpora makrofágů – M 2 makrofágy mohou řadou mechanismů nádorům pomáhat (např. podpora angiogeneze, zvyšování invazivity, produkce imunosupresivních cytokinů)

Imunoterapie nádorů pomocí protilátek • Monoklonální protilátky (Mabb. ) – vazba na nádorový antigen → apoptóza nebo opsonizace nádorových bb. – např. Herceptin (Mab. reagující s HER 2/neu), Mabthera (Mab. reagující s CD 20 • Konjugáty Mabb. + toxiny (imunotoxiny) nebo radioizotopy (radioimunotoxiny) nebo léky (antibody drug conjugates) • Check-point inhibitory – MAbb. proti inhibičním receptorům (CTLA-4, PD-1) → zrušení inhibiční signalizace → odblokování reakce T-lymfocytů

Imunoterapie nádorů pomocí protilátek • Bispecifické protilátky – jedno vazebné místo reaguje s nádorovým antigenem a druhé se váže ne některou molekulu na povrchu T-lymfocytů nebo NK bb. ; Fc-část protilátky může navíc aktivovat Fcreceptory fagocytů nebo NK bb. ; např. blinatumomab (reakce s CD 19 leukemických blastů a CD 3 Tlymfocytů → lýza leukemické bb. )

Imunoterapie nádorů založená na buňkami zprostředkovaných mechanismech • Onkolytické viry – řada nepatogenních nebo mírně patogenních virů má tropismus k nádorovým bb. → lýza nádorových bb. → aktivace protinádorové imunity; zkouší se Reoviry, Adenoviry, modifikované viry HSV nebo Morbilli • Adoptivní T-buněčná terapie – namnožení pacientových T-lymfocytů ex vivo (event. úprava) → aplikace ve formě infúze (LAK z periferní krve, TIL z nádoru) • CAR bb. – podání in vitro geneticky modifikovaných bb. (zjm. T-lymfocytů, NK bb. ); do CAR bb. se pomocí Retroviru in vitro vloží konstrukt obsahující extracelulární část (Ab. ) a intracelulární signalizační doménu → CAR bb. se po specifickém rozpoznání nádorových bb. aktivují a zabijí je

Imunoterapie nádorů založená na buňkami zprostředkovaných mechanismech • Aktivní imunizace nádorovými antigeny a/ použití peptidových nádorových vakcin a DNA vakcin b/ vakciny na bázi virových vektorů – použití virového vektoru s vloženým nádorovým antigenem → indukce imunitní reakce proti antigenům c/ imunoterapie dendritickými buňkami – pomnožení DC in vitro → kultivace s nádorovými bb. → vrácení DC pacientovi • Nespecifická stimulace zánětu – aplikace mykobakteriální vakciny do místa nádoru → nepřímá provokace útoku na nádor • Imunoterapie T-lymfocyty dárce – Gv. L reakce

Transplantační imunologie

Předtransplantační imunologické vyšetření • Zásadní význam při transplantacích má HLA systém • Geny pro HLA vykazují význačný polymorfismus = u jednotlivých členů populace se na daném genovém lokusu mohou nacházet různé varianty genů (alely) • Haplotyp HLA = jedinečná kombinace alel, kódujících molekuly HLA, která se nachází na jednom chromozómu

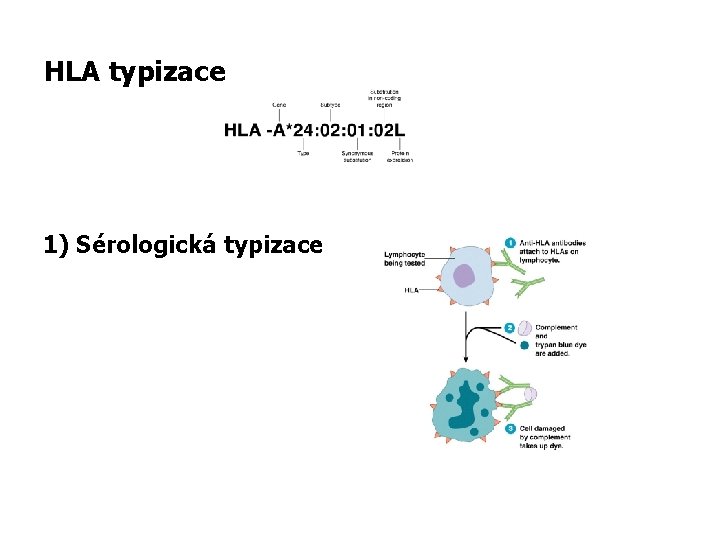
Laboratorní typizace HLA systému 1/ Sérotypizace – identifikace konkrétních HLA molekul I. a II. třídy pomocí typizačních sér - metoda časově méně náročná, ale méně přesná 2/ Genotypizace – vyšetření lidské DNA pomocí PCR - low resolution (skupiny alel), high resolution (jednotlivé alely) - časově náročnější, ale vysoce přesná metoda

HLA typizace 1) Sérologická typizace

2) Molekulárně genetické metody Genotypizace se používá k průkazu genových sekvencí, určujících konkrétní HLA výbavu. 2 a) PCR-Sekvenčně Specifické Primery 2 b) PCR-Sekvenčně Specifické Oligonukleotidy 2 c) PCR- Sequence Based Typing

Předpoklady provedení různých typů transplantace • Transplantace kostní dřeně (BMT) a kmenových buněk (SCT) - kompatibilita krevních skupin (u SCT není nutná), shoda v HLA A, B, C + HLA DR, DP, DQ (vyšetřují se obě alely, přípustné jsou 1 -2 neshody) • Ledviny – shoda v ABO systému, shoda nebo alespoň částečná shoda v HLA (zjm. II. tř. ) + negativní cross-match test na přirozené protilátky • Srdce a plíce – HLA typizace se z časových důvodů neprovádí, silná imunosuprese

Transplantační imunitaaloimunitní reakce • Lymfocyty příjemce rozpoznávají dárcovy HLA, protože jim připomínají komplex vlastních HLA s cizorodým peptidem • Antigeny dárce mohou být rozpoznávány dvěma způsoby: a/ Přímo – dárcovy HLA, přítomné na jeho APC, vážou jiné peptidové fragmenty buněčných proteinů → jsou příjemcovými T-lymfocyty rozpoznávány jako cizorodé b/ Nepřímo – antigeny ze štěpu jsou prezentovány příjemcovými APC a pak rozpoznávány jeho Tlymfocyty



Transplantační imunitaaloimunitní reakce Protilátky proti aloantigenům • Mohou se tvořit proti MHC nebo jiným povrchovým polymorfním antigenům • Negativně působí zjm. protilátky vážící komplement (cytotoxický účinek) • K tvorbě protilátek může dojít již před transplantací (např. po krevní transfúzi, opakovaných těhotenstvích)

Transplantační imunita - pojmy • Směsná lymfocytární reakce (mixed lymphocyte reaction) = lymfocyty dárce a příjemce se smíchají a kultivují in vitro → v případě reaktivity dojde k proliferaci lymfocytů → míra proliferace měřena pomocí inkorporace značeného nukleotidu do DNA → síla výsledné reakce odráží rozsah odlišnosti v HLA systému • Cross match = test na zjištění preformovaných protilátek (sérum příjemce se smíchá s lymfocyty dárce v přítomnosti komplementu → v případě přítomnosti preformovaných cytotoxických protilátek dojde k lýze dárcovských leukocytů)

Rejekce = odhojení transplantátu příjemcem, který jej vnímá jako cizorodý • Hyperakutní rejekce (minuty až hodiny) – zprostředkovaná preformovanými protilátkami (přirozené nebo po předchozích imunizacích) → fixace komplementu poškození endotelu + aktivace koagulace → trombóza cév štěpu; akumulace neutrofilů → amplifikace reakce • Akcelerovaná rejekce (3 -5 dnů) – nejč. vyvolána protilátkami, které neaktivují komplement • Akutní rejekce (dny až týdny) – zprostředkována T-lymfocyty ((Th 1 + Tc) → poškození buněk štěpu, endotelu) a protilátkami (váží se na endotel)

Rejekce • Chronická rejekce (měsíce až roky) – zprostředkována protilátkami (nejčastěji) nebo T-lymfocyty → poškození aloprotilátkami, fibrogenní faktory, cytokiny, stimulující růst cévního endotelu a hladké svaloviny a fibroblastů → poškození cév protilátkami → ischemizace tkáně → fibroprodukce → nahrazování funkční tkáně vazivem → ztráta funkce štěpu


Reakce štěpu proti hostiteli (Graft versus Host, Gv. H) = T-lymfocyty přítomné ve štěpu rozpoznávají tkáňové antigeny příjemce jako cizorodé a reagují proti nim 1/ Akutní Gv. H - několik dní až týdnů po transplantaci → poškození jater, kůže a střevní sliznice 2/ Chronická Gv. H – řadu měsíců až let po transplantaci → infiltrace tkání a orgánů Th 2 lymfocyty, tvorba aloprotilátek, produkce cytokinů → chronický zánět cév, kůže, vnitřních orgánů nebo žláz → náhrada funkční tkáně vazivem, poruchy prokrvení → ztráta funkce příslušných orgánů a tkání

Reakce štěpu proti leukemii (Gv. L) • Reakce dárcových T-lymfocytů vůči zbytkovým leukemickým buňkám • Mechanismus reakce je v zásadě shodný s Gv. HD • Snaha omezit Gv. H a podpořit Gv. L – např. použití suspenze kmenových buněk zbavené Tlymfocytů → po přihojení kostní dřeně aplikovat i. v. malé dávky T-lymfocytů dárce

Terapeutické možnosti potlačení rejekce a Gv. HD • Výběr vhodného dárce • Imunosuprese – po určité době koexistence oslabeného imunitního systému příjemce s allogenním transplantátem se vyvine částečná tolerance (ale je potřeba stále tlumit imunospresivními léky) • Odstranění T-lymfocytů dárce ze štěpu
 Tradicionalni i moderni roman
Tradicionalni i moderni roman Gorski kotar lika
Gorski kotar lika Moralna karakterizacija
Moralna karakterizacija Alegorijska pripovijetka
Alegorijska pripovijetka Arber lika
Arber lika Opseg lika
Opseg lika Dramske vrste 5 razred
Dramske vrste 5 razred Osobine likova ruzno pace
Osobine likova ruzno pace Kiklop vivijana
Kiklop vivijana Načelo lika in podlage
Načelo lika in podlage U registraturi likovi
U registraturi likovi Taktika darba laiks
Taktika darba laiks Tacrolimus
Tacrolimus Dnevnik pauline p.lektira
Dnevnik pauline p.lektira Filip i kyriales
Filip i kyriales Profesorica iz snova ppt
Profesorica iz snova ppt Simetrija naloge
Simetrija naloge Defabularizacija
Defabularizacija Xhosa prophetess
Xhosa prophetess Lika syndrome
Lika syndrome što je opseg
što je opseg Martin de bree
Martin de bree Value stream mapping karen martin
Value stream mapping karen martin Martin ester sfu
Martin ester sfu Protestant
Protestant Professor martin marshall
Professor martin marshall Santi martin
Santi martin Brett martin cascade price list
Brett martin cascade price list Sara strauß upb
Sara strauß upb Martin zielina
Martin zielina Martin lutero
Martin lutero