Ontleding en industrie Hoofdstuk 5 Ontleding en industrie





















- Slides: 22

Ontleding en industrie Hoofdstuk 5

Ontleding en industrie n n Verbrandingsreactie Vormingsreactie n n Oxidatiereactie n n H 2 O (l) H 2 O (g) Ontledingsreactie n n n 2 Fe + O 2 2 Fe. O Faseveranderingen n n N 2 +3 H 2 2 NH 3 Een reactie waarbij uit 1 stof, 2 of meer verschillende reactieprodukten worden gevormd Demo ammoniumdichromaat Ammoniumdichromaat(s) chroomoxide(s) + stikstof(g) + water (l)

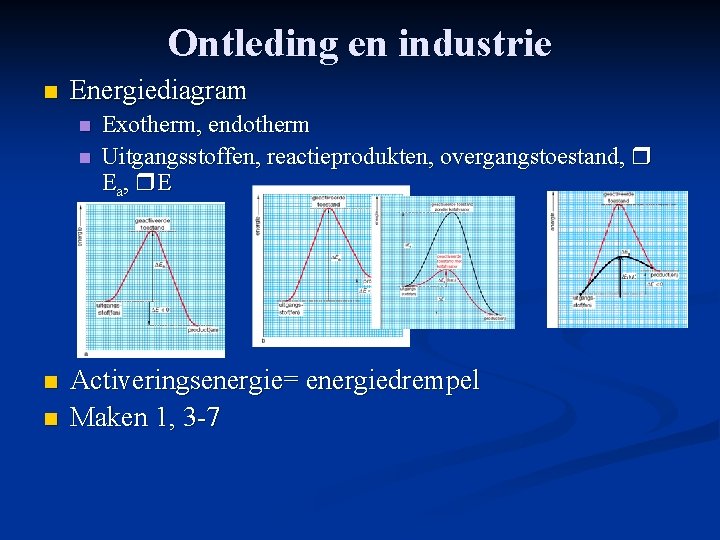
Ontleding en industrie n Energiediagram n n Exotherm, endotherm Uitgangsstoffen, reactieprodukten, overgangstoestand, E a , E Activeringsenergie= energiedrempel Maken 1, 3 -7

n Ontledingsreactie n n Calciumcarbonaat (s) Calciumoxide (s) (ongebluste kalk) en koolstofdioxide (g) n n n Een reactie waarbij uit 1 stof, 2 of meer verschillende reactieprodukten worden gevormd Ca. CO 3 Ca. O + CO 2 Ca. O + H 2 O Ca(OH)2 (gebluste kalk) Bespreken practicum n Suiker water + koolstof + brandbaar gas n n Water waterstofgas en zuurstofgas n n fotolyse = ontleding met behulp van licht Ontleding dynamiet n n electrolyse = ontleding met behulp van electriciteit Zilverchloride zilver en chloorgas n n Thermolyse= ontleding met behulp van verhitten 4 C 3 H 5(NO 3)3 (l)→ 12 CO 2 (g) + 10 H 2 O (g) + 6 N 2 (g) + O 2 (g) Maken 14 -21. (17 niet)

Bespreken t/m 21 n Thermolyse = ontledingsreactie onder invloed van temperatuur n Suiker n IJzererts n n n n 2 Fe 2 O 3 (s) 4 Fe (s) + 3 O 2 (g) Fe 2 O 3 (s) + 3 CO (g) 2 Fe (s) + 3 CO 2 (g) T=3000°C T=2000°C Fe is door C, nog bros. C verwijderen door O 2 over vloeibare ijzer te leiden. Er ontstaat CO Vergelijking? Productie ijzer Maken 22 -26

n Bespreken t/m 26 n Elektrolyse = ontledingsreactie onder invloed van electriciteit n Water, toestel van Hofmann 2 H 2 O (l) 2 H 2 (g) + O 2 (g) n Nadelen: explosief gas, opslag, weinig rendement brandstofcel, stroom nodig om H 2 te maken. n Voordeel: water is afval, H 2 is te maken n

IJsland n Brandstofcel n

Aluminium productie n Bauxiet n Al 2 O 3 n 2 Al 2 O 3 (s) 4 Al (l) + 3 O 2 (g) n Mengen met koper legering n Veel energie. Waar? IJsland n Huiswerk maken t/m 34, 29 niet n

Bespreken t/m 30 n Lezen 5. 6 n Maken 36 t/m 38 n Bespreken n

Elementen Kunnen niet ontleed worden ! Veel gebruikte indeling: metalen en niet-metalen Zie blz 56 voor periodiek systeem

Metalen Algemene kenmerken • Glimmend oppervlak • Geleiden warmte en elektriciteit • Kunnen vervormd worden • Kunnen in gesmolten toestand gemengd worden met andere metalen

Edelheid van metalen • Indeling metalen op basis van edelheid • Wat is corrosie? • Hoe edeler een metaal hoe minder corrosiegevoelig Het oppervlak van metalen is toch glimmend?

Edelheid • Edele metalen worden niet aangetast door water en lucht • Halfedele metalen worden niet aangetast door water en lucht maar wel door sommige zuren • Onedele metalen worden aangetast door water en lucht • Zeer onedele metalen reageren zelfs snel met vochtige lucht en water en moeten onder paraffineolie bewaard worden Filmpje natrium in water

Andere indeling: Lichte en zware metalen Lichte metalen hebben een lage dichtheid Voorbeelden: natrium, magnesium, aluminium, titaan Zware metalen hebben een grote dichtheid Voorbeelden: lood, cadmium, kwik Bij zware metalen denken we aan vergif

Legeringen • Een afgekoeld mengsel van samengesmolten metalen • Heef andere eigenschappen dan de afzonderlijke metalen • Bijv. Staal wordt roestvast (niet roestvrij!) gemaakt door legering met nikkel en chroom (Corus) Huiswerk Maken 42 t/m 47, behalve 46 Let op! Opgave 47 a: bij antwoord 3 moet staan Calcium is een zeer onedel metaal.

Niet-metalen Alle elementen die niet behoren tot de metalen zijn de niet-metalen Zie blz 56 voor periodiek systeem

Groep: edelgassen • Helium, Neon, Argon, Krypton en Xenon • Helemaal rechts in periodiek systeem • Reageren haast niet = inerte gassen • Helium: b. v. ballonvulling • Neon: b. v. neonverlichting! • Argon: zit bijvoorbeeld in gloeilampen zodat de gloeidraad niet verbrand Neonverlichting

Groep: halogenen • tweede groep van rechts in periodiek systeem • fluor, chloor, broom, jood • fluor is bij kamertemperatuur een geelgroen giftig gas • chloor is ook een giftig gas: gifgas in WO 1, chloortreinen • broom is bij kamertemperatuur een agressieve bruine vloeistof • jood is een zwartgrijze vaste stof: in water en alcohol als ontsmettingsmiddel gebruikt chloorgas in een fles

Element: fosfor • twee kristalvormen • witte fosfor: P 4 , is zeer licht ontvlambaar => fosfor brandbommen • rode fosfor: P, minder goed ontvlambaar => hulpstof in lucifers Element: koolstof • verschillende verschijningsvormen • grafiet en diamant: kristallijn koolstof • roet, cokes en Norit: amorf koolstof • grafiet kan elektriciteit geleiden : elektrodemateriaal • grafiet ook in potloden en als smeermiddel • diamant is zeer hard: b. v. diamantboren

Element: zwavel • geel • komt veel voor in vulkanische streken • gebruikt bij vulkaniseren van rubber Elementen: zuurstof en stikstof • hoofdcomponenten van lucht • zuurstof nodig voor verbranding • hoge temp. kunnen stikstof en zuurstof met elkaar reageren => NOx, zure regen

Element: waterstof • kleinste dichtheid • erg brandbaar! • gebruikt voor maken ammoniak, kunstmest en margarine • energiebron van de toekomst? Maken 48 -53 voor volgende keer af

Huiswerk