Nuclear Preguntas rectoras Es la radiacin peligrosa Es












- Slides: 37

Nuclear

Preguntas rectoras ¿Es la radiación peligrosa? ¿Es la energía atómica una buena opción? ¿Cuál es energía nuclear? ¿Son energía nuclear y las bombas nucleares ambas peligro

La energía del núcleo Bravo - 15. 000 kilotons

Desarrollo del átomo

Nuclear Fondo de la revisión Radiación nuclear Fisión Centrales nuclear Período Serie de decaimiento Fusión

Términos dominantes decaimiento alfa partículas alfa transmutación artificial radiación de fondo decaimiento beta partícula beta reacción en cadena palancas de mando masa crítica curie desintegraciones por segundo decaimiento gamma Contador de Geiger período radiación de ionización irradiado isótopo asesor radiactividad natural ecuación nuclear fisión nuclear fusión nuclear núclido plasma positrones radioisótopo rem roentgen trazalíneas transmutación Radiografías

Radiactividad Mucha de nuestra comprensión de la estructura atómica vino de estudios de elementos radiactivos. Radiactividad El proceso por el cual los átomos emiten espontáneo partículas o rayos de la alta energía de su núcleo. Primero observado cerca Enrique Becquerel en 1896

Historia: En el lado humano 1834 Michael Faraday - experimentos de la naturaleza eléctrica sugerida de la materia ánodo de la huelga de los rayos catódicos radiactividad bombardeo de la partícula alfa del berilio el primer radioisótopo artificial Otto 1938 Hahn, Fritz Strassmann, Lise Meitner, y Marie 1896 (Marya Sklodowska) y curie de Pedro - Otto Frisch - fisión nuclear descubierta de descubierto que la radiación es una característica del uranium-235 por el bombardeo del neutrón (Marie nombró este radiactivity de la característica. ) José 1897 J. Thomson - descubrió el electrón con experimentos del tubo de Crookes Curie de Marie 1898 y de Piere - descubrió Edwin 1940 M Mc. Millan y Philip Abelson - átomo, y no debido a la reacción química. Frederick 1934 Joliet y curie de Irene Joliet - producido Enrique 1896 Becquerel - “rayos uránicos descubiertos” y James 1932 Chadwick - descubrió el neutrón cerca 1895 roentgen de Wilhelm - radiografías descubiertas cuando transmutación de átomos electrólisis El Rutherford 1919 de Ernesto - anunció el primer artificial descubrió el primer elemento transuránico, neptunio, por la irradiación de neutrón del uranio en a ciclotrón Glenn 1941 T. Seaborg, Edwin M. Mc. Millan, José

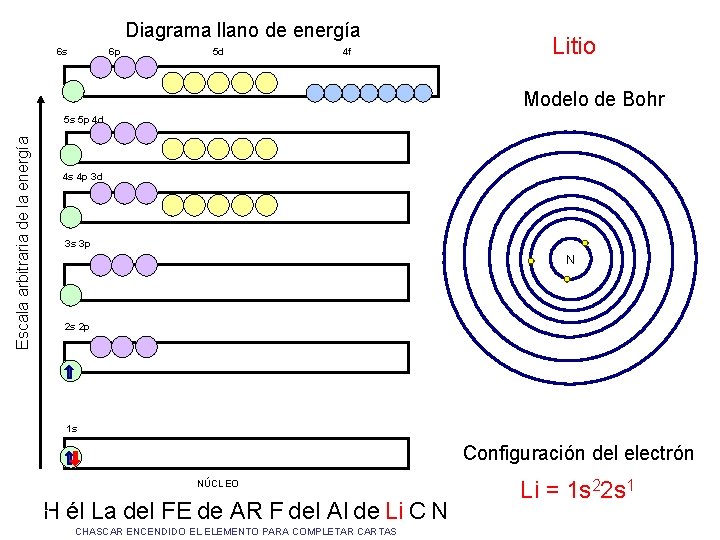
Diagrama llano de energía 6 s 6 p 5 d 4 f Modelo de Bohr 5 s 5 p 4 d Escala arbitraria de la energía Litio 4 s 4 p 3 d 3 s 3 p N 2 s 2 p 1 s Configuración del electrón NÚCLEO H él La del FE de AR F del Al de Li C N CHASCAR ENCENDIDO EL ELEMENTO PARA COMPLETAR CARTAS Li = 1 s 22 s 1

Un átomo emocionado del litio Energía Átomo emocionado de Li Fotón de luz roja emitido Átomo de Li adentro estado de una energía m Zumdahl, De. Coste, mundo de la química 2002, página 326

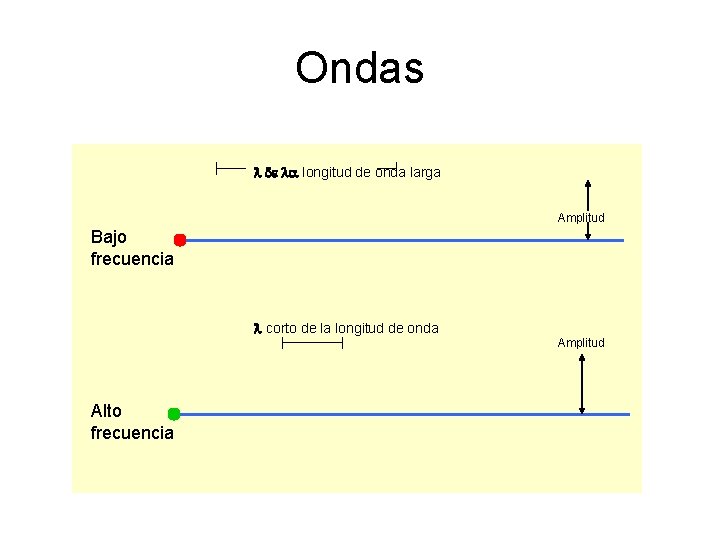
Ondas l de la longitud de onda larga Amplitud Bajo frecuencia l corto de la longitud de onda Alto frecuencia Amplitud

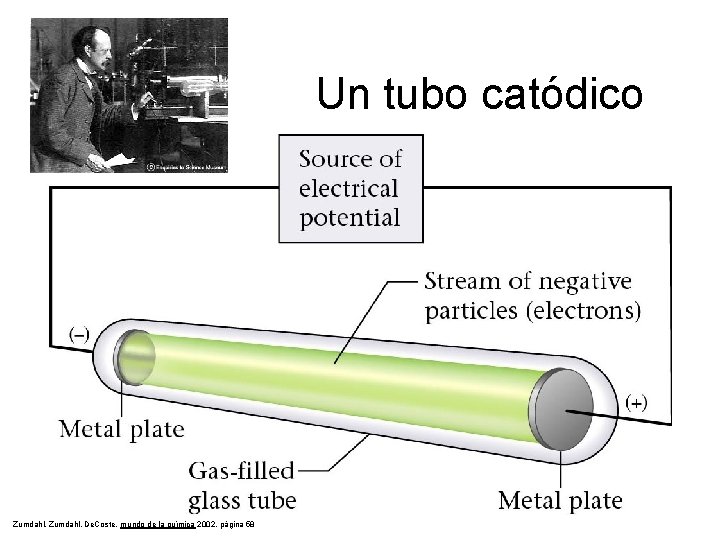
Un tubo catódico Zumdahl, De. Coste, mundo de la química 2002, página 58

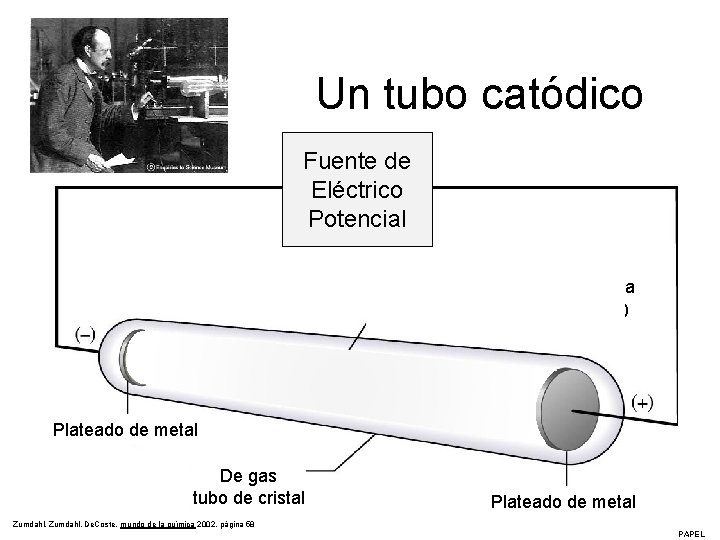
Un tubo catódico Fuente de Eléctrico Potencial Corriente de la negativa partículas (electrones) Plateado de metal De gas tubo de cristal Plateado de metal Zumdahl, De. Coste, mundo de la química 2002, página 58 PAPEL

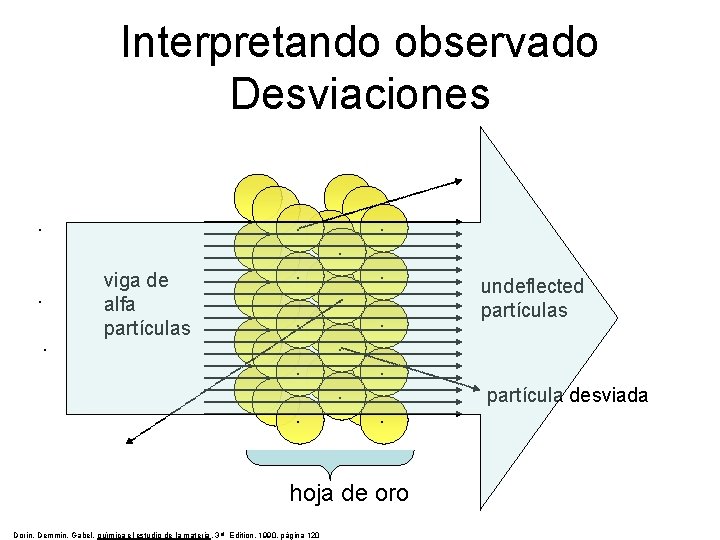
Interpretando observado Desviaciones. . . viga de alfa partículas . . . hoja de oro Dorin, Demmin, Gabel, química el estudio de la materia, 3 rd Edition, 1990, página 120 undeflected partículas partícula desviada

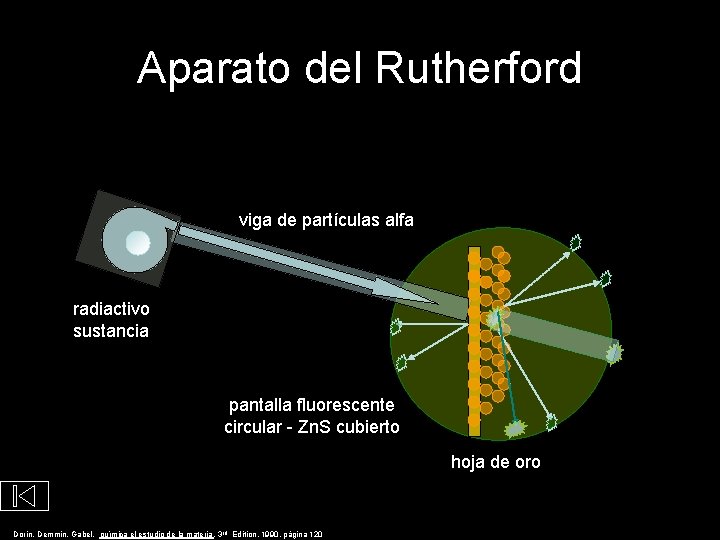
Aparato del Rutherford viga de partículas alfa radiactivo sustancia pantalla fluorescente circular - Zn. S cubierto hoja de oro Dorin, Demmin, Gabel, química el estudio de la materia, 3 rd Edition, 1990, página 120

Fotón • En 1905, Einstein postuló que la luz fue compuesta de partículas de la energía discreta E = hf • Él llamó estos FOTONES de las partículas • Él también sugirió que en el efecto fotoeléctrico cada uno el solo fotón da para arriba toda su energía a un solo electrón • Él sugirió que el electrón fuera expulsado inmediatamente • El aumento de la intensidad de la luz aumenta el número de los electrones pero no de la energía de los electrones

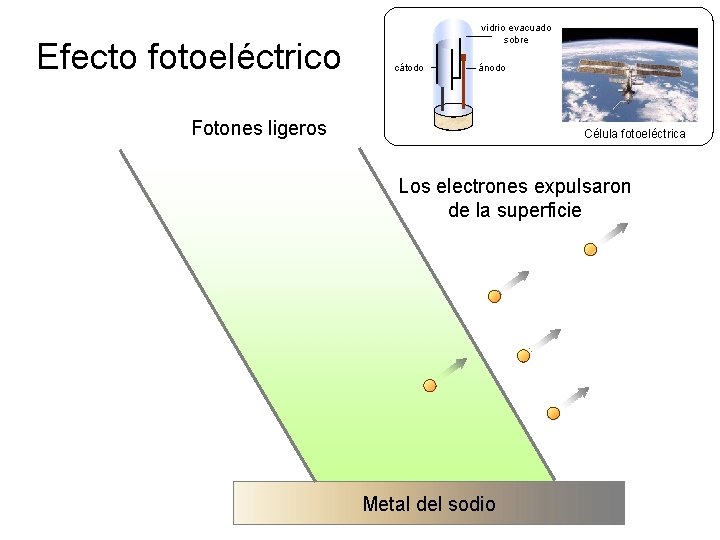
Efecto fotoeléctrico vidrio evacuado sobre cátodo ánodo Representación simbólica de una célula fotoeléctrica Fotones ligeros Célula fotoeléctrica Los electrones expulsaron de la superficie Metal del sodio

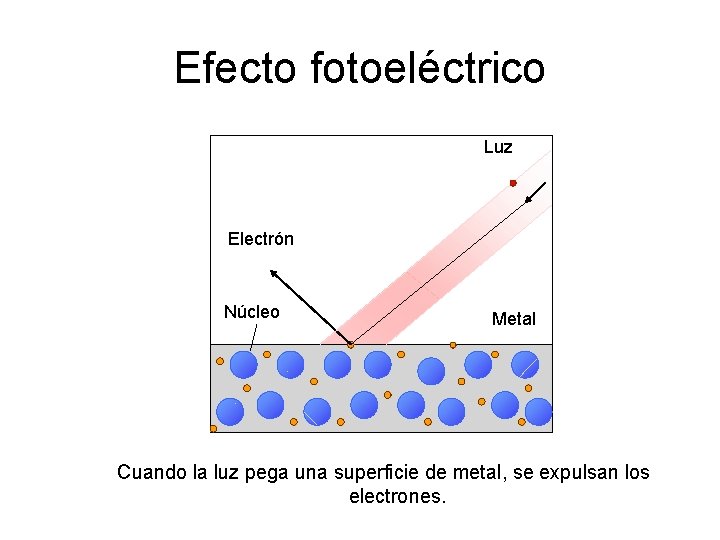
Efecto fotoeléctrico Luz Electrón Núcleo Metal Cuando la luz pega una superficie de metal, se expulsan los electrones.

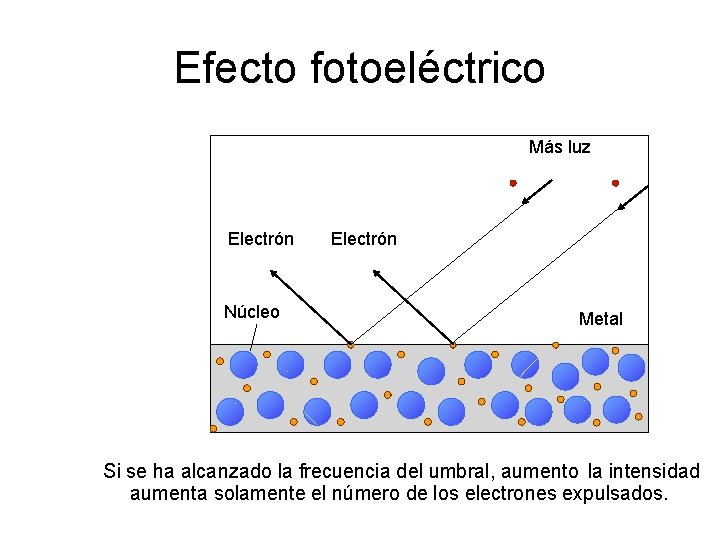
Efecto fotoeléctrico Más luz Electrón Núcleo Electrón Metal Si se ha alcanzado la frecuencia del umbral, aumento la intensidad aumenta solamente el número de los electrones expulsados.

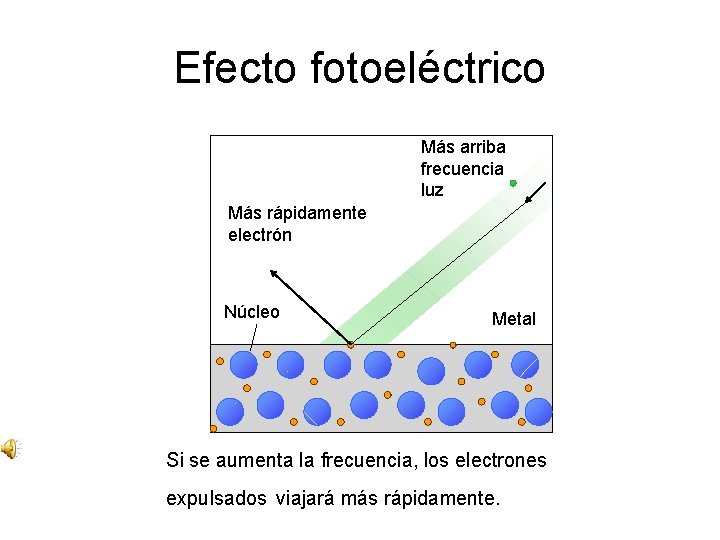
Efecto fotoeléctrico Más arriba frecuencia luz Más rápidamente electrón Núcleo Metal Si se aumenta la frecuencia, los electrones expulsados viajará más rápidamente.

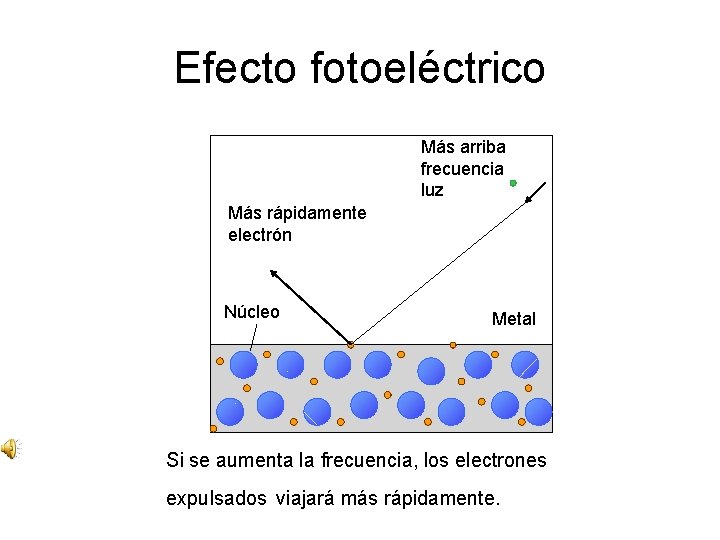
Efecto fotoeléctrico Más arriba frecuencia luz Más rápidamente electrón Núcleo Metal Si se aumenta la frecuencia, los electrones expulsados viajará más rápidamente.

Fuerte contra fuerza débil Fuerza débil: atracciones electrostáticas entre los protones y los electrones en áto Fuerza débil e. g. vinculación covalente, vinculación iónica, vinculación del hidró Granes fuerzas: forzar que mantiene el núcleo unido. Granes fuerzas es decir. El núcleo contiene los protones que rechazan naturalmen otro. Las granes fuerzas mantienen el núcleo unido. Cuando el núcleo está partido, la energía lanzada es energía de las granes fuerzas.

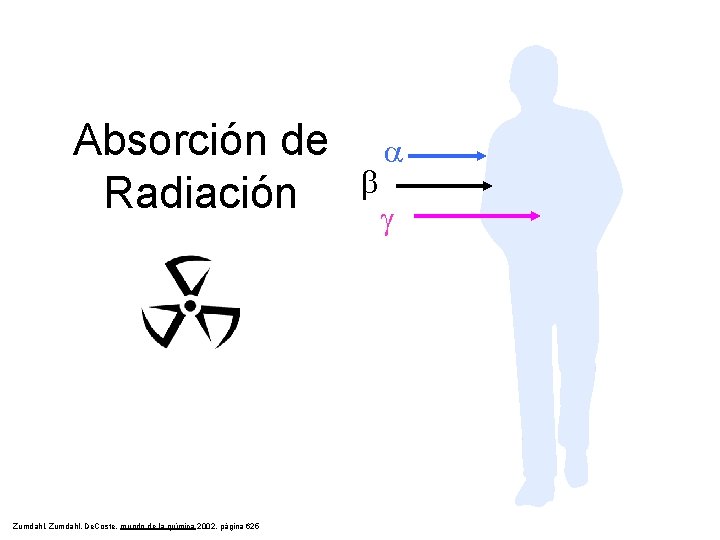
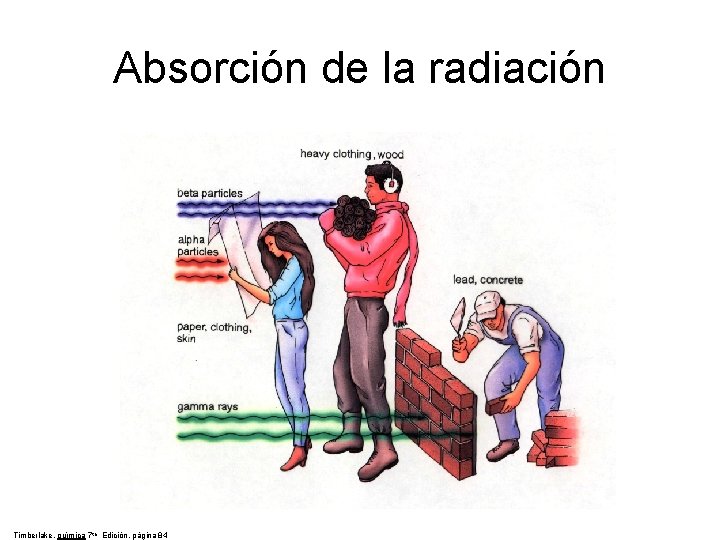
Absorción de Radiación Zumdahl, De. Coste, mundo de la química 2002, página 625 b a g

Absorción de la radiación Timberlake, química 7 th Edición, página 84

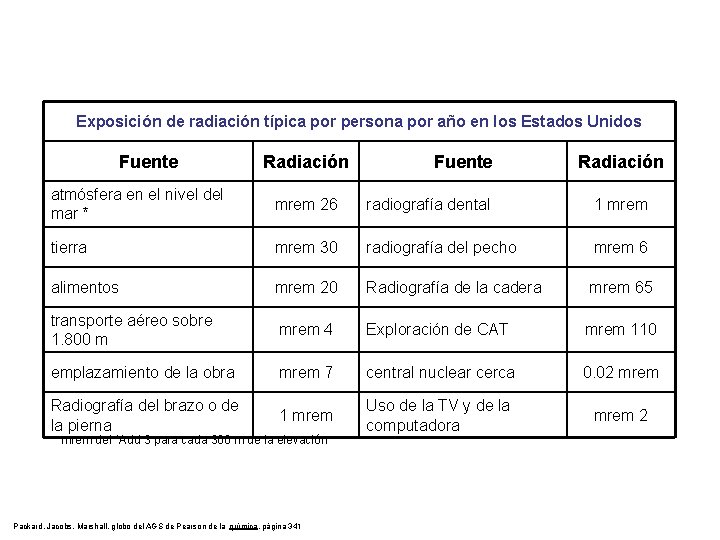
Exposición de radiación típica por persona por año en los Estados Unidos Fuente Radiación atmósfera en el nivel del mar * mrem 26 radiografía dental 1 mrem tierra mrem 30 radiografía del pecho mrem 6 alimentos mrem 20 Radiografía de la cadera mrem 65 transporte aéreo sobre 1. 800 m mrem 4 Exploración de CAT mrem 110 emplazamiento de la obra mrem 7 central nuclear cerca 0. 02 mrem Radiografía del brazo o de la pierna 1 mrem Uso de la TV y de la computadora mrem 2 mrem del *Add 3 para cada 300 m de la elevación Packard, Jacobs, Marshall, globo del AGS de Pearson de la química, página 341

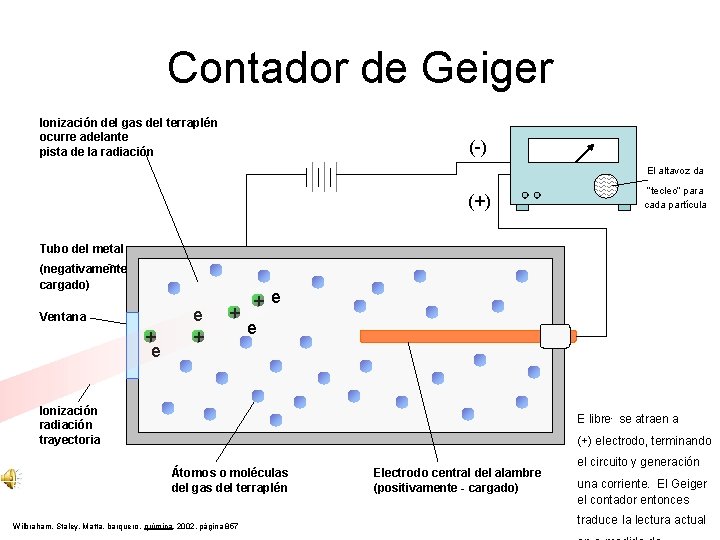
Contador de Geiger Ionización del gas del terraplén ocurre adelante pista de la radiación (-) El altavoz da (+) “tecleo” para cada partícula Tubo del metal (negativamente cargado) Ventana + e e + + + e e Ionización radiación trayectoria E libre- se atraen a (+) electrodo, terminando Átomos o moléculas del gas del terraplén Wilbraham, Staley, Matta, barquero, química, 2002, página 857 Electrodo central del alambre (positivamente - cargado) el circuito y generación una corriente. El Geiger el contador entonces traduce la lectura actual

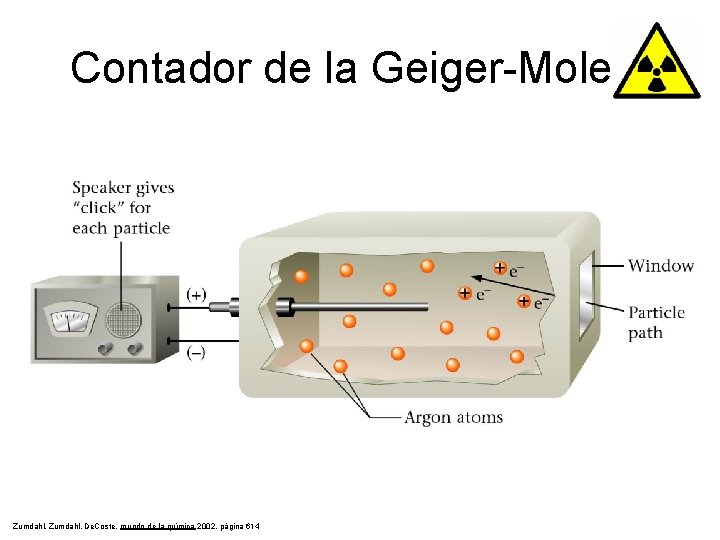
Contador de la Geiger-Moleta Zumdahl, De. Coste, mundo de la química 2002, página 614

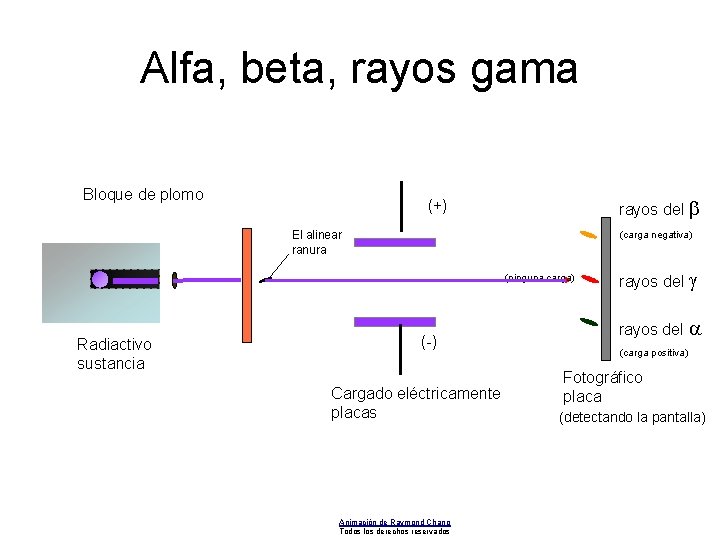
Alfa, beta, rayos gama Bloque de plomo rayos del b (+) (carga negativa) El alinear ranura (ninguna carga) Radiactivo sustancia (-) Cargado eléctricamente placas Animación de Raymond Chang Todos los derechos reservados rayos del g rayos del a (carga positiva) Fotográfico placa (detectando la pantalla)

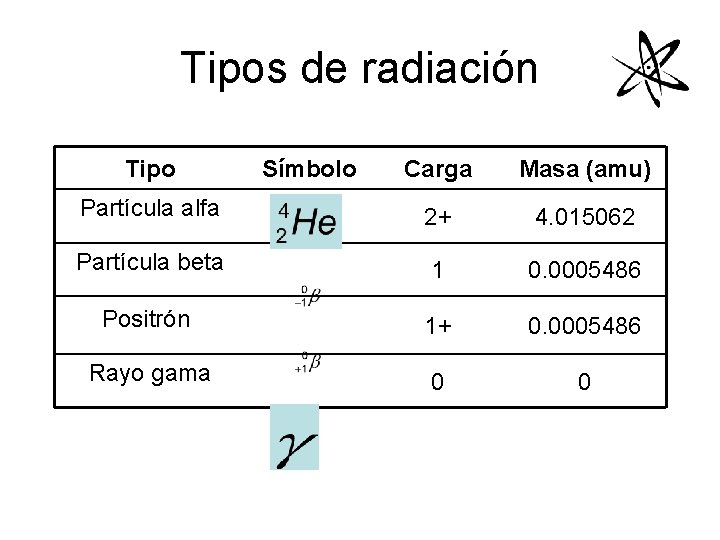
Tipos de radiación Tipo Símbolo Carga Masa (amu) Partícula alfa 2+ 4. 015062 Partícula beta 1 0. 0005486 Positrón 1+ 0. 0005486 Rayo gama 0 0

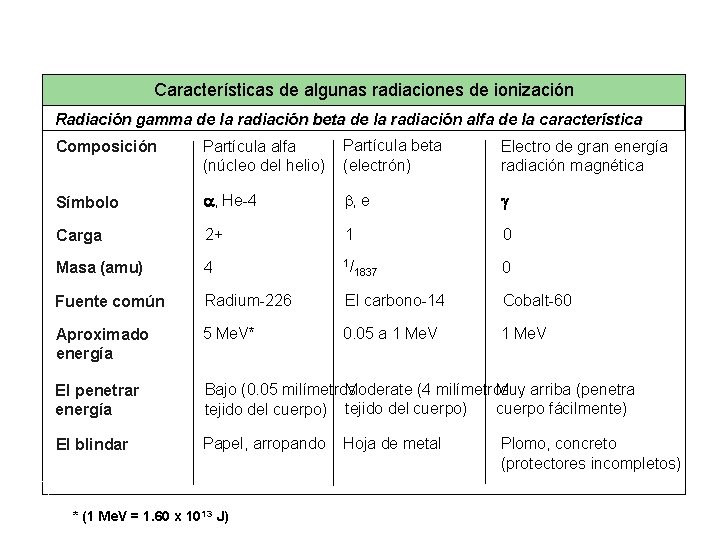
Características de una cierta radiación de ionización Características de algunas radiaciones de ionización Radiación gamma de la radiación beta de la radiación alfa de la característica Composición Partícula alfa (núcleo del helio) Partícula beta (electrón) Electro de gran energía radiación magnética Símbolo a, He-4 b, e g Carga 2+ 1 0 Masa (amu) 4 1/ Fuente común Radium-226 El carbono-14 Cobalt-60 Aproximado energía 5 Me. V* 0. 05 a 1 Me. V El penetrar energía Moderate (4 milímetros Muy arriba (penetra Bajo (0. 05 milímetros cuerpo fácilmente) tejido del cuerpo) El blindar Papel, arropando * (1 Me. V = 1. 60 x 1013 J) 1837 Hoja de metal 0 Plomo, concreto (protectores incompletos)

Reacciones nucleares Demostración nuclear de las ecuaciones cómo los átom Similar a las ecuaciones químicas. - debe todavía balancear la masa y cargar. Diferenciar de ecuaciones químicas porque - podemos cambiar los elementos. … transmutación - el tipo de isótopo es importante.

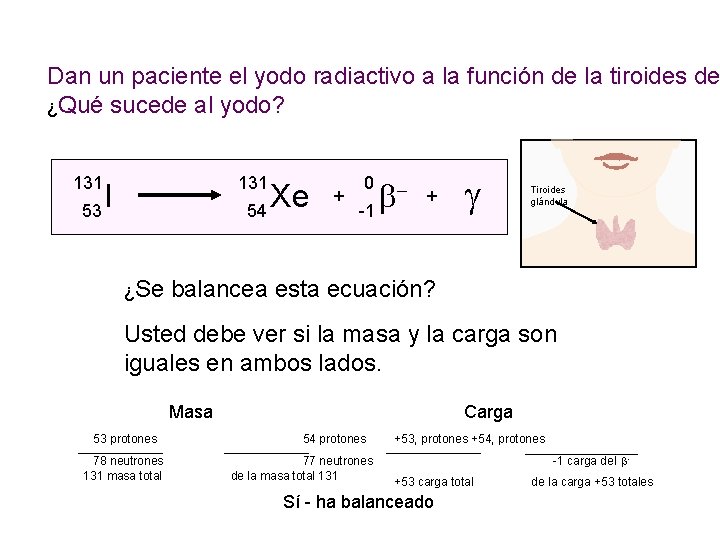
Dan un paciente el yodo radiactivo a la función de la tiroides de ¿Qué sucede al yodo? 131 I 53 Xe 54 + 0 b -1 + g Tiroides glándula ¿Se balancea esta ecuación? Usted debe ver si la masa y la carga son iguales en ambos lados. Masa 53 protones 78 neutrones 131 masa total Carga +53, protones +54, protones 77 neutrones -1 carga del b de la masa total 131 +53 carga total de la carga +53 totales Sí - ha balanceado 54 protones

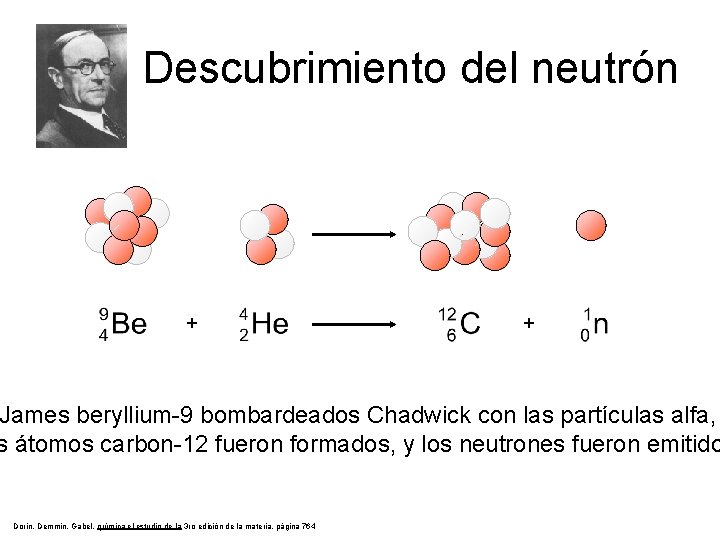
Descubrimiento del neutrón + + James beryllium-9 bombardeados Chadwick con las partículas alfa, s átomos carbon-12 fueron formados, y los neutrones fueron emitido Dorin, Demmin, Gabel, química el estudio de la 3 ro edición de la materia, página 764

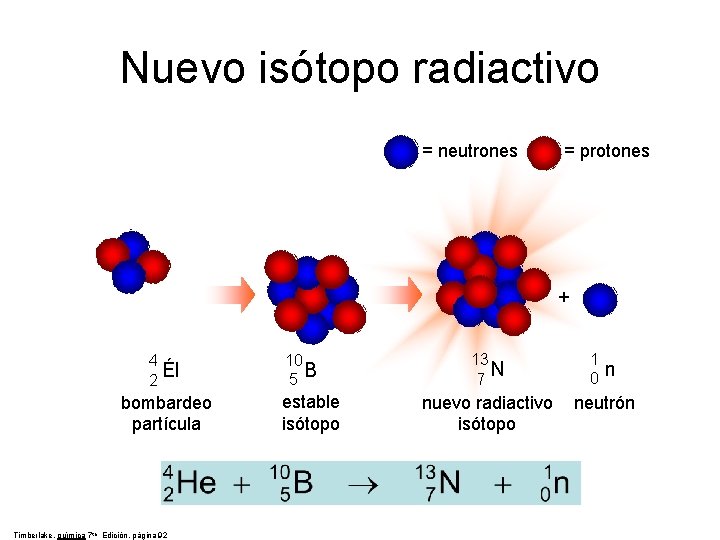
Nuevo isótopo radiactivo = neutrones = protones + 4 Él 2 bombardeo partícula Timberlake, química 7 th Edición, página 92 10 B 5 estable isótopo 13 N 7 nuevo radiactivo isótopo 1 0 n neutrón

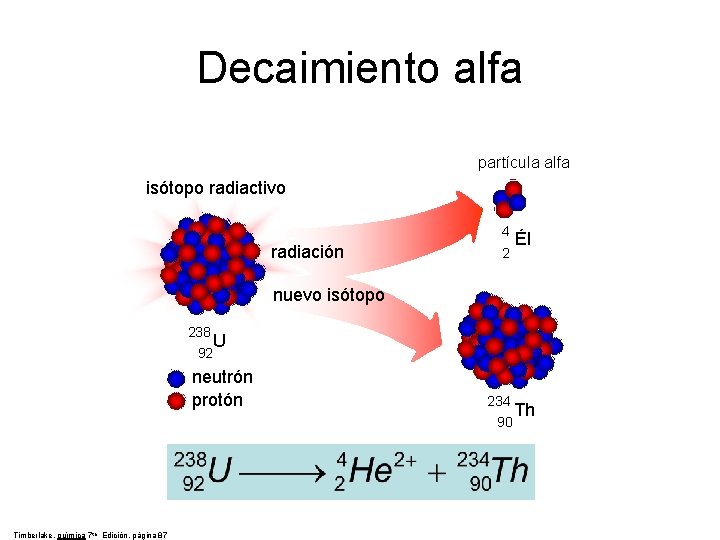
Decaimiento alfa partícula alfa isótopo radiactivo radiación 4 Él 2 nuevo isótopo 238 U 92 neutrón protón Timberlake, química 7 th Edición, página 87 234 Th 90

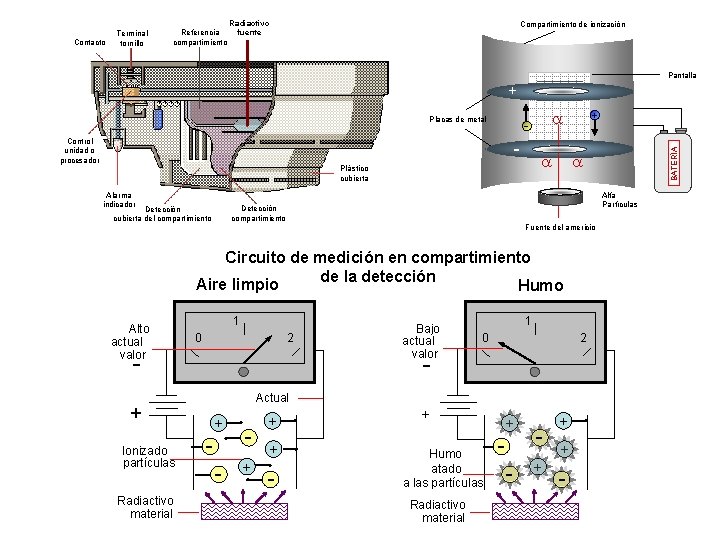
Contacto Terminal tornillo Referencia compartimiento Radiactivo fuente Compartimiento de ionización Pantalla + Control unidad o procesador - Alfa Partículas Detección compartimiento Detección cubierta del compartimiento + a a Plástico cubierta Alarma indicador a - Fuente del americio Circuito de medición en compartimiento de la detección Aire limpio Humo Alto actual valor 1 2 0 - Ionizado partículas Radiactivo material Bajo actual valor 1 0 2 - Actual + + - + + + - BATERÍA Placas de metal + Humo atado a las partículas Radiactivo material + - + + + -

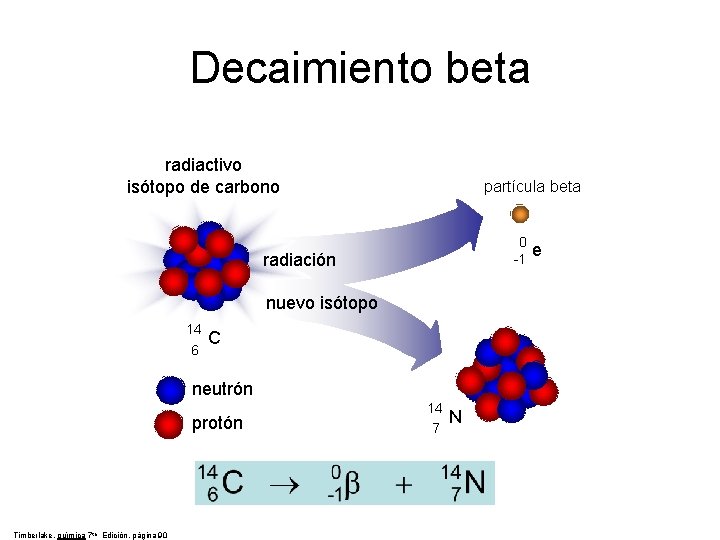
Decaimiento beta radiactivo isótopo de carbono partícula beta 0 e radiación -1 nuevo isótopo 14 6 C neutrón protón Timberlake, química 7 th Edición, página 90 14 7 N