KISRLETI FIZIKA III HTAN BALZS ZOLTN BMF KVK

KISÉRLETI FIZIKA III HŐTAN BALÁZS ZOLTÁN BMF, KVK, MTI 2008.

KISÉRLETI FIZIKA Termodinamika (klasszikus hőtan) A termodinamika fizikának az a tudományága, amelyik azokat a jelenségeket írja le, amelyekben a hőenergiának és a hőmérsékletnek meghatározó szerepe van

KISÉRLETI FIZIKA Termodinamika A hőtan legfontosabb mennyiségei: - hőmérséklet: az SI mértékegység rendszerben alapmennyiség, hatására a testek térfogat változást mutatnak. Jele: T mértékegysége: K (Kelvin) definíciója: gázhőmérő által meghatározott A hőmérséklet állapot változó.

KISÉRLETI FIZIKA Termodinamika A hőtan legfontosabb mennyiségei: - nyomás: a nyomóerő és a nyomott felület hányadosa. Jele: p mértékegysége: N/m 2 (pascal) definíciója: p=F/A, ahol A a nyomott felület A nyomás állapotváltozó.

KISÉRLETI FIZIKA Termodinamika A hőtan legfontosabb mennyiségei: - térfogat: Jele: V mértékegysége: m 3 A térfogat állapotváltozó. Az állapotváltozók (hőmérséklet, nyomás, térfogat) egyértelműen meghatározzák a termodinamikai rendszer állapotát.

KISÉRLETI FIZIKA Termodinamika A hőtan legfontosabb mennyiségei: - hőenergia: másként hő, vagy hőmennyiség, a testek hőmérséklet változásához szükséges energia. Jele: Q mértékegysége: J (joule) definíciója: a testek hőmérséklet változásához szükséges energia. Q=CnΔT=cmΔT ahol C [J/mol. K] a molhő, c [J/kg. K] a fajhő. A hőenergia nem állapotváltozó.

KISÉRLETI FIZIKA Termodinamika Szilárd testek termodinamikája. Lineáris hőtágulás. Térfogat és alaktartó rendszer. l=l 0(1+αΔT) ΔT=T-T 0 ahol, l a test hossza a T hőmérsékleten l 0 a test hossza a T 0 hőmérsékleten T 0 a referencia hőmérséklet T a vizsgálati hőmérséklet α a lineáris hőmérsékleti együttható

KISÉRLETI FIZIKA Termodinamika Szilárd testek termodinamikája. Térfogati hőtágulás V=V 0(1+βΔT) ΔT=T-T 0 ahol, V a test térfogata a T hőmérsékleten V 0 a test térfogata a T 0 hőmérsékleten T 0 a referencia hőmérséklet T a vizsgálati hőmérséklet β a térfogati hőmérsékleti együttható, β=3 α

KISÉRLETI FIZIKA Termodinamika Folyadékok termodinamikája. Térfogati hőtágulás. Térfogattartó rendszer. V=V 0(1+βΔT) ΔT=T-T 0 ahol, V a test térfogata a T hőmérsékleten V 0 a test térfogata a T 0 hőmérsékleten T 0 a referencia hőmérséklet T a vizsgálati hőmérséklet β a térfogati hőmérsékleti együttható, β=3 α

KISÉRLETI FIZIKA Termodinamika Gázok termodinamikája. A három állapotváltozó mindegyike változhat, a vizsgálat során nagyon gyakran az egyiket állandó értéken tartjuk, így egyszerűbb a vizsgálat és a valóságot is ez gyakran leírja. - p=állandó, nyomástartó, vagy izobár rendszer V=V 0(1+βΔT) β=1/273 [1/K] Gay-Lussac I. törvénye.

KISÉRLETI FIZIKA Termodinamika Gázok termodinamikája. - V=állandó, térfogattartó, vagy izochor rendszer V=V 0(1+βΔT) β=1/273 [1/K] Gay-Lussac II. törvénye.

KISÉRLETI FIZIKA Termodinamika Gázok termodinamikája. - T=állandó, hőmérséklettartó, vagy izoterm rendszer p. V=p 0 V 0=állandó Boyle-Mariotte törvény

KISÉRLETI FIZIKA Termodinamika Gázok termodinamikája. Az egyesített gáztörvény. A fenti három egyenlet figyelembevételével, ha mindhárom változó változik, akkor a rendszer az egyesített gáztörvény szerint vizsgálható: p. V/T=p 0 V 0/T 0=állandó ahol a p 0, V 0, T 0 a normál állapotú gáz jellemzői: p 0=1, 01 105 Pa; T 0=273, 15 K; V 0, a normál állapotú gáz térfogata.

KISÉRLETI FIZIKA Termodinamika Gázok termodinamikája. Az egyesített gáztörvény. A fenti egyenletet kis átalakításokkal további egyenletekként is megadhatjuk: p. V/T=n. R=állandó ahol, R az univerzális gázállandó, amely minden gáz esetén azonos: R=8, 314 J/mol. K, n a rendszerben található gáz anyagmennyisége.

KISÉRLETI FIZIKA Termodinamika Anyagmennyiség: az SI rendszerben alapmennyiség: jele: n mértékegysége: mol definiciója: egy molnyi az, az anyagmennyiség, amelyben ugyanannyi részecske van, mint 12 g C 12 –es szénizotópban, azaz NA=6, 023 1023 db/mol.

KISÉRLETI FIZIKA Termodinamika Gázok termodinamikája. Az egyesített gáztörvény. A fenti egyenletet kis átalakításokkal további egyenletekként is megadhatjuk: p. V/T=(m/M)R=állandó ahol, M az egy molnyi anyag tömege, a moltömeg, n a rendszerben található gáz anyagmennyisége.

KISÉRLETI FIZIKA Termodinamika Gázok termodinamikája. Az egyesített gáztörvény. A fenti egyenletet kis átalakításokkal további egyenletekként is megadhatjuk: p. V/T=Nk=állandó ahol, N a rendszerben található anyag részecskéinek száma k a Boltzmann állandó: k=1, 38 10 -23 J/K

KISÉRLETI FIZIKA Termodinamika Gázok állapotváltozásai: -izobár állapotváltozás, p=állandó p 1 V 1/T 1=p 2 V 2/T 2 ezért ahol p 1=p 2=p V 1/T 1=V 2/T 2 Hőenergia hozzávezetése esetén nő a térfogat és a hőmérséklet, a gáz kitágul. Q=CpnΔT Cp az állandó nyomáshoz tartozó molhő Cp =((f+2)/2)R

Termodinamika KISÉRLETI FIZIKA Gázok állapotváltozásai:

Termodinamika KISÉRLETI FIZIKA Gázok állapotváltozásai: p=állandó V/T=áll

Termodinamika KISÉRLETI FIZIKA Gázok állapotváltozásai: -izobár állapotváltozás, p=állandó

KISÉRLETI FIZIKA Termodinamika Gázok állapotváltozásai: -izochor állapotváltozás, V=állandó p 1 V 1/T 1=p 2 V 2/T 2 ezért ahol V 1=V 2=V p 1/T 1=p 2/T 2 Hőenergia hozzávezetése esetén nő a nyomás és a hőmérséklet. A gáz térfogati munkát nem végez, Wt =0 J. Q=CVnΔT CV az állandó nyomáshoz tartozó molhő. CV =(f/2)R
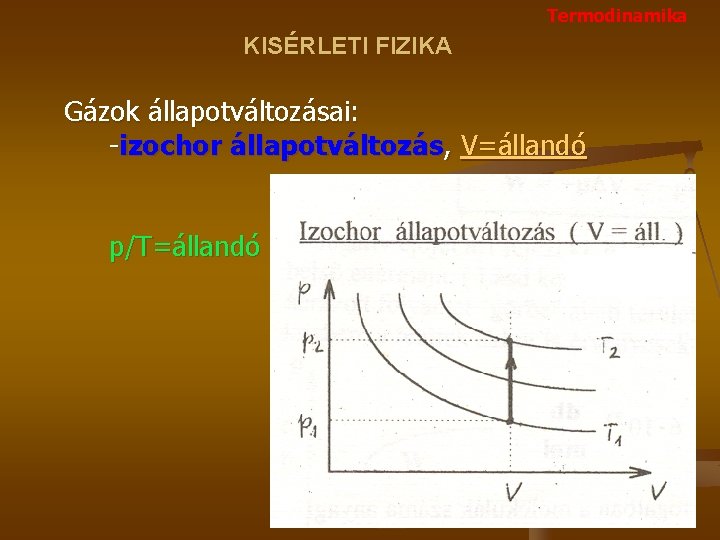
Termodinamika KISÉRLETI FIZIKA Gázok állapotváltozásai: -izochor állapotváltozás, V=állandó p/T=állandó

Termodinamika KISÉRLETI FIZIKA Gázok állapotváltozásai: -izochor állapotváltozás, V=állandó

Termodinamika KISÉRLETI FIZIKA Gázok állapotváltozásai: -izoterm állapotváltozás, T=állandó p 1 V 1/T 1=p 2 V 2/T 2 ezért ahol T 1=T 2=T p 1 V 1=p 2 V 2=állandó Hőenergia hozzávezetése esetén nő a térfogat és a nyomás csökken, a gáz térfogati munkát végez Wt. Q=n. RTln(V 2/V 1) =Wt

Termodinamika KISÉRLETI FIZIKA -izoterm állapotváltozás, T=állandó

Termodinamika KISÉRLETI FIZIKA -izoterm állapotváltozás, T=állandó

KISÉRLETI FIZIKA Termodinamika -adiabatikus állapotváltozás, Q=0 J p 1 V 1 κ =p 2 V 2κ=állandó, ahol κ=Cp/CV A gáz a belsőenergiáját felhasználva növeli a térfogatát, a nyomása csökken, eközben a gáz térfogati munkát végez Wt. - C V n ΔT = W t
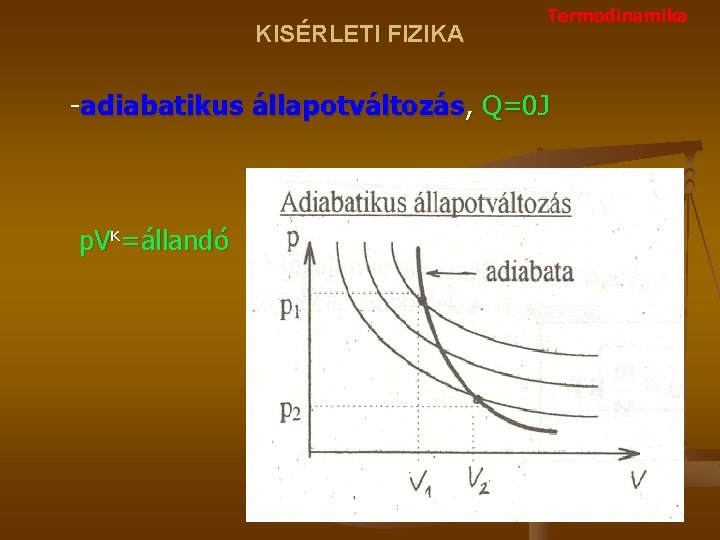
KISÉRLETI FIZIKA Termodinamika -adiabatikus állapotváltozás, Q=0 J p. Vκ=állandó

KISÉRLETI FIZIKA n Termodinamika Körfolyamatok: A körfolyamat az állapotváltozások olyan sorozata, amelynek a végén a termodinamikai rendszer visszatér a kiindulási állapotába, így a folyamat végén a belső energia ugyanakkora mint a kezdeti volt.
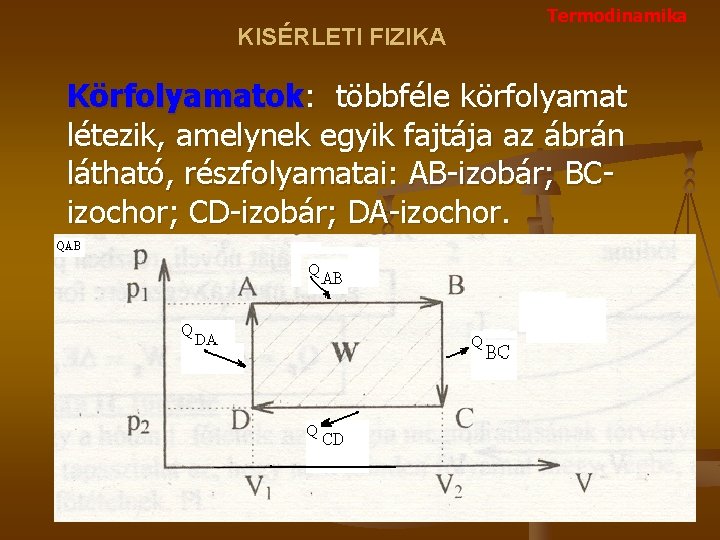
KISÉRLETI FIZIKA Termodinamika Körfolyamatok: többféle körfolyamat létezik, amelynek egyik fajtája az ábrán látható, részfolyamatai: AB-izobár; BCizochor; CD-izobár; DA-izochor.

KISÉRLETI FIZIKA Termodinamika A körfolyamat során hasznos munkát úgy írhatjuk fel, hogy az egyes részfolyamatok során végzett munkákat összegezzük: WAB=p 1(V 2 -V 1) WBC=0 J WCD=p 2(V 1 -V 2) WDA=0 J

KISÉRLETI FIZIKA Termodinamika A körfolyamat során hasznos munkát úgy írhatjuk fel, hogy az egyes részfolyamatok során végzett munkákat összegezzük: Wh=WAB+WBC+WCD+WDA Wh=p 1(V 2 -V 1) +p 2(V 1 -V 2) Wh=(p 1 -p 2 )(V 2 -V 1)

KISÉRLETI FIZIKA Termodinamika

KISÉRLETI FIZIKA Termodinamika

KISÉRLETI FIZIKA Termodinamika

KISÉRLETI FIZIKA Termodinamika

KISÉRLETI FIZIKA Termodinamika

Termodinamika KISÉRLETI FIZIKA Gázkeveredés:

KISÉRLETI FIZIKA Termodinamika
- Slides: 40