KALCIJUM Autor Jelena Muci Nastavnik hemije O Jovan











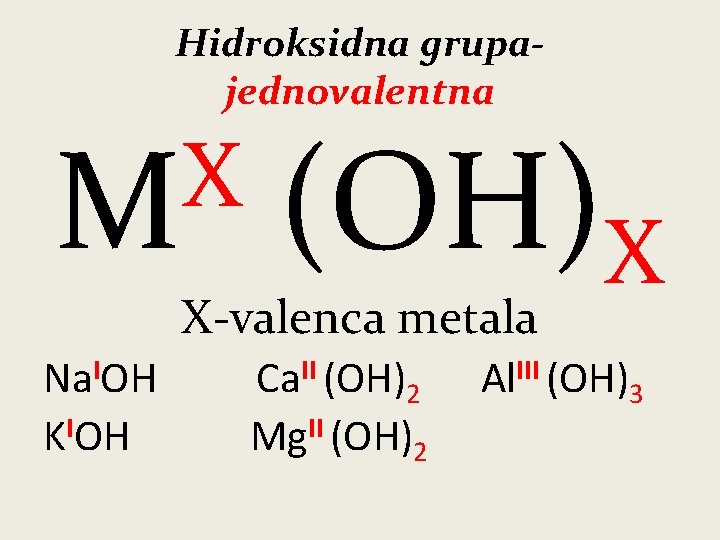









- Slides: 27

KALCIJUM Autor Jelena Mucić Nastavnik hemije OŠ “Jovan Dučić” Beograd

Nalaženje • U prirodi se ne nalazi u elementarnom stanju • U Zemljinoj kori-stene, rude, minerali. . . • U morskoj, rečnoj, mineralnoj vodi (tvrda voda)

PAMUKALE Pamukkale ili dvorac pamuka u Turskoj predstavlja formaciju krečnjaka gde se taloženjem kalcijuma formiraju oblici u vidu terasa koje ispunjava čista prozirna voda. Usled tektonskih raseda dolašlo je do izdizanja i spuštanja tla u bazenu reke Menderes i otvaranja izvora vruće mineralne vode koja snabdeva vodom ove terase prelivajući se iz jedne u drugu stvarajući ovaj prirodni fenomen. Temperatura izvorske vode iznosi oko 33 stepena C.

� Biogeni element

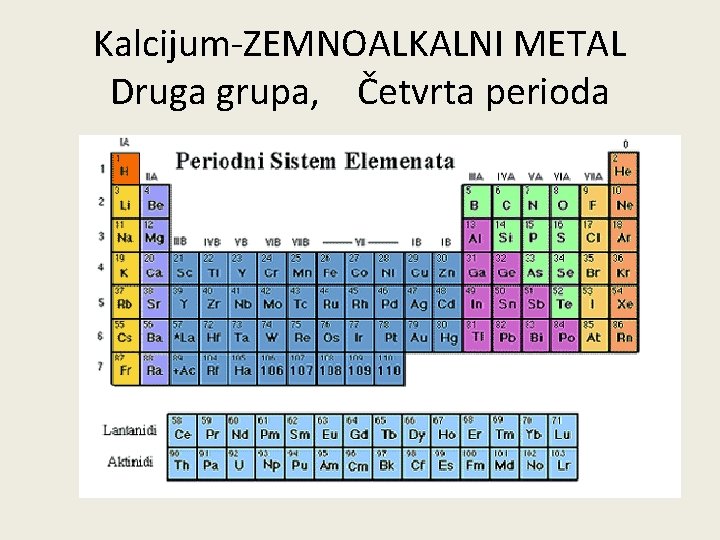
Kalcijum-ZEMNOALKALNI METAL Druga grupa, Četvrta perioda

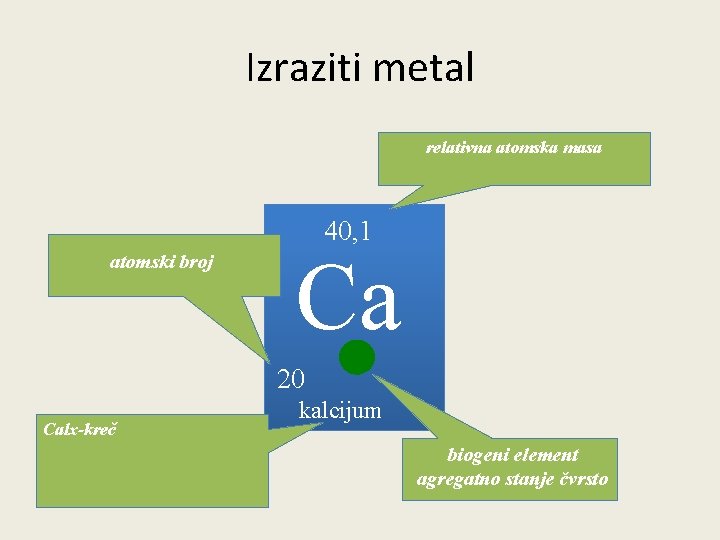
Izraziti metal relativna atomska masa 40, 1 atomski broj Ca 20 Calx-kreč kalcijum biogeni element agregatno stanje čvrsto

Dobijanje-elektrolizom iz svojih jedinjenja Osobine Na Ts u čvrstom stanju Metalno-siv Mekan, može se seći nožem Dobar provodnik toplote i električne struje Čuva se u petroleumu ili u zatvorenim kutijama ZAŠTO? • (reaguje sa vodom, kiseonikom i azotom iz vazduha-tanak sloj na površini) • • •

Koji tip hemijske veze grade alkalni i zemnoalkalni metali? U svim jedinjenjima alkalnih i većine zemnoalkalnih metala (osim berilijuma) zastupljena je jonska veza Koliko iznosi valenca metala u jedinjenjima alkalnih i zemnoalkalnih metala? Alkalni –valenca I, zemnoalkalni valenca II

• Zemnoalkalni metali boje plamen jarkim bojama – pri izradi vatrometa Kalcijum Magnezijum Stroncijum Barijum

Metali sa kiseonikom daju METALNE OKSIDE 4 Li+ O 2→ 2 Li 2 O 4 Na+ O 2→ 2 Na 2 O 4 K+ O 2→ 2 K 2 O 2 Mg+ O 2→ 2 Mg. O 2 Ca+ O 2→ 2 Ca. O

� Hidroksidi alkalnih i većine zemnoalkalnih metala nastaju u reakciji njihovih oksida sa vodom Li 2 O+ H 2 O→ 2 Li. OH Na 2 O+ H 2 O→ 2 Na. OH K 2 O+ H 2 O→ 2 KOH Mg. O+ H 2 O→Mg(OH)2 Ca. O+ H 2 O→Ca(OH)2

Hidroksidi alkalnih i većine zemnoalkalnih metala nastaju i u reakciji tih metala sa vodom 2 Li + 2 H 2 O→ 2 Li. OH +H 2 2 Na + 2 H 2 O→ 2 Na. OH +H 2 2 K + 2 H 2 O→ 2 KOH +H 2 Ca + 2 H 2 O→Ca(OH)2 +H 2 burno manje burno Mg+ 2 H 2 O→Mg(OH)2 +H 2 tek sa ključalom vodom

Zašto su alkalni metali reaktivniji od zemnoalkalnih? Alkalni metali reaguju burnije jer otpuštaju samo po jedan elektron, a zemnoalkalni metali otpuštaju po dva. Zašto je kalcijum reaktivniji od magnezijuma? Kalcijum je reaktivniji od magnezijuma jer su njegovi valentni elektroni udaljeniji od jezgra i ono ih slabije privlači.
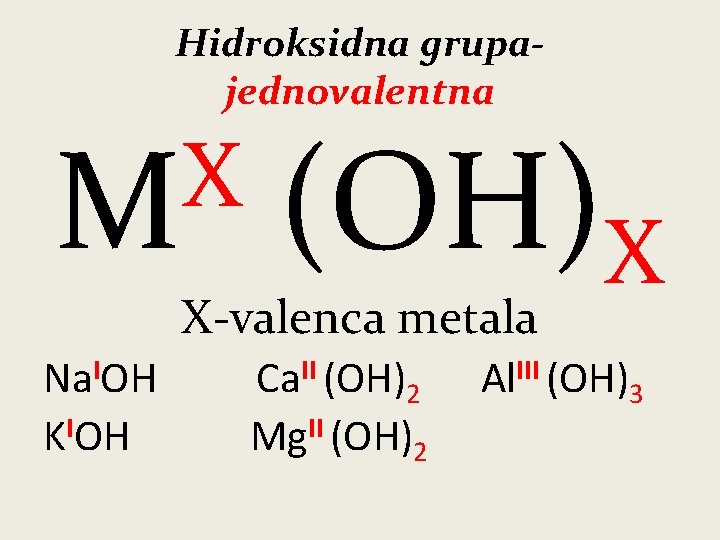
Hidroksidna grupajednovalentna X M (OH)X X-valenca metala Na. IOH KIOH Ca. II (OH)2 Mg. II (OH)2 Al. III (OH)3

Kako možemo dokazati da je neka supstanca hidroksid? Hidroksidi menjaju boju crvene lakmus hartije u plavu • Hidroksidi drugih metala dobijaju se drugim postupcima, ne rastvaraju se u vodi pa samim tim nema reakcije sa lakmus hartijom

Rastvorljivost baza u vodi Baze se mogu dobro rastvarati u vodi Na. OH, KOH-alkalije delimično se rastvarati u vodi Mg(OH)2, Ca(OH)2 ne rastvarati se u vodi Fe(OH)2 Fe(OH)3 , Cu(OH)2

Sa kiseonikom: crveni plamen 2 Ca + O 2 → 2 Ca. O Negašeni kreč U proizvodnji šećera, hartije, stakla, sušenje ulja-opekotine na koži

Negašeni (živi) kreč se gasi vodom • Ca. O + H 2 O →Ca(OH)2 Gašeni kreč Beli prah, slabo rastvoran u vodi Dezinfekcija prostorija, zaštita drveća od glodara

Bistar rastvor gašenog kreča naziva se Krečna voda se zamuti reakcijom sa ugljen (IV)-oksidom Ca(OH)2+ CO 2→ Ca. CO 3↓+H 2 O Kalcijum-karbonat Gašeni kreč razmućen u vodi – Krečno mleko (krečenje zidova)

Mešanjem gašenog kreča sa vodom i peskom - malter Ca(OH)2+ CO 2→ Ca. CO 3 ↓ +H 2 O Kalcijum-karbonat Očvršćavanje maltera zasniva se na reakciji kalcijum-hidroksida i ugljen(IV)-oksida iz vazduha. Kalcijum-karbonat slepljuje zrnca peska i time malter očvršćava.

Ca. CO 3 Koristi se kao građevinski materijal i za dobijanje kalcijum-oksida t Ca. CO 3 → Ca. O+ CO 2 Krečnjak Ca. CO 3 Živi kreč Ca. O Gašeni kreč Ca(OH)2

Mermerne pećine u Čileu Tadz Mahal-Mauzolej ljubavi u. Indiji sagrađen od mermera Ca. CO 3 Mikelanđelo se oslanjao na znanje hemije kada je oslikavao slavnu Sikstinsku kapelu. Slikao je freske — tehnika slikanja na vlažne gipsane površine zida ili tavanice. Kalcijum- hidroksid u gipsu reaguje sa vazduhom dok se suši, stvarajući kalcijum- karbonat. Zbog te hemijske reakcije boja se kristalizuje i postaje deo gipsa.

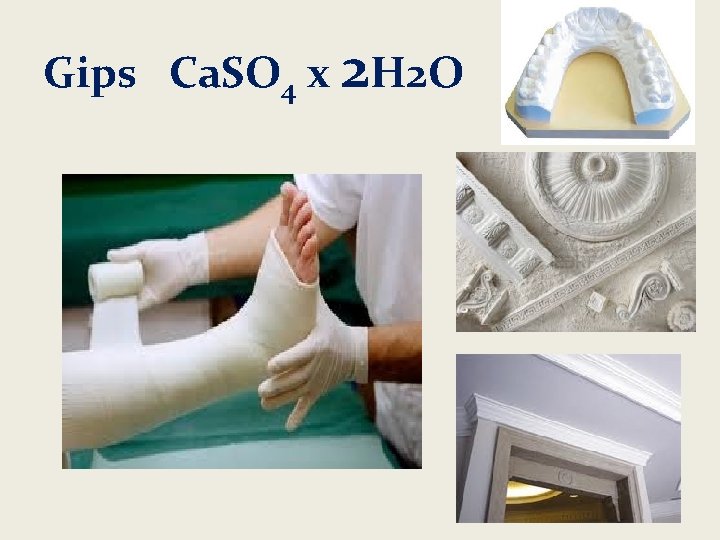
Gips Ca. SO 4 x 2 H 2 O

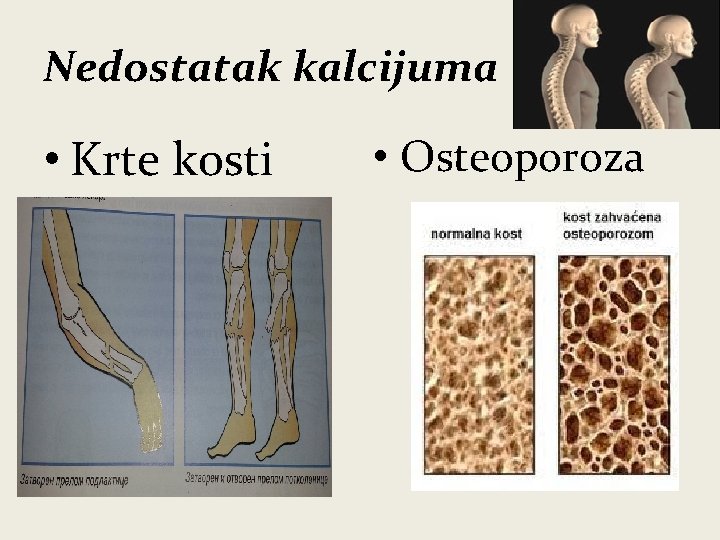
Nedostatak kalcijuma • Krte kosti • Osteoporoza


