Kovalentna veza Autor Jelena Muci VRSTA VEZE MOLEKULI












- Slides: 29

Kovalentna veza Autor: Jelena Mucić

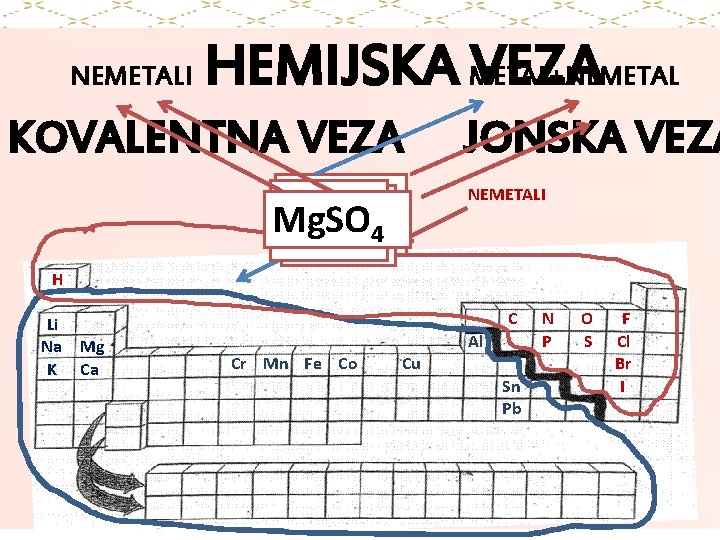
VRSTA VEZE MOLEKULI su stabilne celine udruženih atoma Privlačne sile koje drže čestice na okupu nazivaju se hemijske veze atomi mogu graditi molekule: * udruživanjem svojih valentnih elektrona sa elektronima drugih atoma u zajedničke elektronske parove KOVALENTNA VEZA - grade je nemetali među sobom * primanjem ili otpuštanjem elektrona JONSKA VEZA - grade je metali i nemetali

NEMETALI HEMIJSKA METAL+NEMETAL VEZA KOVALENTNA VEZA Mg. SO Na. Cl METALI Ca. O Hso 2 O 24 H Li Na K JONSKA VEZA NEMETALI C Mg Ca Al Cr Mn Fe Co Cu Sn Pb N P O S F Cl Br I

KOVALENTNA VEZA ZAŠTO SU VALENTNI ELEKTRONI “MOĆNI” ELEKTRONI? KAKO NASTAJU MOLEKULI? KO GRADI KOVALENTNU VEZU? KAKVA KOVALENTNA VEZA MOŽE BITI?

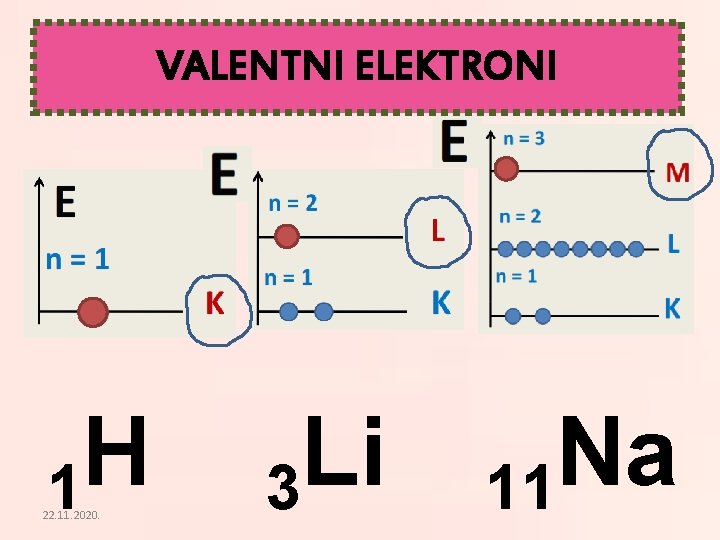
VALENTNI ELEKTRONI Valensija – MOĆ Valentni elektroni u jednom atomu imaju najvišu energiju Valentni elektroni omogućavaju atomima da se međusobno povezuju – grade molekule 22. 11. 2020.

VALENTNI ELEKTRONI H 1 22. 11. 2020. Li 3 Na 11

ELEKTRONSKA KONFIGURACIA PLEMENITIH GASOVA plemeniti gasovi su izuzetno stabilni poslednji energetski nivo plemenitih gasova popunjen je maksimalnim brojem elektrona helijum- dva, a ostali osam dublet oktet Sve u prirodi teži da postigne što veću stabilnost! Svi elementi teže da postignu stabilnu elektronsku konfiguraciju najbližeg plemenitog

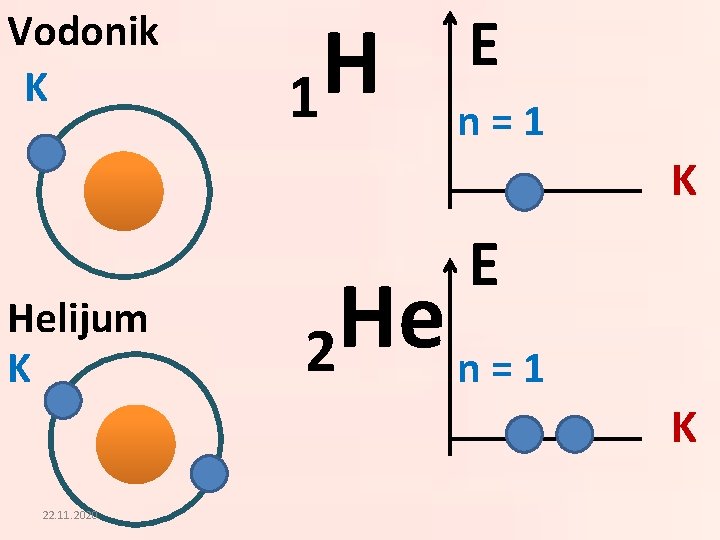
Vodonik K H 1 E n=1 K Helijum K E He 2 n=1 K 22. 11. 2020.

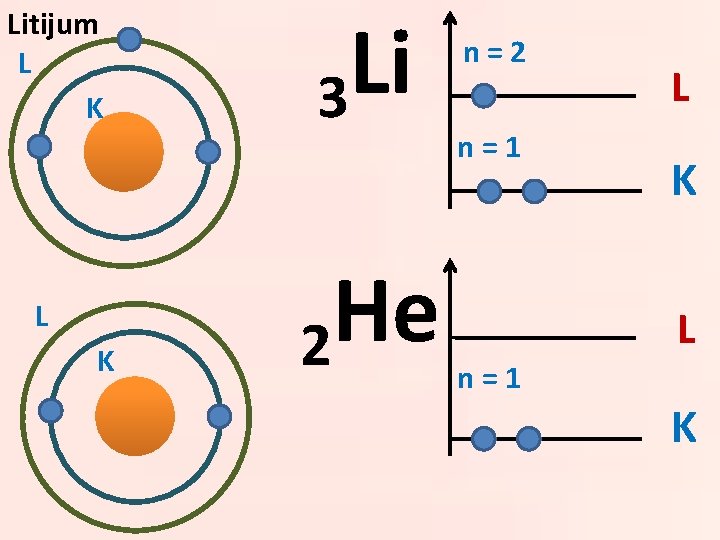
Litijum L K Li 3 He 2 n=1 L K L n=1 K

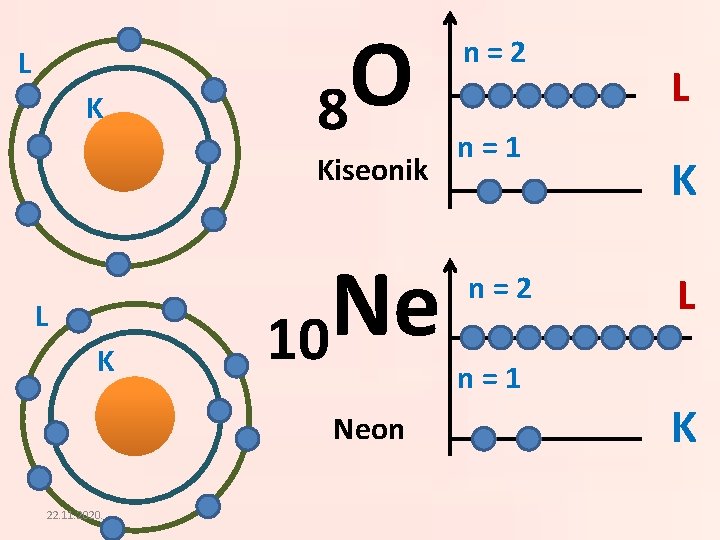
L K O 8 Kiseonik L K Ne 10 Neon 22. 11. 2020. n=2 n=1 n=2 L K L n=1 K

KOVALENTNA VEZA Kovalentna veza je hemijska veza koja nastaje udruživanjem elektrona u zajednički elektronski par Grade je isti ili različiti nemetali mađu sobom

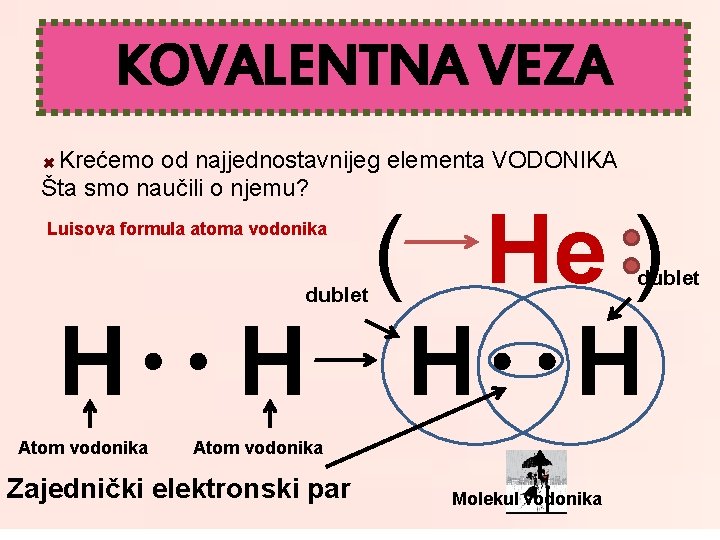
KOVALENTNA VEZA Krećemo od najjednostavnijeg elementa VODONIKA Šta smo naučili o njemu? ( He ) H H H Luisova formula atoma vodonika dublet H Atom vodonika Zajednički elektronski par Molekul vodonika

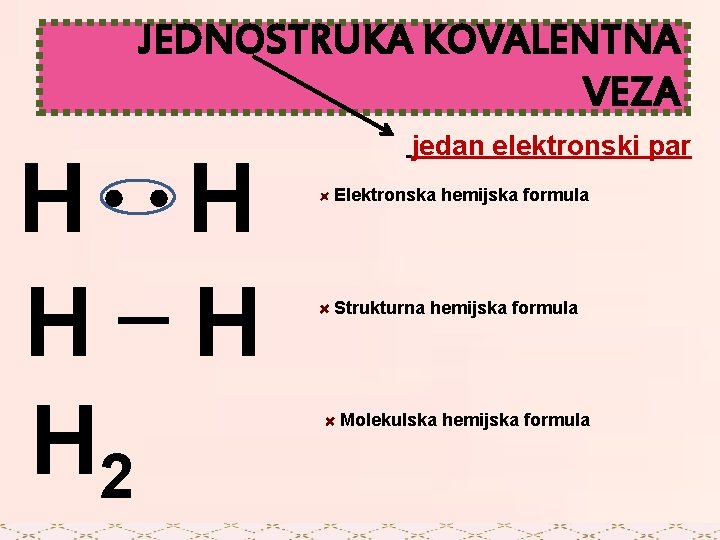
JEDNOSTRUKA KOVALENTNA VEZA H H H 2 jedan elektronski par Elektronska hemijska formula Strukturna hemijska formula Molekulska hemijska formula

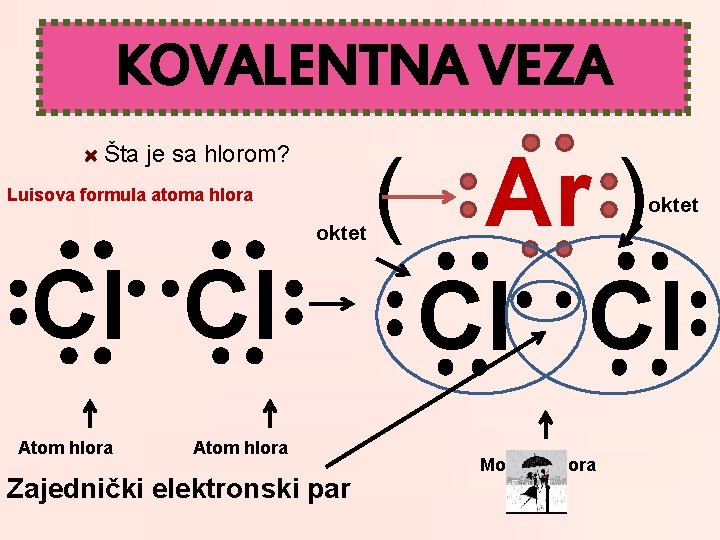
KOVALENTNA VEZA ( Ar ) Cl Cl Šta je sa hlorom? Luisova formula atoma hlora oktet Atom hlora Zajednički elektronski par Molekul hlora

JEDNOSTRUKA KOVALENTNA VEZA Cl Cl Cl 2 jedan elektronski par Elektronska hemijska formula Strukturna hemijska formula Molekulska hemijska formula

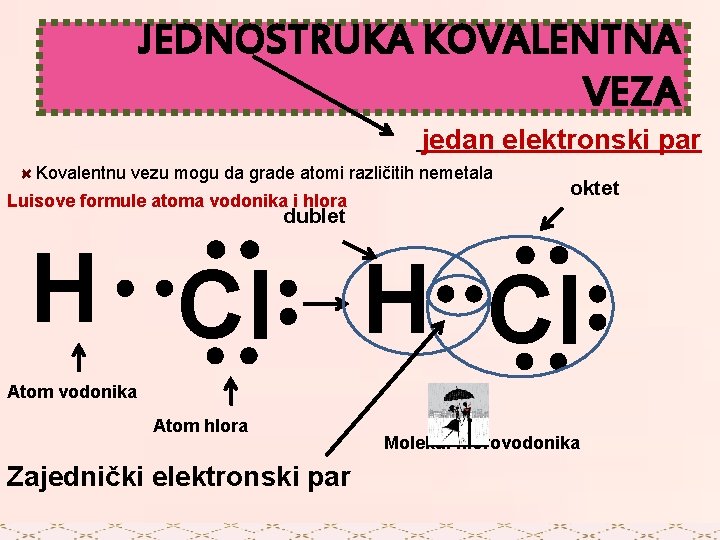
JEDNOSTRUKA KOVALENTNA VEZA jedan elektronski par Kovalentnu vezu mogu da grade atomi različitih nemetala Luisove formule atoma vodonika i hlora oktet dublet H Cl Atom vodonika Atom hlora Zajednički elektronski par Molekul hlorovodonika

JEDNOSTRUKA KOVALENTNA VEZA H Cl HCl jedan elektronski par Elektronska hemijska formula Strukturna hemijska formula Molekulska hemijska formula

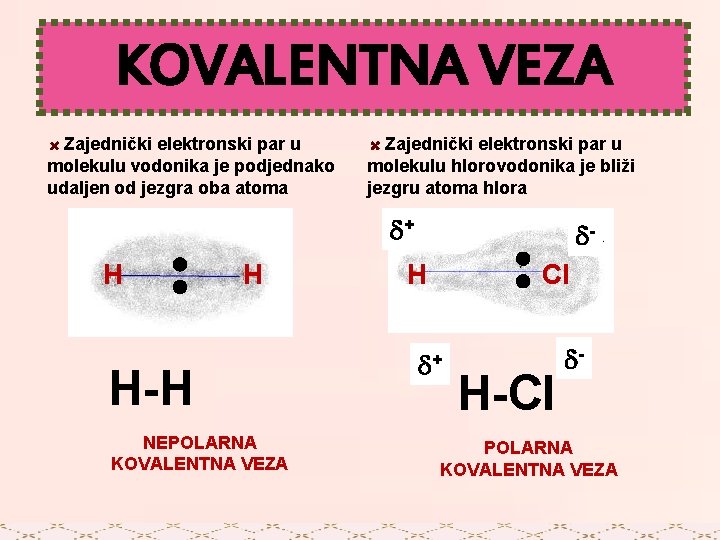
KOVALENTNA VEZA Zajednički elektronski par u molekulu vodonika je podjednako udaljen od jezgra oba atoma Zajednički elektronski par u molekulu hlorovodonika je bliži jezgru atoma hlora + H H H-H NEPOLARNA KOVALENTNA VEZA - H Cl + H-Cl - POLARNA KOVALENTNA VEZA

ELEKTRONEGATIVNOST- sposobnost atoma da privlači elektrone u hemijskoj vezi Veze između istovrsnih atoma su NEPOLARNE, a veze između raznovrsnih atoma su uglavnom POLARNE Vrednost elektronegativnosti u PSE raste u periodi sa leva na desno, a u grupi odozdo na gore

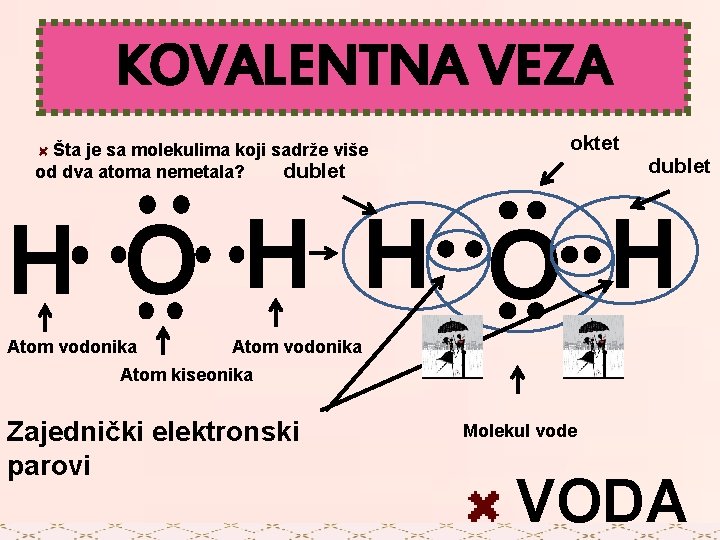
KOVALENTNA VEZA Šta je sa molekulima koji sadrže više od dva atoma nemetala? dublet oktet dublet H O H Atom vodonika Atom kiseonika Zajednički elektronski parovi Molekul vode VODA

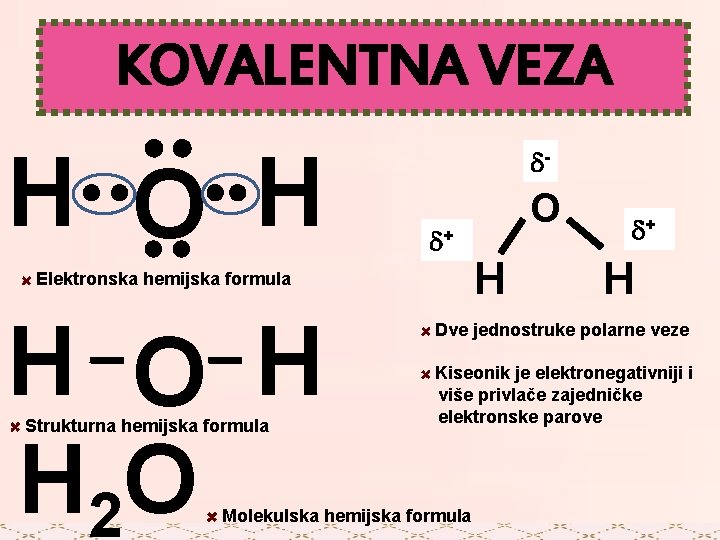
KOVALENTNA VEZA H O H + Elektronska hemijska formula H O H H 2 O Strukturna hemijska formula O H + H Dve jednostruke polarne veze Kiseonik je elektronegativniji i više privlače zajedničke elektronske parove Molekulska hemijska formula

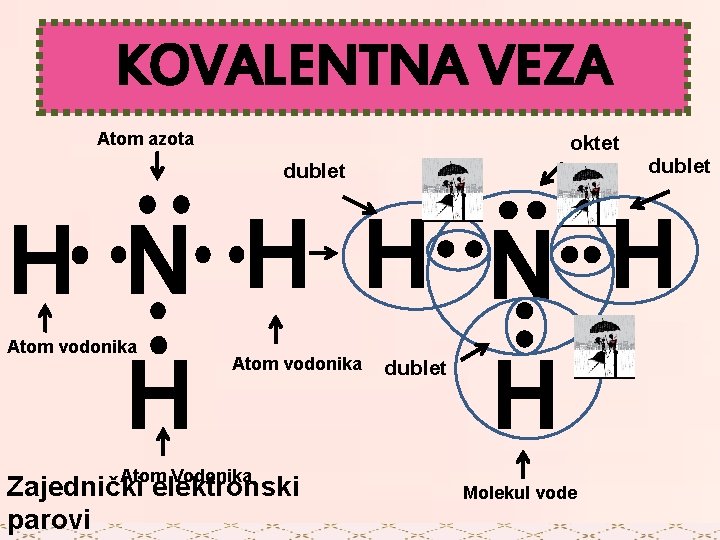
KOVALENTNA VEZA Atom azota oktet dublet H N H H H Atom vodonika Atom Vodonika Zajednički elektronski parovi dublet Molekul vode

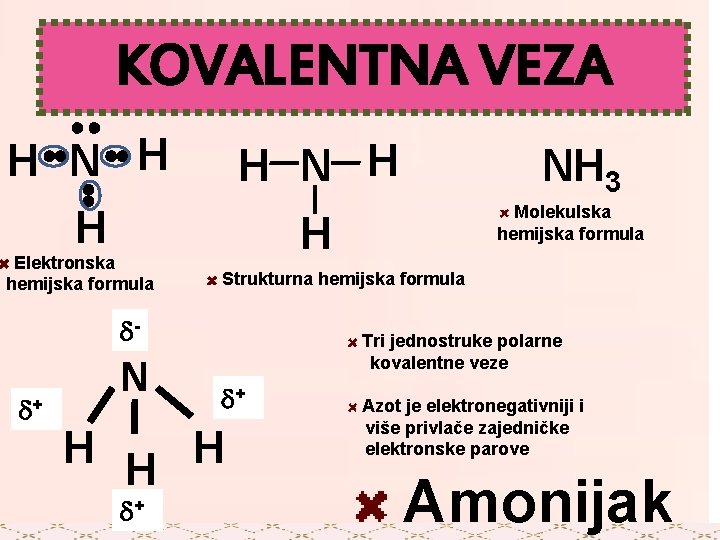
KOVALENTNA VEZA H N H H Elektronska hemijska formula + H H + Molekulska hemijska formula H Strukturna hemijska formula - N NH 3 Tri jednostruke polarne kovalentne veze + H Azot je elektronegativniji i više privlače zajedničke elektronske parove Amonijak

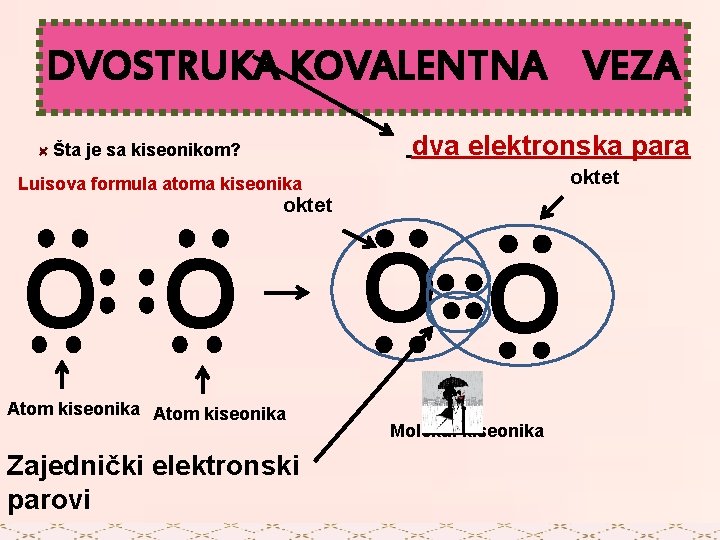
DVOSTRUKA KOVALENTNA VEZA dva elektronska para Šta je sa kiseonikom? oktet Luisova formula atoma kiseonika oktet O O Atom kiseonika Zajednički elektronski parovi O O Molekul kiseonika

DVOSTRUKA KOVALENTNA VEZA O O O 2 dva elektronska para NEPOLARNA KOVALENTNA VEZA Elektronska hemijska formula Strukturna hemijska formula Molekulska hemijska formula

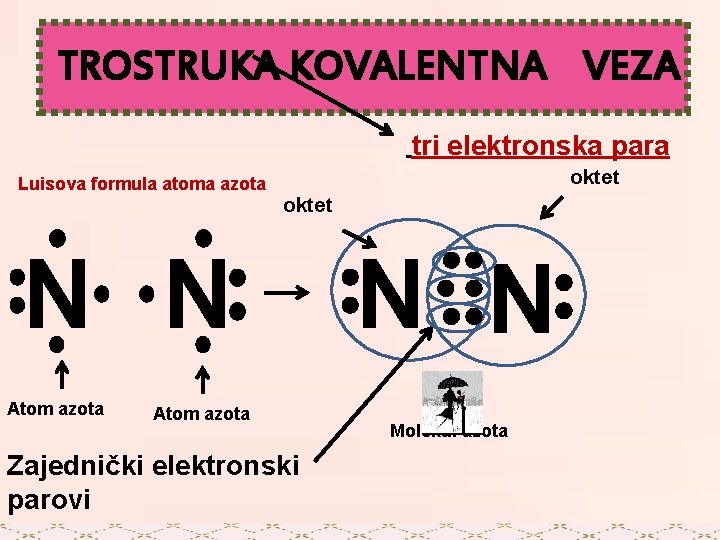
TROSTRUKA KOVALENTNA VEZA tri elektronska para Luisova formula atoma azota oktet N N Atom azota Zajednički elektronski parovi N N Molekul azota

TROSTRUKA KOVALENTNA VEZA N N N 2 tri elektronska para NEPOLARNA KOVALENTNA VEZA Elektronska hemijska formula Strukturna hemijska formula Molekulska hemijska formula

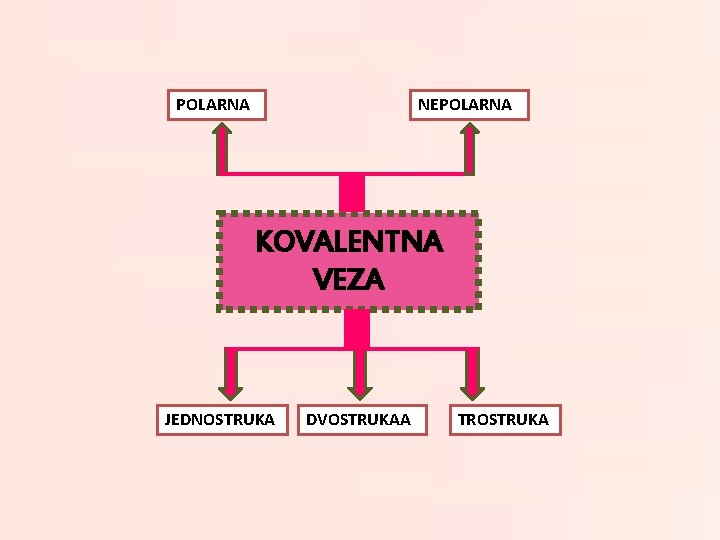
POLARNA NEPOLARNA KOVALENTNA VEZA JEDNOSTRUKA DVOSTRUKAA TROSTRUKA

VEŽBAJMO! Napiši elektronske, strukturne i molekulske formule molekula koji se sastoje iz: dva atoma broma dva atoma kiseonika i jednog atoma ugljenika jednog atoma fosfora i tri atoma vodonika atoma joda i atoma vodonika atoma ugljenika i četiri atoma vodonika