Europejska Akademia Pacjentw w obszarze innowacyjnych terapii Opracowywanie

Europejska Akademia Pacjentów w obszarze innowacyjnych terapii Opracowywanie leków: podstawowe zasady dotyczące odkrywania i rozwoju leków

Omówienie Europejska Akademia Pacjentów w obszarze innowacyjnych terapii § Przeprowadzenie wszystkich badań i prac koniecznych do wprowadzenia nowego leku na rynek zajmuje ponad 12 lat i kosztuje średnio ponad 1 mld euro. § Odkrywanie nowych leków jest przedsięwzięciem o wysokim ryzyku. Ø Około 98% opracowywanych leków nie trafia ostatecznie na rynek. Ø W większości powodem tego jest fakt, że korzyści i ryzyka nowo opracowanego produktu nie wytrzymują porównania z lekami już dostępnymi dla pacjentów. 2
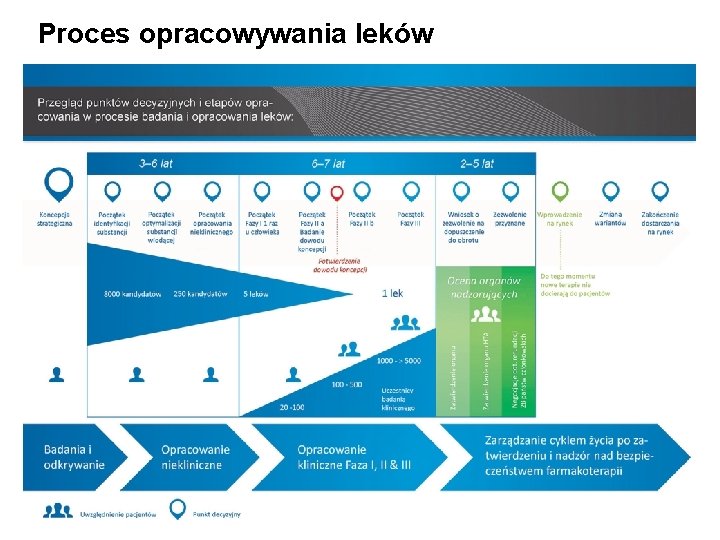
Proces opracowywania leków

ETAP 1: Odkrywanie (1) Europejska Akademia Pacjentów w obszarze innowacyjnych terapii § Okres poprzedzający rozwój leku i określenie, czy istnieje jakaś „niezrealizowana potrzeba”. Ø W okresie poprzedzającym opracowywanie leku naukowcy pracujący na uniwersytetach i w przemyśle (firmy farmaceutyczne) zdobywają wiedzę na temat danej choroby. § „Niezrealizowana potrzeba” dotyczy choroby, w której przypadku: Ø brak dostępnego odpowiedniego leku lub Ø lek jest dostępny, ale niektórzy pacjenci nie mogą go przyjmować ze względu na występujące u nich nieakceptowalne działania niepożądane. 4

ETAP 1: Odkrywanie (2) Europejska Akademia Pacjentów w obszarze innowacyjnych terapii § Proces badań i opracowywania wymaga wielu zasobów i jest bardzo kosztowny. § Istnieje wiele niezrealizowanych potrzeb, w których przypadku nowe leki nie są obecnie opracowywane. § Przed wprowadzeniem leku na rynek musi zostać złożony wniosek o wydanie pozwolenia na dopuszczenie do obrotu i musi zostać uzyskane zatwierdzenie. 5

ETAP 1: Odkrywanie (3) Europejska Akademia Pacjentów w obszarze innowacyjnych terapii § Każda faza opracowywania wymaga uzyskania zgody dotyczącej pieniędzy (inwestycje) i zatrudnienia osób do wykonania pracy (zasoby). Taka zgoda określana jest jako decyzja inwestycyjna (Investment Decision, ID). § Po uzyskaniu ID można rozpocząć następną fazę badań. Ten wzorzec „ID — działanie — wyniki — ID” powtarza się w ciągu całego procesu rozwoju produktu. 6

ETAP 2: Wybór celu (1) Europejska Akademia Pacjentów w obszarze innowacyjnych terapii § Choroby występują, kiedy normalne procesy organizmu ulegają zmianom lub przestają prawidłowo przebiegać. § Podczas opracowywania leku trzeba dokładnie wiedzieć (na poziomie komórek), gdzie wystąpiła nieprawidłowość. Dzięki temu można skupić się na nieprawidłowym procesie („celowanie”). § „Cel” może być: Ø Cząsteczką, która wytwarzana w nadmiarze zaburzyła normalne funkcje organizmu, Ø Cząsteczką wytwarzaną w nieprawidłowej ilości lub Ø Cząsteczką o nieprawidłowej strukturze. 7
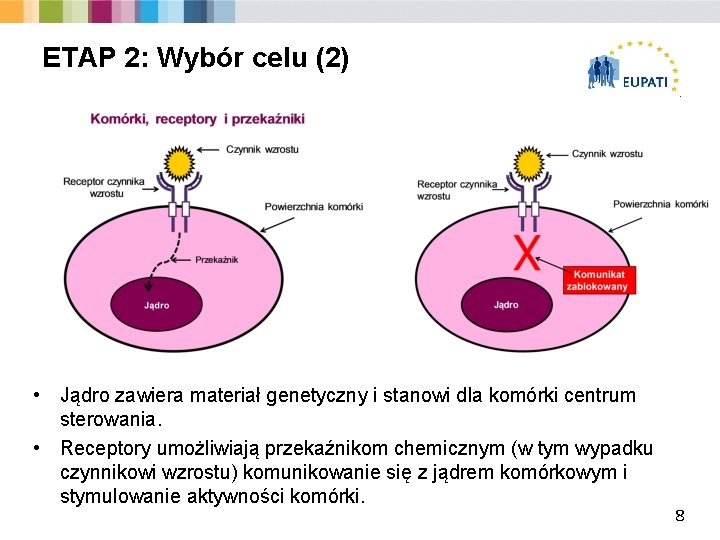
ETAP 2: Wybór celu (2) Europejska Akademia Pacjentów w obszarze innowacyjnych terapii • Jądro zawiera materiał genetyczny i stanowi dla komórki centrum sterowania. • Receptory umożliwiają przekaźnikom chemicznym (w tym wypadku czynnikowi wzrostu) komunikowanie się z jądrem komórkowym i stymulowanie aktywności komórki. 8

ETAP 2: Wybór celu (3) Europejska Akademia Pacjentów w obszarze innowacyjnych terapii § Przykład: Nowotwór Ø Przekaźnik chemiczny łączy się z receptorem czynnika wzrostu na powierzchni komórki, wewnątrz komórki jest generowany komunikat. Ø Jeśli sygnały są niekontrolowane, rozrost komórki prowadzi do raka. Ø Zablokowanie receptora w komórkach nowotworowych zapobiega przekazywaniu komunikatu, a w konsekwencji niekontrolowanemu rozrostowi komórki. § Zablokowanie receptora w komórkach nowotworowych ma następujące skutki: Ø przerwanie wysyłania komunikatu i Ø zapobieżenie niekontrolowanemu rozrostowi komórki 9

ETAP 2: Wybór celu (4) Europejska Akademia Pacjentów w obszarze innowacyjnych terapii • Naukowcy często nie potrafią dokładnie powiedzieć, która nieprawidłowość lub cel odpowiada za chorobę, dlatego próby wprowadzenia zmian w „celu” mogą nie leczyć choroby. • W takim wypadku projekt rozwoju leku może zmierzać w złym kierunku, a ostatecznie zakończyć się niepowodzeniem. • Wybór najlepszego celu i skupienie wokół niego prac projektowych ma kluczowe znaczenie dla sukcesu. 10

ETAP 3: Generowanie związku wiodącego Europejska Akademia Pacjentów w obszarze innowacyjnych terapii § Ten etap obejmuje znajdowanie cząsteczki, która będzie oddziaływać z celem. Są to tak zwane „substancje wiodące”. Ø Substancje wiodące mogą być cząsteczkami występującymi naturalnie lub wytwarzanymi chemicznie. Ø Substancje wiodące mogą być także dużymi cząsteczkami lub białkami. Są to tak zwane „leki biologiczne”. § Testowanie pod kątem związku wiodącego nosi nazwę procesu przesiewu. Ø Zrobotyzowane technologie określane jako „badania przesiewowe o dużej przepustowości” umożliwiają szybkie testowanie milionów cząsteczek. § Po utworzeniu lub znalezieniu związku wiodącego proces może przejść do następnego etapu. 11

ETAP 4: Optymalizacja związku wiodącego (1) Europejska Akademia Pacjentów w obszarze innowacyjnych terapii § Wybrana substancja wiodąca może słabo oddziaływać w miejscu docelowym. Chemicy muszą więc zmienić wybraną cząsteczkę wiodącą, aby to działanie wzmocnić. Ø Aby wzmocnić działanie oryginalnego związku wiodącego, dodaje się do niego (lub usuwa z niego) różne składniki, co powoduje wytworzenie wielu nieznacznie różniących się cząsteczek. 12
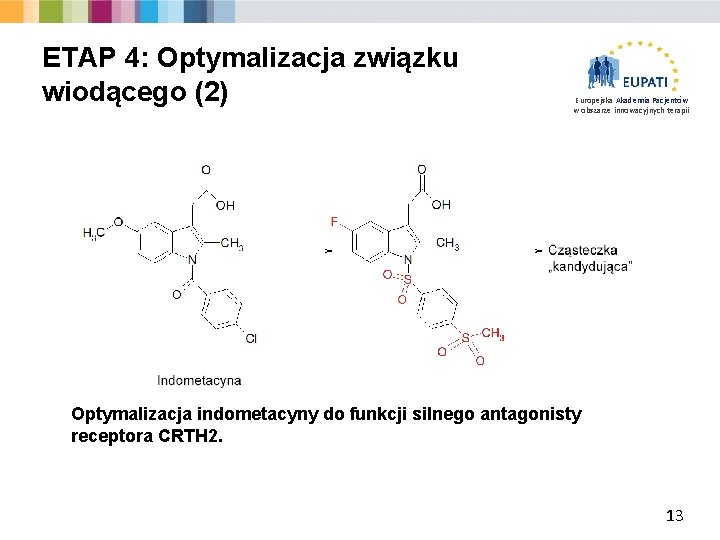
ETAP 4: Optymalizacja związku wiodącego (2) Europejska Akademia Pacjentów w obszarze innowacyjnych terapii Optymalizacja indometacyny do funkcji silnego antagonisty receptora CRTH 2. 13

ETAP 4: Optymalizacja związku wiodącego (3) Europejska Akademia Pacjentów w obszarze innowacyjnych terapii § Zmodyfikowane cząsteczki są następnie poddawane testom, aby określić, która struktura ma najlepszą skuteczność i jest lepiej tolerowana przez organizm (bezpieczeństwo). § Cząsteczki wykazujące wyższą skuteczność i bezpieczeństwo mogą zostać przekazane do dalszych badań jako „kandydat na lek”. § Na tym etapie informacje naukowe i techniczne dotyczące cząsteczki „kandydującej”, takie jak jego struktura cząsteczkowa i efekty działania, są zwykle rejestrowane lub patentowane, aby chronić je jako własność intelektualną. 14

ETAP 5: Badania niekliniczne dotyczące bezpieczeństwa stosowania (1) Europejska Akademia Pacjentów w obszarze innowacyjnych terapii § Kolejny etap procesu rozwoju leku obejmuje testowanie bezpieczeństwa na zwierzętach, prowadzone zgodnie z regułami i przepisami Dobrej Praktyki Laboratoryjnej. § Przepisy określają, jakie badania należy wykonać i jakie gatunki zwierząt powinny zostać wykorzystane, aby uzyskać odpowiednie informacje. 15

ETAP 5: Badania niekliniczne dotyczące bezpieczeństwa stosowania (2) Europejska Akademia Pacjentów w obszarze innowacyjnych terapii § Dobra Praktyka Laboratoryjna i przepisy dotyczące badań nieklinicznych wymagają zebrania informacji na temat działania leku: Ø Na zwierzę ogólnie Ø Na wszystkie tkanki i narządy zwierzęcia (badania toksyczności układowej) Ø Na zdolność zwierząt do rozrodu i normalnego rozwoju (badania toksyczności reprodukcyjnej) Ø Na skórę lub oczy (badania toksyczności miejscowej) Ø Na chromosomy i geny (badania genotoksyczności) Ø Wszelkiego wpływu na powstawanie nowotworów (badania kancerogenności) 16

ETAP 5: Badania niekliniczne dotyczące bezpieczeństwa stosowania (3) Europejska Akademia Pacjentów w obszarze innowacyjnych terapii 17

ETAP 5: Badania niekliniczne dotyczące bezpieczeństwa stosowania (4) Europejska Akademia Pacjentów w obszarze innowacyjnych terapii § Te badania nie tylko pozwalają określić profil bezpieczeństwa u zwierząt, ale także dostarczają ważnych informacji na temat: Ø sposobu dostawania się substancji do organizmu (Absorpcji) Ø dystrybucji w organizmie (Dystrybucji) Ø rozkładania substancji przez organizm (Metabolizmu) Ø usuwania substancji z organizmu (Eliminacji). § Niekiedy określa się to skrótem „ADME”. § Wszystkie te informacje pozwalają zdecydować, czy cząsteczka „kandydująca” może zostać wykorzystana w pierwszych badaniach z udziałem ludzi (klinicznych), a jeśli tak, to w jakich dawkach. 18

ETAP 6: Badania typu „Proof of Mechanism” — badania kliniczne Fazy I (1) Europejska Akademia Pacjentów w obszarze innowacyjnych terapii § Przed rozpoczęciem badania klinicznego konieczne jest przesłanie do właściwego organu krajowego wniosku o badanie kliniczne (CTA). § Uzyskuje się także opinię Komisji Bioetycznej. § Najwyższym priorytetem jest bezpieczeństwo, toteż badania na ludziach nie mogą się rozpocząć bez uzyskania zgody: Ø wewnętrznej komisji kwalifikacyjnej, Ø zewnętrznej Komisji Bioetycznej oraz Ø zewnętrznego organu nadzorującego. 19

ETAP 6: Badania typu „Proof of Mechanism” — badania kliniczne Fazy I (2) Europejska Akademia Pacjentów w obszarze innowacyjnych terapii § Badania z udziałem ochotników (lub badania kliniczne Fazy I) dają lekarzom i naukowcom możliwość testowania leku pod kątem bezpieczeństwa dla ludzi. Są one określane jako badania typu „proof of mechanism”. Ø Badania kliniczne Fazy I umożliwiają stwierdzenie, czy zachowanie leku u ludzi jest takie samo jak w przypadku zwierząt. § Wszystkie informacje dotyczące badania są gromadzone w dokumencie o nazwie Karta Obserwacji Klinicznej (CRF, Case Record Form). 20

ETAP 6: Badania typu „Proof of Mechanism” — badania kliniczne Fazy I (2) Europejska Akademia Pacjentów w obszarze innowacyjnych terapii § Dwa niezwykle ważne elementy to: Ø Świadoma zgoda (zapewniająca, że uczestnicy rozumieją, co będzie miało miejsce, i zgadzają się na uczestnictwo w badaniu) oraz Ø ocena i opinia Komisji Bioetycznej; § Ponieważ bezpieczeństwo jest najważniejsze, podawanie leku w badaniu zaczyna się od pojedynczej, bardzo niskiej dawki. Następnie dawka jest zwiększana. Ø Takie badania noszą nazwę badań metodą jednorazowej dawki rosnącej (Single Ascending Dose, SAD). Po nich zwykle następuje badanie metodą wielorazowej dawki rosnącej (Multiple Ascending Dose, MAD), w którym każdemu ochotnikowi podaje 21 się wiele dawek.

ETAP 6: Badania typu „Proof of Mechanism” — badania kliniczne Fazy I (3) Europejska Akademia Pacjentów w obszarze innowacyjnych terapii § Wyniki badania są następnie analizowane, a wszystkie badania bezpieczeństwa ocenione, włącznie z: Ø Farmakokinetyką: jak organizm przetwarza lek. Można zmierzyć stężenia leku we krwi, aby ocenić ADME. Ø Farmakodynamiką — wpływem leku na organizm („działaniem”). 22

ETAP 7: Badania typu „Proof of Principle” — badania kliniczne Fazy II (1) Europejska Akademia Pacjentów w obszarze innowacyjnych terapii § Jeśli badania kliniczne Fazy I wykażą, że prace można bezpiecznie kontynuować, kolejnym etapem jest rozpoczęcie badań klinicznych z udziałem pacjentów cierpiących na leczoną chorobę. § Zwykle istnieją dwie grupy leczenia: Ø jedna grupa otrzymuje aktywny lek, Ø druga grupa otrzymuje lek niewpływający na organizm (placebo). § W badaniach tego typu zwykle bierze udział od 100 do 500 pacjentów. Mają one dostarczać informacji dotyczących oddziaływania leku na rzeczywistą chorobę (badanie typu „Proof of principle”). 23

ETAP 7: Badania typu „Proof of Principle” — badania kliniczne Fazy II (2) Europejska Akademia Pacjentów w obszarze innowacyjnych terapii § Te badania są zwykle prowadzone w kilku ośrodkach szpitalnych przez lekarzy noszących nazwę badaczy. Jednoczesne prowadzenie badań w kilku ośrodkach jest bardziej skomplikowane niż w przypadku jednego ośrodka. § Do zakończenia badań Fazy II program: Ø zajmuje średnio 8, 5 roku. Ø kosztuje średnio 1 mld euro. § Spośród 10 leków badanych w Fazie I i Fazie II średnio zaledwie 2 przechodzą do kolejnej fazy badań. 24

ETAP 8: Badania potwierdzające — badania kliniczne Fazy III (1) Europejska Akademia Pacjentów w obszarze innowacyjnych terapii § Celem badań Fazy III (badań potwierdzających) jest potwierdzenie skuteczności i bezpieczeństwa stosowania leku w dużej populacji pacjentów. § Ważne decyzje, w tym dotyczące ostatecznej postaci leku i dawki do testowania, są podejmowane na podstawie wszystkich informacji z wcześniejszych etapów. § Badania kliniczne Fazy III mogą obejmować tysiące pacjentów i odbywać się w wielu krajach. Ich efektywny przebieg wymaga wielkiego doświadczenia, toteż są bardzo kosztowne i czasochłonne. 25

ETAP 8: Badania potwierdzające — badania kliniczne Fazy III (1) Europejska Akademia Pacjentów w obszarze innowacyjnych terapii § Jest to jednak jedyny sposób, aby uzyskać jasne informacje dotyczące skuteczności leku (jak dobrze działa) i bezpieczeństwa jego stosowania (czy jest dobrze tolerowany). § Badania ponad 50% leków osiągające Fazę III kończą się niepowodzeniem. Całościowy współczynnik niepowodzenia projektów począwszy od fazy odkrywania przekracza 97%. § Przychody z kilku leków wprowadzonych na rynek pokrywają koszty wszystkich projektów, zarówno zakończonych sukcesem, jak i niepowodzeniem. 26

ETAP 9: Wniosek o rejestrację (1) Europejska Akademia Pacjentów w obszarze innowacyjnych terapii § Jeśli wyniki badań klinicznych Fazy III wykazują akceptowalną relację korzyści do ryzyka, można przygotować wniosek o wydanie pozwolenia na dopuszczenie do obrotu (MAA). § We wniosku wszystkie informacje o leku (niekliniczne, kliniczne i dotyczące produkcji) zostają zebrane i przedstawione przy użyciu wcześniej określonego formatu pod nazwą „dossier”. Dossier zostaje wysłane do organów nadzorujących. § Jeśli organ nadzorujący uzna, że wyniki (relacja ryzykokorzyść) są zadowalające, wydaje pozwolenie na dopuszczenie nowego leku do obrotu. 27

ETAP 9: Wniosek o rejestrację (2) Europejska Akademia Pacjentów w obszarze innowacyjnych terapii § Ten proces kontrolny trwa zwykle od 12 do 18 miesięcy. Lek nie uzyska zgody na wprowadzenie na rynek, dopóki nie zostaną spełnione wszystkie wymagania organów nadzorujących i uzyskane ich zatwierdzenia. § Wiele krajów wymaga także przeprowadzenia badań dotyczących ekonomiki stosowania nowego leku. Takie dokumenty umożliwią rządowi lub towarzystwom ubezpieczeniowym korzystającym z usług grup oceny technologii medycznych (Health Technology Assessment, HTA) podejmowanie decyzji i formułowanie zaleceń dotyczących zezwoleń na przepisywanie leku i umieszczanie go na krajowych listach leków refundowanych. 28

ETAP 10: Wprowadzenie do obrotu i ocena bezpieczeństwa po wprowadzeniu produktu na rynek Europejska Akademia Pacjentów w obszarze innowacyjnych terapii § Proces wprowadzania na rynek obejmuje informowanie o nowym leku lekarzy i innych pracowników ochrony zdrowia, aby mieli świadomość jego działania i mogli go przepisywać, jeśli w ich przekonaniu mógłby okazać się korzystny dla pacjentów. § Nadal jednak trzeba zbierać i analizować informacje dotyczące bezpieczeństwa leku stosowanego w „rzeczywistym życiu”. Ten proces określa się jako „nadzór nad bezpieczeństwem farmakoterapii”. § Zarówno dane z badań klinicznych, jak i dane zgromadzone po wprowadzeniu leku do obrotu są konieczne do uzyskania pełnej wiedzy na temat faktycznej relacji korzyści do ryzyka. 29

ETAP 10: Zarządzanie cyklem życia produktu Europejska Akademia Pacjentów w obszarze innowacyjnych terapii § Na koniec w procesie opracowania nowego leku bada się nadal: Ø Inne możliwe zastosowania (wskazania do stosowania) leku. Jeśli na przykład pierwotne zastosowanie dotyczyło pacjentów z astmą, nowe wskazania mogą obejmować pacjentów z różnymi chorobami płuc. Ø Lepsze sposoby sporządzania i używania leku (nowe postacie farmaceutyczne). Może na przykład powstać specjalna postać farmaceutyczna dla dzieci. § Te wszystkie działania określa się jako „zarządzanie cyklem życia”. 30

ETAP 10: Inne zmiany w cyklu życia leku Europejska Akademia Pacjentów w obszarze innowacyjnych terapii § Lek wprowadzany na rynek po raz pierwszy jest chroniony patentem. To oznacza, że inne firmy nie mogą wprowadzić na rynek podobnego leku. Po zakończeniu okresu ochrony patentowej lub ochrony danych inne firmy będą produkować i wprowadzać na rynek taki sam produkt. Taki produkt określa się jako „generyczny”. § Nowe leki są zwykle dopuszczane do wydawania wyłącznie na receptę (Prescription-Only Medicines, POM). To znaczy, że w ciągu pierwszych kilku lat lekarze mogą nadzorować ich stosowanie. Później mogą być dostępne w sprzedaży odręcznej jako tak zwane leki OTC (Over-The-Counter). Wymaga to zmian statusu prawnego leku. 31
- Slides: 31