ESTUDO DOS GASES O estado fsico de um











- Slides: 22

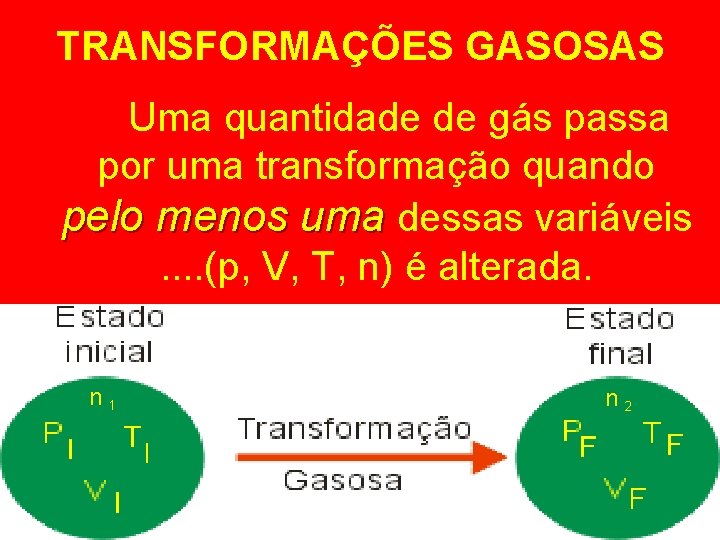
ESTUDO DOS GASES O estado físico de um gás qualquer pode ser descrito a partir de quatro grandezas: a)PRESSÃO (p); b)VOLUME (V); c)TEMPERATURA (T); d) Quantidade de matéria (n).

TRANSFORMAÇÕES GASOSAS Uma quantidade de gás passa por uma transformação quando pelo menos uma dessas variáveis. . (p, V, T, n) é alterada. n 1 n 2


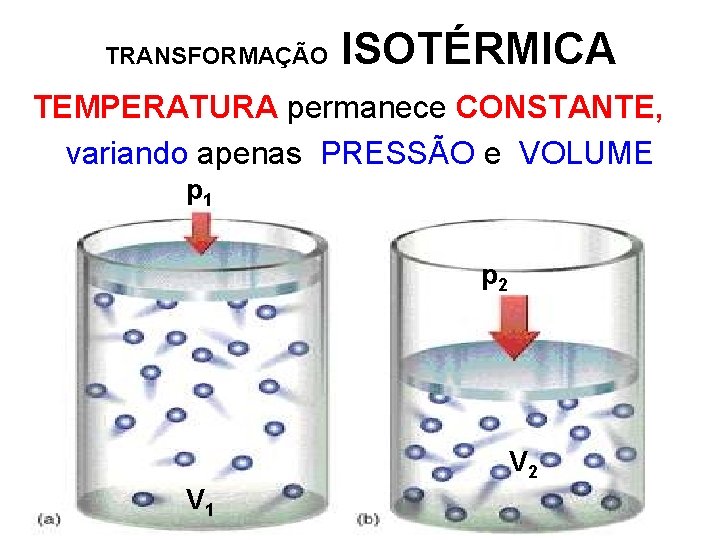
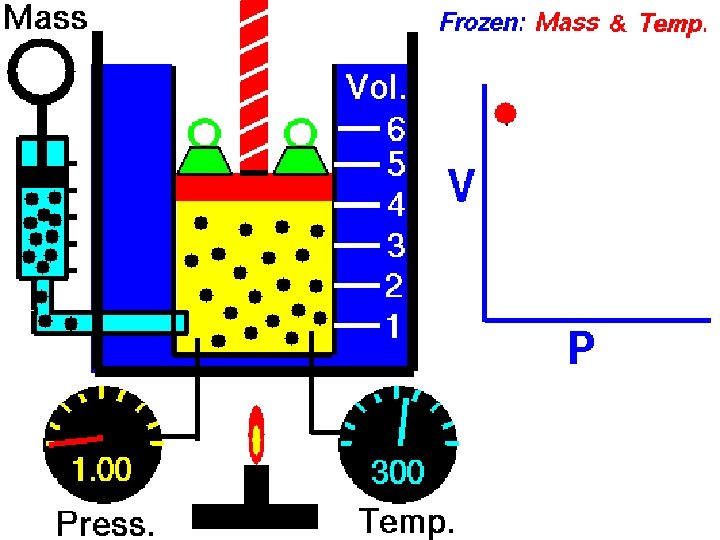
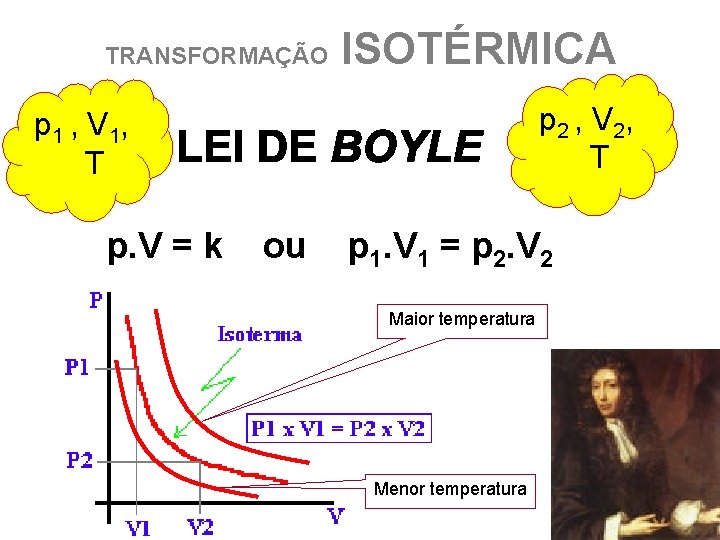
TRANSFORMAÇÃO ISOTÉRMICA TEMPERATURA permanece CONSTANTE, variando apenas PRESSÃO e VOLUME p 1 p 2 V 1

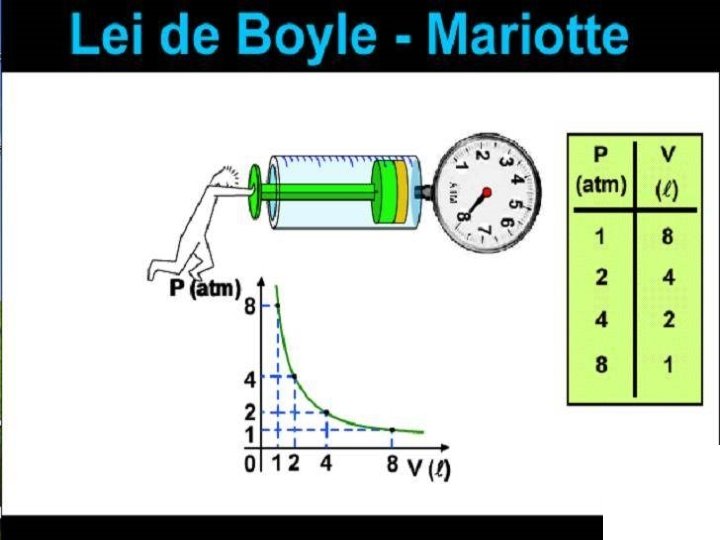
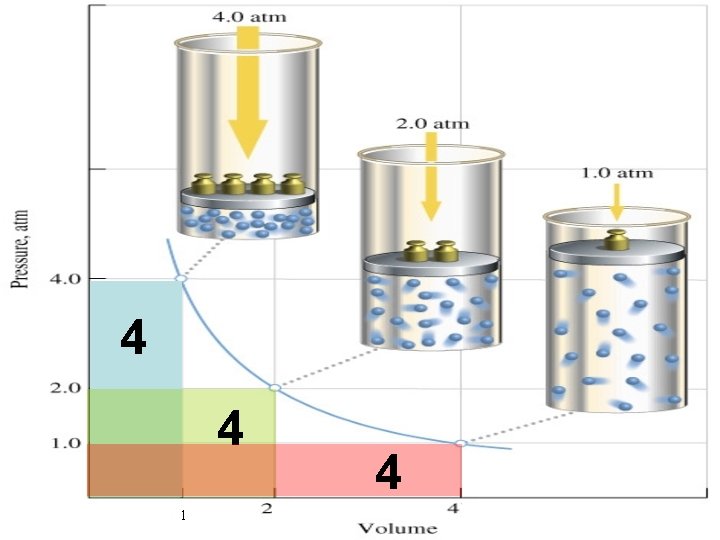
Obedece a lei de BOYLE 25 de janeiro de 1627 - 31 de dezembro de 1691 Se a temperatura do gás for mantida constante, então sua pressão será inversamente proporcional ao seu volume Século XVII



4 4 1 4

TRANSFORMAÇÃO ISOTÉRMICA p 2 , V 2, T p 1 , V 1, T p. V = k ou p 1. V 1 = p 2. V 2 Maior temperatura Menor temperatura

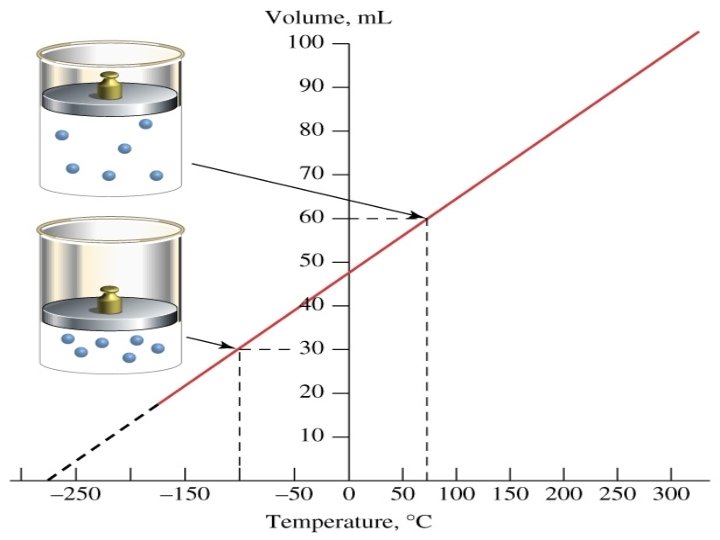
TRANSFORMAÇÃO ISOBÁRICA PRESSÃO permanece CONSTANTE, variando apenas VOLUME e TEMPERATURA

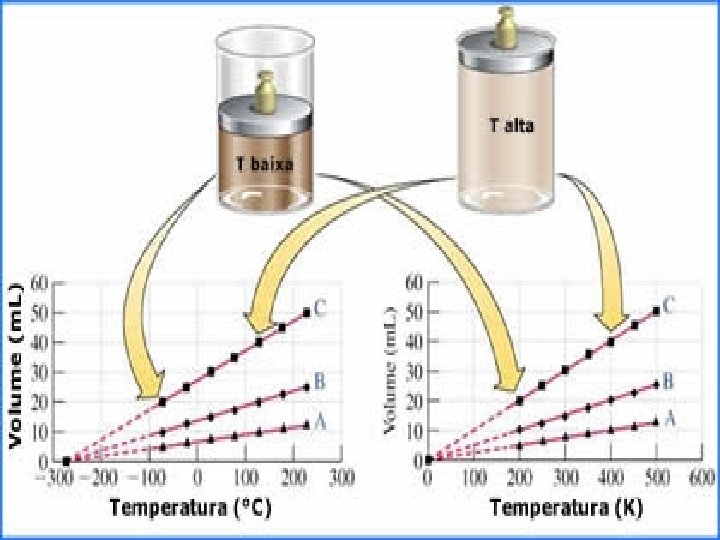
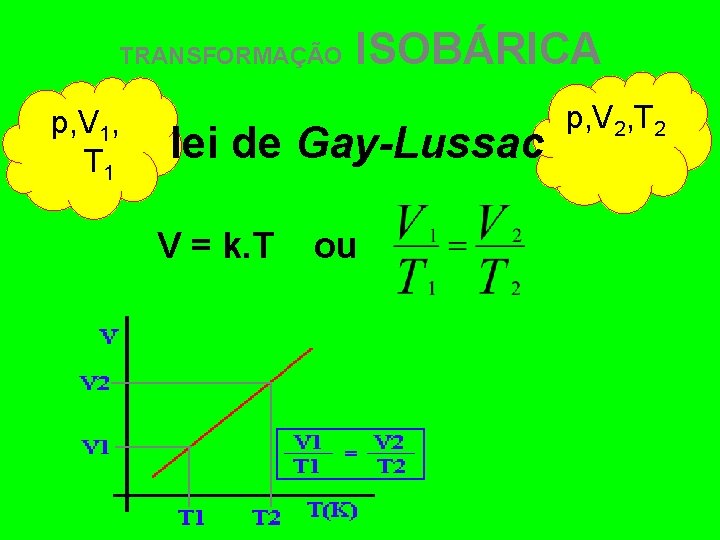
TRANSFORMAÇÃO ISOBÁRICA Obedece a lei de Gay-Lussac 6 de Dezembro de 1778. 9 de Maio de 1850 Século XIX Se a pressão do gás for mantida constante, então seu volume será diretamente proporcional a sua temperatura absoluta (Kelvin), qualquer que seja o gás V T




TRANSFORMAÇÃO p, V 1, T 1 ISOBÁRICA lei de Gay-Lussac V = k. T ou p, V 2, T 2

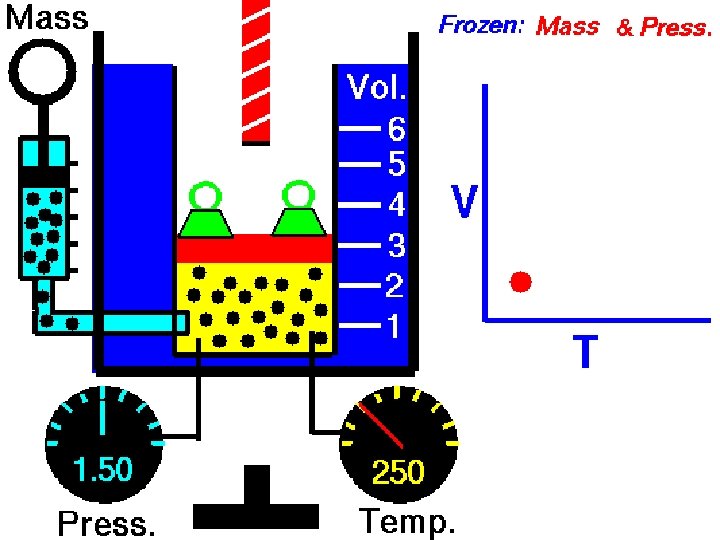
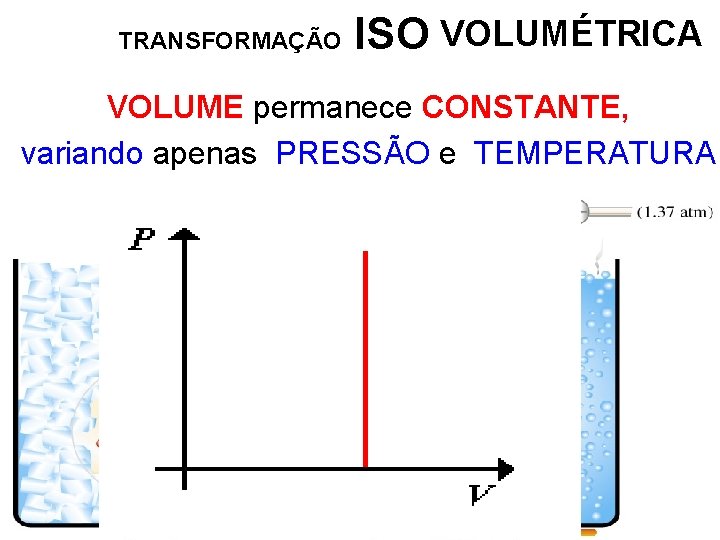
TRANSFORMAÇÃO VOLUMÉTRICA ISOCÓRICA VOLUME permanece CONSTANTE, variando apenas PRESSÃO e TEMPERATURA

ISOVOLUMÉTRICA Obedece a lei de CHARLES TRANSFORMAÇÃO 12 de Novembro de 1746 - 7 de Abril de 1823 Século XIX Se o volume do gás for mantido constante, então sua pressão será diretamente proporcional a sua temperatura absoluta

TRANSFORMAÇÃO p 1, V, T 1 ISOMÉTRICA lei de Charles p = k. T ou p 2, V, T 2

LEI “GERAL” DOS GASES Para uma quantidade constante de gás. . . ou

Lição de Casa Unidade 3 Gases e termodinâmica – Cap. 8 Ler pg. 161 a 166 (fazer resumo) Questões propostas 1 a 6.

Certa massa gasosa sob pressão de 3 atm ocupa o volume de 20 litros à temperatura de 27 °C. Determine: a) o volume ocupado pelo gás a 127 °C, sob a mesma pressão; b) a pressão que o gás exerce a 27 °C quando ocupa o volume de 40 litros; c) em que temperatura o volume de 20 litros do gás exerce a pressão de 5 atm. (E. E. Mauá-SP) Um balão é inflado com oxigênio (M = 32 g), suposto um gás ideal, ficando com volume V = 2, 0 litros e pressão p = 1, 5 atm. Esse enchimento é feito à temperatura t = 20 °C. O balão arrebenta se a pressão atingir 2, 0 atm. Aquecendo-se o balão, observa-se que, imediatamente antes de arrebentar, o seu volume é 3, 0 litros. a) calcule a temperatura em que ocorre arrebentamento. b) calcule a massa do oxigênio que foi colocada no balão.
