Estructuras de Lewis para compuestos y Fuerzas Intermoleculares














- Slides: 22

Estructuras de Lewis para compuestos y Fuerzas Intermoleculares ( Fuerzas de atracción entre compuestos) SEMANA 3 -----2017 Licda. Isabel Fratti de Del Cid Diseño de diapositivas con imágenes e ilustraciones cortesía de Licda: Lilian Judith Guzmán Melgar

Estructuras de Lewis ó fórmulas electrón punto para compuestos En éstas estructuras, se colocan alrededor del símbolo de los átomos participantes, sus electrones de valencia , tratando de que en las uniones formadas, se completen octetos, es decir queden 8 electrones alrededor de cada átomo participante. Los octetos se obtienen cuando los átomos al unirse establecen enlaces iónicos o covalentes ( simples, dobles, triples, coordinados) En algunos casos no se cumplen octetos ( Ejemplo: octetos incompletos ( menos de 8 e-) y expandidos ( más de 8 e -. ) 2 se verán unos ejemplos.

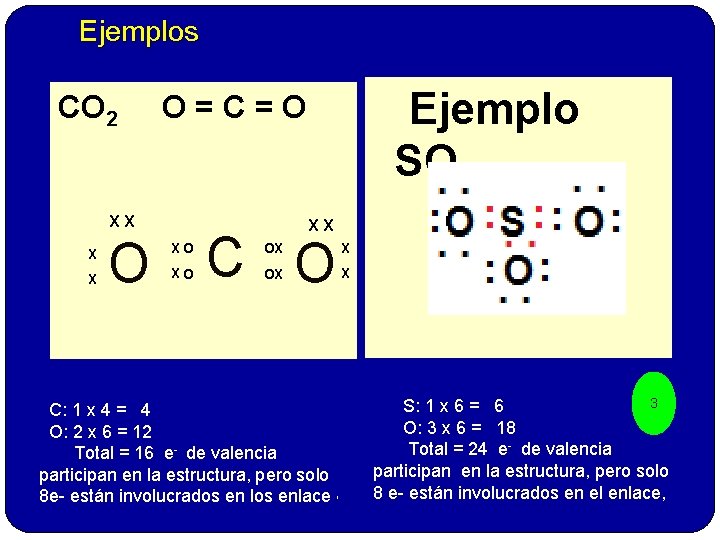
Ejemplos CO 2 XX X X O Ejemplo SO 2 O=C=O XX XO XO C O OX X C: 1 x 4 = 4 O: 2 x 6 = 12 Total = 16 e- de valencia participan en la estructura, pero solo 8 e- están involucrados en los enlace , 3 S: 1 x 6 = 6 O: 3 x 6 = 18 Total = 24 e- de valencia participan en la estructura, pero solo 8 e- están involucrados en el enlace,

Consideraciones generales de las estructuras de LEWIS 1 - Si la fórmula tiene 3 ó más elementos diferentes, se coloca un elemento central( generalmente un no metal diferente al oxígeno como: ( C, N, S, Cl, Br, I). 2 - Si es un oxácido ( Ejs : HNO 3, H 2 CO 3, H 3 PO 4), aunque el H en la fórmula se observa unido al elemento central, no es así, sino se halla unido a uno de los oxígenos formando un enlace simple y ese oxigeno se une al elemento central también formando un enlace simple. Es decir por cada Hidrógeno en el oxácido va a ver un enlace simple H-O y otro enlace simple O-Elemento central, el resto de oxígenos formaran enlaces covalentes dobles (2 e- el oxígeno y 2 e- el elemento central) ó coordinados, donde el par de electrones los 4 pone el elemento central, HASTA COMPLETAR

33 - En oxisales ( K 3 PO 4, Na 2 CO 3), el metal ( Na, K) no se halla unido al elemento central, sino al oxígeno, formando generalmente un enlace iónico( por diferencia de electronegatividad), donde el metal pierde e- y el oxígeno los gana. Este oxigeno se unirá al elemento central a través de un enlace covalente simple. Los otros oxígenos se unirán al elemento central a través de enlaces dobles ó coordinados. Cuando se forman enlaces iónicos en las estructuras de Lewis, no se observan octetos al rededor de los metales que pierden sus electrones de valencia, pues al perder e- los metales logran un octeto interno y éstos no se muestran en 5 éstas estructuras. En los átomos que forman enlaces

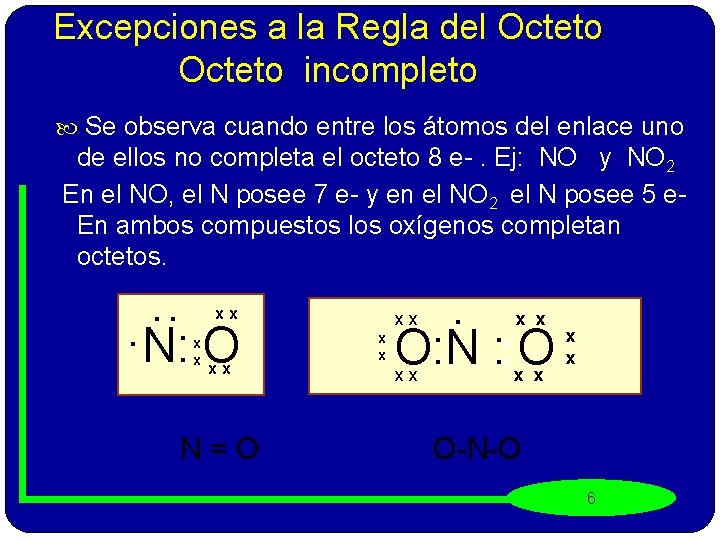
Excepciones a la Regla del Octeto incompleto Se observa cuando entre los átomos del enlace uno de ellos no completa el octeto 8 e-. Ej: NO y NO 2 En el NO, el N posee 7 e- y en el NO 2 el N posee 5 e. En ambos compuestos los oxígenos completan octetos. . xx N: O x x xx N=O xx x x O: N : O xx x x x O-N-O 6

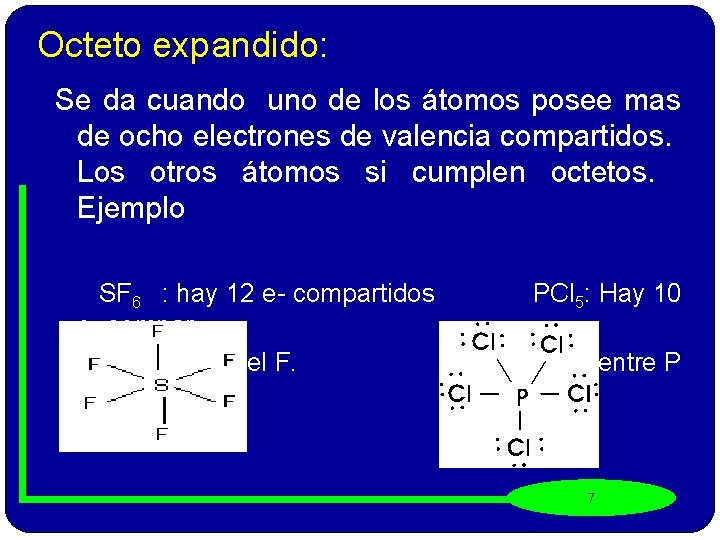
Octeto expandido: Se da cuando uno de los átomos posee mas de ocho electrones de valencia compartidos. Los otros átomos si cumplen octetos. Ejemplo SF 6 : hay 12 e- compartidos e- comparentre el S y el F. y Cl. PCl 5: Hay 10 tidos entre P 7

Elabore las estructuras de Lewis, para los siguientes compuestos, e indique los tipos de enlaces presentes: Iónicos, covalentes simples, dobles, coordinados. H 2 CO 3 K 3 PO 4

HNO 3 SO 2

Na. HCO 3 K 2 SO 4

FUERZAS INTERMOLECULARES (Fuerzas de Atracción Intermoleculares) Las fuerzas intermoleculares son las atracciones mutuas entre moléculas, son mucho mas débiles que los enlaces covalentes y iónicos pero contribuyen a determinar las propiedades físicas de la sustancias moleculares. Como grupo también reciben el nombre de Fuerzas de van der Waals o Fuerzas atractivas en compuestos. 11

Tipos de Fuerzas Intermoleculares ( Atracciones entre compuestos) Fuerzas dipolares (dipolo-dipolo) Puentes de hidrógeno Fuerzas de dispersión ( Fuerzas de London) 12

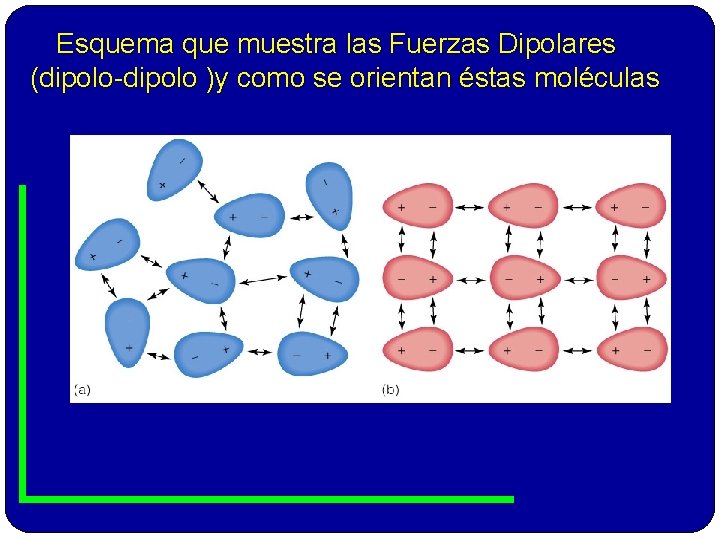
Fuerzas Dipolares (dipolo-dipolo) Se da si la molécula presenta enlace covalente polar ( diferencia de electronegatividad >0. 4 y < 1. 8 ). El extremo parcialmente positivo ( + ) se atrae con el extremo parcialmente negativo ( - ). Estas atracciones son permanentes. Los símbolos δ+ y δ-, indican parcialmente positivo ó negativo, quiere decir, que ningún átomo del enlace perdió ó gano e( no se formaron iones), solo los comparten de forma desigual 13

Esquema que muestra las Fuerzas Dipolares (dipolo-dipolo )y como se orientan éstas moléculas Insert figure 13. 2

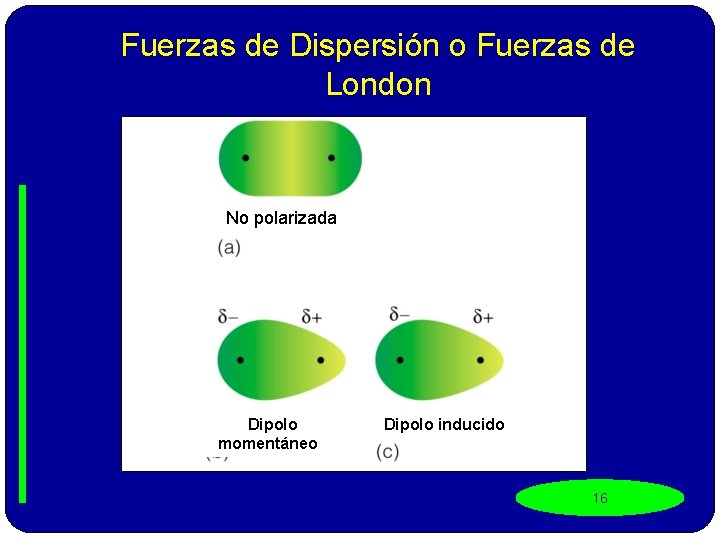
Fuerzas de Dispersión (Fuerzas de London ó dipolos transitorios). Son transitorias , se dan entre moléculas NO polares ( Diferencia de electronegatividad entre o. o-o. 4). Ej: Elementos diatómicos (H 2 ; O 2 ; N 2 ; F 2 ; Cl 2 ; Br 2 ; I 2 ) o moléculas como Si. H 4, Sb. H 3 Los electrones en movimiento, se localizan en una región momentáneamente dándole a esa región una carga parcialmente negativa (δ-), y el otro extremo queda parcialmente positivo (δ+). En éste momento hay atracción. Al moverse los e-, se pierden la polarización y la atracción desaparece, luego vuelven a polarizarse y nuevamente, hay atracción ( por eso se llaman fuerzas de dispersión 15 ó dipolos transitorios).

Fuerzas de Dispersión o Fuerzas de London No polarizada Dipolo momentáneoo Dipolo inducido 16

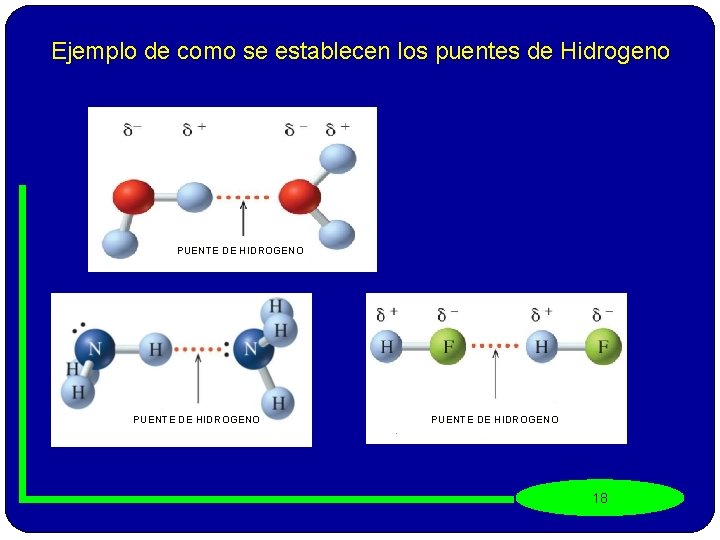
Puentes de Hidrógeno Son las fuerzas intermoleculares entre moléculas polares que contienen átomos de hidrógeno unidos a flúor, oxígeno o nitrógeno. El Hidrogeno menos electronegativo que el F, O y N manifiesta una carga parcialmente positiva, que se atrae con las cargas parcialmente negativas del O y N y F. No basta con que la moléculas poseen H, N, F u O, debe haber una unión directa entre el Hidrógeno y el N, ó el F ó el O. Los puentes de Hidrógenos son más fuertes o intensos, que las fuerzas dipolo-dipolo y las de London. Ej: NH 3, H 2 O, HF La estructura tridimensional de moléculas de gran importancia biológica como proteínas y ácidos 17 nucleicos, se debe en gran parte a éstas fuerzas.

Ejemplo de como se establecen los puentes de Hidrogeno PUENTE DE HIDROGENO 18

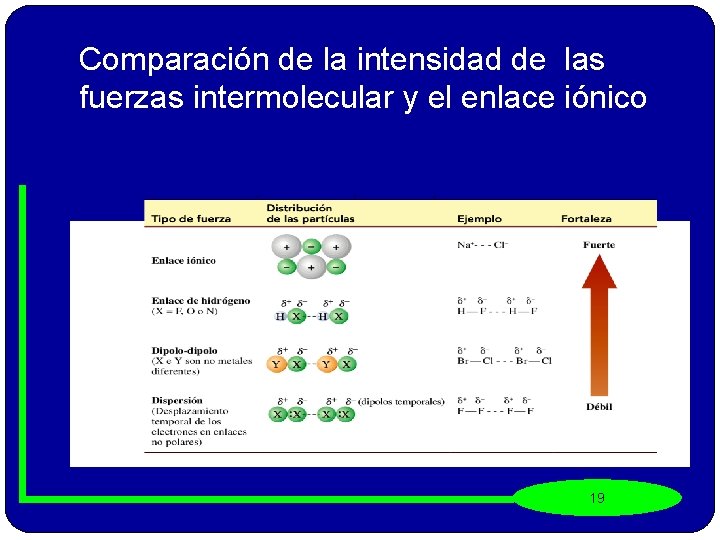
Comparación de la intensidad de las fuerzas intermolecular y el enlace iónico 19

Ejercicio : diga que tipo de fuerzas intermoleculares, presentan los siguientes compuestos a) HBr _________ b) H 2 O_________ c) Br 2_________ d) NH 3______________ e) H 2 S__________ BH 3____________ g) H 2 Se____________ f) 20

Ejercicios adicionales 1 A-Con cual (cuales) de los siguientes átomos : ( O, Cl , N, S, H , Br, Ge) al combinarse el Hidrogeno, formara: A- Enlace covalente polar : ____ B- Puente de Hidrógeno : _____ C- Fuerzas de dispersión o London : _______ 1 B- Haga un esquema de como se producirían los enlaces de hidrogeno , entre NH 3 y H 2 O

2 - Escriba la estructura de Lewis de una molécula hipotética ( A 3 B X 4 ) donde cada átomo de A, forme un enlace covalente simple con X y que a la vez X, forme un enlace covalente simple con B y que el otro átomo de X forme un enlace covalente coordinado con B, donde únicamente B ponga el par de e-, recuerde en éste caso los átomos B y X cumplen octeto, los átomos A solo poseen un electrón de valencia, por lo tanto no muestran octeto, sino que solo se observaran 2 electrones entre A y X)