Die Zukunft soll man nicht voraussehen wollen sondern


















- Slides: 27

Die Zukunft soll man nicht voraussehen wollen, sondern möglich machen. Antoine de Saint-Exupery Die Forschungsziele der Umweltchemie begründen sich auf dem in den vergangenen Jahrzehnten erwachten Umweltbewusstsein der Gesellschaft und der damit verbundenen neuen Verantwortung des Chemikers. Durch den technischen Fortschritt ist vieles machbar geworden, das früher unmöglich erschien, und wird ohne Rücksicht auf die Bedürfnisse der Ökosysteme in großem Maßstab weltweit umgesetzt. Jedes mit den Bedürfnissen der Natur inkompatible Verhalten des Menschen führt zur Degradation von Ökosystemen und zum Schwund der Artenvielfalt unseres Planeten. Gravierende Umweltprobleme, welche die Funktionsfähigkeit der Ökosysteme beeinträchtigen und die Menschheit zunehmend belasten, harren derzeit einer Lösung. Hier kann die umweltchemische Forschung einen unverzichtbaren Beitrag leisten, indem sie die chemischen Vorgänge in der natürlichen Umwelt untersucht. Zum Einsatz kommen Methoden der analytischen und präparativen Chemie. Die Entwicklung neuartiger Technologien zur Vermeidung von Umweltproblemen gehört mit zu den Forschungszielen. Die beobachteten natürlichen Systeme sind äußerst komplex. Daher kann in vielen Fällen nur ein interdisziplinärer Ansatz zum Erfolg führen d. h. Kooperationen mit Umwelt-Geowissenschaften, Umwelt. Physik, Umwelt-Meteorologie, Umwelt-Mikrobiologie, Ökologie u. a. Vorlesung Anorganische Chemie I Vorlesungsteil Umweltchemie

A (slightly vandalized) warning sign cautioning against consuming too many bass caught in Everglades National Park due to high mercury content. The sign is located at Nine Mile Pond. From Wikipedia

Lehrbücher: • Hollemann-Wiberg, Lehrbuch der Anorganischen Chemie, 102. Auflage. Berlin, New York: de Gruyter, 2007. • W. Kaim, B. Schwederski: Bioanorganische Chemie. Zur Funktion chemischer Elemente in Lebensprozessen. Teubner, 4. Auflage 2005. • L. Sigg, W. Stumm: Aquatische Chemie - eine Einführung in die Chemie wässriger Lösungen und natürlicher Gewässer. vdf Hochschulverlag an der ETH Zürich. Teubner, 1996. • Claus Bliefert: Umweltchemie. Wiley-VCH, Weinheim 2002.

Umweltproblem Plastikmüll • • http: //www. derbagger. org/artikel/der_alte_muell_und_das_meer http: //onebigbadwolf. blogspot. com/2011/01/save-world-saturday-sea-of-garbage. html

Basstölpel auf Helgoland heute Quelle: Wikpedia

http: //thingsthatmakeyougogreen. com/plastics-are-evil-part-1 -the-great / -pacific-garbage-patch/2008/05/28

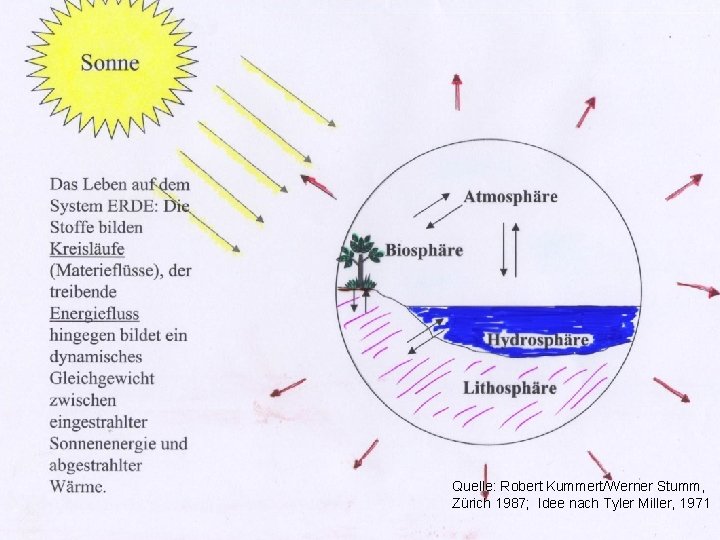
Quelle: Robert Kummert/Werner Stumm, Zürich 1987; Idee nach Tyler Miller, 1971



CO 2 • Kohlendioxid steht im Zentrum der geochemischen Kreisläufe • spielt eine zentrale Rolle in der Biosphäre: Photosynthese – Respiration • und in geochemischen Prozessen, welche Gesteine auflösen und Minerale bilden • In der Hydrosphäre wird Kohlenstoff vor allem als Ca(HCO 3)2 transportiert • Ca. CO 3 wird in Seen und im Ozean ausgefällt

Kohlenstoff-Flüsse (1015 g/a) • • • Netto-Primärproduktion der terrestrischen Biosphäre 57 – 58 Netto-Primärproduktion der marinen Biosphäre 54 – 59 Bildung von Kalkskeletten im Ozean (Coccolithophoriden, Foraminiferen, Kalkalgen, Korallen) 1 Marine physikalische Kohlenstoffpumpe 40 Marine biologische Kohlenstoffpumpe 11 – 16 C-Speicherung in Böden 1 • Diese natürlichen Senken werden durch natürliche Quellen (Atmung, Vulkanismus, Ausgasen aus dem Meer) kompensiert • In 5 Jahren wird das gesamte CO 2 der Atmosphäre ausgetauscht • Anthropogene CO 2 Freisetzung aus fossilen Brennstoffen 7


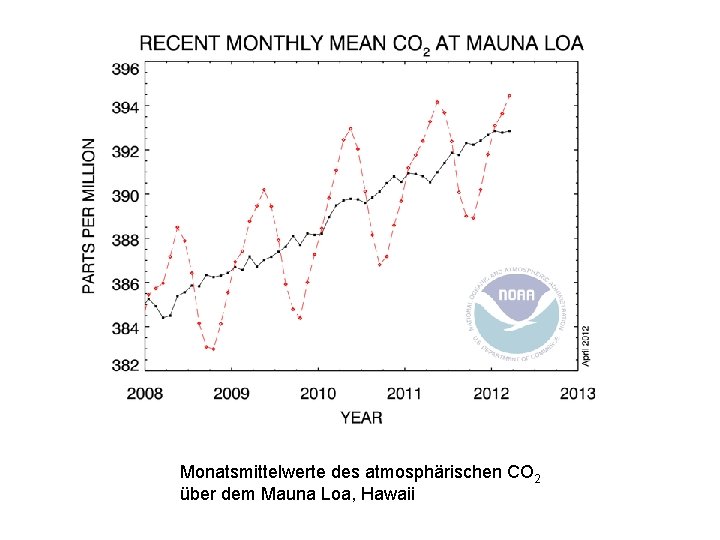
Monatsmittelwerte des atmosphärischen CO 2 über dem Mauna Loa, Hawaii

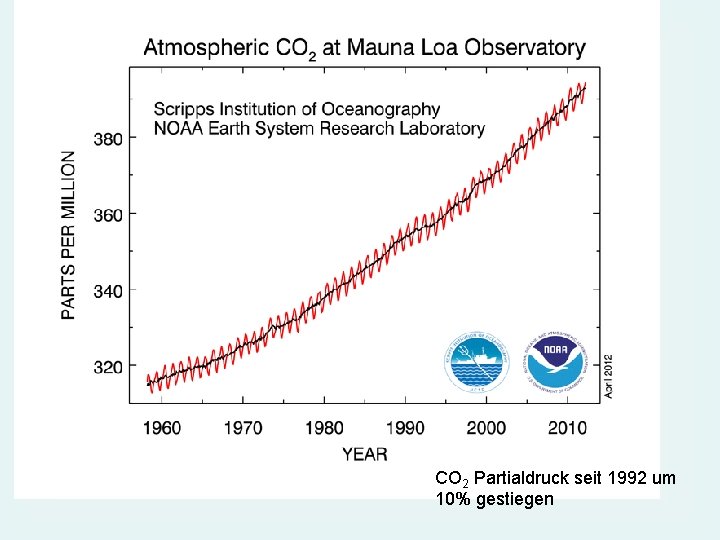
INSTITUT FÜR ANORGANISCHE CHEMIE Arbeitsgruppe Umwelt- und Radiochemie CO 2 Partialdruck seit 1992 um 10% gestiegen

INSTITUT FÜR ANORGANISCHE CHEMIE Anthropogene CO 2 Quellen Arbeitsgruppe Umwelt- und Radiochemie • Verbrennen fossiler Energieträger, Zementherstellung • Brandrodung tropischer Wälder, Torfbrände • Tauender Permafrostboden, Entwässerung von Mooren

Tauender Permafrost INSTITUT FÜR ANORGANISCHE CHEMIE Arbeitsgruppe Umwelt- und Radiochemie • • • 1700 Gt org. C lagern in Permafrostböden (in der Atmosphäre derzeit ca. 720 Gt C als CO 2) In den nächsten 30 Jahren werden durch Auftauen von Permafrostböden ca. 45 Gt Kohlenstoff zusätzlich in die Atmosphäre gelangen, als Kohlendioxid oder Methan Quelle: E. A. G. Schuur und B. Abbott (2011). Climate change: High risk of permafrost thaw; Nature 480, 32– 33 (2011). http: //stephenleahy. net/2011/02/22/permafrost -melt-soon-irreversible-without-major-fossilfuel-cuts/ http: //www. klimanotizen. de/html/newsletter_14. html Jon Randon, NASA

INSTITUT FÜR ANORGANISCHE CHEMIE Arbeitsgruppe Umwelt- und Radiochemie

INSTITUT FÜR ANORGANISCHE CHEMIE Arbeitsgruppe Umwelt- und Radiochemie Antarktischer Eisbohrkern http: //www. gzg. uni-goettingen. de/studium/rundgang. htm

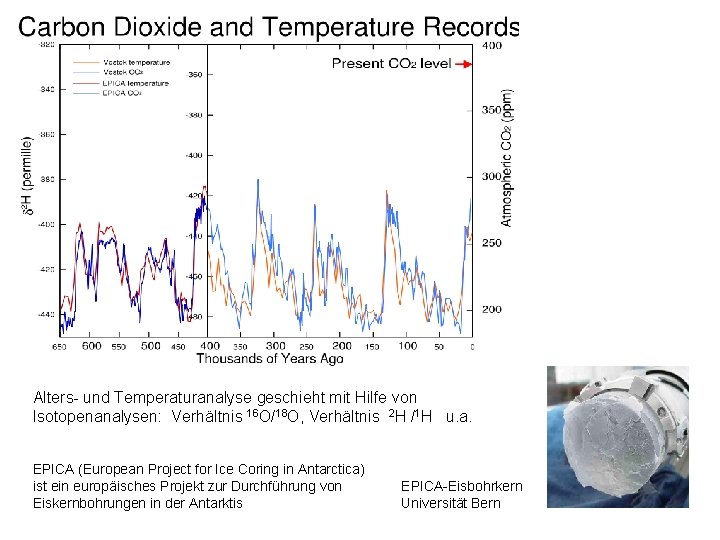
Alters- und Temperaturanalyse geschieht mit Hilfe von Isotopenanalysen: Verhältnis 16 O/18 O, Verhältnis 2 H /1 H u. a. EPICA (European Project for Ice Coring in Antarctica) ist ein europäisches Projekt zur Durchführung von Eiskernbohrungen in der Antarktis EPICA-Eisbohrkern Universität Bern

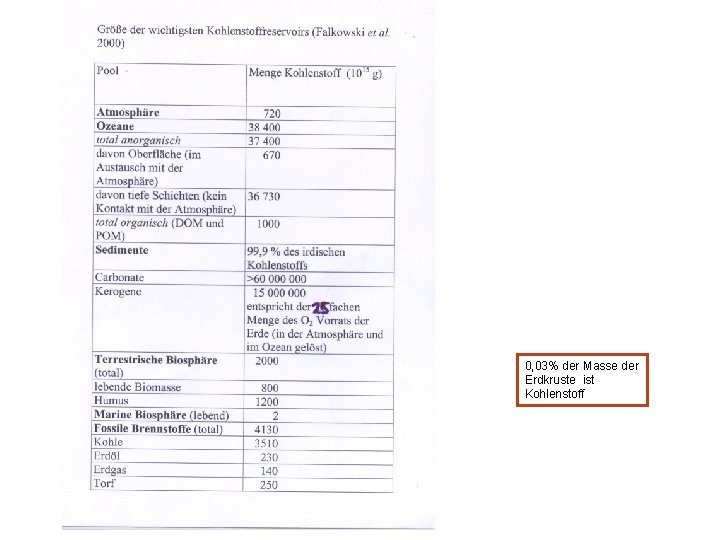
0, 03% der Masse der Erdkruste ist Kohlenstoff

Das Carbonatsystem der Ozeane und Binnengewässer HCO 3 -, CO 32 - Enthält 60 x soviel Kohlenstoff wie die Atmosphäre Ist das größte Kohlenstoffreservoir der Biosphäre

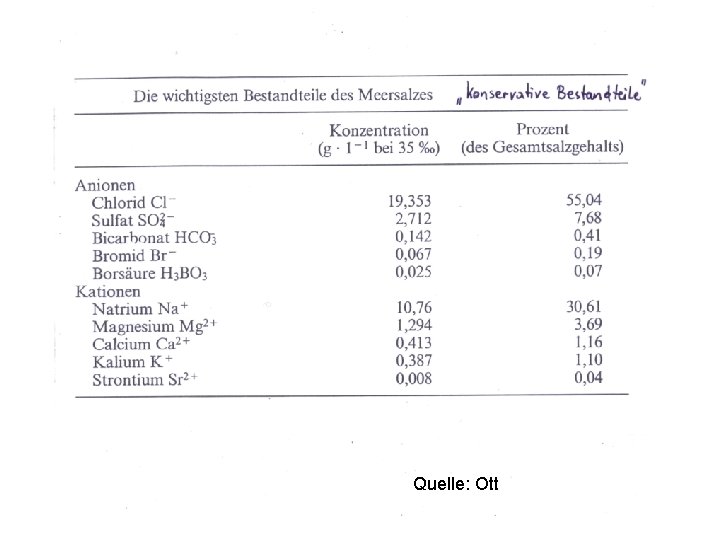
Quelle: Ott


Bei der Verwitterung der Silicate der Erdkruste wird CO 2 verbraucht: z. B. Kalkfeldspat (Anorthit) Ca. Al 2 Si 2 O 8 + 2 H 2 O + 2 CO 2 = H 2 Al 2 Si 2 O 8 + Ca(HCO 3)2 (gelöst) Beim Ausfallen der Carbonate im Ozean wird die Hälfte des bei der Verwitterung der Silicate verbrauchten CO 2 wieder frei: Ca 2+ + 2 HCO 3 - = Ca. CO 3 + H 2 O + CO 2

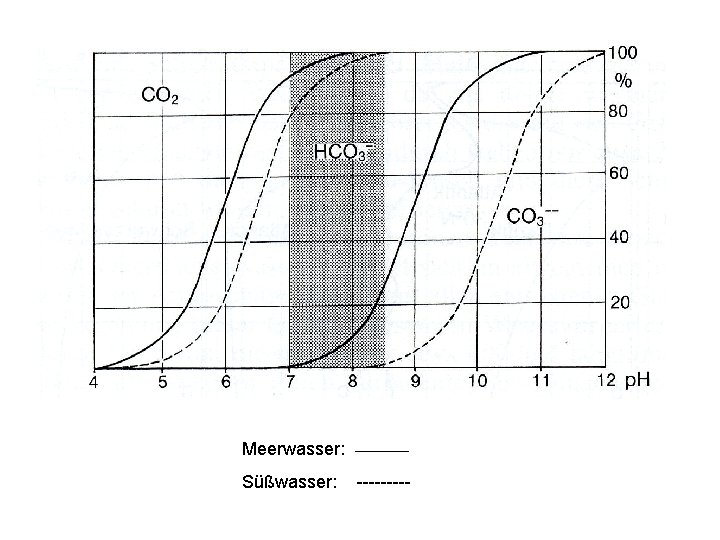
Meerwasser: ____ Süßwasser: -----

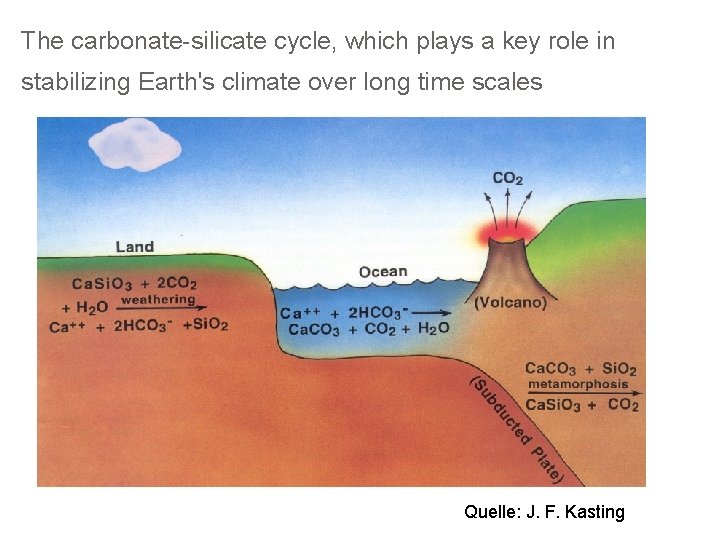
Geochemischer Carbonat-Silicat Kreislauf Verwitterung von Kalk- oder Silicatgestein verbraucht CO 2 Ca 2 Si. O 4+4 H 2 O+4 CO 2→ 2 Ca(HCO 3)2+Si(OH)4 (gelöst) Im Meer scheidet sich Kalk ab 2 Ca(HCO 3)2→ 2 Ca. CO 3↓+2 H 2 O+2 CO 2↑ Es bilden sich Kalksedimente. In diesem Reservior verbleibt der Kohlenstoff Jahrmillionen. An den Kontinentalrändern schiebt sich der Meeresboden unter die Landmassen (Subduktion), unter hohen Drucken und Temperaturen reagiert dort das Calciumcarbonat mit Quarz 2 Ca. CO 3+Si. O 2→Ca 2 Si. O 4+2 CO 2↑

The carbonate-silicate cycle, which plays a key role in stabilizing Earth's climate over long time scales Quelle: J. F. Kasting