CAPITOLO La struttura dellatomo 4 Indice 1 La










- Slides: 17

CAPITOLO La struttura dell’atomo 4 Indice 1. La carica elettrica 2. Le particelle subatomiche 3. Radioattività 4. Il modello atomico di Rutherford Mappa concettuale: Atomo 5. Numero atomico e numero di massa 6. Isotopi 7. Ioni 8. Massa degli atomi individuali 9. Massa atomica di un elemento 10. Massa molecolare © Paolo Pistarà © Istituto Italiano Edizioni Atlas 1

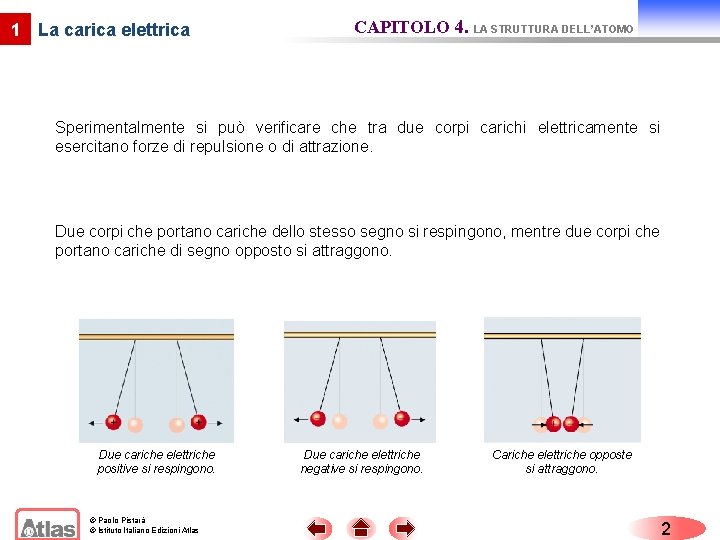
1 La carica elettrica CAPITOLO 4. LA STRUTTURA DELL’ATOMO Sperimentalmente si può verificare che tra due corpi carichi elettricamente si esercitano forze di repulsione o di attrazione. Due corpi che portano cariche dello stesso segno si respingono, mentre due corpi che portano cariche di segno opposto si attraggono. Due cariche elettriche positive si respingono. © Paolo Pistarà © Istituto Italiano Edizioni Atlas Due cariche elettriche negative si respingono. Cariche elettriche opposte si attraggono. 2

2 Le particelle subatomiche CAPITOLO 4. LA STRUTTURA DELL’ATOMO Le particelle subatomiche più importanti per la chimica sono: gli elettroni, i protoni e i neutroni. u Elettroni Gli elettroni sono particelle con carica negativa. All’elettrone si assegna convenzionalmente carica 1. Gli elettroni costituiscono i raggi catodici. Tubo catodico. © Paolo Pistarà © Istituto Italiano Edizioni Atlas 3

2 Le particelle subatomiche CAPITOLO 4. LA STRUTTURA DELL’ATOMO u Protoni I protoni sono particelle la cui massa, determinata sperimentalmente, è: 1, 673 10 24 g. Ciascun protone ha una massa 1836 volte quella di un elettrone. Per convenzione al protone si assegna carica + 1. u Neutroni Il neutrone è una particella subatomica che non presenta carica elettrica (carica elettrica zero). La massa di un neutrone è circa uguale a quella di un protone: 1, 675 10 24 g © Paolo Pistarà © Istituto Italiano Edizioni Atlas 4

3 Radioattività CAPITOLO 4. LA STRUTTURA DELL’ATOMO La radioattività è l’emissione spontanea di energia e di particelle dal nucleo atomico. Gli elementi radioattivi possono emettere tipi di radiazioni: • radiazioni alfa ( ) • radiazioni beta (β) • radiazioni gamma (γ) © Paolo Pistarà © Istituto Italiano Edizioni Atlas 5

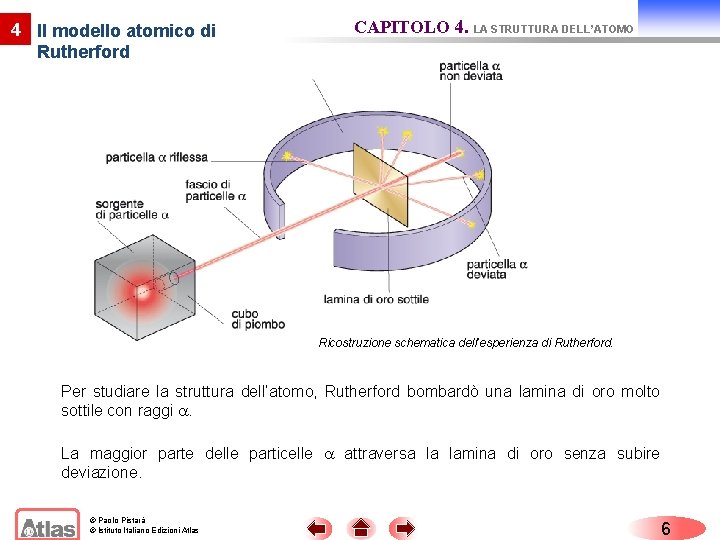
4 Il modello atomico di Rutherford CAPITOLO 4. LA STRUTTURA DELL’ATOMO Ricostruzione schematica dell’esperienza di Rutherford. Per studiare la struttura dell’atomo, Rutherford bombardò una lamina di oro molto sottile con raggi . La maggior parte delle particelle attraversa la lamina di oro senza subire deviazione. © Paolo Pistarà © Istituto Italiano Edizioni Atlas 6

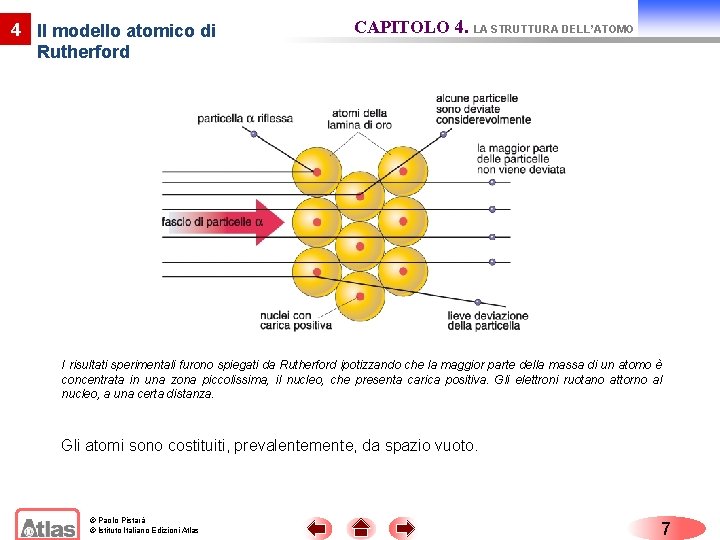
4 Il modello atomico di Rutherford CAPITOLO 4. LA STRUTTURA DELL’ATOMO I risultati sperimentali furono spiegati da Rutherford ipotizzando che la maggior parte della massa di un atomo è concentrata in una zona piccolissima, il nucleo, che presenta carica positiva. Gli elettroni ruotano attorno al nucleo, a una certa distanza. Gli atomi sono costituiti, prevalentemente, da spazio vuoto. © Paolo Pistarà © Istituto Italiano Edizioni Atlas 7

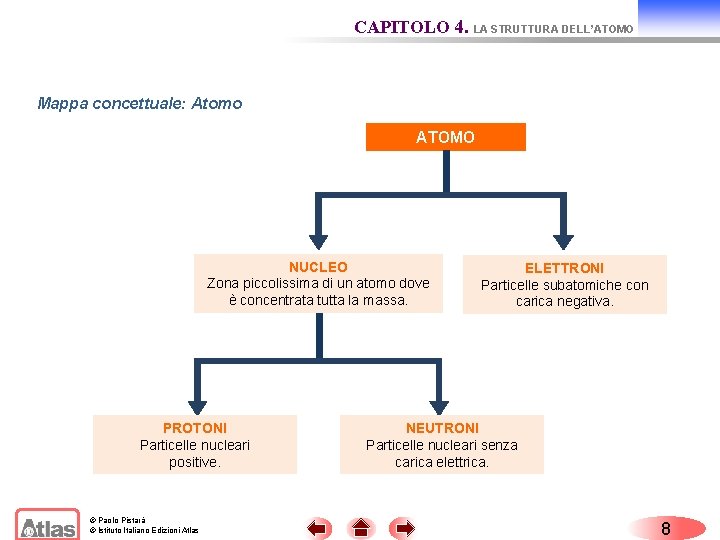
CAPITOLO 4. LA STRUTTURA DELL’ATOMO Mappa concettuale: Atomo ATOMO NUCLEO Zona piccolissima di un atomo dove è concentrata tutta la massa. PROTONI Particelle nucleari positive. © Paolo Pistarà © Istituto Italiano Edizioni Atlas ELETTRONI Particelle subatomiche con carica negativa. NEUTRONI Particelle nucleari senza carica elettrica. 8

5 Numero atomico e numero di massa CAPITOLO 4. LA STRUTTURA DELL’ATOMO Il numero di protoni presenti nel nucleo di un atomo è detto numero atomico e si indica con Z. Il numero atomico viene evidenziato in basso, a sinistra del simbolo dell’elemento: 6 C Il carbonio con Z uguale a 6 ha sei protoni e, quindi, sei elettroni perché un atomo è elettricamente neutro. © Paolo Pistarà © Istituto Italiano Edizioni Atlas 9

CAPITOLO 4. LA STRUTTURA DELL’ATOMO 5 Numero atomico e numero di massa Il numero di massa corrisponde al numero totale di protoni e di neutroni contenuti nel nucleo di un atomo e si indica con A. 12 C Il numero di massa viene riportato in alto, a sinistra del simbolo dell’elemento. Il carbonio con A uguale a 12 contiene 6 protoni e 6 neutroni. © Paolo Pistarà © Istituto Italiano Edizioni Atlas 10

CAPITOLO 4. LA STRUTTURA DELL’ATOMO 6 Isotopi Per isotopi s’intendono gli atomi di uno stesso elemento che hanno numeri differenti di neutroni. Il rame, ad esempio, presenta due isotopi che possono essere così rappresentati: 63 Cu 29 65 29 Cu (simboli nucleari) oppure rame-63 rame-65 numero di massa numero atomico = numero di neutroni © Paolo Pistarà © Istituto Italiano Edizioni Atlas 11

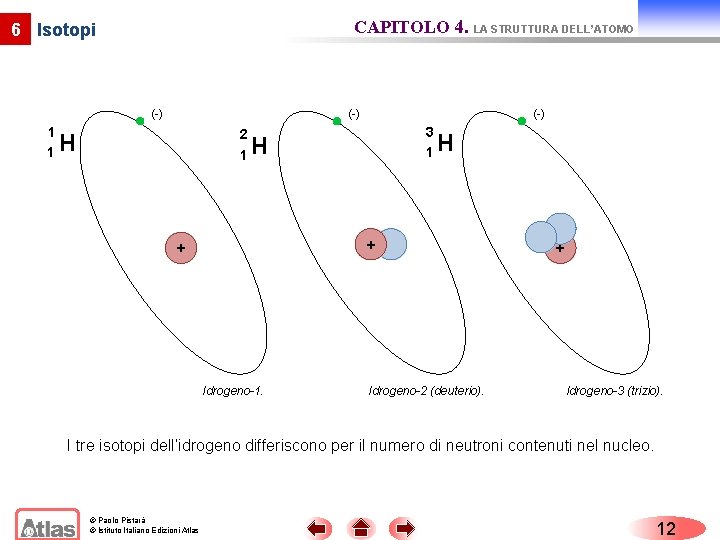
CAPITOLO 4. LA STRUTTURA DELL’ATOMO 6 Isotopi (-) 1 1 (-) 2 1 H (-) 3 1 H H + + Idrogeno-1. Idrogeno-2 (deuterio). + Idrogeno-3 (trizio). I tre isotopi dell’idrogeno differiscono per il numero di neutroni contenuti nel nucleo. © Paolo Pistarà © Istituto Italiano Edizioni Atlas 12

CAPITOLO 4. LA STRUTTURA DELL’ATOMO 7 Ioni In una reazione chimica gli atomi neutri possono perdere o acquistare elettroni. Le particelle elettricamente cariche si formano sono chiamate ioni. Gli ioni positivi sono chiamati cationi. Gli ioni negativi sono chiamati anioni. I composti che contengono cationi e anioni sono chiamati composti ionici. © Paolo Pistarà © Istituto Italiano Edizioni Atlas 13

CAPITOLO 4. LA STRUTTURA DELL’ATOMO 8 Massa degli atomi individuali La massa di un singolo atomo, determinata con lo spettrometro di massa, indica quante volte la massa dell’atomo è maggiore (più pesante) rispetto all’unità di massa atomica. L’unità di massa atomica (simbolo u) corrisponde a 1/12 della massa del carbonio-12. Massa delle particelle subatomiche © Paolo Pistarà © Istituto Italiano Edizioni Atlas Nome Massa (g) Massa (u) Protone 1, 673 x 10− 24 1, 007276 Neutrone 1, 675 x 10− 24 1, 008665 Elettrone 9, 109 x 10− 28 0, 000549 14

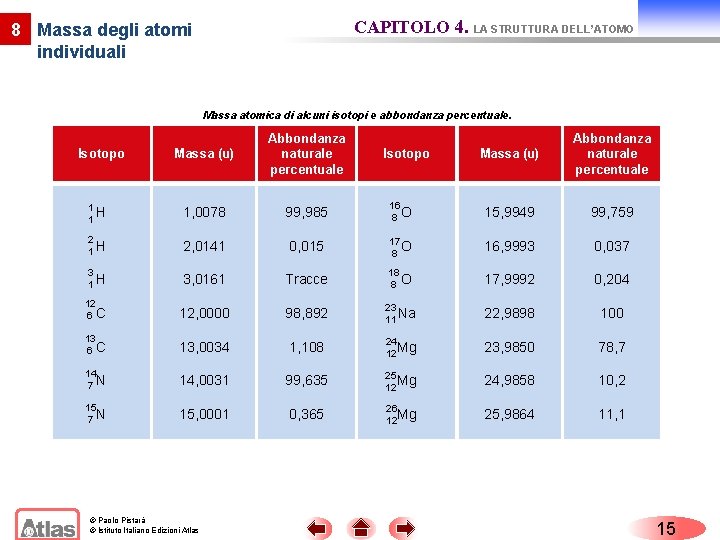
CAPITOLO 4. LA STRUTTURA DELL’ATOMO 8 Massa degli atomi individuali Massa atomica di alcuni isotopi e abbondanza percentuale. Massa (u) Abbondanza naturale percentuale 1 H 1 1, 0078 99, 985 16 8 O 15, 9949 99, 759 2 1 H 2, 0141 0, 015 17 O 8 16, 9993 0, 037 3 1 H 3, 0161 Tracce 18 8 O 17, 9992 0, 204 12 6 C 12, 0000 98, 892 23 11 Na 22, 9898 100 13 6 C 13, 0034 1, 108 24 Mg 12 23, 9850 78, 7 14 7 N 14, 0031 99, 635 25 Mg 12 24, 9858 10, 2 15 7 N 15, 0001 0, 365 26 Mg 12 25, 9864 11, 1 Isotopo © Paolo Pistarà © Istituto Italiano Edizioni Atlas Isotopo 15

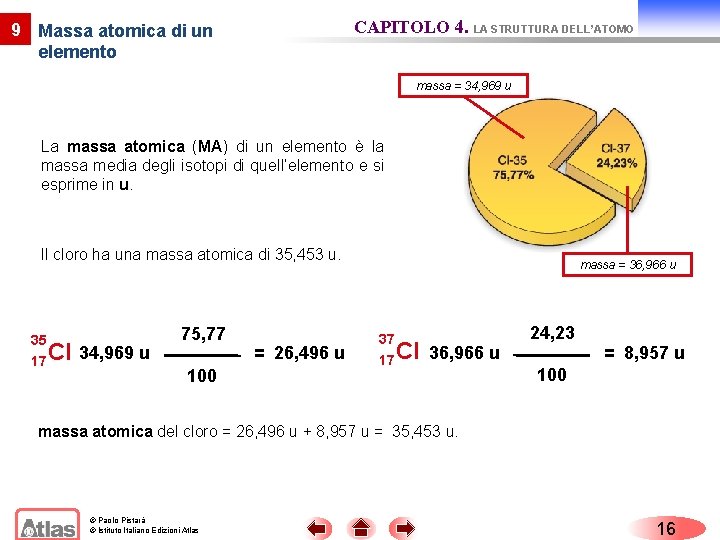
CAPITOLO 4. LA STRUTTURA DELL’ATOMO 9 Massa atomica di un elemento massa = 34, 969 u La massa atomica (MA) di un elemento è la massa media degli isotopi di quell’elemento e si esprime in u. Il cloro ha una massa atomica di 35, 453 u. 35 17 Cl 34, 969 u 75, 77 100 = 26, 496 u massa = 36, 966 u 37 17 Cl 36, 966 u 24, 23 = 8, 957 u 100 massa atomica del cloro = 26, 496 u + 8, 957 u = 35, 453 u. © Paolo Pistarà © Istituto Italiano Edizioni Atlas 16

10 CAPITOLO 4. LA STRUTTURA DELL’ATOMO Massa molecolare La massa molecolare (MM) di un composto è uguale alla somma delle masse di tutti gli atomi presenti nella sua formula. Calcolo della massa molecolare del cloroetano, CH 3 CH 2 Cl: 2 atomi di C = 2 12, 01 = 24, 02 u 5 atomi di H = 5 1, 01 = 1 atomo di Cl = 1 35, 45 = 35, 45 u massa molecolare © Paolo Pistarà © Istituto Italiano Edizioni Atlas 5, 05 u Modello molecolare del cloroetano 64, 52 u 17