Dalle soluzioni alla chimica del carbonio Capitolo 8

Dalle soluzioni alla chimica del carbonio

Capitolo 8 Reazioni chimiche Unità 25 Reazioni ed equazioni chimiche 8. 1 Le equazioni chimiche 8. 2 Bilanciamento delle equazioni chimiche Unità 26 Stechiometria e tipi di reazioni 8. 3 Stechiometria della reazioni chimiche 8. 4 Il reagente limitante 8. 5 Stechiometria delle reazioni in soluzione 8. 6 Stechiometria delle reazioni in fase gassosa 8. 7 La resa di reazione 8. 8 Classificazione delle reazioni chimiche Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 2

8. 1 Le equazioni chimiche Con il termine reazione chimica si intende il processo in cui, a partire ad una o più sostanze, i reagenti, si assiste alla formazione di uno o più composti, i prodotti. Il processo può essere scritto come A+B+C→D+E Nelle opportune condizioni ogni composto può combinarsi con un altro e dare origine a nuovi prodotti purché diminuisca l’energia complessiva dei legami. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 3

8. 1 Le equazioni chimiche In genere lo svolgimento di una reazione chimica è segnalato da variazioni nel sistema chimico, come: mutamento di colore di alcune sostanze sviluppo di energia termica o luminosa liberazione di gas Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 4

8. 1 Le equazioni chimiche In genere lo svolgimento di una reazione chimica è segnalato da variazioni nel sistema chimico, come: cambiamento di sapore formazione di un precipitato Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 5
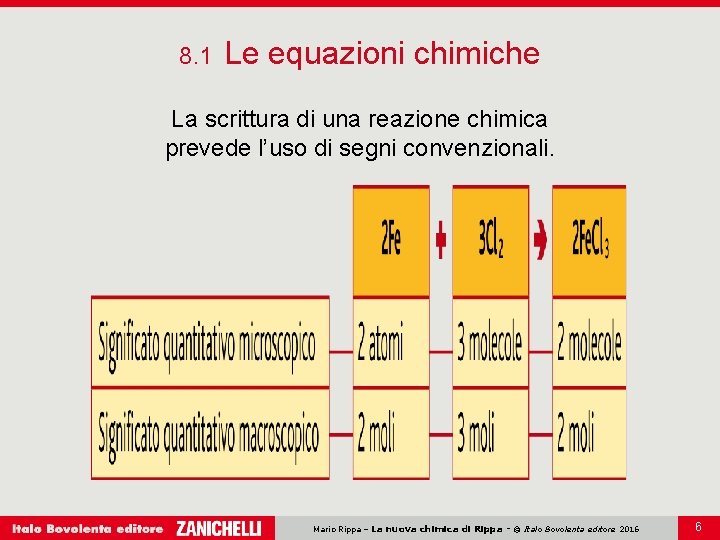
8. 1 Le equazioni chimiche La scrittura di una reazione chimica prevede l’uso di segni convenzionali. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 6

8. 2 Bilanciamento delle equazioni chimiche La descrizione completa di una reazione richiede il bilanciamento delle masse di tutti gli elementi in gioco. Per bilanciare una reazione si pongono davanti alle formule di ciascuna specie chimica dei coefficienti stechiometrici in modo da mantenere l’uguaglianza tra il numero di atomi nei reagenti e nei prodotti (legge di conservazione della massa di Lavoisier). Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 7

8. 2 Bilanciamento delle equazioni chimiche Si procede bilanciando in ordine: i metalli, i non metalli, l’idrogeno. Al termine si verifica che le quantità di ossigeno corrispondano. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 8

8. 3 Stechimetria delle reazioni chimiche La stechiometria è lo studio delle relazioni quantitative tra le sostanze in una reazione chimica. I coefficienti stechiometrici di una reazione chimica indicano sia il numero di particelle delle sostanze coinvolte sia il loro numero di moli. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 9

8. 3 Stechiometria delle reazioni chimiche La quantità di prodotti che si formano duranti una reazione può essere calcolata considerando i rapporti stechiometrici tra le sostanze coinvolte. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 10

8. 4 Il reagente limitante La sostanza reagente presente in quantità minore, rispetto al rapporto molare della reazione bilanciata, viene consumata completamente ed è chiamata reagente limitante. Il reagente limitante è la sostanza che si esaurisce per prima durante una reazione e che limita la quantità di prodotto che si ottiene. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 11

8. 5 Stechiometria nelle reazioni in soluzione La maggior parte delle reazioni chimiche avvengono in soluzione. Nelle soluzioni la quantità dei reagenti e dei prodotti sono espresse tramite la loro concentrazione e il loro volume. La titolazione è un procedimento analitico che permette di determinare la concentrazione di una soluzione attraverso la misura del volume di una soluzione a concentrazione nota che viene fatta reagire in modo completo con un dato volume della soluzione incognita. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 12

8. 5 Stechiometria nelle reazioni in soluzione In una titolazione il titolante viene aggiunto lentamente a una quantità nota di titolato. Nel momento in cui tutta la soluzione incognita ha reagito, si interrompe l’aggiunta di soluzione titolante e si registra il valore del volume aggiunto. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 13

8. 6 Stechiometria delle reazioni in fase gassosa I calcoli stechiometrici per le reazioni in cui sono presenti composti allo stato gassoso, oltre alla massa e al volume, prendono in considerazione anche temperatura e pressione. L’equazione di stato dei gas perfetti lega tutte le grandezze in gioco in una unica relazione PV = n. RT Secondo il principio di Avogadro una mole di qualsiasi gas in condizioni normali (t= 0°C e p=1, 013 bar) occupa un volume di 22, 4 L. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 14

8. 6 Stechiometria delle reazioni in fase gassosa Nel caso di composti gassosi i coefficienti stechiometrici indicano i rapporti tra volumi di gas coinvolti nella reazione. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 15

8. 7 La resa di reazione La resa teorica di una reazione è la quantità di prodotto che si otterrebbe se tutta la massa dei reagenti fosse trasformata nei prodotti. Le procedure analitiche comportano una inevitabile perdita di sostanze, per cui la quantità di prodotto risulta inferiore di quella prevista dalla stechiometria della reazione. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 16

8. 7 La resa di reazione La resa effettiva è la quantità di prodotto che si ottiene al termine della reazione. La resa effettiva è sempre minore della resa teorica. La resa percentuale di una reazione è la quantità di prodotto ottenuta in rapporto a quella massima ottenibile. Resa percentuale (%) = Resa effettiva Resa teorica X 100 Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 17

8. 8 Classificazione delle reazioni chimiche Le reazioni chimiche possono essere classificate in base al comportamento degli atomi in: reazioni di sintesi; reazioni di decomposizione; reazioni di sostituzione semplice; reazioni di doppio scambio; reazioni di neutralizzazione; reazioni di dissociazione ionica; reazioni di ossidoriduzione. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 18

8. 8 Classificazione delle reazioni chimiche Nelle reazioni di sintesi due o più atomi o molecole reagiscono tra loro per dare un unico composto come prodotto finale. A+B AB Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 19

8. 8 Classificazione delle reazioni chimiche Nelle reazioni di decomposizione o di scissione da un unico composto si ottengono due o più composti o elementi. AB A+B Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 20
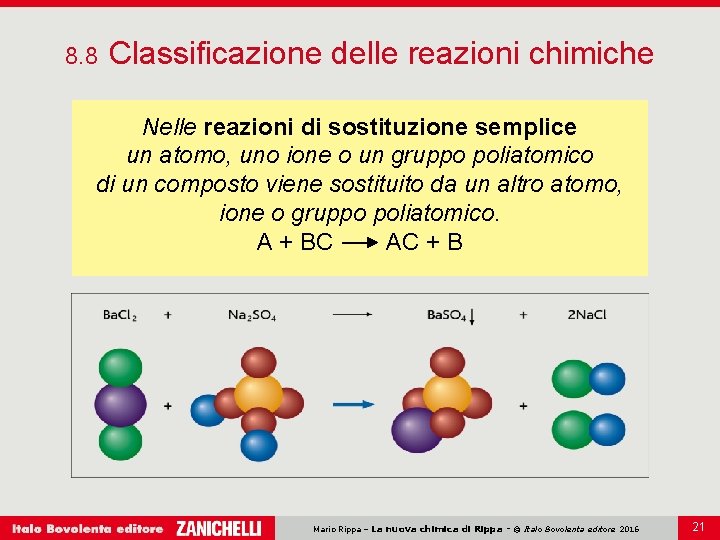
8. 8 Classificazione delle reazioni chimiche Nelle reazioni di sostituzione semplice un atomo, uno ione o un gruppo poliatomico di un composto viene sostituito da un altro atomo, ione o gruppo poliatomico. A + BC AC + B Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 21

8. 8 Classificazione delle reazioni chimiche Nelle reazioni di doppio scambio vi è uno scambio di atomi, di ioni o di gruppi poliatomici tra due composti. AB + CD AD + CB Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 22

8. 8 Classificazione delle reazioni chimiche Alcune reazioni di doppio scambio avvengono con formazione di un prodotto poco solubile detto precipitato. Precipitato Altre sviluppano un gas. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 23

8. 8 Classificazione delle reazioni chimiche Importanti reazioni di doppio scambio sono le reazioni di neutralizzazione in cui un acido e un idrossido formano un sale e l’acqua. HA + BOH AB + H 2 O Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 24

8. 8 Classificazione delle reazioni chimiche Nelle reazioni di dissociazione ionica sali, acidi o basi si scompongono negli ioni corrispondenti. AB A + + B– Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 25

8. 8 Classificazione delle reazioni chimiche Nelle reazioni di ossidoriduzione o redox si ha un trasferimento di elettroni da una specie chimica a un’altra. Sono reazioni di ossidoriduzione: le reazioni tra metalli e non-metalli; le reazioni tra le sostanze e l’ossigeno. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 26

8. 8 Classificazione delle reazioni chimiche Le reazioni tra una sostanza e l’ossigeno con formazione di composti contenenti ossigeno e liberazione di calore sono le reazioni di combustione. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 27
- Slides: 27