Univerzita Karlova v Praze 1 lkask fakulta Psychiatrick












































- Slides: 62

Univerzita Karlova v Praze - 1. lékařská fakulta – Psychiatrická klinika Úvod do biologické psychiatrie Psychiatrická klinika 1. LF UK přednosta: prof. MUDr. Jiří Raboch, Dr. Sc.

Biologická psychiatrie n n Biologická psychiatrie se zabývá duševními poruchami a poruchami chování z hlediska přírodovědeckého, tzn. hledá, zkoumá a vysvětluje jejich příčiny, důsledky a možnosti léčby na základě pozorování změn fyzikálních a chemických procesů v organismech. Výchozí postulát: Při duševních poruchách dochází k narušení přenosu signálu v CNS.

Biologická psychiatrie n n Není dosud jasné, co je primární příčinou vzniku většiny duševních poruch a jaké jsou molekulární mechanismy vedoucí k terapeutickým účinkům používaných léčiv. Ze zřejmých etických důvodů jsou přitom studovány hlavně modelové systémy. Při formulaci a ověřování hypotéz o molekulárních mechanismech provázejících vznik nebo léčbu duševních poruch vychází autoři hlavně z pozorování mechanismů účinků látek s psychotropními účinky. Dosavadní pozorování svědčí o tom, že při duševních poruchách je porušen normální přenos nervového signálu, a to zvláště v oblasti chemických synapsí

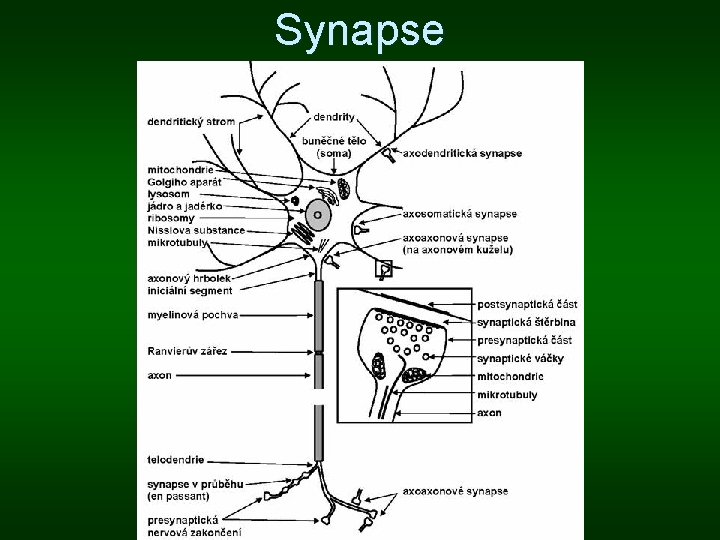
Synapse

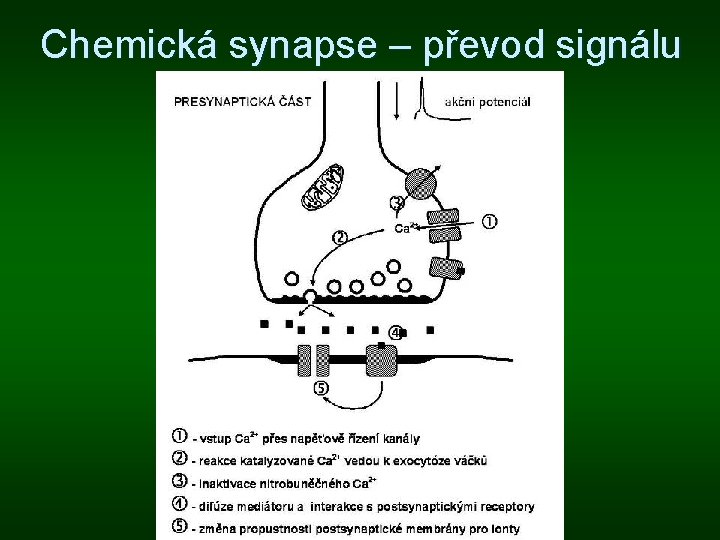
Chemická synapse – převod signálu

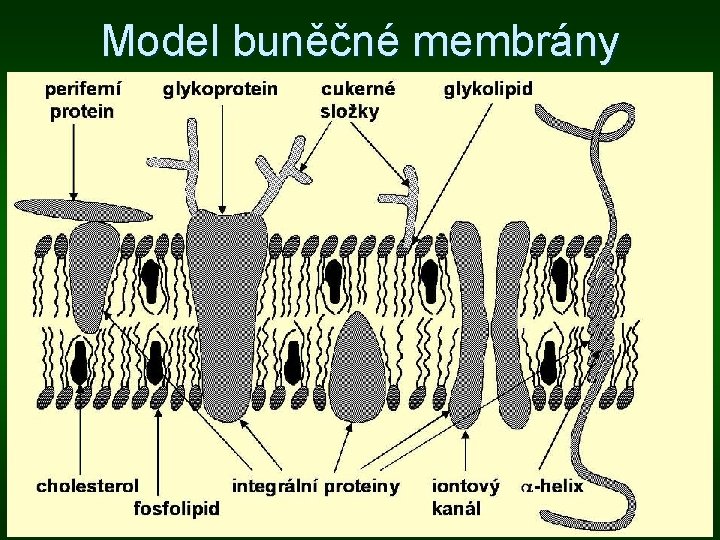
Model buněčné membrány

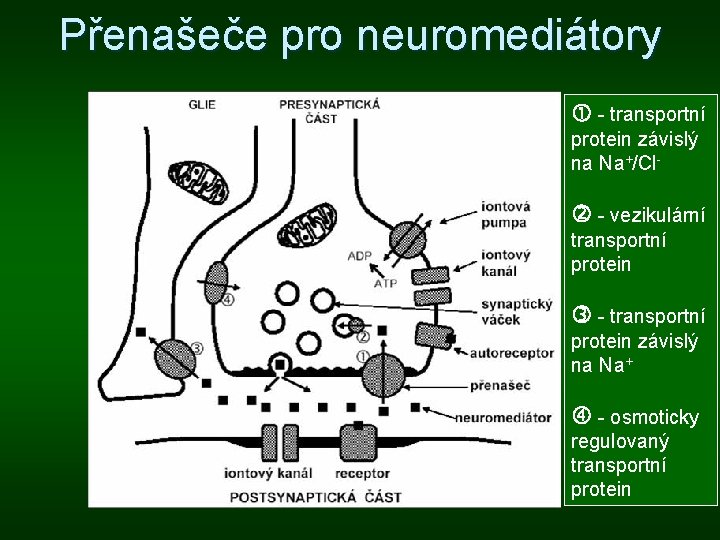
Přenašeče pro neuromediátory - transportní protein závislý na Na+/Cl - vezikulární transportní protein - transportní protein závislý na Na+ - osmoticky regulovaný transportní protein

Důsledky aktivity přenašečů 1. koncentrace neuromediátoru ve štěrbině je snižována rychleji, než při pouhé difúzi, což umožňuje lepší časové rozlišení následných dějů 2. účinky neuromediátoru jsou omezeny na menší plochu, což dovoluje funkci anatomicky blízkých chemicky identických ale funkčně odlišných synapsí 3. neuromediátor může být po přenosu do presynaptického zakončení znovu použit

Dlouhodobá potenciace (LTP)

Kritéria pro identifikaci neuromediátoru 1. výskyt ve vysokých koncentracích v presynaptických nervových zakončeních 2. syntéza v presynaptickém neuronu 3. uvolňování v dostatečném množství z neuronu při depolarizaci membrány a existence mechanismu pro ukončení jeho působení 4. indukce fyziologických účinků odpovídajících normální synaptické transmisi i při exogenní aplikaci 5. existence specifického receptoru pro tento neuromediátor

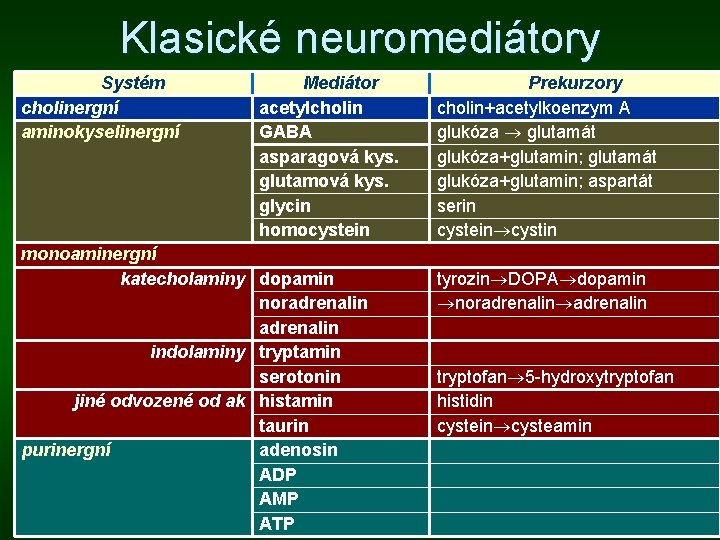
Klasické neuromediátory Systém cholinergní aminokyselinergní Mediátor acetylcholin GABA asparagová kys. glutamová kys. glycin homocystein monoaminergní katecholaminy dopamin noradrenalin indolaminy tryptamin serotonin jiné odvozené od ak histamin taurin purinergní adenosin ADP AMP ATP Prekurzory cholin+acetylkoenzym A glukóza glutamát glukóza+glutamin; aspartát serin cystein cystin tyrozin DOPA dopamin noradrenalin tryptofan 5 -hydroxytryptofan histidin cysteamin

Neuropeptidy a jiné bioaktivní peptidy Peptid látka P (substance P, SP), látka K (tachykininy) neurotenzin cholecystokinin (CCK) gastrin bombesin galanin neuromedin K neuropeptid Y (NPY) peptid YY (PYY) hormon uvolňující kortikotropin (CRH) hormon uvolňující růstový hormon (GHRH) hormon uvolňující gonadotropin (Gn. RH) somatostatin hormon uvolňující tyrotropin (TRH) Zařazení mozkové a gastrointestinální neuronové hypotalamové uvolňovací faktory

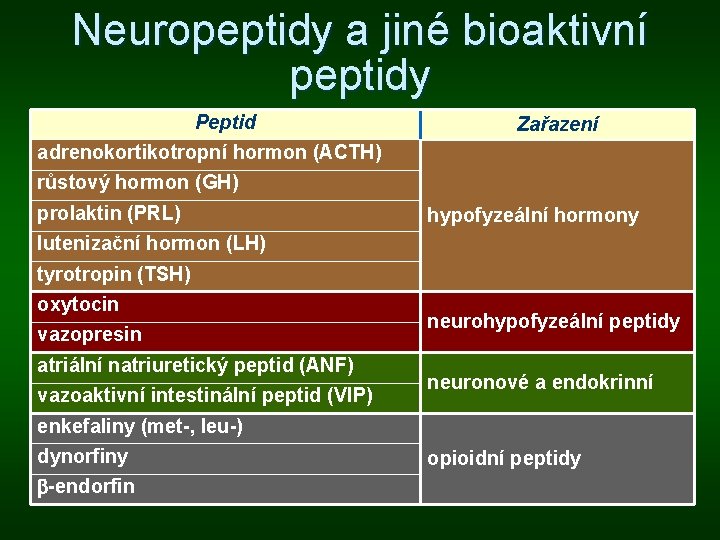
Neuropeptidy a jiné bioaktivní peptidy Peptid Zařazení adrenokortikotropní hormon (ACTH) růstový hormon (GH) prolaktin (PRL) hypofyzeální hormony lutenizační hormon (LH) tyrotropin (TSH) oxytocin vazopresin atriální natriuretický peptid (ANF) vazoaktivní intestinální peptid (VIP) neurohypofyzeální peptidy neuronové a endokrinní enkefaliny (met-, leu-) dynorfiny -endorfin opioidní peptidy

Biosyntéza katecholaminů

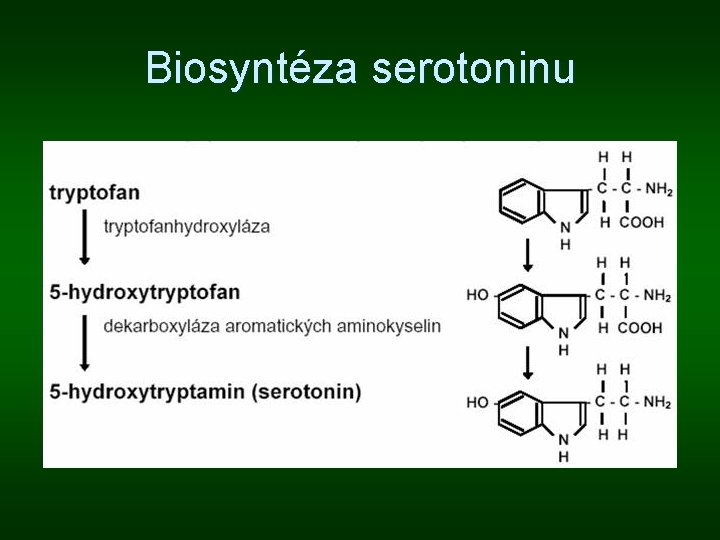
Biosyntéza serotoninu

Růstové faktory v nervovém systému nervový růstový faktor (NGF) mozkový-odvozený neurotrofní faktor (BDNF) neurotrofiny neurotrofin 3 neurotrofin 4/5 ciliární neurotrofní faktor leukemický inhibiční faktor neurokiny interleukin (IL-6) kardiotrofin 1 fibroblastové růstové faktory FGF-1 (kyselý FGF) (FGF) FGF-2 (zásaditý FGF) transformující růstové faktory superrodina transformujících kostní morfogenetické faktory růstových faktorů gliový-odvozený neurotrofní faktor neurturin epidermální růstový faktor superrodina epidermálních transformující růstový faktor růstových faktorů neureguliny trombocytový-odvozený růstový faktor jiné růstové faktory inzulinu-podobný růstový faktor I

Receptory n n Receptor je makromolekula specializovaná na přenos informace. Lze jej definovat jako specifické vazebné místo s funkčními vztahy. Funkčními vztahy se při synaptickém přenosu nervového signálu rozumí procesy, které jsou vyvolané vazbou neuromediátoru nebo jeho agonisty a které vedou ke změně propustnosti synaptické membrány pro určité ionty (tj. k neurotransmisi) nebo k jiným specifickým změnám vlastností cílových buněk, jako je regulace obecného metabolického stavu, syntézy, ukládání a uvolňování neuromediátorů, senzibility receptorů, organizace a struktury cytoskeletu, genové exprese apod. (tj. k neuromodulaci).

Vlastnosti receptorů Receptorový komplex 1. rozpoznávací místo 2. transdukční prvek 3. efektorový systém Regulace receptorů 1. regulace změnou počtu receptorů 2. regulace vlastností receptorů

Rozdělení receptorů podle jejich efektorového systému 1. ligandem řízené iontové kanály 2. receptory spojené s G proteiny 3. receptory s vnitřní guanylátcyklázovou aktivitou 4. receptory s vnitřní tyrozinkinázovou aktivitou

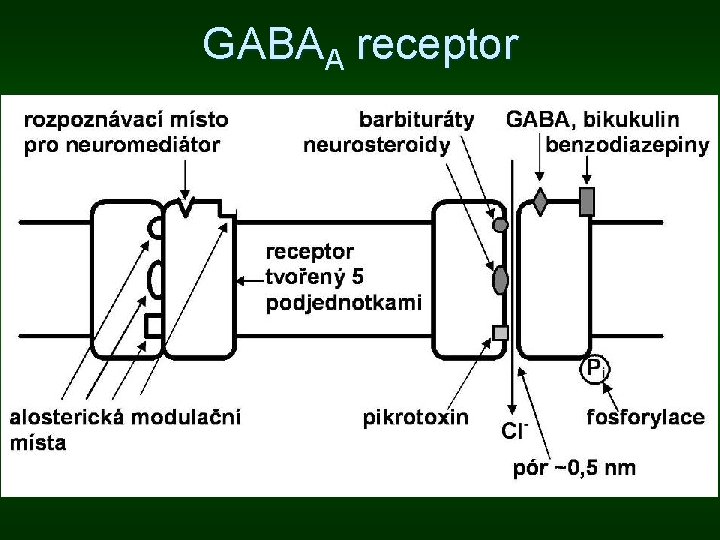
GABAA receptor

Schéma pro hypotézu druhých poslů první poslové receptory G proteiny efektorové proteiny druzí poslové proteinkinázy třetí poslové biologická odezva genová exprese a jiné procesy

Adenylátcyklázový přenosový systém

Fosfoinositidový přenosový systém

Typy receptorů Mediátorový systém acetylcholinový monoaminový aminokyselinový peptidový purinový Receptorový typ acetylcholinové nikotinové receptory acetycholinové muskarinové receptory 1 -adrenoceptory 2 -adrenoceptory dopaminové receptory serotoninové receptory GABA receptory glutamátové ionotropní receptory glutamátové metabotropní receptory glycinové receptory histaminové receptory opioidní receptory jiné peptidové receptory adenosinové receptory (P 1 purinoceptory) P 2 purinoceptory

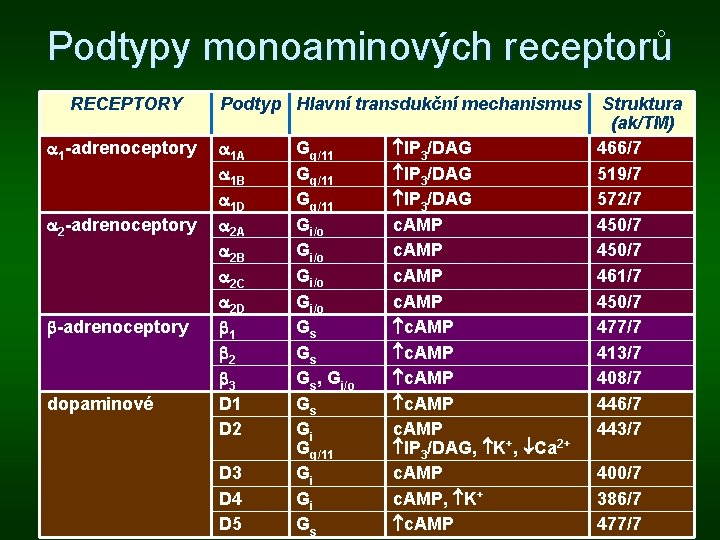
Podtypy monoaminových receptorů RECEPTORY 1 -adrenoceptory 2 -adrenoceptory dopaminové Podtyp Hlavní transdukční mechanismus 1 A 1 B 1 D 2 A 2 B 2 C 2 D 1 2 3 D 1 D 2 D 3 D 4 D 5 Gq/11 Gi/o Gs Gs, Gi/o Gs Gi Gq/11 Gi Gi Gs IP 3/DAG c. AMP c. AMP IP 3/DAG, K+, Ca 2+ c. AMP, K+ c. AMP Struktura (ak/TM) 466/7 519/7 572/7 450/7 461/7 450/7 477/7 413/7 408/7 446/7 443/7 400/7 386/7 477/7

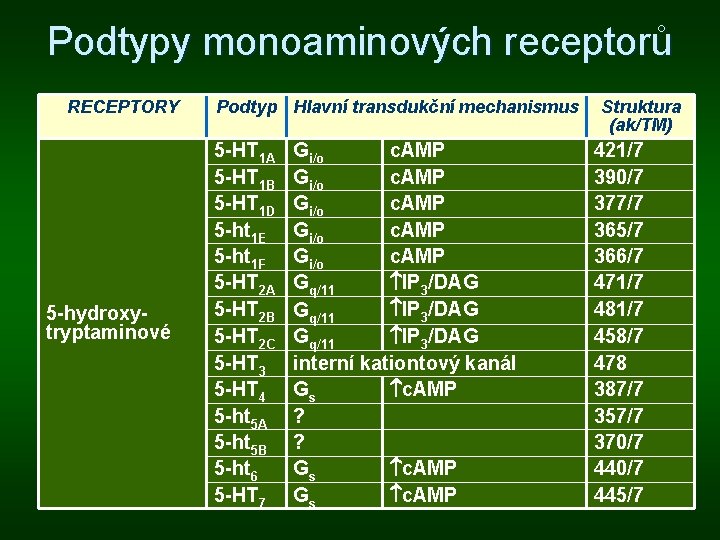
Podtypy monoaminových receptorů RECEPTORY 5 -hydroxytryptaminové Podtyp Hlavní transdukční mechanismus 5 -HT 1 A 5 -HT 1 B 5 -HT 1 D 5 -ht 1 E 5 -ht 1 F 5 -HT 2 A 5 -HT 2 B 5 -HT 2 C 5 -HT 3 5 -HT 4 5 -ht 5 A 5 -ht 5 B 5 -ht 6 5 -HT 7 Gi/o c. AMP Gq/11 IP 3/DAG interní kationtový kanál Gs c. AMP ? ? Gs c. AMP Struktura (ak/TM) 421/7 390/7 377/7 365/7 366/7 471/7 481/7 458/7 478 387/7 357/7 370/7 445/7

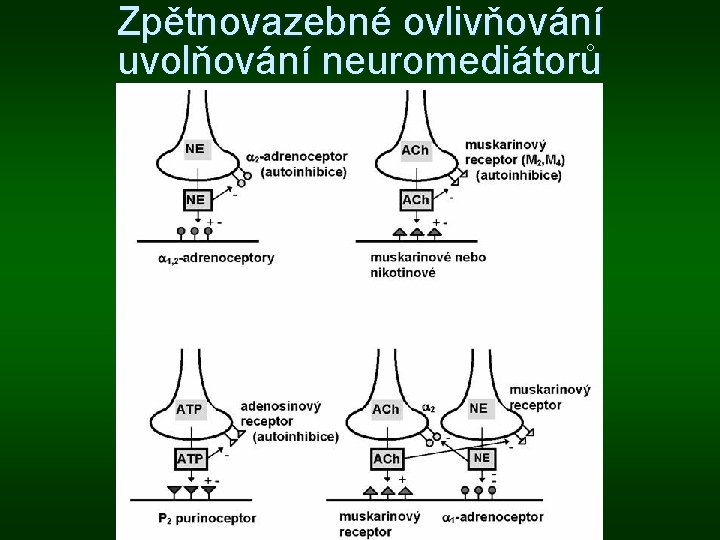
Zpětnovazebné ovlivňování uvolňování neuromediátorů

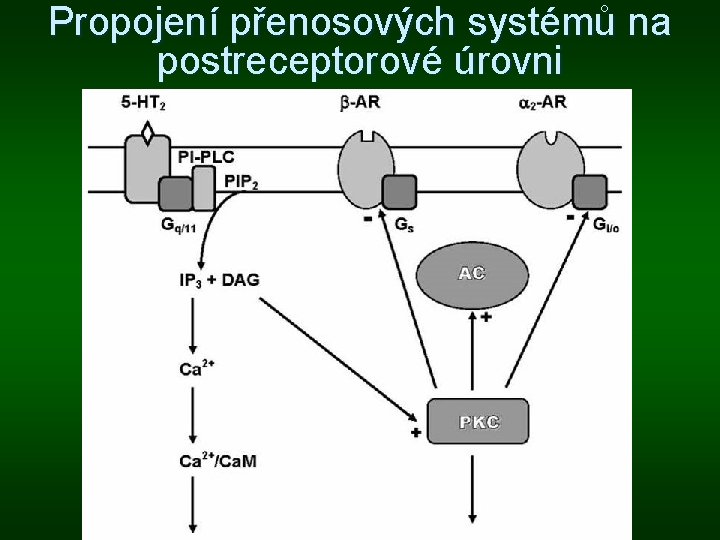
Propojení přenosových systémů na postreceptorové úrovni

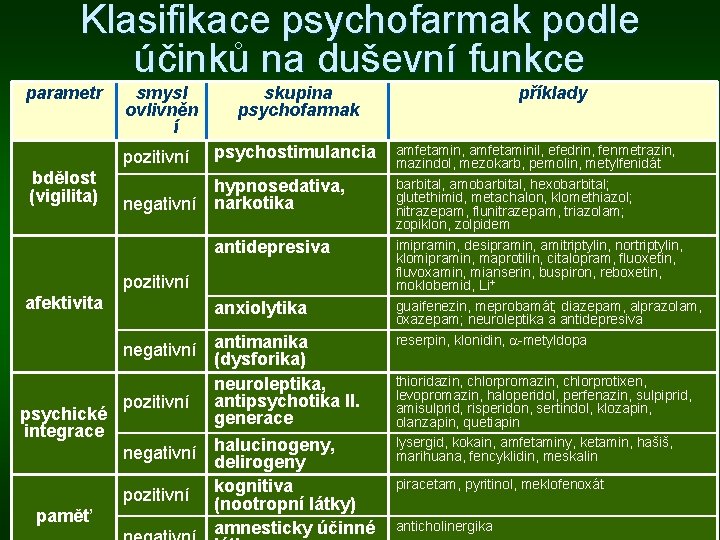
Klasifikace psychofarmak podle účinků na duševní funkce parametr bdělost (vigilita) smysl ovlivněn í skupina psychofarmak příklady pozitivní psychostimulancia amfetamin, amfetaminil, efedrin, fenmetrazin, mazindol, mezokarb, pemolin, metylfenidát barbital, amobarbital, hexobarbital; glutethimid, metachalon, klomethiazol; nitrazepam, flunitrazepam, triazolam; zopiklon, zolpidem imipramin, desipramin, amitriptylin, nortriptylin, klomipramin, maprotilin, citalopram, fluoxetin, fluvoxamin, mianserin, buspiron, reboxetin, moklobemid, Li+ guaifenezin, meprobamát; diazepam, alprazolam, oxazepam; neuroleptika a antidepresiva reserpin, klonidin, -metyldopa hypnosedativa, negativní narkotika antidepresiva pozitivní afektivita anxiolytika negativní antimanika (dysforika) neuroleptika, pozitivní antipsychotika II. psychické generace integrace negativní halucinogeny, delirogeny pozitivní kognitiva (nootropní látky) paměť amnesticky účinné thioridazin, chlorpromazin, chlorprotixen, levopromazin, haloperidol, perfenazin, sulpiprid, amisulprid, risperidon, sertindol, klozapin, olanzapin, quetiapin lysergid, kokain, amfetaminy, ketamin, hašiš, marihuana, fencyklidin, meskalin piracetam, pyritinol, meklofenoxát anticholinergika

Rozdělení antipsychotik skupina příklady konvenční antipsychotika (neuroleptika): bazální (sedativní) antipsychotika chlorpromazin, chlorprotixen, clopenthixol, levopromazin, periciazin, thioridazin droperidol, flupentixol, fluphenazin, fluspirilen, haloperidol, melperon, incisivní antipsychotika oxyprothepin, penfluridol, perphenazin, pimozid, prochlorperazin, trifluoperazin amisulprid, clozapin, atypická antipsychotika olanzapin, quetiapin, (antipsychotika II. generace) risperidon, sertindol, sulpirid

Mechanismy účinku antipsychotik konvenční antipsychotika blokáda postsynaptických D 2 receptorů v meso-limbické dráze (potlačení pozitivních symptomů); zvýšené uvolňování DA a blokáda 5 -HT 2 A atypická receptorů v meso-kortikální dráze antipsychotika (potlačení negativních symptomů); vazba na další receptory (účinnost v terapii afektivních symptomů, zlepšení kognitivních funkcí)

Receptorové systémy ovlivněné některými atypickými antipsychotiky risperidon D 2, 5 -HT 2 A, 5 -HT 7, 1, 2 sertindol D 2, 5 -HT 2 A, 5 -HT 2 C, 5 -HT 6, 5 -HT 7, D 3, 1 ziprasidon D 2, 5 -HT 2 A, 5 -HT 1 D, 5 -HT 2 C, 5 -HT 7, D 3, 1, NRI, SRI loxapin D 2, 5 -HT 2 A, 5 -HT 6, 5 -HT 7, D 1, D 4, 1, M 1, H 1, NRI zotepin D 2, 5 -HT 2 A, 5 -HT 2 C, 5 -HT 6, 5 -HT 7, D 1, D 3, D 4, 1, H 1, NRI D 2, 5 -HT 2 A, 5 -HT 1 A, 5 -HT 2 C, 5 -HT 3, 5 -HT 6, 5 -HT 7, D 1, D 3, D 4, 1, 2, M 1, H 1 D 2, 5 -HT 2 A, 5 -HT 2 C, 5 -HT 3, 5 -HT 6, D 1, D 3, D 4, D 5, 1, M 1 -5, H 1 D 2, 5 -HT 2 A, 5 -HT 6, 5 -HT 7, 1, 2, H 1 clozapin olanzapin quetiapin

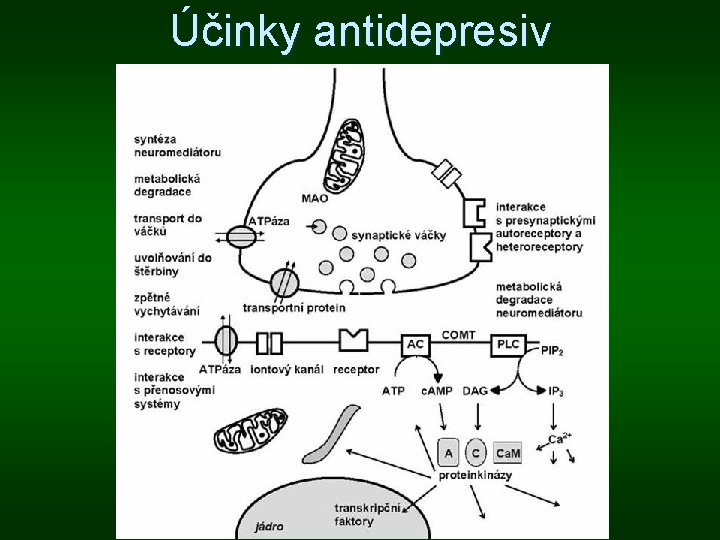
Účinky antidepresiv

Rozdělení antidepresiv podle primárního biochemického účinku inhibitory katabolismu neuromediátorů (IMAO) blokátory reuptake neuromediátorů (SRI/NRI, SSRI, SNRI) agonisté receptorových systémů (5 -HT 1 A) antagonisté receptorových systémů ( 2 -AR, 5 -HT 2) inhibitory či stimulátory jiných složek transdukce signálu (G proteinů, AC, PL, PK, fosfatáz, ATPáz, proteinů závislých na membránových fosfolipidech, transkripčních faktorů, systémů 2. a 3. poslů)

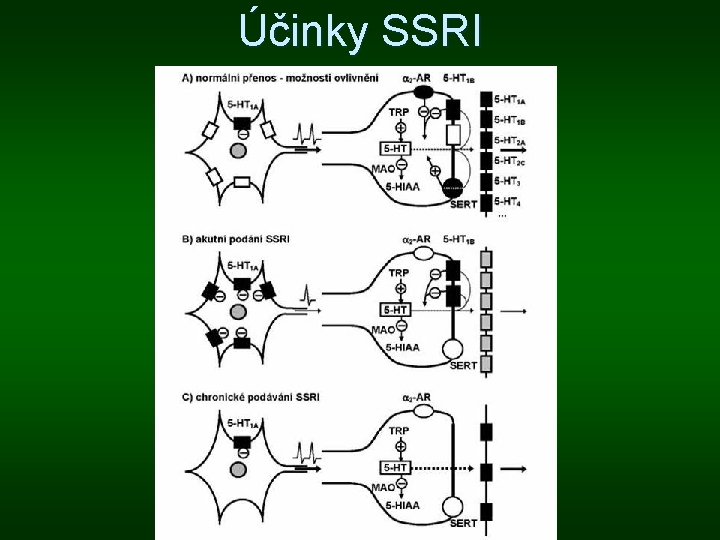
Účinky SSRI

Schizofrenie n n n schizofrenie je specificky lidské onemocnění dosud neznámé etiologie projevující se poruchami myšlení, jednání, vnímání, emocí a vůle jedná se onemocnění heterogenní etiologie („skupina schizofrenií“) předpokládá se multifaktoriální etiologie a mnohočetné patogenetické vlivy

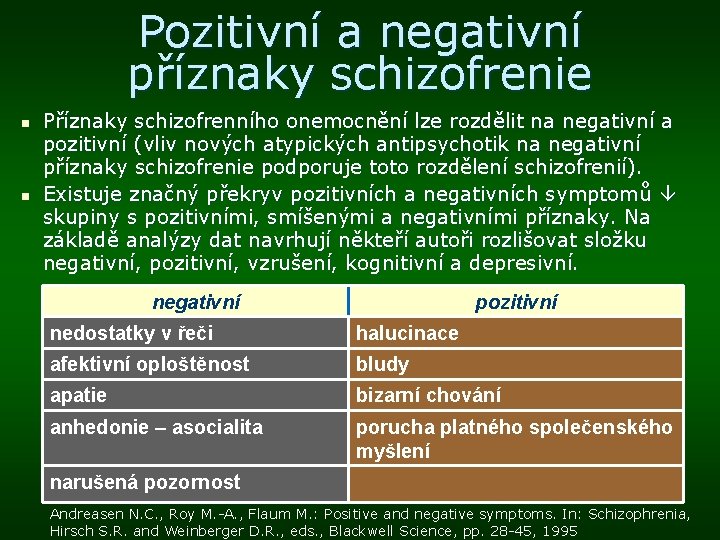
Pozitivní a negativní příznaky schizofrenie n n Příznaky schizofrenního onemocnění lze rozdělit na negativní a pozitivní (vliv nových atypických antipsychotik na negativní příznaky schizofrenie podporuje toto rozdělení schizofrenií). Existuje značný překryv pozitivních a negativních symptomů skupiny s pozitivními, smíšenými a negativními příznaky. Na základě analýzy dat navrhují někteří autoři rozlišovat složku negativní, pozitivní, vzrušení, kognitivní a depresivní. negativní pozitivní nedostatky v řeči halucinace afektivní oploštěnost bludy apatie bizarní chování anhedonie – asocialita porucha platného společenského myšlení narušená pozornost Andreasen N. C. , Roy M. -A. , Flaum M. : Positive and negative symptoms. In: Schizophrenia, Hirsch S. R. and Weinberger D. R. , eds. , Blackwell Science, pp. 28 -45, 1995

Environmentální modely schizofrenie model vyvolávající faktory psychosociální situace vyžadující akci nebo (s vyvolávajícím rozhodnutí vlivem komplexních složitost, dvojznačnost či nejasnost sociálních informací poskytovaných k vyřešení požadavků) úkolu situace vyžadující akci nebo rozhodnutí přetrvává, aniž byla vyřešena osoba nemá možnost únikové cesty nepsychosociální porodní komplikace (se specifickým nitroděložní virová infekce poškozením mozku citlivost na gluten a jeho funkcí) malformace mozku, atd.

Genetické modely schizofrenie MONOGENOVÉ MODELY Všechny případy schizofrenního onemocnění sdílejí stejný jediný hlavní lokus; proměnná je expresivita daného genu nebo penetrance znaku. Tyto modely byly zamítnuty. MODEL VÝRAZNÉ RŮZNORODOSTI Schizofrenie je soubor několika různých nemocí, z nichž každá je spojena s jediným hlavním lokusem, který může být děděn buď dominantně, nebo recesivně; navíc existují sporadická, okolním prostředím způsobená onemocnění.

Genetické modely schizofrenie MULTIFAKTOROVÝ-POLYGENOVÝ MODEL S PRAHOVÝM EFEKTEM Genetické faktory vzniku schizofrenie jsou dány aditivním efektem mnoha genů, z nichž každý má malý efekt, a které se mohou vyskytovat na různých lokusech. Náchylnost ke vzniku schizofrenie je výsledkem spojeného účinku více různých genů spolu s účinky nedědičných faktorů. Náchylnost k vývoji nemoci se považuje za spojitě rozdělenou proměnnou ve sledované populaci a osoby, u nichž se objeví klinické projevy onemocnění, jsou považovány za ty, jejichž náchylnost překročí určitou prahovou hodnotu.

Genetické modely schizofrenie SMÍŠENÉ NEBO KOMBINOVANÉ MODELY 1. Exprese jednoho hlavního genu je pozměněna interakcí nebo spolupůsobením s větším počtem dalších genů, které mají samy o sobě malý efekt. 2. V časném vývoji mozku dochází ke vzniku vývojových abnormalit projevujících se v kognitivních a řečových funkcích, na čemž se podílí více genů produkujících defektní růstové faktory; až v časné dospělosti se aktivizuje nějaký SLM, což vede ke vzniku klinických příznaků schizofrenie.

Neurovývojová hypotéza schizofrenie Významná část osob s diagnózou schizofrenie získanou v dospělém věku prodělala poruchu vývoje mozku desítky let před symptomatickou fází onemocnění. Narušení vývoje mozku může způsobit buď: 1. takové poškození mozku, které se v dospělosti vlivem interakcí s dosud neznámými faktory projeví vznikem psychotických symptomů, nebo 2. toto časné poškození CNS vede k ovlivnění dalšího vývoje mozku a vzniku náchylnosti ke schizofrenii v pozdějším věku Tento model může vysvětlit: 1. vysokou pravděpodobnost vzniku klinických projevů onemocnění v pozdní adolescenci nebo časné dospělosti 2. úlohu stresu při vzniku onemocnění a jeho relapsu 3. terapeutickou účinnost antipsychotik

Vývojová neuropatologie vztah ke schizofrenii in vivo: poněkud zvětšené mozkové komory a širší kortikální štěrbiny a rýhy post mortem: rozdíly ve velikosti mozkových komor, v různých oblastech mozkové kůry, v hipokampální formaci (vč. parahipokampálního kortexu) a morfometrické abnormality v různých periventrikulárních subkortikálních jádrech; konzistentní data o chybění gliózy anomální lateralizace: méně vyvinutá normální anatomická asymetrie hemisfér orientace hipokampálních pyramidových abnormality buněk, laminární organizace neuronů cytoarchitektury v neokortexu a limbické kůře, vzájemné vztahy mezi neurony

Východiska klasické dopaminové hypotézy schizofrenie 1. Psychózu lze aktivovat psychostimulancii, která jsou agonisty dopaminu, jako je amfetamin, meskalin, dietylamid kyseliny lysergové (LSD, lysergid); jedná se zřejmě o látky vhodné pro vyvolání modelového psychotického stavu. 2. Společným znakem látek účinných při terapii schizofrenie (neuroleptik, resp. antipsychotik 1. generace) je jejich působení na dopaminergní systém; skoro všechny tyto léky přitom ovlivňují pozitivní příznaky, pravděpodobně tím, že blokují účinky dopaminu a jiných dopaminergních agonistů v určitých oblastech mozku. 3. Neuroleptika zvyšují obrat dopaminu; může se jednat o důsledek blokády postsynaptických DA receptorů, nebo nedostatečného počtu či citlivosti inhibičních DA autoreceptorů na buněčných tělech.

Klasická dopaminová hypotéza schizofrenie • Psychotické symptomy u schizofrenie jsou vztaženy k dopaminergní hyperaktivitě v mozku. Hyperaktivita dopaminergních systémů spojená se schizofrenií je důsledkem zvýšení citlivosti a počtu dopaminových D 2 receptorů. Tato zvýšená aktivita se může týkat jen určité oblasti mozku.

Revidovaná dopaminová hypotéza V revidované dopaminové hypotéze schizofrenie se předpokládá, že snížené inhibiční působení na talamus zprostředkované přes striatum a způsobené buď zvýšenou dopaminergní, nebo sníženou glutamátergní aktivitou, vede ke zvýšení vzrušení a psychomotorické aktivity a ke zvýšenému senzorickému vstupu přenášenému do kůry. Pokud tyto změny přesáhnou určitou hladinu, potom je integrační kapacita kůry nedostatečná a to vede k psychóze s převážně pozitivními příznaky. Nadměrná dopaminergní funkce může také vést k dezintegraci motorických funkcí. V důsledku excitačního nebo inhibičního vlivu dopaminu na přímé nebo nepřímé dráhy může dopamin sloužit jako regulátor rovnováhy mezi pozitivní a negativní zpětnou vazbou ve striatu.

Afektivní poruchy n n Afektivní poruchy se projevují patickou náladou v epizodách trvajících od několika dnů do několika měsíců. Při bipolárním typu onemocnění dochází ke střídání depresivních a manických epizod, unipolární typ zahrnuje pouze epizody depresivní, nebo manické. Těžká podoba postihuje asi 1% populace a je obvykle dobře léčitelná. Anatomické změny v mozku jsou podobné jako u chronické schizofrenie. Biologická psychiatrie se snaží popsat a vysvětlit vznik a léčbu afektivních poruch na základě poznatků získaných jak klinickým hodnocením, tak měřením biochemických a fyziologických změn. Biochemické základy afektivních poruch jsou hledány: • v genetických faktorech • v neuroendokrinních změnách • ve funkci neuromediátorových systémů

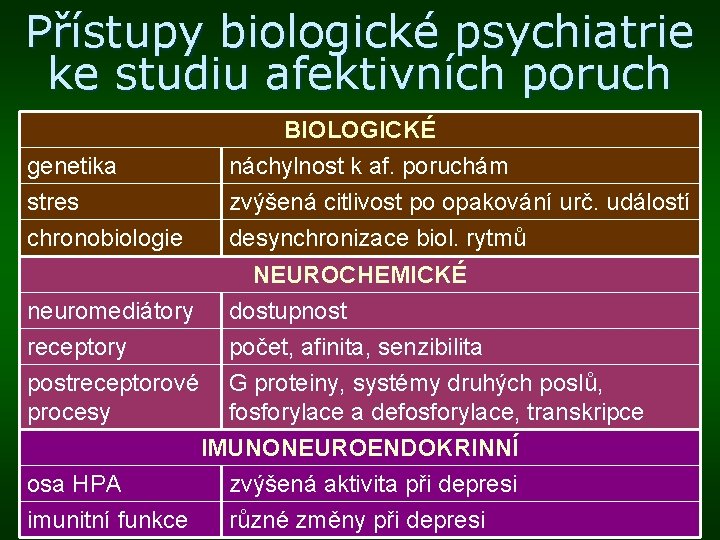
Přístupy biologické psychiatrie ke studiu afektivních poruch genetika stres chronobiologie BIOLOGICKÉ náchylnost k af. poruchám zvýšená citlivost po opakování urč. událostí desynchronizace biol. rytmů NEUROCHEMICKÉ neuromediátory dostupnost receptory počet, afinita, senzibilita postreceptorové G proteiny, systémy druhých poslů, procesy fosforylace a defosforylace, transkripce IMUNONEUROENDOKRINNÍ osa HPA zvýšená aktivita při depresi imunitní funkce různé změny při depresi

Genetické faktory n Genetické a stresové faktory mohou přes imunoneuroendokrinní a neurochemické účinky ovlivňovat přenos signálu v CNS a vést ke vzniku afektivních poruch. Byla potvrzena vrozená náchylnost pro vznik afektivních poruch, ale dosud se nepodařilo spolehlivě identifikovat příslušný gen; genetické faktory samy o sobě nejsou postačující pro vznik onemocnění a jejich úloha a přenos nejsou dostatečně známy. Vliv genetických faktorů na vznik náchylnosti k afektivním poruchám 1. zvýšení citlivosti jednotlivých osob k opakujícím se událostem indukujícím depresi 2. nedostatečná funkce určitých homeostatických mechanismů

Abnormality v ose HPA při depresi hypersekrece kortizolu zvýšený volný kortizol v moči zvýšený CRF v mozkomíšním moku zvýšené cirkulující ACTH abnormální denní rytmy kortizolu abnormální dexametazonová suprese snížená citlivost glukokortikoidních receptorů snížené uvolňování ACTH v odezvě na CRF zvětšená velikost nadledvin

Neuroendokrinní hypotézy afektivních poruch 1. Endokrinní abnormality spojené s depresí jsou výsledkem zvýšeného uvolňování CRF v hypotalamu i mimo něj. 2. Nedostatečné zpětnovazebné působení kortizolu při depresi je způsobeno sníženou hustotou kortikosteroidních receptorů v hipokampu a v hypotalamu, tedy pravděpodobně poruchou v regulaci genové exprese těchto receptorů (hypotéza o narušené glukokortikoidní zpětné vazbě při depresi).

Neurochemické faktory při afektivních poruchách neuromediátory receptory postreceptorové systémy dostupnost rychlost metabolismu počet nebo hustota afinita senzibilita počet a aktivita G proteinů efektorové enzymy systémy druhých poslů proteinkinázy fosfatázy transkripční faktory

Podklady pro neuromediátorové hypotézy účinky tricyklických antidepresiv blokáda reuptake noradrenalinu nebo serotoninu mající za následek zvýšení hladin těchto neuromediátorů v synaptické štěrbině a prodloužení doby jejich působení na specifické receptory účinky inhibitorů zvýšení dostupnosti monoaminových monoaminoxidázy neuromediátorů v presynaptické části účinky reserpinu snížení koncentrací biogenních aminů v nervových zakončeních, které je dáváno do souvislosti se vznikem depresivních symptomů u části osob, kterým je tento lék podáván

Neuromediátorové hypotézy afektivních poruch katecholaminová hypotéza indolaminová hypotéza cholinergní-adrenergní rovnovážná hypotéza „permisivní“ hypotéza dopaminová hypotéza biogenních aminů monoaminová hypotéza „Permisivní“ hypotéza: Nedostatečná centrální indolaminergní transmise „připouští“ afektivní poruchu, ale není postačující pro její vznik. Blízkou příčinou pro vznik afektivního stavu je za této situace změna v centrální katecholaminové transmisi, která je při mánii zvýšená a při depresi snížená. Korekce nízkých hladin 5 -HT by tedy měla zmírňovat afektivní onemocnění

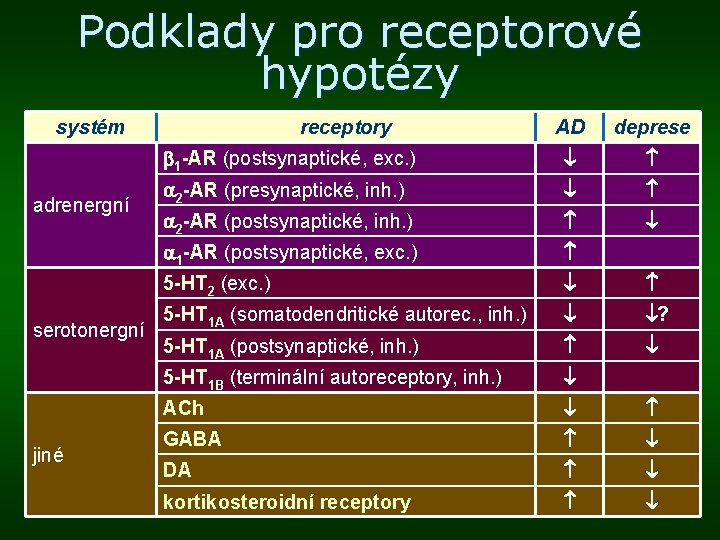
Podklady pro receptorové hypotézy systém adrenergní serotonergní jiné receptory AD deprese 1 -AR (postsynaptické, exc. ) 2 -AR (presynaptické, inh. ) 2 -AR (postsynaptické, inh. ) 1 -AR (postsynaptické, exc. ) 5 -HT 2 (exc. ) 5 -HT 1 A (somatodendritické autorec. , inh. ) ? 5 -HT 1 A (postsynaptické, inh. ) 5 -HT 1 B (terminální autoreceptory, inh. ) ACh GABA DA kortikosteroidní receptory

Receptorové hypotézy afektivních poruch neuromediátorová rovnovážná sjednocená neurochemická o propojení NA a 5 -HT systémů dopaminergní o dostupnosti L-TRP dysregulační endogenního ligandu cholinergní-adrenergní obecná katecholaminová obecná serotoninová peptidergní sjednocující adrenoceptorová o úloze postynaptických 2 -AR o spojení 5 -HT a NA systémů obecná katecholaminová inositolová klasická noradrenalinová biogenních aminů

Receptorové hypotézy afektivních poruch Klasická noradrenalinová receptorová hypotéza: Depresivní porucha může být spojena se zvýšenou senzitivitou centrálních noradrenergních receptorů. Terapeutické účinky antidepresiv jsou potom vztaženy k adaptivním změnám v senzitivitě adenylátcyklázového systému spojeného s postsynaptickými noradrenergními receptory. Tato hypotéza byla upřesněna tím, že desenzitizace adenylátcyklázy po chronickém podávání antidepresiv je způsobena snížením počtu 1‑adrenoceptorů. Obecná katecholaminová hypotéza: Supersenzitivita určitých katecholaminových receptorů při nízkých hladinách 5 -HT je biochemickým základem deprese. Tato hypotéza je elegantní, ale nelze ji považovat za prokázanou, neboť klinické studie dostatečně nepotvrdily přítomnost takových supersenzitivních receptorů u nemocných. Obecná serotoninová receptorová hypotéza: Deprese je vztažena k těmto abnormalitám serotoninových receptorů: 1. 2. 3. upregulace 5 -HT 2 desenzibilizace 5 -HT 1 A abnormální transdukce signálu po vazbě 5 -HT k receptoru.

Postreceptorové hypotézy afektivních poruch inositolová hypotéza nerovnováhy druhých poslů G proteinová hypotéza deprese molekulární model molekulární a buněčná teorie deprese

Postreceptorové hypotézy afektivních poruch Inositolová hypotéza: Vznik afektivních poruch je spojen se změnami ve fosfoinositidovém přenosovém systému. Východiskem této hypotézy byly inhibiční účinky lithia na inositolmonofosfatázu. Podle hypotézy o vyčerpání inositolu účinkuje Li+ přes snížení hladin inositolu a tím způsobuje desenzibilizaci receptorů, které pro svou funkci potřebují PIP 2. Hypotéza byla upřesněna předpokladem, že Li+ inhibuje fosfoinositidovou přenosovou kaskádu pouze při zvýšené aktivaci tohoto systému a nemá vliv na jeho základní funkci. Příliš stimulované receptorové systémy spojené s aktivací PLC jsou tak lithiem tlumeny. Hypotéza nerovnováhy druhých poslů: Afektivní poruchy vznikají v důsledku narušení rovnováhy mezi adenylátcyklázovým a fosfoinositidovým systémem. Deprese je výsledek snížené buněčné odezvy zprostředkované c. AMP při současné absolutní nebo relativní převaze odezvy zprostředkované IP 3 a DG. U mánie je tomu obráceně.

Postreceptorové hypotézy afektivních poruch Molekulární model: Klinická heterogenita zjištěná u pacientů s bipolární poruchou může být vysvětlena změnami v těch částech přenosu signálu, které regulují dva nebo více neuromediátorových systémů s opačnými účinky na aktivitu neuronu. V tomto modelu jsou uvažovány změny funkce těchto tří postreceptorových složek schopných interagovat s více než jedním receptorovým systémem: 1. G proteinů, 2. fosfatáz, 3. transkripčních faktorů. Kromě stimulační a inhibiční přenosové dráhy je uvažována i stimulační dráha obsahující inhibiční zpětnovazebné působení na sebe samu nebo na jinou stimulační dráhu. Tímto způsobem je vysvětlován přesmyk z manické do depresivní fáze.

Postreceptorové hypotézy afektivních poruch Molekulární a buněčná teorie deprese: Transkripční faktor CREB je možným intrabuněčným cílem dlouhodobé léčby antidepresivy a gen pro mozkový neurotrofní faktor BDNF je možným cílovým genem CREB. Náchylnost k depresi může vzniknout v důsledku poškození neuronů po chronickém stresu, který snižuje expresi BDNF v hippokampu. Přežití neuronů snižuje také dlouhodobé zvýšení hladin glukokortikoidů, hypoglykémie, ischémie, neurotoxiny a některé virové infekce. Dlouhodobé podávání antidepresiv zvyšuje expresi BDNF i jeho receptoru trk. B přes zvýšení funkce 5 -HT nebo NA systému.

Model pro molekulární mechanismus účinků dlouhodobé léčby antidepresivy Antidepresivní terapie (AT) Inhibice reuptake 5 -HT a NA nebo jejich štěpení Krátkodobá AT: Zvýšení mimobuněčných hladin 5 -HT nebo NA Dlouhodobá AT: Snížení funkce a exprese 5 -HT a NA receptorů Zvýšení přenosu v signální dráze c. AMP (zvýšené hladiny adenylátcyklázy a PKA a translokace PKA do buněčného jádra) Zvýšení exprese transkripčního faktoru CREB (c. AMP response element-binding protein); předpokládá se, že CREB je společným postreceptorovým cílem pro antidepresiva. Zvýšená aktivita v signální dráze c. AMP naznačuje, že funkční výstupy 5 -HT a NA jsou upregulovány, i když určité serotoninové a noradrenalinové receptory jsou downregulovány. Exprese BDNF (brain-derived neurotrophic factor) a trk. B je také zvýšena po dlouhodobém podávání antidepresiv ( zvýšené přežití neuronů, jejich funkce a přetváření synapsí) Duman et al. 1997
 Univerzita v praze
Univerzita v praze Psychiatrick
Psychiatrick Epizeuxis
Epizeuxis Dopravní fakulta jana pernera
Dopravní fakulta jana pernera Fm vše studijní oddělení
Fm vše studijní oddělení Filozofická fakulta univerzity jana evangelisty purkyně
Filozofická fakulta univerzity jana evangelisty purkyně Uniza stavebna fakulta
Uniza stavebna fakulta Univerzita carolina
Univerzita carolina Inese karlova
Inese karlova Lkask
Lkask Lkask
Lkask Lkask
Lkask Urothel
Urothel Zdrl
Zdrl Lkask
Lkask Lkask
Lkask Lkask
Lkask Mendelova univerzita lednice
Mendelova univerzita lednice Univerzita palckého
Univerzita palckého Univerzita mateja bela odbory
Univerzita mateja bela odbory Tf moodle
Tf moodle Prešovská univerzita
Prešovská univerzita













































