Titrimetrija volumetrija Analitika kemijavjebe Dijana Juri prof Zdravstvena

Titrimetrija (volumetrija) Analitička kemija-vježbe Dijana Jurić, prof Zdravstvena škola Split

Ishodi-učenik će moći • Definirati analit i titrand • Objasniti razliku primarnog standarda i standarda • Opisati ulogu indikatora u titrimetriji • Analizirati završnu točku titracije • Praktično primjeniti očitani volumen kod titracije • Izračunati nepoznatu koncentraciju analita • Prepoznati važnost preciznosti i točnosti u praktičnim radu
Ponovimo • Stehiometrijski račun: napiši kemijske izraze za- n, c, W • Navedi volumetrijsko posuđe sa slike! • Što su indikatori? • Navedi poznate indikatore?

Titrimetrija(volumetrija) je metoda kvantitativne kemijske analize pri kojoj se određuje volumen • Titracija je postupak određivanja volumena reagensa • Titrand je reagens kojem se određuje volumen • Iz volumena utrošenog titranda poznate koncentracije izračunava se količina određene komponente analita-stehiometrijski račun • Pri svakoj titraciji posebno važno je točno ustanoviti kraj titracije-ZTT (završna točka titracije) • ZTT se najčešće uočava promjenom boje indikatora ili promjenom boje otopine

Za volumetrijsko određivanje potrebno je: • Pripremiti standardnu otopinu-otopinu točne koncentracije kojom će se titrirati • Pripremiti indikator • Pripremiti analit-uzorak za titraciju • Titrirati pripremljenu otopinu • Izračunati i prikazati rezultat u željenom obliku

Standardna otopina • Standardna otopina je reagens poznate i točno određene koncentracije • Otopina nazivne koncentracije je otopina približne koncentracije (označava se s jednim decimalnim mjestom, pr. c=0, 1 mol/L HCl) • Otopina prave koncentracije je otopina precizno određene koncentracije (označava se s četiri decimalna mjesta, pr. c=0, 1054 mol/l HCl-a) • Za određivanje koncentracije standardnih otopina primjenjuju se dvije metode: • direktnom odvagom primarnog standarda ili pripremom otopine približne koncentracije i naknadnom standardizacijom

Primarni standard • Je tvar čija se otopina priprema izravnim vaganjem i otapanjem određene količine u odmjernoj tikvici Zahtjevi: • Visoka čistoća (p. a) • Stabilnost na zraku • Ne smije biti higroskopna • Ne smije kemijski reagirati s otapalom Najčešći primarni standardi: natrijev karbonat, natrijev oksalat, kalijev dikromat i srebrov nitrat

Titracija • Mjerenje volumena pomoću birete Postupak: • Bireta se napuni otopinom poznate koncentracije(standardna otopina) • Uzorak se otpipetira u Erlenmeyerovu tikvicu • Ispod tikvice se stavi bijeli papir radi boljeg uočavanja promjene boje • Pomoću pipca regulira se brzina istjecanja otopine iz birete jednom rukom • Drugom rukom se otopina stalno miješa kružnim okretanjem tikvice
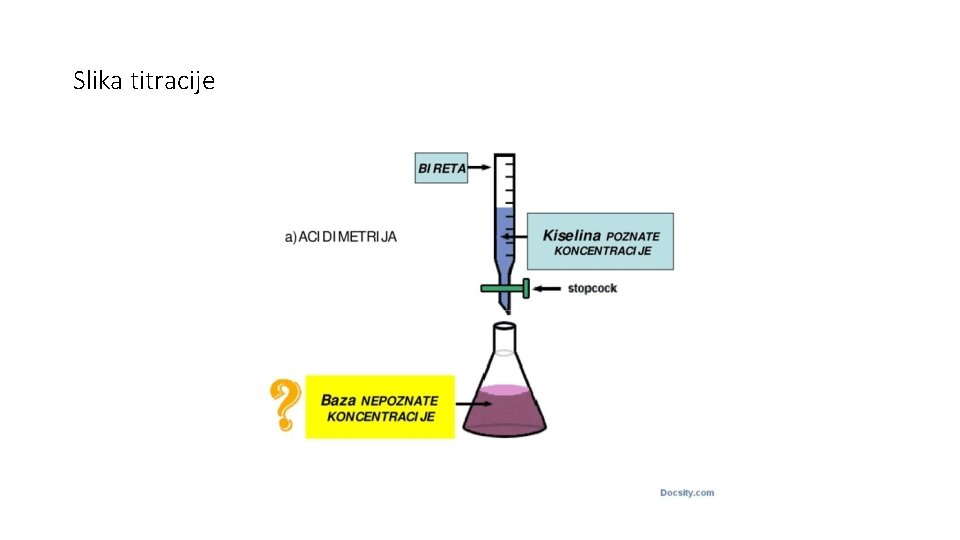
Slika titracije
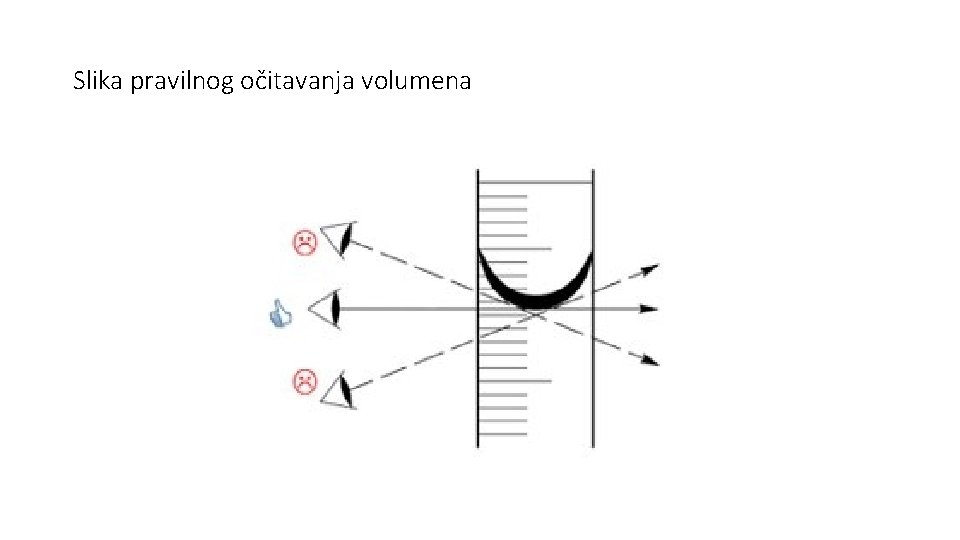
Slika pravilnog očitavanja volumena

slika promjene boje s indikatorom metiloranžom u ZTT • Titrira se triput • Uzima se srednja vrijednost titracija • Razlika između dva mjerenja smije biti između 0, 05 -0, 1 ml (2 kapi) • Titracija je završena kada je završena kemijska reakcija između analita I titranda

Točka ekvivalencije je teorijska točka koja se postiže kada su u otopinu dodane ekvivalentne količine analita i titranda Završna točka titracije je točka u titraciji kada opažamo fizikalnu promjenu koja se zbiva pri stanju kemijske ekvivalencije Pogrješka titracije je odstupanje točke ekvivalencije i završne točke titracije

Indikator • Pokazuje završetak titracije U ZTT indikator: • mijenja boju • boja indikatora može nastati ili nestati • može nastati ili nestati zamućenje

Zadatak 1: Odpipetira se 20 m. L otopine klorovodične kiseline nepoznate koncentracije koja se ispusti u Erlenmeyerovu tikvicu i nakon toga se doda nekoliko kapi fenolftaleina. U kiselinu se zatim, polagano, kap po kap, iz birete dodaje kalijeva lužina množinske koncentracije 0, 10 mol L – do promjene boje indikatora. Ako se za titraciju utroši 20 m. L kalijeve lužine, izračunajte množinsku koncentraciju klorovodične kiseline Zadano je: V(HCl)=20 m. L c(KOH)=0, 10 mol. L− 1 V(KOH, utrošenog za neutralizaciju)=20 m. L Traži se: c(HCl)=?

Izradak: Titracija se temelji na reakciji neutralizacije jake lužine s jakom kiselinom prema sljedećoj jednadžbi kemijske reakcije: HCl(aq)+KOH(aq)�KCl(aq)+H 2 O(l) Na temelju jednadžbe kemijske reakcije može se zaključiti da su množine klorovodične kiseline i kalijeve lužine jednake. n(kiseline)=n(lužine) c(HCl) x V(HCl)=c(KOH) x V(KOH) c(KOH)=c(HCl) x V(HCl) / V(KOH) c(HCl)=0, 100 mol. L− 0, 020 L / 0, 020 L = 0, 10 mol/L Množinska koncentracija klorovodične kiseline je 0, 10 mol L– 1

Ponovimo • Što je titrimetrija? • Navedite faze titrimetrijskog određivanja • Što je titracija, a što titrand? • Što je primarni standard i čemu služi? • Što je točka ekvivalencije? • Da li je dobro da se točka ekvivalencije i završna točka titracije podudaraju? Objasni! • Objasni ulogu indikatora u titraciji!

Domaći rad • Opiši četiri acido bazna indikatora • Ponovi ispravno pipetiranje pomoću propipete Riješi zadatak: • Kolika je koncentracija klorovodične kiseline ako je za titraciju 20, 0 m. L natrijeva karbonata, c(Na 2 CO 3) = 0, 0500 mol L– 1, utrošeno 19, 80 m. L klorovodične kiseline? Jednandžba kemijske reakcije: Na 2 CO 3 + 2 HCl — H 2 CO 3 + 2 Na. Cl RJ: 0, 1010 mol/L

Izvori • Z. Weihnacht, S. Rupčić Petelinc, S. Žužek, Praktikum analitičke kemije, Školska knjiga, Zagreb, 2009. • M. Banović, Analitička kemija za zdravstvene škole, Školska knjiga, Zagreb, 1999. • internet
- Slides: 18