SEMANA 2 UNIONES Y ENLACES QUMICOS QUMICA 2021











- Slides: 23

SEMANA 2 UNIONES Y ENLACES QUÍMICOS QUÍMICA 2021 1

SEMANA 02 UNIONES Y ENLACES QUÍMICOS Uniones y enlaces químicos. -Definición de electronegatividad. -Ejercicio sobre su variación en los grupos y periodos y diferencias de electronegatividad en compuestos binarios. Regla del Octeto. Estructura de Lewis: elementos, iones y compuestos binarios -Clasificación de enlaces: Enlace iónico Enlace covalente: Polar y No polar. Simple, doble, triple y coordinado -Comparación de propiedades físicas de compuestos iónicos y covalentes. -Aplicación de los conceptos en la salud y el ambiente: Lecturas en libro de texto - La Química en la Salud: “Algunos Iones importantes en el cuerpo” Laboratorio: Equipo básico de laboratorio de química 2

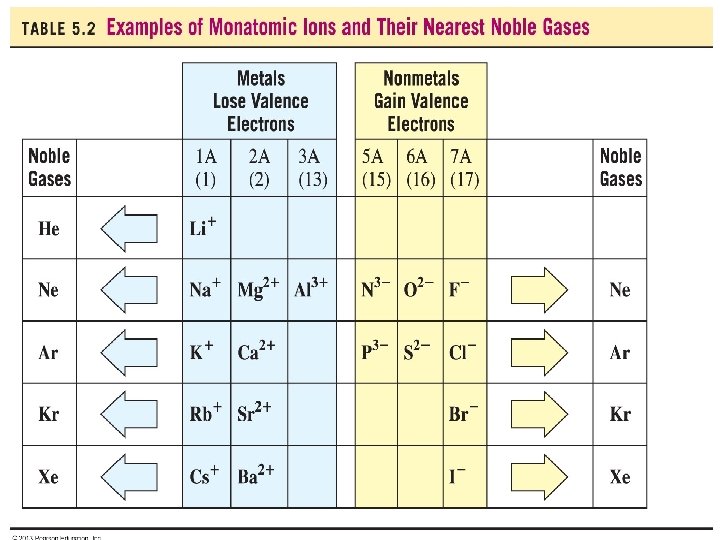
¿PORQUÉ SE ENLAZAN LOS ÁTOMOS? • Los átomos libres (como se encuentran escritos en la tabla periódica) son poco estables. • Para lograr la estabilidad, deben de cumplir la REGLA DEL OCTETO que consiste en lo siguiente: Es la tendencia de los átomos a tener 8 electrones en su último nivel para ganar estabilidad y que sus configuraciones electrónicas se parezcan a la de los gases nobles que son muy estables porque tienen octetos en su último nivel. ¿Cómo lo logran? Formando enlaces químicos con otros átomos cuando forman compuestos. 3

OCTETOS DE LOS GASES NOBLES 4


ENLACE QUÍMICO Es la unión de dos o más átomos para formar un compuesto ya sea, ganando, perdiendo o compartiendo electrones. TIPOS DE ENLACES: Iónico y Covalente • Lo que determina el tipo de enlace que se formara entre dos átomos será la diferencia entre sus ELECTRONEGATIVIDADES. 6

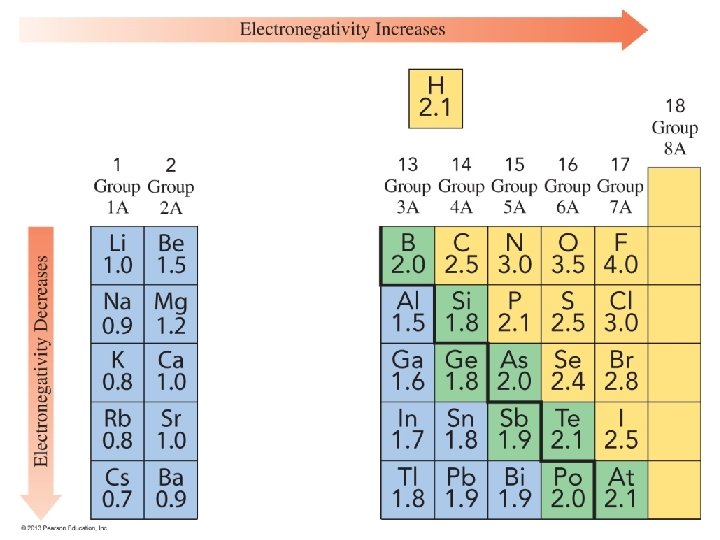
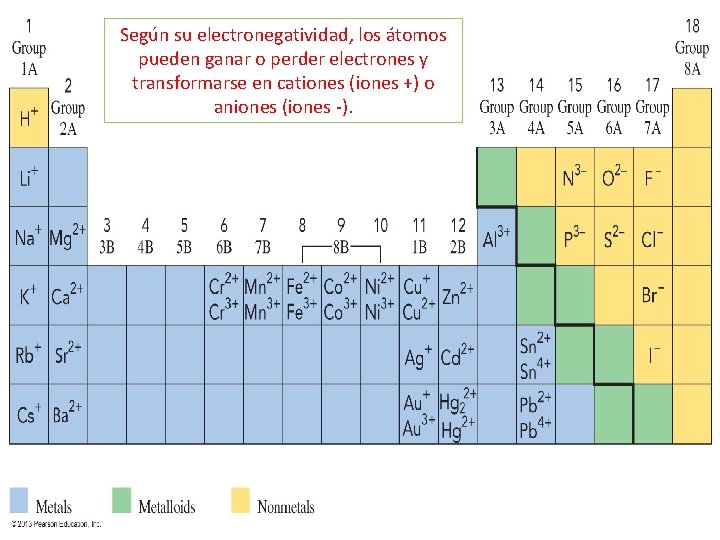
ELECTRONEGATIVIDAD Es capacidad que tiene un átomo de atraer y acercar los electrones que forman el enlace. (este valor se encuentra en la tabla periódica). • El átomo menos electronegativo es el Francio y el más electronegativo el Flúor. • En los períodos aumenta de izquierda a derecha En las columnas disminuye de arriba hacia abajo. • Los METALES por ser menos electronegativos tienden a perder sus electrones de valencia cuando forman enlaces. • Los NO METALES por ser más electronegativos tienden a ganar electrones cuando forman enlaces. 7


Según su electronegatividad, los átomos pueden ganar o perder electrones y transformarse en cationes (iones +) o aniones (iones -).

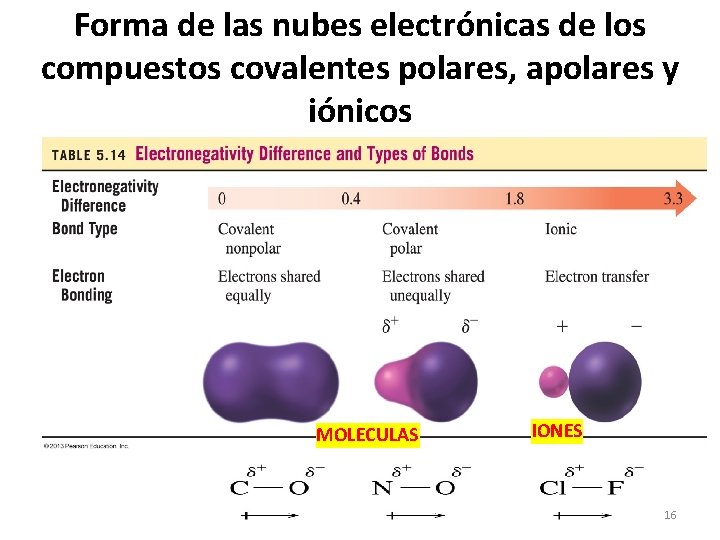
CLASIFICACIÓN DE LOS ENLACES Según la diferencia (resta) de las electronegatividades de los 2átomos que se enlazan se clasifican en: • • ENLACE COVALENTE PURO: diferencia de 0 ENLACE COVALENTE APOLAR: de 0 a 0. 4 ENLACE COVALENTE POLAR: mayor de 0. 4 a menor de 1. 8 ENLACE IÓNICO: de 1. 8 en adelante 0 0. 4 ELECTRONEGATIVIDAD 1. 8 en adelante 10

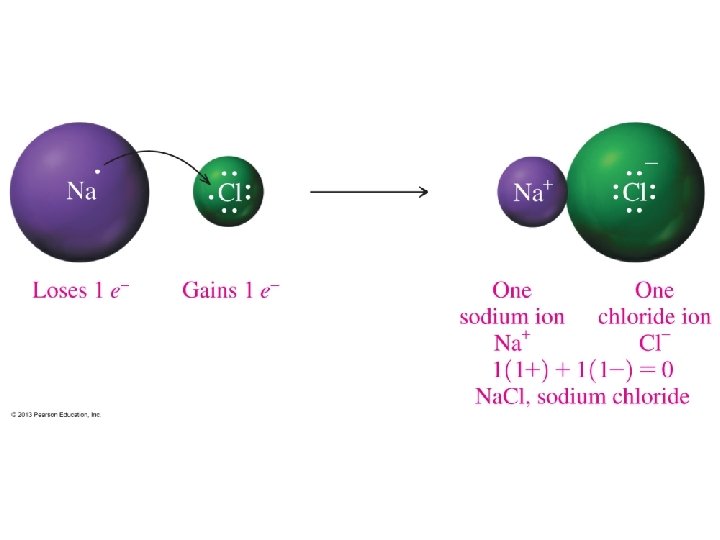
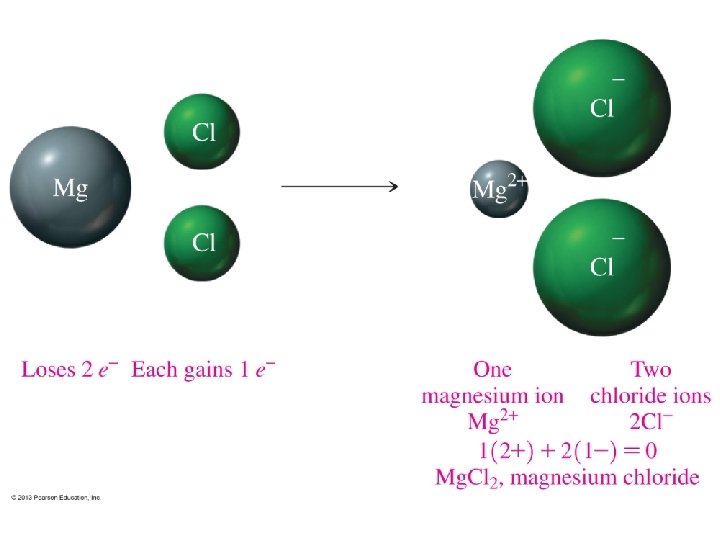
ENLACE IÓNICO Ejemplo: Na. Cl al restar sus electronegatividades Na: 0. 93 – Cl: 3. 16 = 2. 23 (mayor de 1. 8). • En el enlace iónico hay transferencia de electrones del átomo menos electronegativo hacia el más electronegativo. • Lo que provoca la formación de iones +(cationes) de Na+ y de iones - (aniones) de Cl. Como las cargas eléctricas opuestas se atraen, esto formará el enlace iónico. Na+ Cl- = Na. Cl • Generalmente se forma entre átomos de un Metal y un Nometal. Los compuestos que contienen enlaces iónicos se llaman COMPUESTOS IÓNICOS. 11



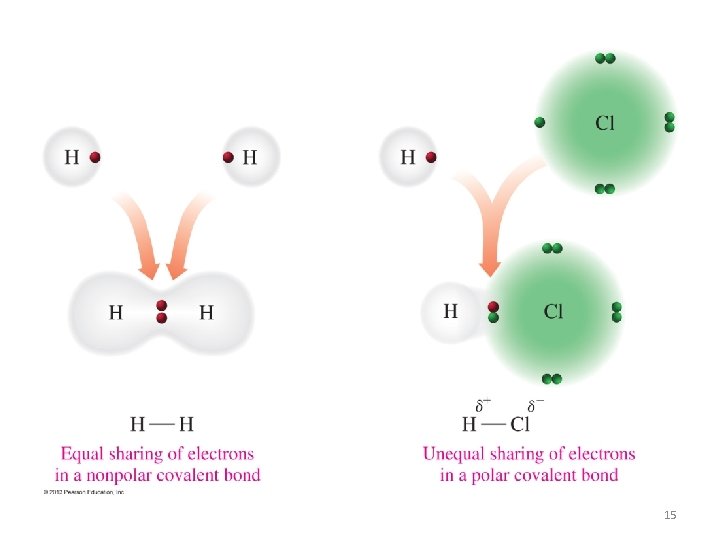
ENLACE COVALENTE Ejemplo: HCl al restar sus electronegatividades H: 2. 10 – Cl: 3. 16 = 1. 06 (menor de 1. 8) • En el enlace covalente se comparten electrones entre los dos átomos (no se forman iones). Se forman MOLÉCULAS. H-Cl = HCl • Generalmente se forma entre dos átomos de Nometales ó entre Hidrógeno y Nometal. Los compuestos que contienen enlaces covalentes e llaman COMPUESTOS COVALENTES. 14

15

Forma de las nubes electrónicas de los compuestos covalentes polares, apolares y iónicos MOLECULAS IONES 16

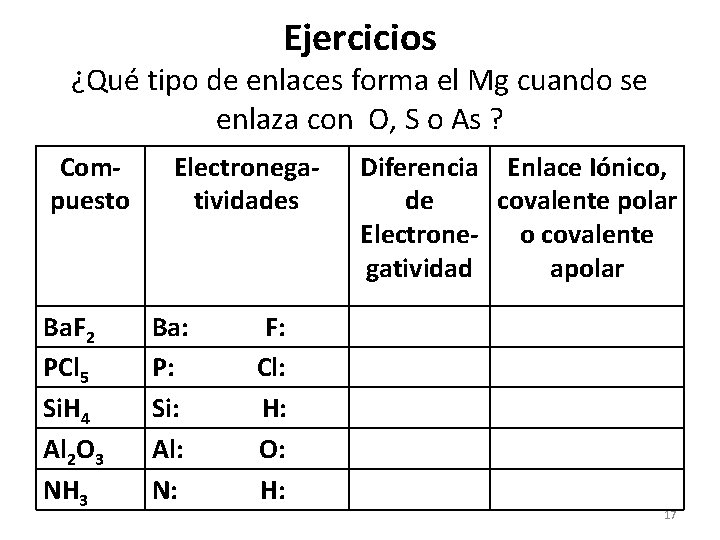
Ejercicios ¿Qué tipo de enlaces forma el Mg cuando se enlaza con O, S o As ? Compuesto Ba. F 2 PCl 5 Si. H 4 Al 2 O 3 NH 3 Electronegatividades Ba: P: Si: Al: N: Diferencia Enlace Iónico, de covalente polar Electrone- o covalente gatividad apolar F: Cl: H: O: H: 17

CLASIFICACIÓN DEL ENLACE COVALENTE Por la diferencia de electronegatividad: • COVALENTE PURO: Diferencia de 0 • COVALENTE APOLAR: de 0 a 0. 4 • COVALENTE POLAR: de mayor de 0. 4 a menor de 1. 8 • • Por los pares de electrones que se comparten en el enlace: COVALENTE SIMPLE COVALENTE DOBLE COVALENTE TRIPLE COVALENTE DATIVO o COORDINADO 18

ESTRUCTURAS DE LEWIS o electrón punto • Diagrama utilizado para representa los electrones de valencia de los átomos. • Se escribe el símbolo del átomo con sus electrones de valencia con figuras ( *, +, x, . ) • Permite representar el tipo de enlace que une los átomos en los compuestos. (SE UTILIZAN PARA DETERMINAR SI LOS ENLACES COVALENTES DE UN COMPUESTO SON SIMPLES, DOBLES, TRIPLES O COORDINADOS). 19

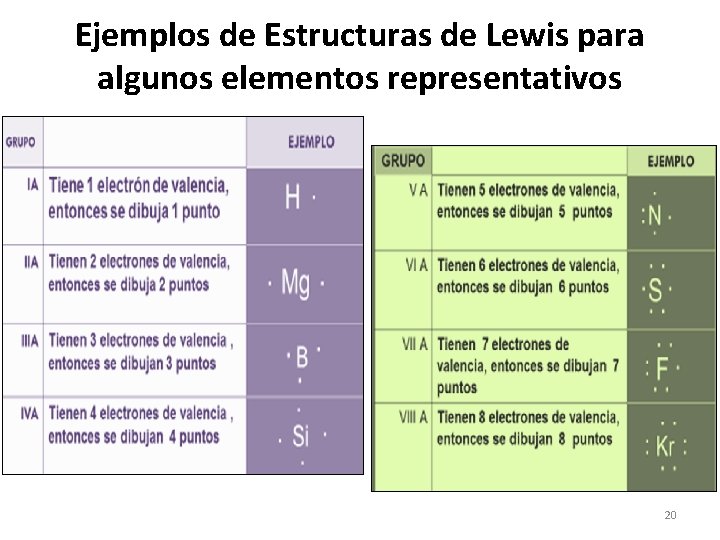
Ejemplos de Estructuras de Lewis para algunos elementos representativos 20

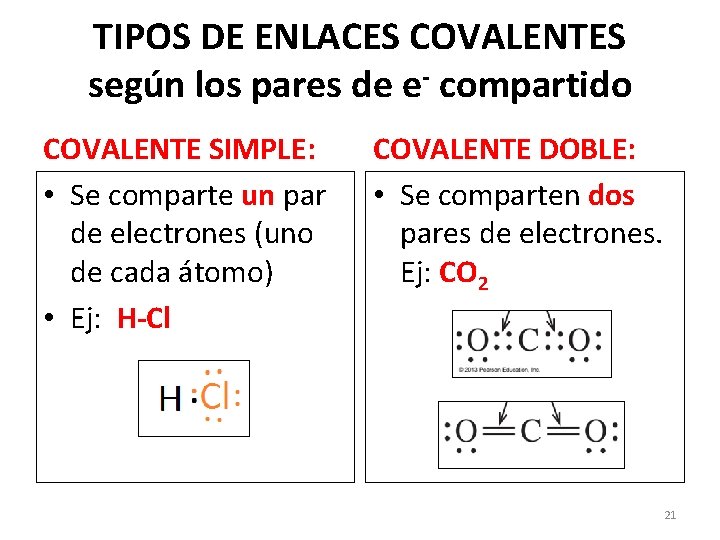
TIPOS DE ENLACES COVALENTES según los pares de e- compartido COVALENTE SIMPLE: • Se comparte un par de electrones (uno de cada átomo) • Ej: H-Cl COVALENTE DOBLE: • Se comparten dos pares de electrones. Ej: CO 2 21

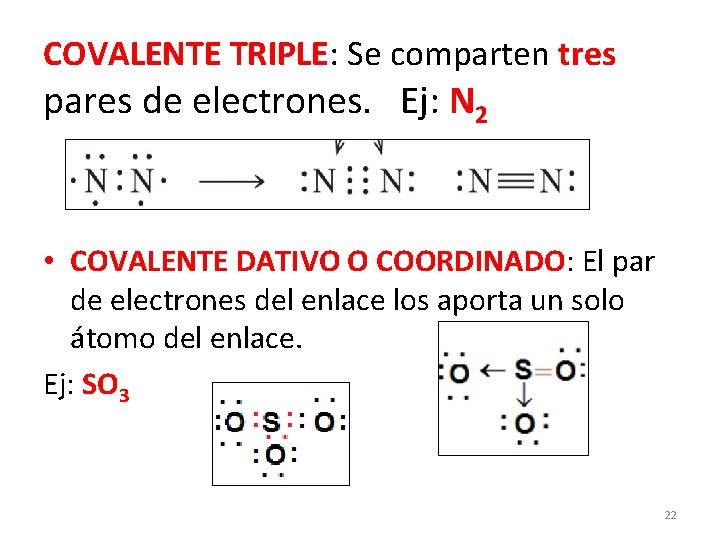
COVALENTE TRIPLE: Se comparten tres pares de electrones. Ej: N 2 • COVALENTE DATIVO O COORDINADO: El par de electrones del enlace los aporta un solo átomo del enlace. Ej: SO 3 22

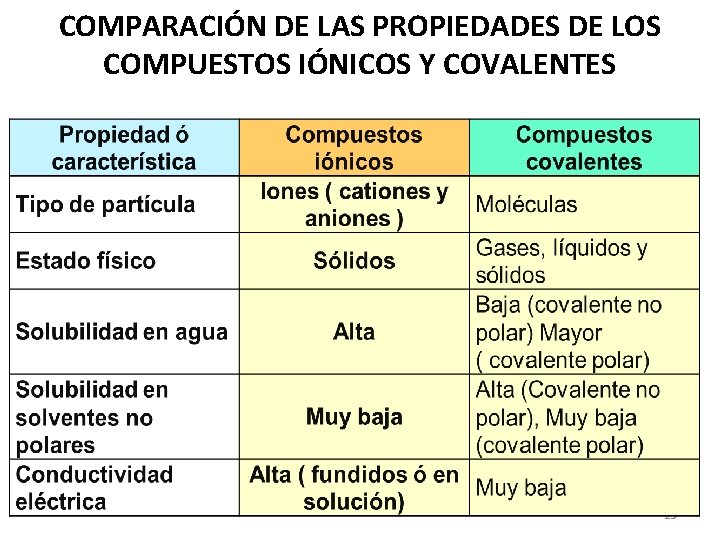
COMPARACIÓN DE LAS PROPIEDADES DE LOS COMPUESTOS IÓNICOS Y COVALENTES 23