QFL 0341 Estrutura e propriedades de Compostos Orgnicos


- Slides: 18

QFL- 0341 – Estrutura e propriedades de Compostos Orgânicos 2. Ligações químicas localizadas Em moléculas orgânicas Prof. Dr. Daniel Nopper Silva Rodrigues dannopper@usp. br

QFL 0341 – Estrutura e Propriedades de Compostos Orgânicos Tópicos da Aula A) Comparações 2

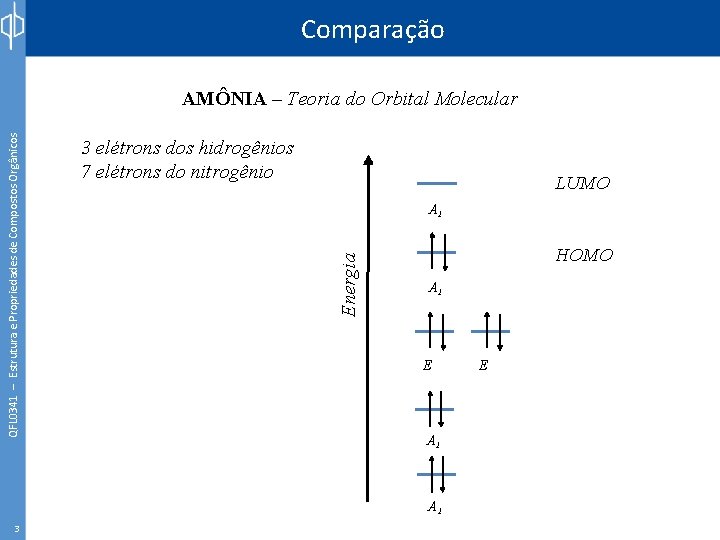
Comparação 3 elétrons dos hidrogênios 7 elétrons do nitrogênio LUMO A 1 Energia QFL 0341 – Estrutura e Propriedades de Compostos Orgânicos AMÔNIA – Teoria do Orbital Molecular HOMO A 1 E A 1 3 E

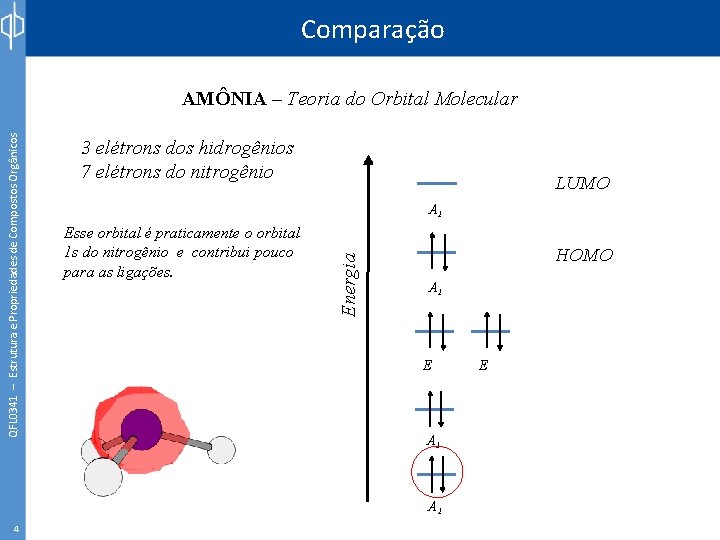
Comparação 3 elétrons dos hidrogênios 7 elétrons do nitrogênio LUMO A 1 Esse orbital é praticamente o orbital 1 s do nitrogênio e contribui pouco para as ligações. Energia QFL 0341 – Estrutura e Propriedades de Compostos Orgânicos AMÔNIA – Teoria do Orbital Molecular HOMO A 1 E A 1 4 E

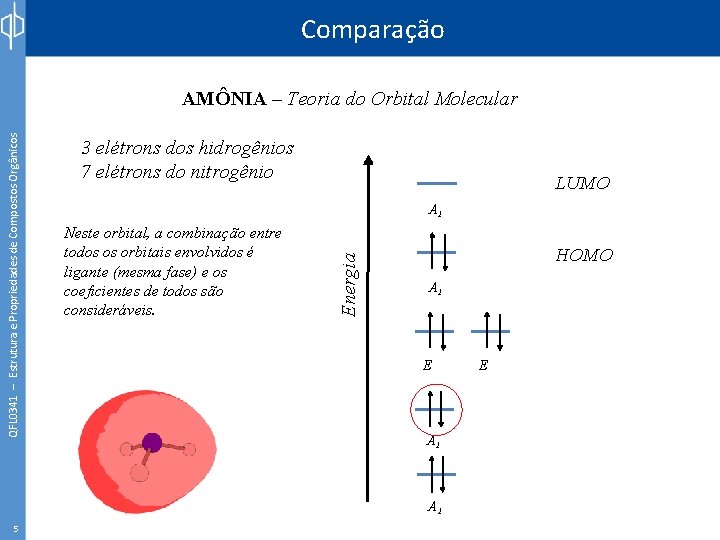
Comparação 3 elétrons dos hidrogênios 7 elétrons do nitrogênio LUMO A 1 Neste orbital, a combinação entre todos os orbitais envolvidos é ligante (mesma fase) e os coeficientes de todos são consideráveis. Energia QFL 0341 – Estrutura e Propriedades de Compostos Orgânicos AMÔNIA – Teoria do Orbital Molecular HOMO A 1 E A 1 5 E

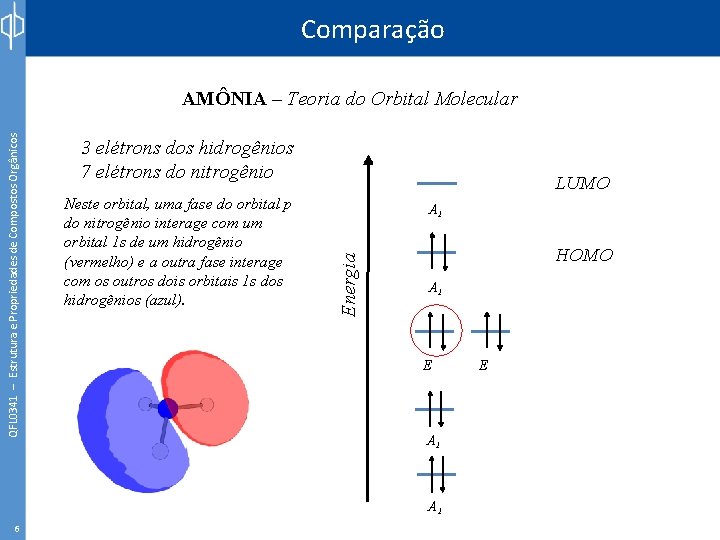
Comparação 3 elétrons dos hidrogênios 7 elétrons do nitrogênio Neste orbital, uma fase do orbital p do nitrogênio interage com um orbital 1 s de um hidrogênio (vermelho) e a outra fase interage com os outros dois orbitais 1 s dos hidrogênios (azul). LUMO A 1 Energia QFL 0341 – Estrutura e Propriedades de Compostos Orgânicos AMÔNIA – Teoria do Orbital Molecular HOMO A 1 E A 1 6 E

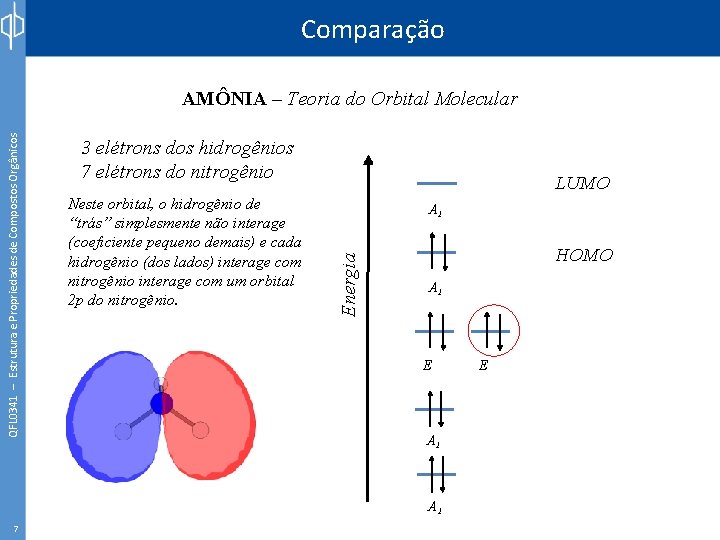
Comparação 3 elétrons dos hidrogênios 7 elétrons do nitrogênio Neste orbital, o hidrogênio de “trás” simplesmente não interage (coeficiente pequeno demais) e cada hidrogênio (dos lados) interage com nitrogênio interage com um orbital 2 p do nitrogênio. LUMO A 1 Energia QFL 0341 – Estrutura e Propriedades de Compostos Orgânicos AMÔNIA – Teoria do Orbital Molecular HOMO A 1 E A 1 7 E

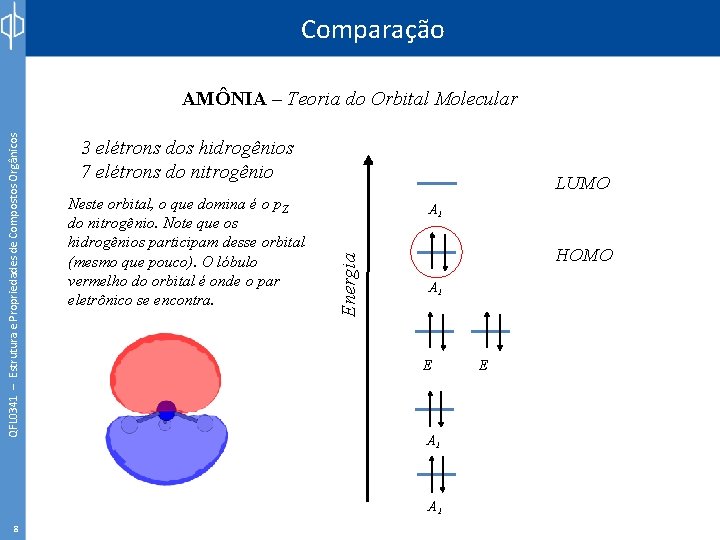
Comparação 3 elétrons dos hidrogênios 7 elétrons do nitrogênio Neste orbital, o que domina é o p. Z do nitrogênio. Note que os hidrogênios participam desse orbital (mesmo que pouco). O lóbulo vermelho do orbital é onde o par eletrônico se encontra. LUMO A 1 Energia QFL 0341 – Estrutura e Propriedades de Compostos Orgânicos AMÔNIA – Teoria do Orbital Molecular HOMO A 1 E A 1 8 E

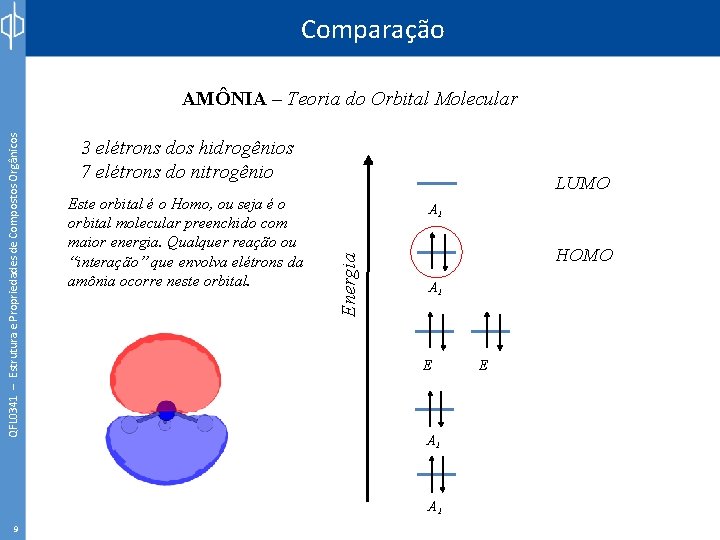
Comparação 3 elétrons dos hidrogênios 7 elétrons do nitrogênio Este orbital é o Homo, ou seja é o orbital molecular preenchido com maior energia. Qualquer reação ou “interação” que envolva elétrons da amônia ocorre neste orbital. LUMO A 1 Energia QFL 0341 – Estrutura e Propriedades de Compostos Orgânicos AMÔNIA – Teoria do Orbital Molecular HOMO A 1 E A 1 9 E

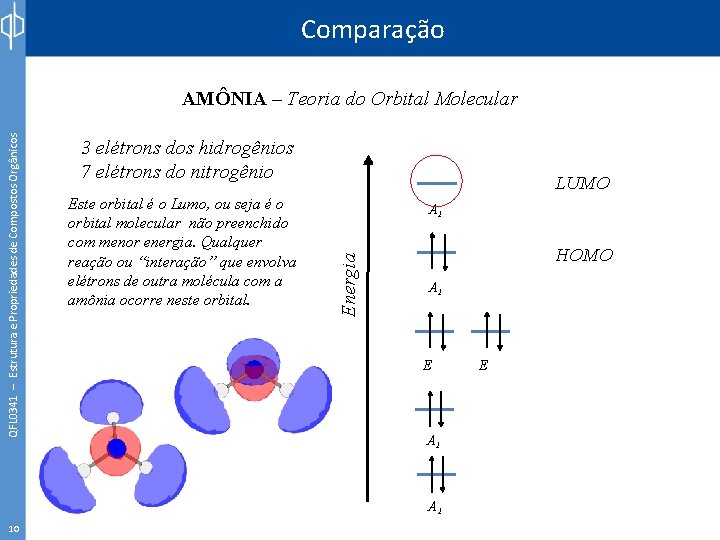
Comparação 3 elétrons dos hidrogênios 7 elétrons do nitrogênio Este orbital é o Lumo, ou seja é o orbital molecular não preenchido com menor energia. Qualquer reação ou “interação” que envolva elétrons de outra molécula com a amônia ocorre neste orbital. LUMO A 1 Energia QFL 0341 – Estrutura e Propriedades de Compostos Orgânicos AMÔNIA – Teoria do Orbital Molecular HOMO A 1 E A 1 10 E

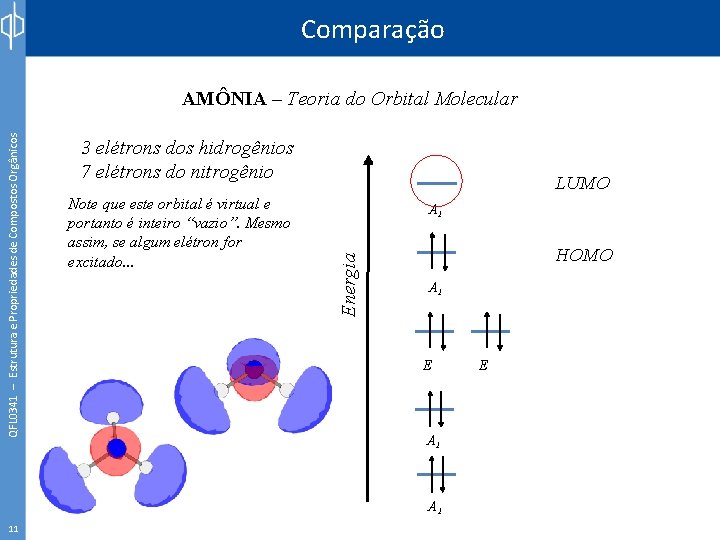
Comparação 3 elétrons dos hidrogênios 7 elétrons do nitrogênio Note que este orbital é virtual e portanto é inteiro “vazio”. Mesmo assim, se algum elétron for excitado. . . LUMO A 1 Energia QFL 0341 – Estrutura e Propriedades de Compostos Orgânicos AMÔNIA – Teoria do Orbital Molecular HOMO A 1 E A 1 11 E

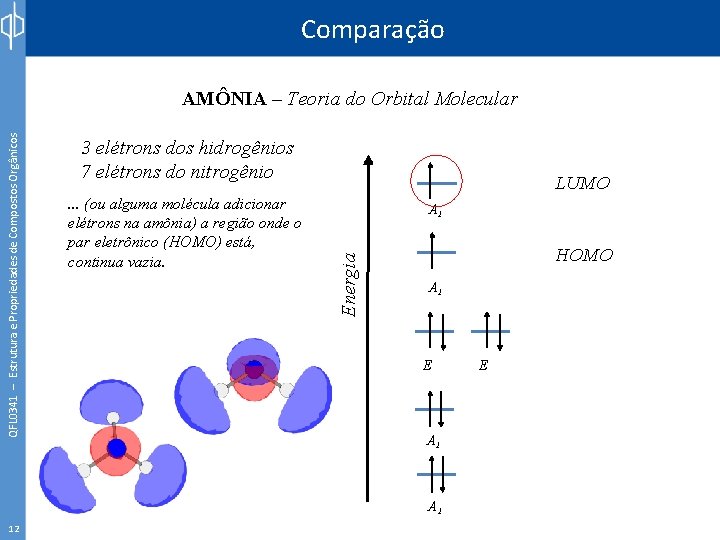
Comparação 3 elétrons dos hidrogênios 7 elétrons do nitrogênio. . . (ou alguma molécula adicionar elétrons na amônia) a região onde o par eletrônico (HOMO) está, continua vazia. LUMO A 1 Energia QFL 0341 – Estrutura e Propriedades de Compostos Orgânicos AMÔNIA – Teoria do Orbital Molecular HOMO A 1 E A 1 12 E

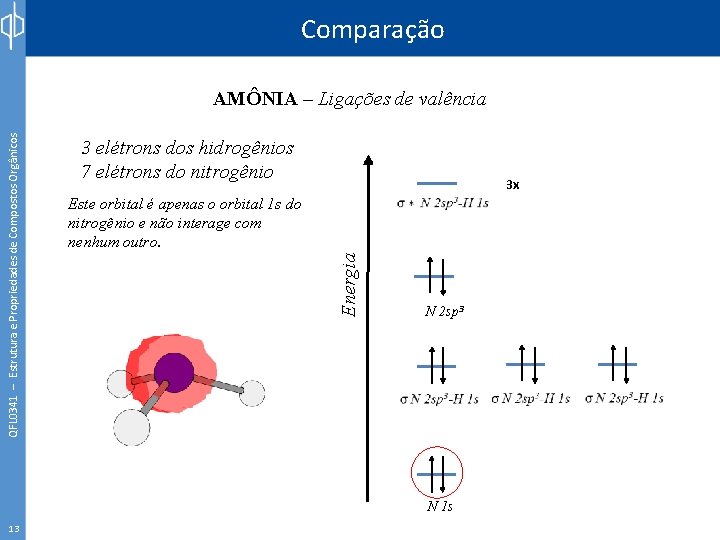
Comparação 3 elétrons dos hidrogênios 7 elétrons do nitrogênio 3 x Este orbital é apenas o orbital 1 s do nitrogênio e não interage com nenhum outro. Energia QFL 0341 – Estrutura e Propriedades de Compostos Orgânicos AMÔNIA – Ligações de valência N 2 sp 3 N 1 s 13

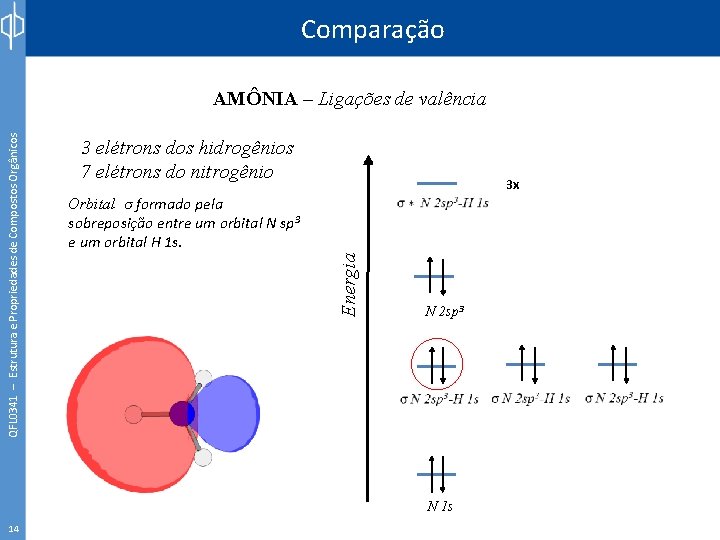
Comparação 3 elétrons dos hidrogênios 7 elétrons do nitrogênio 3 x Orbital σ formado pela sobreposição entre um orbital N sp 3 e um orbital H 1 s. Energia QFL 0341 – Estrutura e Propriedades de Compostos Orgânicos AMÔNIA – Ligações de valência N 2 sp 3 N 1 s 14

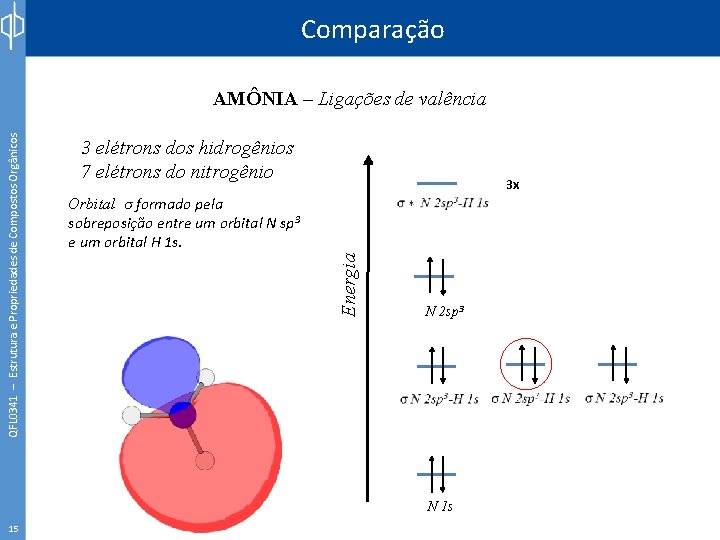
Comparação 3 elétrons dos hidrogênios 7 elétrons do nitrogênio 3 x Orbital σ formado pela sobreposição entre um orbital N sp 3 e um orbital H 1 s. Energia QFL 0341 – Estrutura e Propriedades de Compostos Orgânicos AMÔNIA – Ligações de valência N 2 sp 3 N 1 s 15

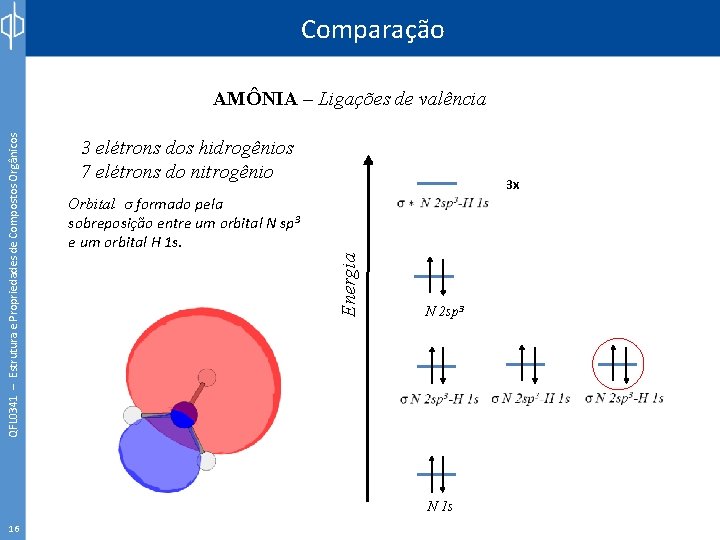
Comparação 3 elétrons dos hidrogênios 7 elétrons do nitrogênio 3 x Orbital σ formado pela sobreposição entre um orbital N sp 3 e um orbital H 1 s. Energia QFL 0341 – Estrutura e Propriedades de Compostos Orgânicos AMÔNIA – Ligações de valência N 2 sp 3 N 1 s 16

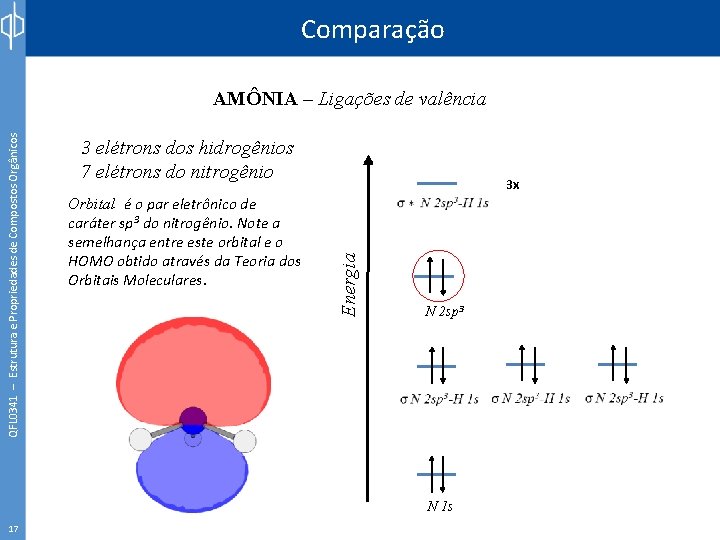
Comparação 3 elétrons dos hidrogênios 7 elétrons do nitrogênio Orbital é o par eletrônico de caráter sp 3 do nitrogênio. Note a semelhança entre este orbital e o HOMO obtido através da Teoria dos Orbitais Moleculares. 3 x Energia QFL 0341 – Estrutura e Propriedades de Compostos Orgânicos AMÔNIA – Ligações de valência N 2 sp 3 N 1 s 17

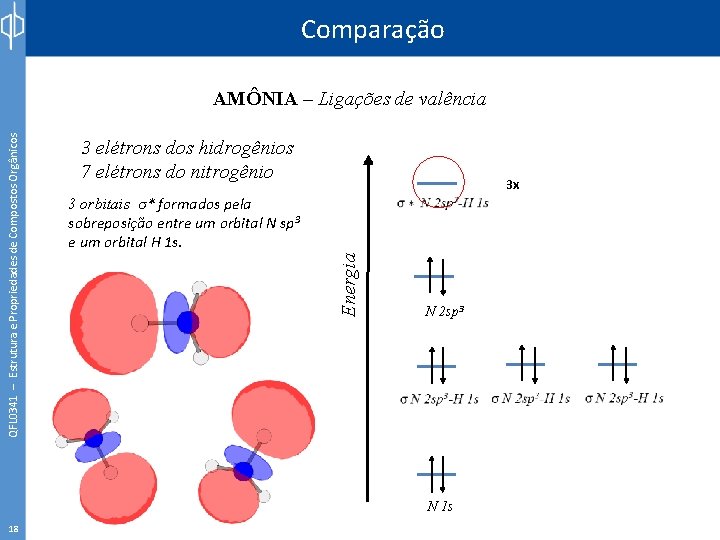
Comparação 3 elétrons dos hidrogênios 7 elétrons do nitrogênio 3 x 3 orbitais σ* formados pela sobreposição entre um orbital N sp 3 e um orbital H 1 s. Energia QFL 0341 – Estrutura e Propriedades de Compostos Orgânicos AMÔNIA – Ligações de valência N 2 sp 3 N 1 s 18