PODSTAWY CHEMII ANALITYCZNEJ Analiza wagowa 1 ANALIZA WAGOWA







- Slides: 19

PODSTAWY CHEMII ANALITYCZNEJ Analiza wagowa 1

ANALIZA WAGOWA (GRAWIMETRIA) Oddziel i zważ Dokładność!! Błąd bezwzględny < 0, 1% Metoda bezwzględna i żmudna Pośrednia/ bezpośrednia Gazowa (H 2 O; CO 2 ale też Si. O 2; Sn. O 2…) Elektrograwimetria: Katodowa Cu 2+ + 2 e- Cu 0 Anodowa Pb 2+ + 2 H 2 O Pb. O 2 + 2 e- + 4 H+ Strąceniowa!! (precypitacyjna)

ANALIZA WAGOWA Oddzielenie Selektywne Ilościowe Zdefiniowany skład (mnożnik analityczny) Odczynnik do grawimetrii Specyficzny/ Selektywny (ew. oddzielanie i maskowanie) Tworzący trudnorozpuszczalny osad Osad łatwo odsączalny i przemywalny (najlepiej gruboziarnisty) Osad trwały i o stałym składzie (po wysuszeniu/wyprażeniu)

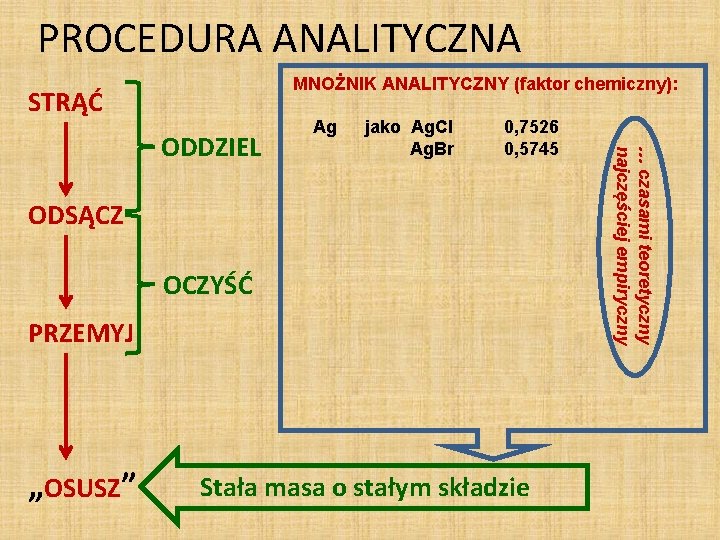
PROCEDURA ANALITYCZNA MNOŻNIK ANALITYCZNY (faktor chemiczny): STRĄĆ Cr ODSĄCZ OCZYŚĆ PRZEMYJ 0, 7526 0, 5745 jako Ba. Cr. O 4 Pb. Cr. O 4 Cr 2 O 3 jako Ba. Cr. O 4 Pb. Cr. O 4 0, 2053 0, 1609 0, 3000 0, 2352 Cu 0, 7986 0, 6648 0, 9996 1, 252 Cu. O P „OSUSZ” jako Ag. Cl Ag. Br jako Cu 2 S Cu. S jako Cu 2 S Cu jako (NH 4)3 PO 4*12 Mo. O 3 Stała masa o stałym składzie … czasami teoretyczny najczęściej empiryczny ODDZIEL Ag 0, 01639

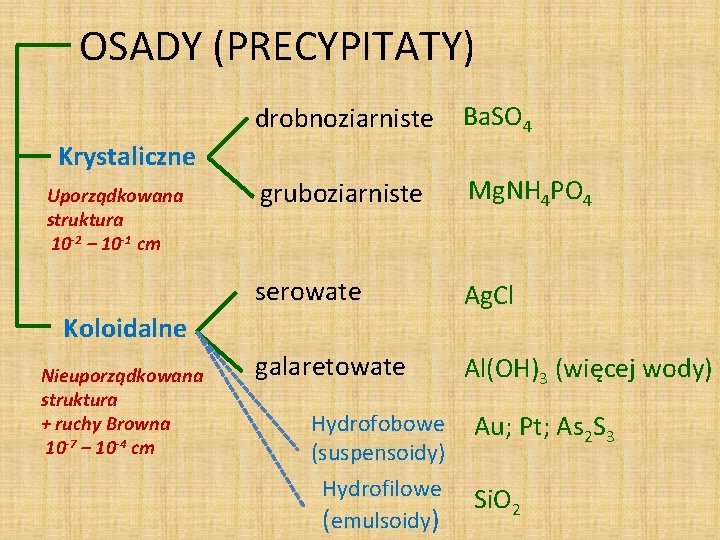
OSADY (PRECYPITATY) drobnoziarniste Ba. SO 4 gruboziarniste Mg. NH 4 PO 4 serowate Ag. Cl galaretowate Al(OH)3 (więcej wody) Krystaliczne Uporządkowana struktura 10 -2 – 10 -1 cm Koloidalne Nieuporządkowana struktura + ruchy Browna 10 -7 – 10 -4 cm Hydrofobowe (suspensoidy) Hydrofilowe (emulsoidy) Au; Pt; As 2 S 3 Si. O 2

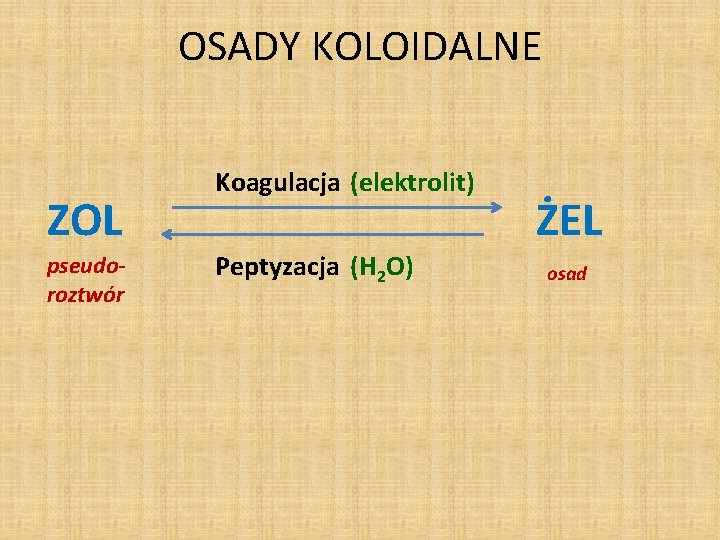
OSADY KOLOIDALNE ZOL pseudoroztwór Koagulacja (elektrolit) Peptyzacja (H 2 O) ŻEL osad

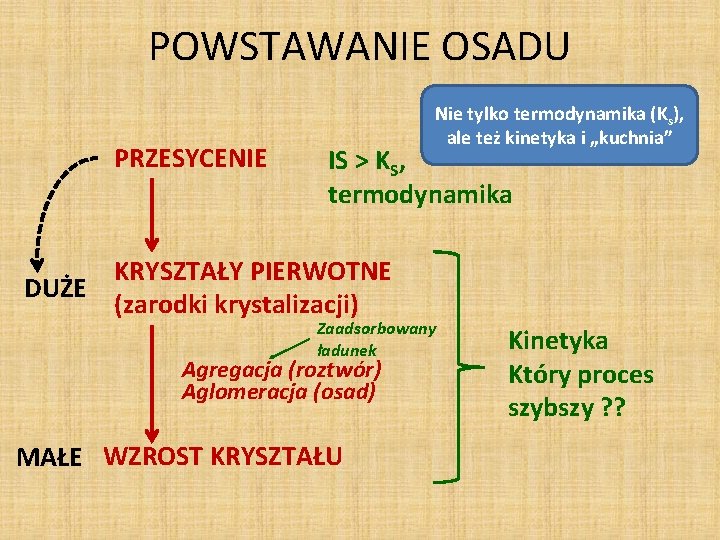
POWSTAWANIE OSADU PRZESYCENIE Nie tylko termodynamika (Ks), ale też kinetyka i „kuchnia” IS > KS, termodynamika KRYSZTAŁY PIERWOTNE DUŻE (zarodki krystalizacji) Zaadsorbowany ładunek Agregacja (roztwór) Aglomeracja (osad) MAŁE WZROST KRYSZTAŁU Kinetyka Który proces szybszy ? ?

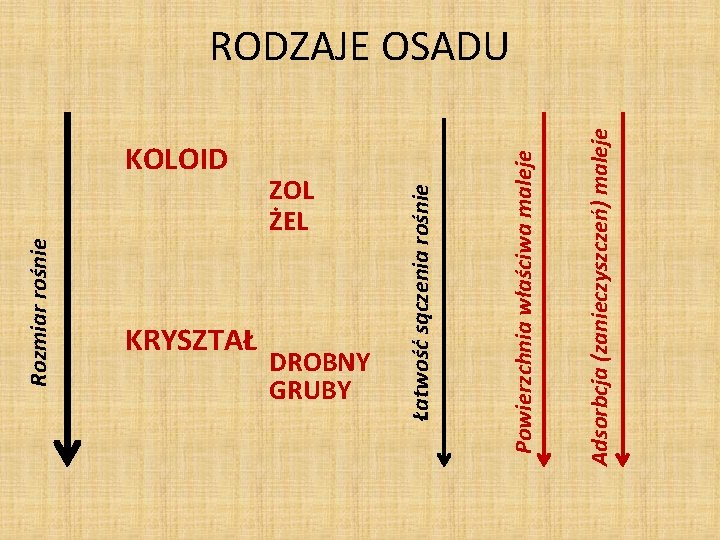
Rozmiar rośnie KOLOID KRYSZTAŁ ZOL ŻEL DROBNY GRUBY Adsorbcja (zanieczyszczeń) maleje Powierzchnia właściwa maleje Łatwość sączenia rośnie RODZAJE OSADU

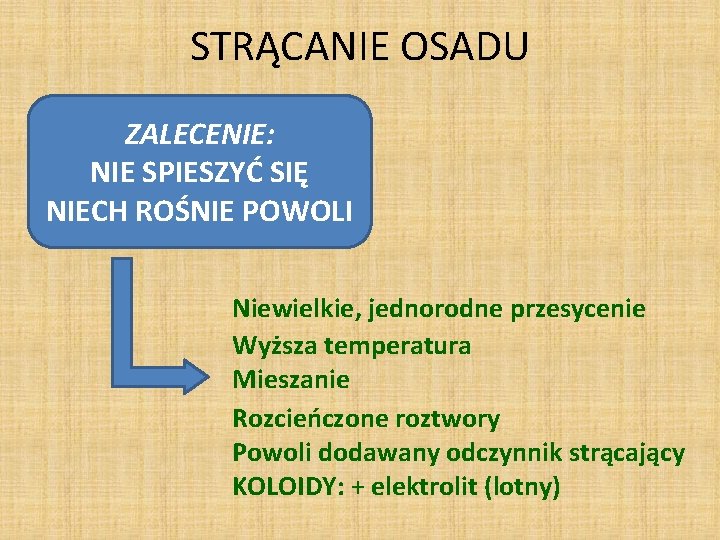
STRĄCANIE OSADU ZALECENIE: NIE SPIESZYĆ SIĘ NIECH ROŚNIE POWOLI Niewielkie, jednorodne przesycenie Wyższa temperatura Mieszanie Rozcieńczone roztwory Powoli dodawany odczynnik strącający KOLOIDY: + elektrolit (lotny)

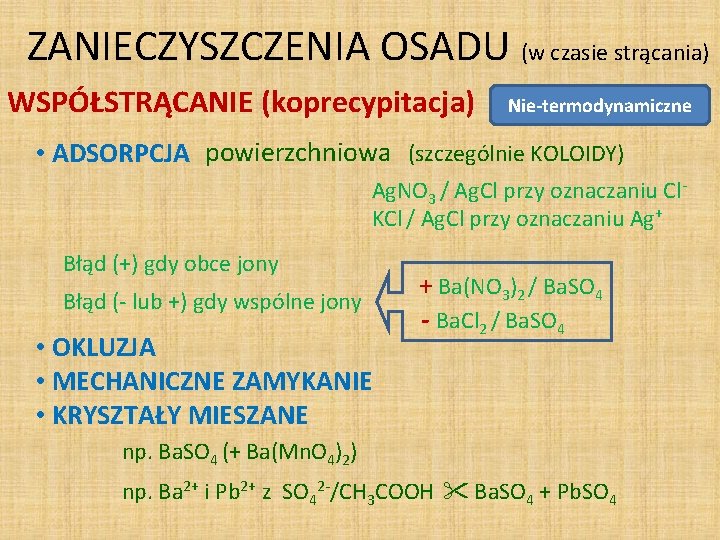
ZANIECZYSZCZENIA OSADU (w czasie strącania) WSPÓŁSTRĄCANIE (koprecypitacja) Nie-termodynamiczne • ADSORPCJA powierzchniowa (szczególnie KOLOIDY) Ag. NO 3 / Ag. Cl przy oznaczaniu Cl. KCl / Ag. Cl przy oznaczaniu Ag+ Błąd (+) gdy obce jony Błąd (- lub +) gdy wspólne jony • OKLUZJA • MECHANICZNE ZAMYKANIE • KRYSZTAŁY MIESZANE + Ba(NO 3)2 / Ba. SO 4 - Ba. Cl 2 / Ba. SO 4 np. Ba. SO 4 (+ Ba(Mn. O 4)2) np. Ba 2+ i Pb 2+ z SO 42 -/CH 3 COOH Ba. SO 4 + Pb. SO 4

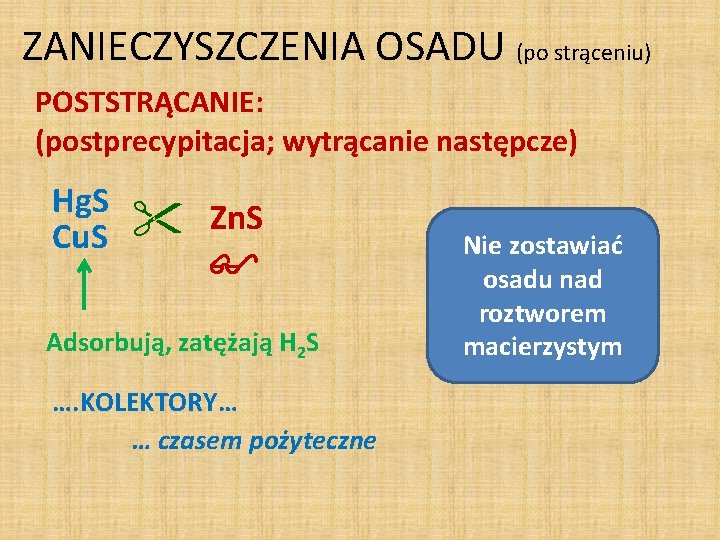
ZANIECZYSZCZENIA OSADU (po strąceniu) POSTSTRĄCANIE: (postprecypitacja; wytrącanie następcze) Hg. S Cu. S Zn. S Adsorbują, zatężają H 2 S …. KOLEKTORY… … czasem pożyteczne Nie zostawiać osadu nad roztworem macierzystym

OCZYSZCZANIE OSADU Starzenie osadu (np. uwalnianie H 2 O przez koloid) Dojrzewanie osadu (rekrystalizacja drobno grubo) Przemywanie osadu • wodą (ale nie koloidy) • roztworem ze wspólnym jonem (tym drugim ) • elektrolitem obojętnym/lotnym (szczególnie koloidy) • rozpuszczalnikiem organicznym (szczególnie emulsoidy: Et. OH Aceton Strącanie wielokrotne Et. OH CS 2 (gdy S 0) np. Fe(OH)3 NH 3 / HNO 3 / NH 3 /HNO 3 / …. np. Ag. Cl Strącanie homogeniczne

STRĄCANIE HOMOGENICZNE CH 3 CSNH 2 + 2 H 2 O CH 3 COOH + NH 3 + H 2 S (H 2 N)2 CO + H 2 O CO 2 + 2 NH 3 C 6 H 12 N 4 + 6 H 2 O 6 CH 2 O + 4 NH 3 IO 3 - + 5 I- + 3 H 2 O 3 I 2 + 6 OHCCl 3 COO- + OH- CHCl 3 + H 2 O + CO 32(C 2 H 5)2 C 2 O 4 + 2 H 2 O 2 C 2 H 5 OH + H 2 C 2 O 4 (CH 3)2 SO 4 + 2 H 2 O 2 CH 3 OH + H 2 SO 4 (CH 3)3 PO 4 + 3 H 2 O 3 CH 3 OH + H 3 PO 4 … powolne usuwanie rozpuszczalnika np. Al(Ox)3 / aceton

SUSZENIE / PRAŻENIE Uzyskanie „Postaci ważonej osadu”, czyli osadu o stałej (niezmiennej w czasie) masie i o zdefiniowanym składzie mnożnik analityczny Suszarki Tygle Eksykatory Bezpopiołowe sączki

PROCESY FIZYCZNE I CHEMICZNE H 2 O wilgoć woda koordynacyjna, krystaliczna, zeolityczna woda konstytucyjna Usunięcie lotnych elektrolitów i innych soli NH 3; NH 4 NO 3; NH 4 Cl HCl; HNO 3; CH 3 COOH H 2 C 2 O 4; (NH 4)2 C 2 O 4 …. . Si. F 4; Sn. I 4; Hg. S; …. Przemiany chemiczne np. 2 Zn. S + 3 O 2 2 Zn. O + 2 SO 2 np. Ba. SO 4 + 4 C Ba. S + 4 CO Ba. S + 2 O 2 Ba. SO 4

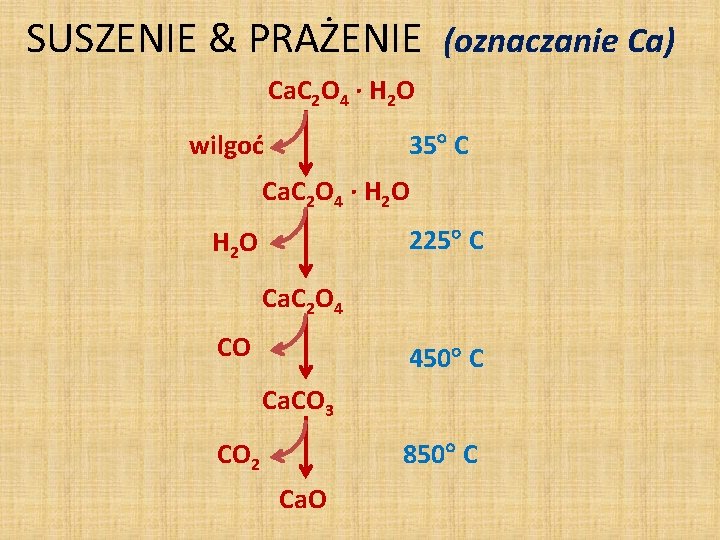
SUSZENIE & PRAŻENIE (oznaczanie Ca) Ca. C 2 O 4 · H 2 O wilgoć 35 C Ca. C 2 O 4 · H 2 O 225 C H 2 O Ca. C 2 O 4 CO 450 C Ca. CO 3 CO 2 850 C Ca. O

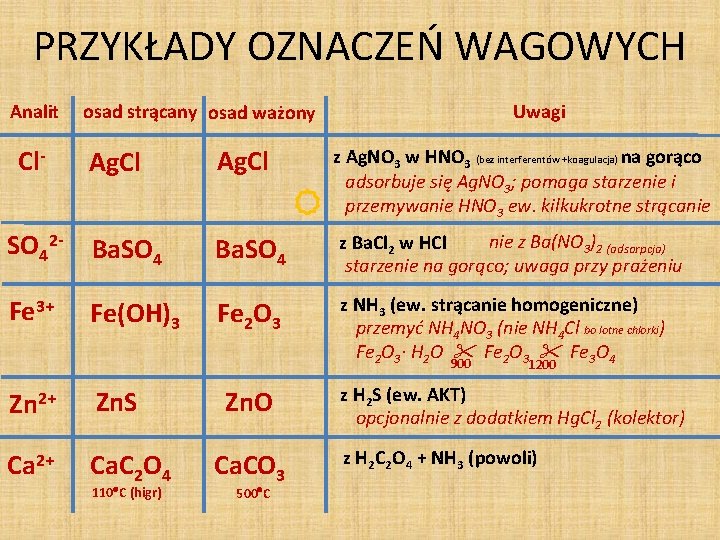
PRZYKŁADY OZNACZEŃ WAGOWYCH Analit Cl- osad strącany osad ważony Uwagi Ag. Cl z Ag. NO 3 w HNO 3 (bez interferentów +koagulacja) na gorąco adsorbuje się Ag. NO 3; pomaga starzenie i przemywanie HNO 3 ew. kilkukrotne strącanie SO 42 - Ba. SO 4 nie z Ba(NO 3)2 (adsorpcja) z Ba. Cl 2 w HCl starzenie na gorąco; uwaga przy prażeniu Fe 3+ Fe 2 O 3 z NH 3 (ew. strącanie homogeniczne) przemyć NH 4 NO 3 (nie NH 4 Cl bo lotne chlorki) Fe 2 O 3· H 2 O Fe 2 O 3 Fe 3 O 4 Ag. Cl Fe(OH)3 900 Zn 2+ Zn. S Ca 2+ Ca. C 2 O 4 110 C (higr) Zn. O Ca. CO 3 500 C 1200 z H 2 S (ew. AKT) opcjonalnie z dodatkiem Hg. Cl 2 (kolektor) z H 2 C 2 O 4 + NH 3 (powoli)

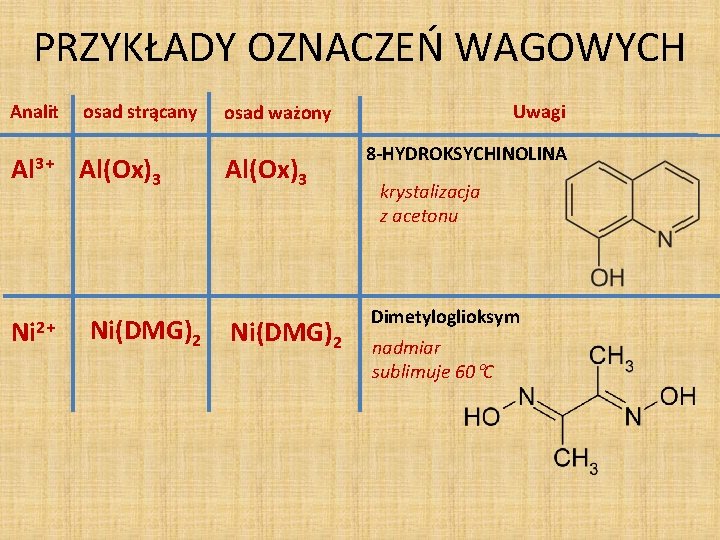
PRZYKŁADY OZNACZEŃ WAGOWYCH Analit Al 3+ Ni 2+ osad strącany Al(Ox)3 Ni(DMG)2 Uwagi osad ważony Al(Ox)3 Ni(DMG)2 8 -HYDROKSYCHINOLINA krystalizacja z acetonu Dimetyloglioksym nadmiar sublimuje 60 C

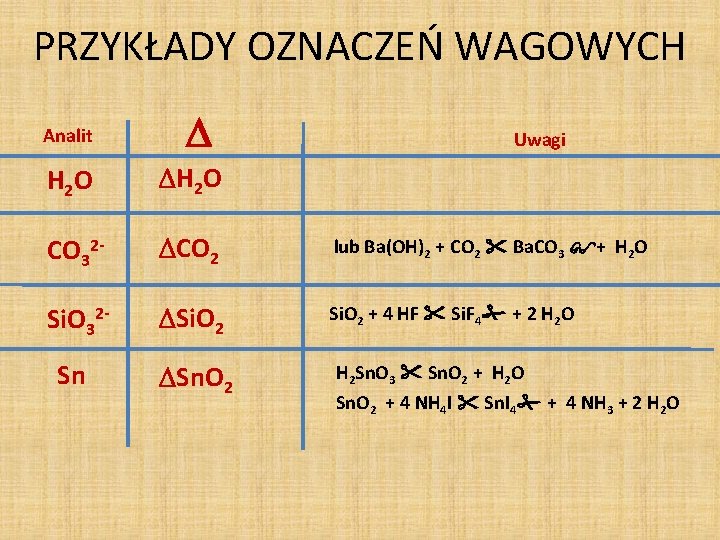
PRZYKŁADY OZNACZEŃ WAGOWYCH Analit Uwagi H 2 O CO 32 - CO 2 lub Ba(OH)2 + CO 2 Ba. CO 3 + H 2 O Si. O 32 - Si. O 2 + 4 HF Si. F 4 + 2 H 2 O Sn Sn. O 2 H 2 Sn. O 3 Sn. O 2 + H 2 O Sn. O 2 + 4 NH 4 I Sn. I 4 + 4 NH 3 + 2 H 2 O
 Analiza wagowa zadania
Analiza wagowa zadania Adrianna stawarz
Adrianna stawarz Kolory w chemii nieorganicznej
Kolory w chemii nieorganicznej Radiochemia
Radiochemia Przetwornik ca wagowy
Przetwornik ca wagowy Podstawy tworzenia stron internetowych
Podstawy tworzenia stron internetowych Spis liter cyfr i innych znaków danego kroju pisma
Spis liter cyfr i innych znaków danego kroju pisma Teoretyczne podstawy informatyki
Teoretyczne podstawy informatyki Edukacja formalna i nieformalna
Edukacja formalna i nieformalna Php podstawy
Php podstawy Html podstawy
Html podstawy Studnia potencjału
Studnia potencjału Warunki realizacji podstawy programowej
Warunki realizacji podstawy programowej Vhdl automat
Vhdl automat Podstawy sztucznej inteligencji
Podstawy sztucznej inteligencji Oznaczenia na skalach mierników
Oznaczenia na skalach mierników Realizacja podstawy programowej z religii sprawozdanie
Realizacja podstawy programowej z religii sprawozdanie Podstawy fizykochemii spalania
Podstawy fizykochemii spalania Podstawy fizykochemii spalania
Podstawy fizykochemii spalania Podstawy statyki budowli
Podstawy statyki budowli





































