PODSTAWY CHEMII ANALITYCZNEJ Wykad 11 Wstp do Analizy







- Slides: 16

PODSTAWY CHEMII ANALITYCZNEJ Wykład 11 Wstęp do Analizy Jakościowej 1

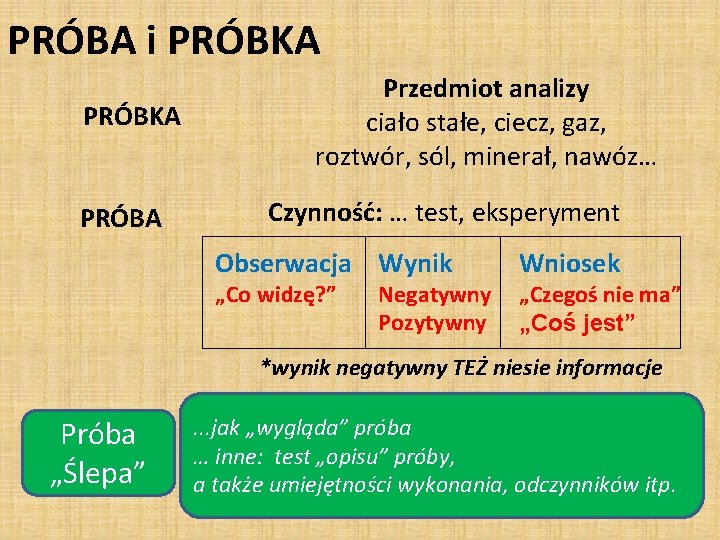
PRÓBA i PRÓBKA PRÓBA Przedmiot analizy ciało stałe, ciecz, gaz, roztwór, sól, minerał, nawóz… Czynność: … test, eksperyment Obserwacja Wynik „Co widzę? ” Negatywny Pozytywny Wniosek „Czegoś nie ma” „Coś jest” *wynik negatywny TEŻ niesie informacje Próba „Ślepa” . . . jak „wygląda” próba … inne: test „opisu” próby, a także umiejętności wykonania, odczynników itp.

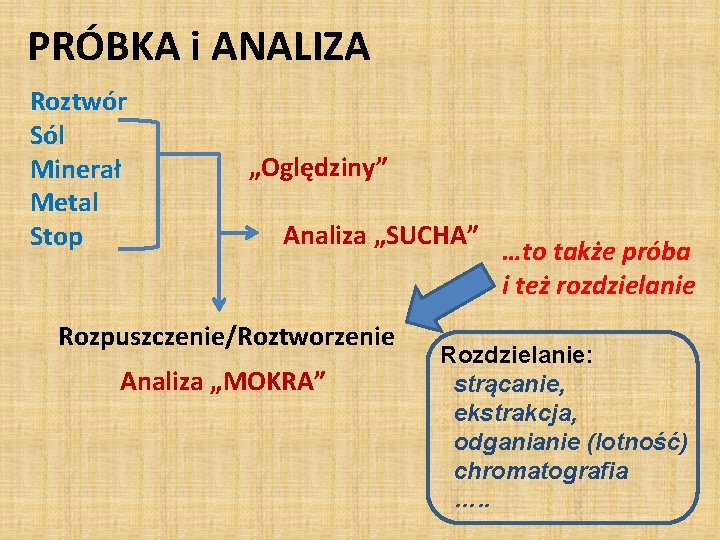
PRÓBKA i ANALIZA Roztwór Sól Minerał Metal Stop „Oględziny” Analiza „SUCHA” Rozpuszczenie/Roztworzenie Analiza „MOKRA” …to także próba i też rozdzielanie Rozdzielanie: strącanie, ekstrakcja, odganianie (lotność) chromatografia …. .

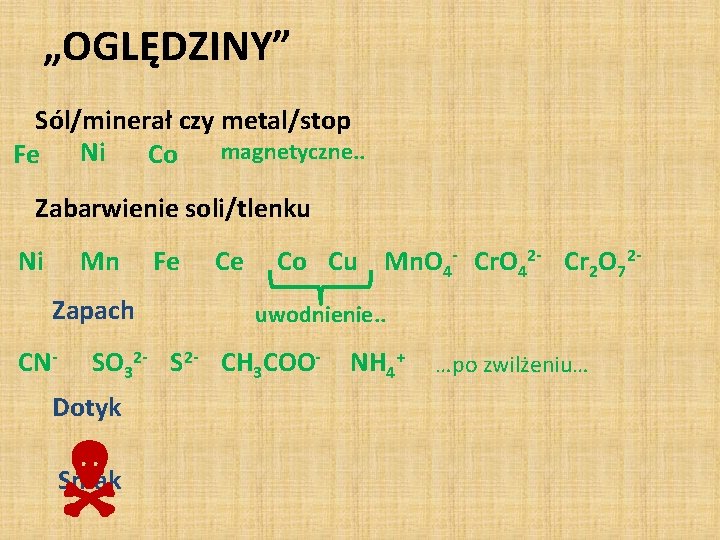
„OGLĘDZINY” Sól/minerał czy metal/stop magnetyczne. . Fe Ni Co Zabarwienie soli/tlenku Ni Mn Zapach CN- Fe Ce Co Cu Mn. O 4 - Cr. O 42 - Cr 2 O 72 uwodnienie. . SO 32 - S 2 - CH 3 COO- Dotyk Smak NH 4+ …po zwilżeniu…

ANALIZA „SUCHA” „Rozkład” termiczny: zmiany koloru odwracalne żółty → czerwony Cd. S biały → żółty Zn. O, Sn. O nieodwracalne … wydzielanie gazu węglany, siarczki, siarczyny sublimacja Hg 2 Cl 2 Hg. I 2 As 2 S 3 „sublimacja” NH 4 Cl Emisyjna „Spektrometria” Atomowa Perły

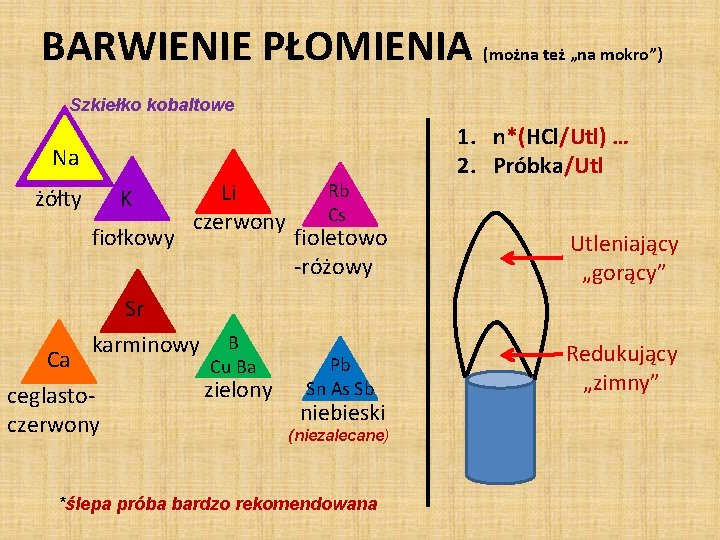
BARWIENIE PŁOMIENIA (można też „na mokro”) Szkiełko kobaltowe Na żółty K fiołkowy Li czerwony Rb Cs 1. n*(HCl/Utl) … 2. Próbka/Utl fioletowo -różowy Utleniający „gorący” Pb Sn As Sb Redukujący „zimny” Sr Ca karminowy ceglastoczerwony B Cu Ba zielony niebieski (niezalecane) *ślepa próba bardzo rekomendowana

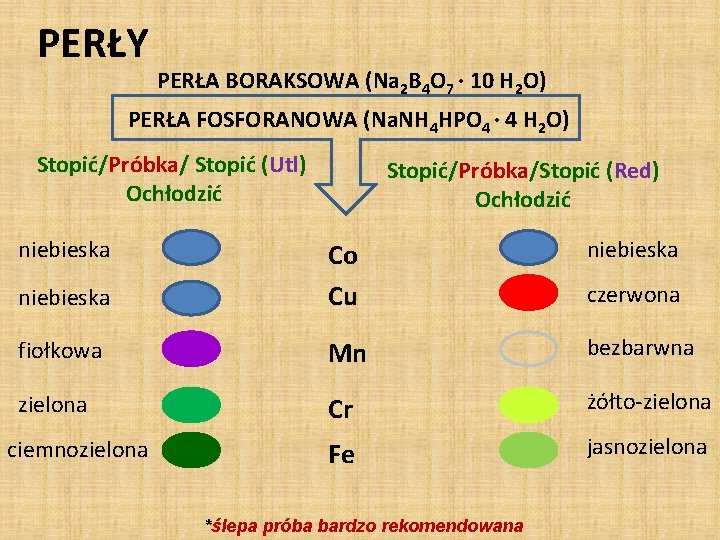
PERŁY PERŁA BORAKSOWA (Na 2 B 4 O 7 · 10 H 2 O) PERŁA FOSFORANOWA (Na. NH 4 HPO 4 · 4 H 2 O) Stopić/Próbka/ Stopić (Utl) Ochłodzić niebieska Stopić/Próbka/Stopić (Red) Ochłodzić niebieska Co Cu fiołkowa Mn bezbarwna zielona Cr żółto-zielona Fe jasnozielona ciemnozielona *ślepa próba bardzo rekomendowana czerwona

ANALIZA „MOKRA” ANALIZA WYBIÓRCZA (próby „specyficzne”) „ ” - nie dla każdego analitu jest dostępny reagent/próba - wynik fałszowany przez składniki próbki ANALIZA SYSTEMATYCZNA „ ” - Aniony wg schematu Bunsena 7 grup anionów: Próby wstępne Próby charakterystyczne (bez rozdzielania) - Kationy wg schematu Freseniusa 5 grup kationów: Rozdzielanie (strąceniowe) Próby charakterystyczne

ROZPUSZCZANIE/ROZTWARZANIE SOLE ( … tlenki, minerały, rudy, nawozy, glinokrzemiany, węglany, fosforyty, piryty, siarczany. . ) - w H 2 O wygrałeś , sprawdź p. H - w CH 3 COOH słaby kwas CO 32 -; S 2 -(niektóre) ; SO 32 -; NO 2 -…. IV gr. anal. Mg. Cr. O 4 Ca. Cr. O 4 Sr. Cr. O 4 Ba. Cr. O 4 Pb. Cr. O 4 - rozpuszczalny p. Ks 5 (CH 3 COOH) p. Ks 10 (rozc. HCl) p. Ks 14 (stęż. HCl lub Na. OH) 2 Cr. O 42 - + 2 H+ Cr 2 O 72 - + H 2 O 2 Ba. Cr. O 4 + 2 H+ 2 Ba 2+ + Cr 2 O 72 - + H 2 O Pb 2+ + 4 OH- Pb(OH)42 - + H 2 O Pb. Cr. O 4 + 4 OH- Pb(OH)42 - + Cr. O 42 - - w HCl - w H 2 SO 4 mocny kwas, kompleksujący, redukujący Mn. O 2; Pb 3 O 4…. mocny kwas, pierwszy małolotny : Ca. F 2… - w HNO 3 mocny kwas, utleniający: S 2 - (wszystkie) … rozdzielenie przez ługowanie np. KI/Ba. Cr. O 4…

ROZPUSZCZANIE/ROZTWARZANIE SOLE - w HF - w NH 3 - w KOH ( … tlenki, minerały, rudy, nawozy, glinokrzemiany, węglany, fosforyty, piryty, siarczany. . ) słaby kwas, kompleksujący… (krzemiany Si. F 4 ) kompleksujący (Ag. Cl) amfoteryczne tlenki/wodorotlenki; słabo rozp. Kwasy… - niestandardowe CO 32 - + Ba. SO 4 Ba. CO 3 + SO 42 p. Ks 10 p. Ks 8. 4 w roztworze ? ! Ba. CO 3 + 2 H+ → Ba 2+ + CO 2↑ + H 2 O K 2 CO 3 + Ba. SO 4 → Ba. CO 3 + K 2 SO 4 K 2 CO 3 + Mg. Si. O 3 → Mg. CO 3 + K 2 Si. O 3 4 KOH + Zn. Si. O 3 → K 2 Zn. O 2 + K 2 Si. O 3 + 2 H 2 O NIE w roztworze ! - stapianie z Na 2 CO 3 /K 2 CO 3 z KOH

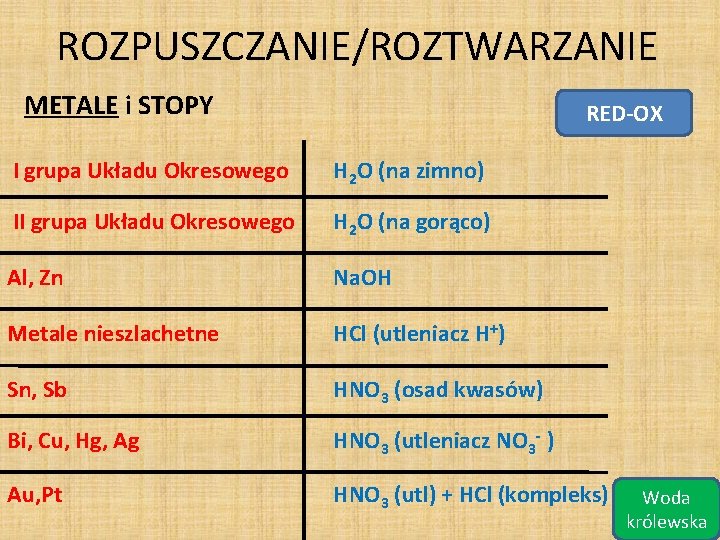
ROZPUSZCZANIE/ROZTWARZANIE METALE i STOPY RED-OX I grupa Układu Okresowego H 2 O (na zimno) II grupa Układu Okresowego H 2 O (na gorąco) Al, Zn Na. OH Metale nieszlachetne HCl (utleniacz H+) Sn, Sb HNO 3 (osad kwasów) Bi, Cu, Hg, Ag HNO 3 (utleniacz NO 3 - ) Au, Pt HNO 3 (utl) + HCl (kompleks) Woda królewska

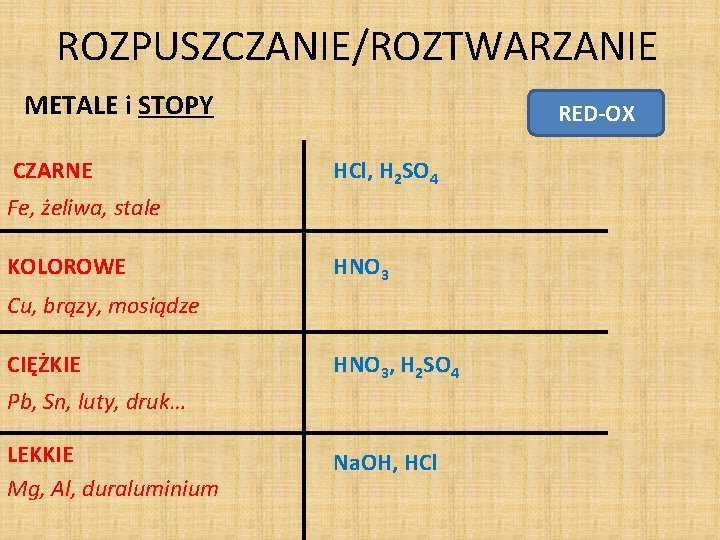
ROZPUSZCZANIE/ROZTWARZANIE METALE i STOPY CZARNE RED-OX HCl, H 2 SO 4 Fe, żeliwa, stale KOLOROWE HNO 3 Cu, brązy, mosiądze CIĘŻKIE HNO 3, H 2 SO 4 Pb, Sn, luty, druk… LEKKIE Mg, Al, duraluminium Na. OH, HCl

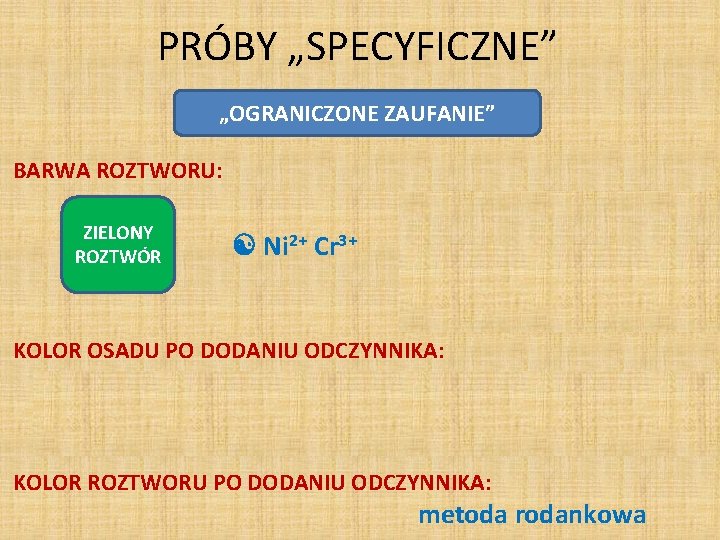
PRÓBY „SPECYFICZNE” „OGRANICZONE ZAUFANIE” BARWA ROZTWORU: ZIELONY ROZTWÓR Ni 2+ Cr 3+ ale może Cu 2+ + Fe 3+ może Cu 2+ + Co 2+ a bezbarwne? KOLOR OSADU PO DODANIU ODCZYNNIKA: Ag+ Cl-, Br-, I-, Cr. O 42 - a te co się nie strąciły? KOLOR ROZTWORU PO DODANIU ODCZYNNIKA: metoda rodankowa

METODA RODANKOWA / Fe Fe 3+ + n SCN- Fe. SCN 2+ + … Fe(SCN)63 - SPECYFICZNA (coraz bardziej) CZERWONA BARWA Fe(SCN)n; lgβ 2 -6 5 Dużo SCN- (20%), aceton Fe(OH)n; lgβ 2 20 Fe(OH)3 ; p. Ks 38 HSCN; p. Ka 1 Fe 3+ + H 2 O Fe. OH 2+ + H+ SCN- + H+ HSCN p. H < 3 p. H > 0

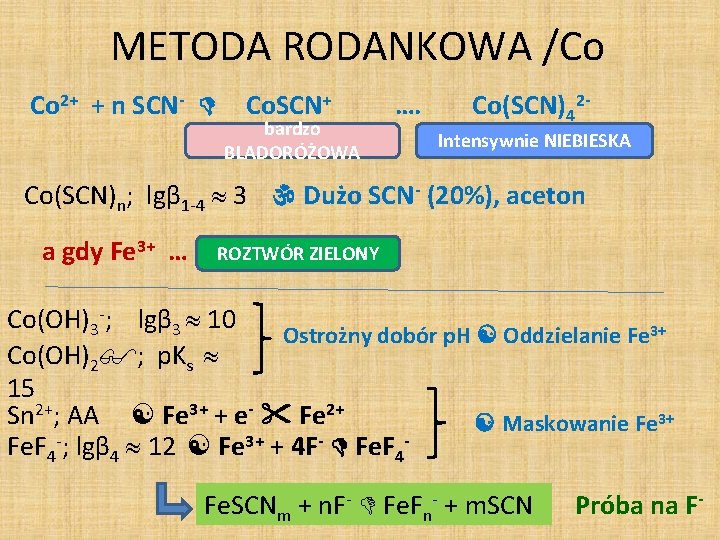
METODA RODANKOWA /Co Co 2+ + n SCN- Co. SCN+ bardzo BLADORÓŻOWA …. Co(SCN)42 Intensywnie NIEBIESKA Co(SCN)n; lgβ 1 -4 3 Dużo SCN- (20%), aceton a gdy Fe 3+ … ROZTWÓR ZIELONY Co(OH)3 -; lgβ 3 10 Ostrożny dobór p. H Oddzielanie Fe 3+ Co(OH)2 ; p. Ks 15 Sn 2+; AA Fe 3+ + e- Fe 2+ Maskowanie Fe 3+ Fe. F 4 -; lgβ 4 12 Fe 3+ + 4 F- Fe. F 4 Fe. SCNm + n. F- Fe. Fn- + m. SCN Próba na F-

… praktyka … nadkrycia/niedokrycia • cierpliwość + obserwacja • ślepe próby • ograniczone zaufanie / alternatywna weryfikacja • „próbka ze ślepą próbą”