Pacetale hemiacetale i acetale budowa mechanizm reakcji przykady

Półacetale – hemiacetale i acetale - budowa - mechanizm reakcji - przykłady (formy cykliczne glukozy i fruktozy)
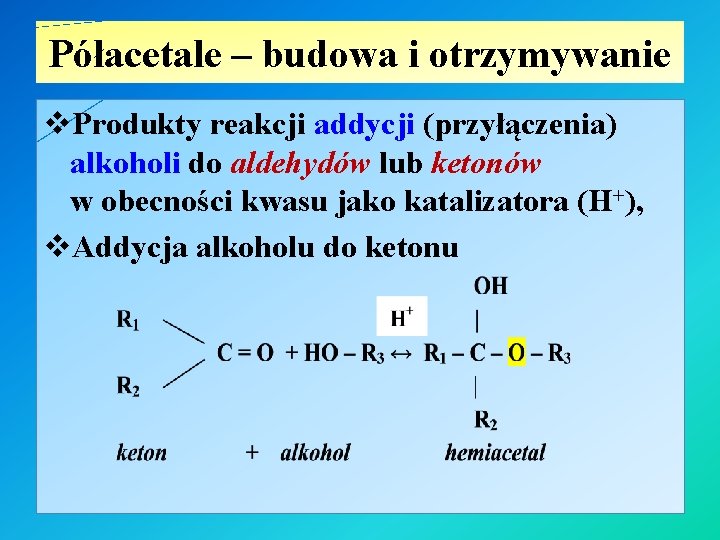
Półacetale – budowa i otrzymywanie v. Produkty reakcji addycji (przyłączenia) alkoholi do aldehydów lub ketonów w obecności kwasu jako katalizatora (H+), v. Addycja alkoholu do ketonu
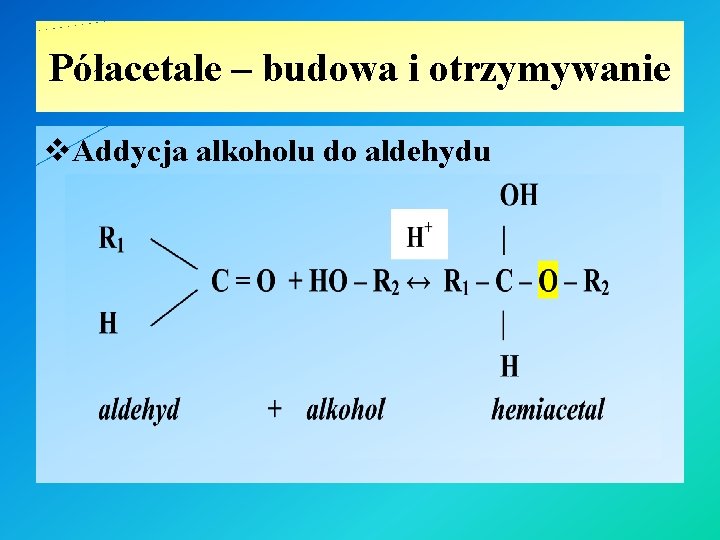
Półacetale – budowa i otrzymywanie v. Addycja alkoholu do aldehydu
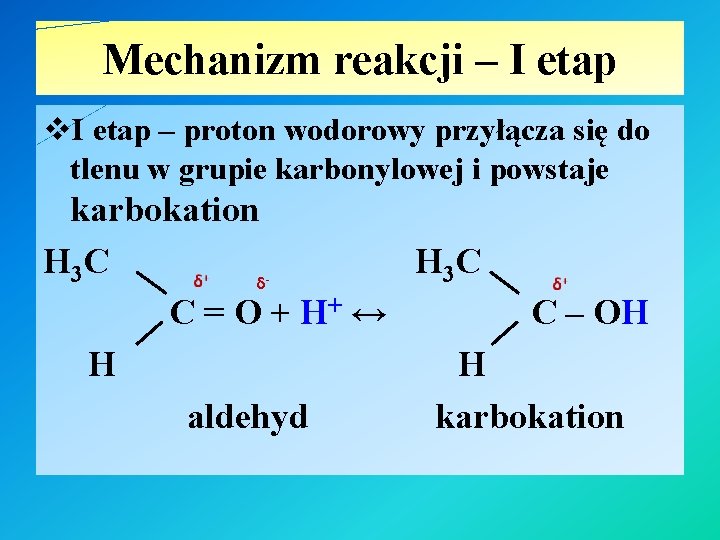
Mechanizm reakcji – I etap v. I etap – proton wodorowy przyłącza się do tlenu w grupie karbonylowej i powstaje karbokation H 3 C H C 3 δ C = O + H+ ↔ C – OH H H aldehyd karbokation -
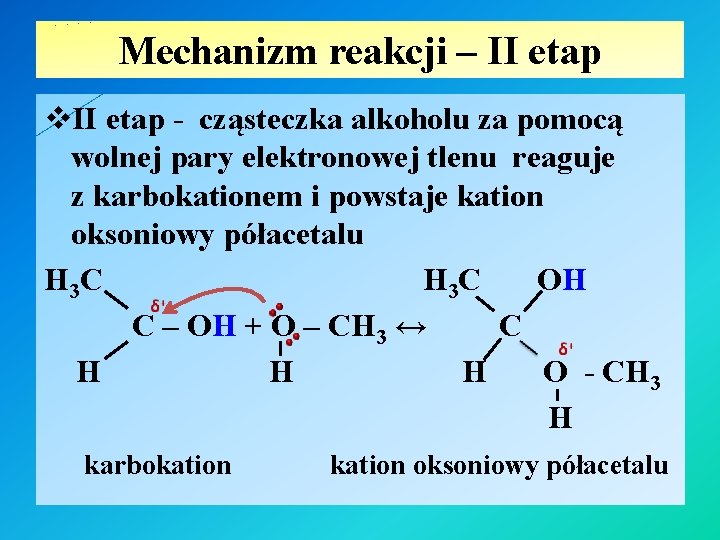
Mechanizm reakcji – II etap v. II etap - cząsteczka alkoholu za pomocą wolnej pary elektronowej tlenu reaguje z karbokationem i powstaje kation oksoniowy półacetalu H 3 C OH C – OH + O – CH 3 ↔ C H H H O - CH 3 H karbokation oksoniowy półacetalu
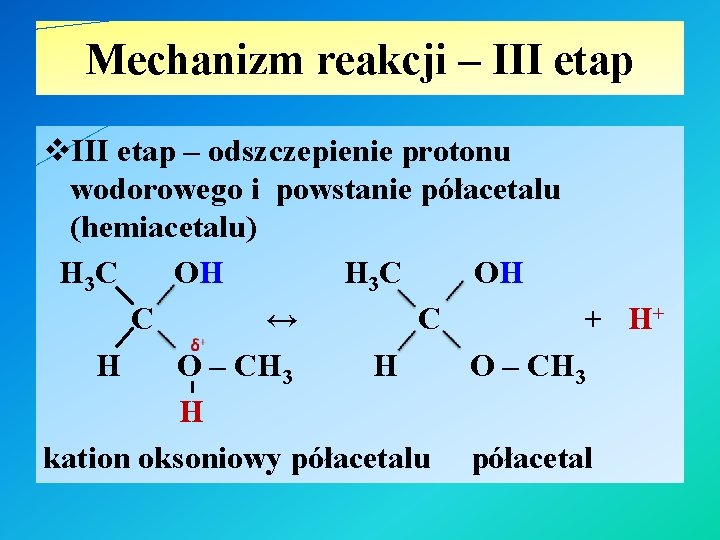
Mechanizm reakcji – III etap v. III etap – odszczepienie protonu wodorowego i powstanie półacetalu (hemiacetalu) H 3 C OH C ↔ C + H+ H O – CH 3 H kation oksoniowy półacetalu półacetal
Hemiacetal cykliczny w obrębie cząsteczki – glukozy vglukoza (aldoheksoza): Ø wiązanie powstaje między grupą – OH na 5 lokancie i grupą – CHO (lokant 1) cukier ten występuje głównie w formie cyklicznej – hemiacetal: ü α-D-(+)-glukopiranoza ü lub β-D-(+)-glukopiranoza
Hemiacetal cykliczny w obrębie cząsteczki – glukozy vglukoza (aldoheksoza): Ø wiązanie powstaje między grupą – OH na 5 lokancie i grupą – CHO (lokant 1) cukier ten występuje głównie w formie cyklicznej – hemiacetal: ü α-D-(+)-glukopiranoza ü lub β-D-(+)-glukopiranoza
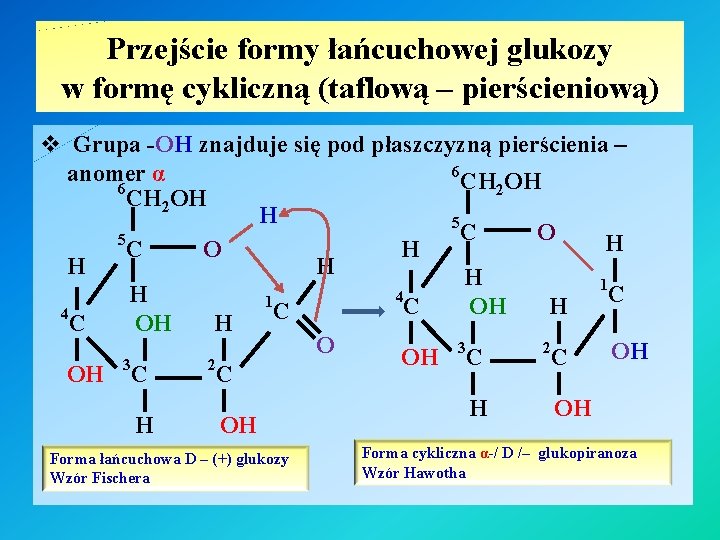
Przejście formy łańcuchowej glukozy w formę cykliczną (taflową – pierścieniową) v Grupa -OH znajduje się pod płaszczyzną pierścienia – 6 anomer α CH 2 OH 6 CH 2 OH H 5 C O 5 H C O H H 1 4 H C 1 C OH H 4 C C OH H 3 2 O OH OH C C 3 2 OH C C H OH Forma łańcuchowa D – (+) glukozy Wzór Fischera Forma cykliczna α-/ D /– glukopiranoza Wzór Hawotha
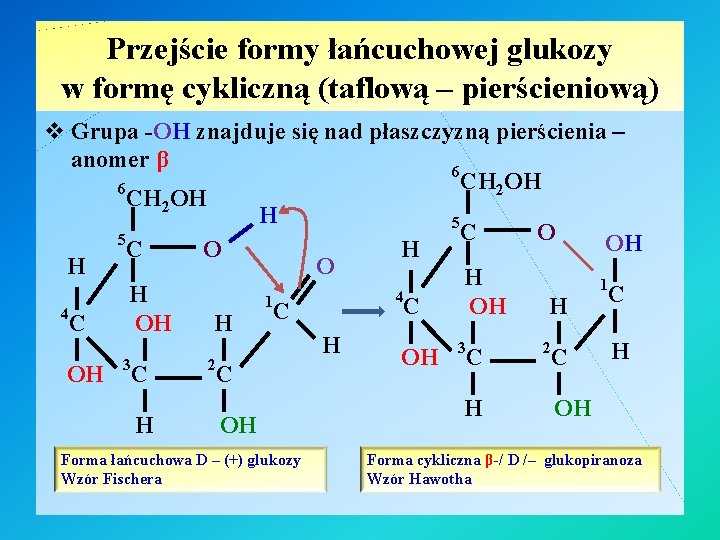
Przejście formy łańcuchowej glukozy w formę cykliczną (taflową – pierścieniową) v Grupa -OH znajduje się nad płaszczyzną pierścienia – anomer β 6 CH 2 OH H 5 C O 5 OH C O H H O H 1 4 H C 1 C OH H 4 C C OH H 3 2 H H OH C C 3 2 OH C C H OH Forma łańcuchowa D – (+) glukozy Wzór Fischera Forma cykliczna β-/ D /– glukopiranoza Wzór Hawotha
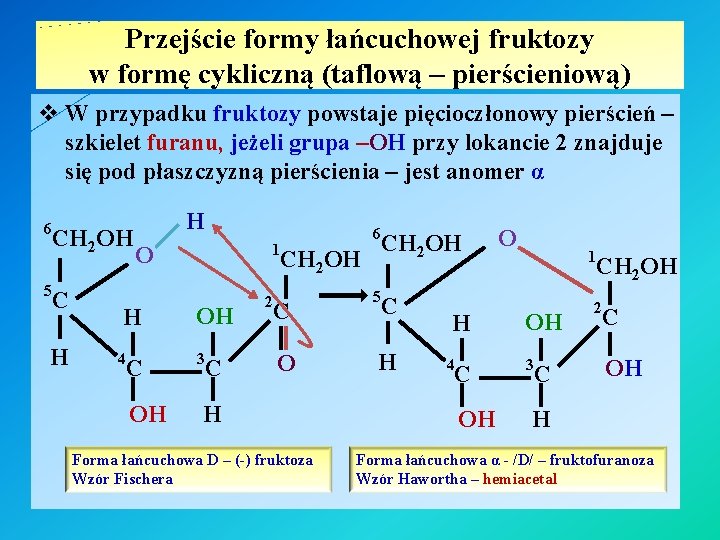
Przejście formy łańcuchowej fruktozy w formę cykliczną (taflową – pierścieniową) v W przypadku fruktozy powstaje pięcioczłonowy pierścień – szkielet furanu, jeżeli grupa –OH przy lokancie 2 znajduje się pod płaszczyzną pierścienia – jest anomer α H CH 2 OH 1 O CH 2 OH 5 H H 4 C OH HO C 6 3 C 2 C O H Forma łańcuchowa D – (-) fruktoza Wzór Fischera CH 2 OH O 1 CH 2 OH 5 C H H 4 C OH HO 6 3 C 2 C OH H Forma łańcuchowa α - /D/ – fruktofuranoza Wzór Hawortha – hemiacetal
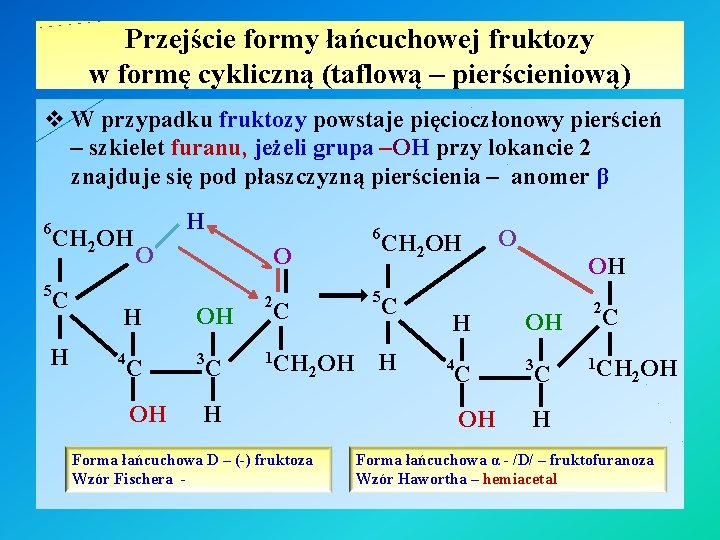
Przejście formy łańcuchowej fruktozy w formę cykliczną (taflową – pierścieniową) v W przypadku fruktozy powstaje pięcioczłonowy pierścień – szkielet furanu, jeżeli grupa –OH przy lokancie 2 znajduje się pod płaszczyzną pierścienia – anomer β H CH 2 OH O 4 C OH HO H H CH 2 OH O 5 C 6 3 C OH 5 C 2 C 1 CH O 2 OH H Forma łańcuchowa D – (-) fruktoza Wzór Fischera - H H 4 C OH HO 6 3 C 2 C 1 CH 2 OH H Forma łańcuchowa α - /D/ – fruktofuranoza Wzór Hawortha – hemiacetal

Mechanizm powstawania acetali v Acetale związki organiczne posiadające dwie grypy eterowe ( etery R 1 – O – R 2) przyłączone do tego samego atomu węgla. v Acetale powstają w wyniku kondensacji hemiacetalu (półacetalu - jedna grupa eterowa – OR i jedna grupa hydroksylowa – OH ) i alkoholu w obecności H+ (środowisku kwasowym). v Acetale są trwałe w środowisku zasadowym, w środowisku kwasowym acetale hydrolizują do hemiacetali, a te z kolei do aldehydu / ketonu i alkoholu.
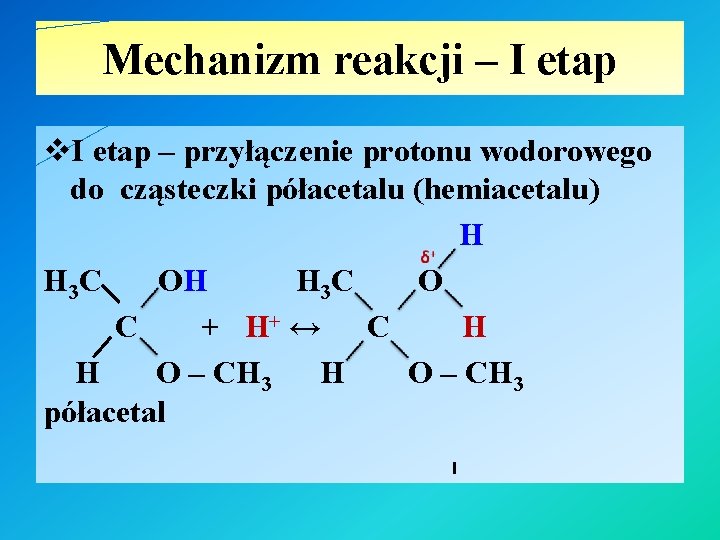
Mechanizm reakcji – I etap v. I etap – przyłączenie protonu wodorowego do cząsteczki półacetalu (hemiacetalu) H H 3 C O C + H+ ↔ C H H O – CH 3 półacetal
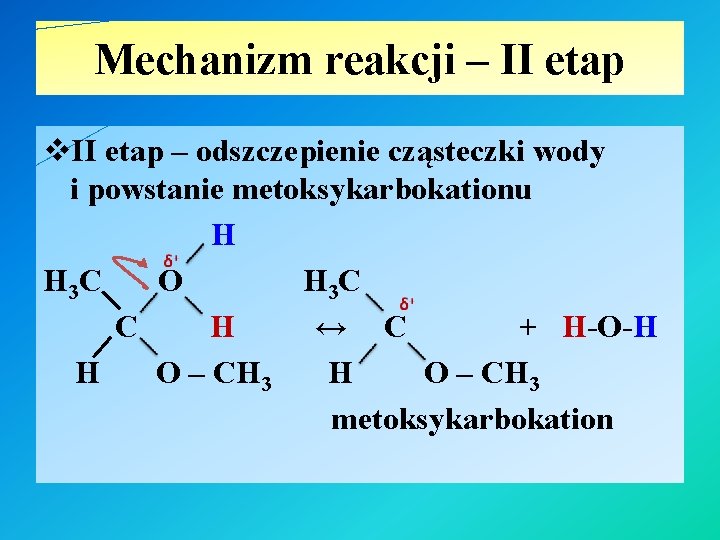
Mechanizm reakcji – II etap v. II etap – odszczepienie cząsteczki wody i powstanie metoksykarbokationu H H 3 C O H 3 C C H ↔ C + H-O-H H O – CH 3 metoksykarbokation
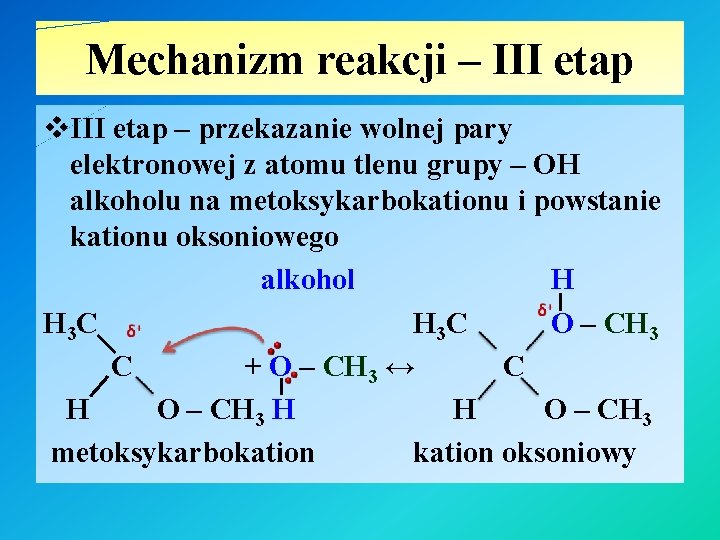
Mechanizm reakcji – III etap v. III etap – przekazanie wolnej pary elektronowej z atomu tlenu grupy – OH alkoholu na metoksykarbokationu i powstanie kationu oksoniowego alkohol H H 3 C O – CH 3 C + O – CH 3 ↔ C H O – CH 3 H H O – CH 3 metoksykarbokation oksoniowy
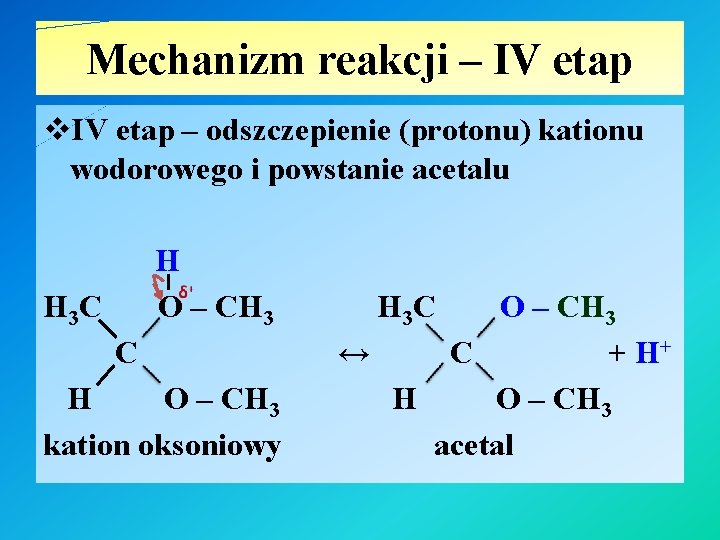
Mechanizm reakcji – IV etap v. IV etap – odszczepienie (protonu) kationu wodorowego i powstanie acetalu H O – CH 3 H 3 C C H O – CH 3 kation oksoniowy H 3 C O – CH 3 ↔ C + H+ H O – CH 3 acetal
- Slides: 17