Metabolizam ugljenih hidrata Varenje i razgradnja ugljenih hidrata

Metabolizam ugljenih hidrata Varenje i razgradnja ugljenih hidrata

Varenje �Varenje je niz hemijskih procesa razgradnje makromolekula skroba, proteina i lipida �Varenje se 3 obavlja u sistemu organa za varenje- digestivni trakt �Prolaskom hrane kroz digestrivni trakt makromolekuli podležu uticaju sokova za varenje koji, sa izuzetkom žuči, predstavljaju vodeni rastvor enzima �Neki nepromenjeni sastojci hrane ili degradacioni proizvodi odstranjuju se organima za izlučivanje

Varenje ugljenih hidrata �U hrani se nalaze uglavnom ugljeni hidrati biljnog porekla: skrob, celulozai disaharidi, i u manjim količinama životinjskog porekla: glikogen �Više od 50% UH je skrob �Može sadržavati i monosaharide : glukozu i fruktozu �Varenje počinje u ustima dejstvom enzima α- amilaze iz pljuvačke koja hidrolizuju α (1 → 4) glikozidnu vezu

Varenje ugljenih hidrata �Dalje se razgrađuju u tankom crevu dejstvom amilaze iz pankreasa �Pošto α-amilaza hidrolizuje samo α (1 → 4) glikozidnu vezu, to se razgrađuje potpuno amiloza, a amilopektin do mesta račvanja α (1 → 6)

Varenje ugljenih hidrata �Iz amilo pektina nastaju dekstrini koji sadrže α (1 → 6) glikozidnu vezu �Ove veze se hidrolozuju posebnim enzimom α (1 → 6) glukozidaze �Kao krajnji proizvodi hidrolize skroba nastaju maltoza i glukoza �Maltoza i drugi disaharidi se razlažu dejstvom enzima disaharidaza ( svaki ima svoj specifični enzim)

Varenje ugljenih hidrata �Varenjem hrane nastaje više vrsta monosaharida, a u crevnom traktu apsorbuju se samo glukoza, fruktoza i galaktoza. �Glukoza je najvažniji monosaharid koji nastaje varenjem �Hranom se unosi i celuloza koju čovek ne može da vari jer nema enzim za razlaganje β(1 → 4) glikozidne veze, tako da ona prolazi kroz digestivni trakt nepromenjena

Varenje ugljenih hidrata �U crevnom epitelu apsorbovana glukoza se prenosi krvlju do ćelija, a posebno do ćelija jetre �Hormon insulin ubrzava prolaz glukoze u ćelije �U većini ćelija se glukoza procesom glikolize razgrađuje do pirogrožđane kiseline (PGA) i acetil Co. A uz oslobađanje male količine energije. �acetil Co. A stupa u ciklus limunske kiseline kojim se obezbeđuje veća količina energije

Višak - manjak �Ukoliko ima viška glukoze u ćeliji ugrađuje se u glikogen – GLUKOGENEZA �Nedostatak glukoze nadoknađuje se hidrolizom glikogena – GLIKOGENOLIZA ili sintezom iz drugih jedinjenja- GLUKONEOGENEZA

Uloga jetre �U metabolizmu ugljenih hidrata jetra ima važnu ulogu �To je organ sinteze i služi kao “depo” (skladište) �Količina glukoze u krvi se vrlo tačno reguliše hormonima �Ti hormoni deluju najčešće u jetri koja, kao izvršni organ, izgrađuje glikogen , ako postoji višak UH i time stvara rezervu �Iz rezerve se pri akutnom nedostatku, glukoza opet stvara i predaje u krv �To je olakšano time što su ćelije jetre potpuno permeabilne( propustljive) za glukozu �U ostalim ćelijama peremeabilnost glukoze reguliše insulin �Tako se dobija neprestano pretvaranje između glikogena i slobodne glukoze �Drugi važan zadatak jetre je sinteza glukoze iz laktata (mišići) tako i iz proizvoda razgradnje proteina

Glikoliza: anaerobna oksidacija �Proces glikolize koji se odvija u citosolu, obuhvata razgradnju glukoze preko piruvata do laktata u anaerobnim uslovima, a realizuje se u dve faze �A - faza glikolize u kojoj se razgradnja glukoze odvija preko niza intermedijera i uz učešće više enzima do gliceraldehid- 3 -fosfata i � B - faza glikolize u kojoj se produžava razgradnja glukoze od gliceraldehid-3 -fosfata do laktata.

Glikoliza �Glikoliza je početna faza razgradnje glukoze i zajednička je praktično svim ćelijama. �Glikoliza se odigrava u odsutnosti kiseonika pa anaerobnim organizmima može osigurati svu potrebnu metaboličku energiju. �U aerobnim ćelijama glikoliza je prva faza razgradnje glukoze.

Razgradnja glukoze �Reakcije glikolize razgrađuju glukozu do pirogrožđane kiseline uz oslobađanje dva molekula ATP-a. �Početne reakcije na glikolitičkom putu u stvari troše energiju u vidu molekula ATP za fosforilaciju glukoze do glukozo-6 -fosfata i zatim fruktoze-fosfata do fruktozo-1, 6 bisfosfata. �Enzimi koji kataliziraju ove dve reakcije, heksokinaza i fosfofruktokinaza, važne su regulacijske tačke glikolitičkog puta. �Ključna je fosfofruktokinaza, koju inhibira visoki nivo ATP. Inhibicija fosfofruktokinaze izaziva nagomilavanje glukoza -6 -fosfata, koji tada inhibira heksokinazu. �Na taj se način koči razgradnja glukoze kad ćelija ima dovoljno raspoložive metaboličke energije u obliku ATP.
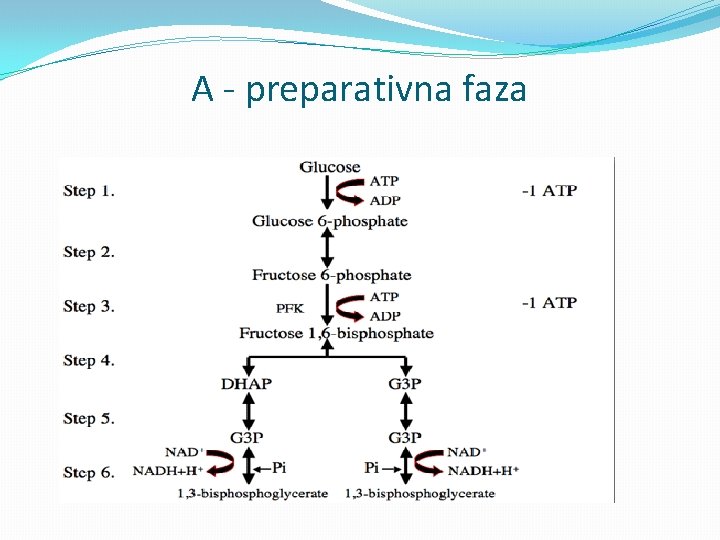
A - preparativna faza

Proizvodnja ATP-a �Reakcije koje dolaze posle stvaranja fruktozo-1, 6 -bisfosfata pripadaju delu glikolitičkog puta kojim se proizvodi energija. �Raspadom fruktozo-1, 6 -bisfosfata nastaju dva molekula šećera s tri ugljenikova atoma. Gliceraldehid-3 -fosfat se oksidiše u 1, 3 -bisfosfoglicerat. �Fosfatna grupa tog jedinjenja ima vrlo veliku slobodnu energiju hidrolize pa se koristi u sledećoj reakciji glikolize za pokretanje sinteze ATP iz ADP. �Produkt te reakcije, 3 -fosfoglicerat, prevodi se zatim u fosfoenolpiruvat, drugi visoko-energijski intermedijar u glikolizi.
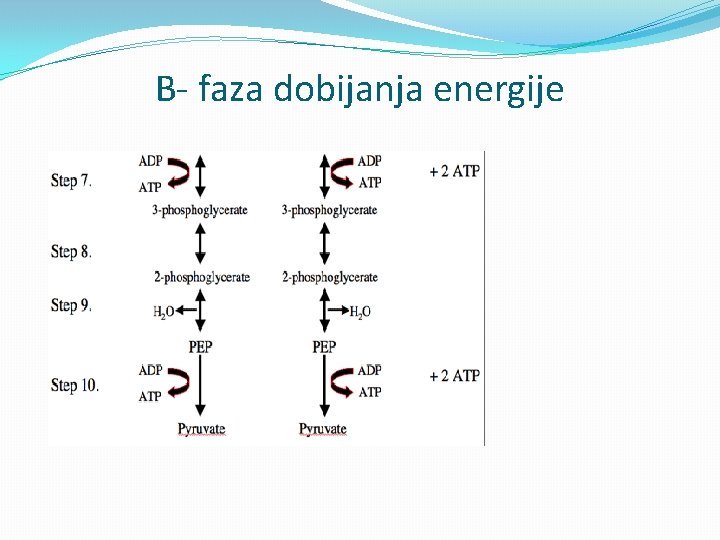
B- faza dobijanja energije

Energetski bilans glikolize �Hidroliza visokoenergijskog fosfata u fosfoenolpiruvatu teče pa se konverzija fosfoenolpiruvata u piruvat povezuje sa sintezom ATP. �Svaki molekul gliceraldehid-3 -fosfata, koja se prevede u piruvat, povezan je s proizvodnjom dva molekula ATP. �Od početnog molekula glukoze ukupno se sintetiše četiri molekula ATP. �Pošto su dva molekula ATP bila potrebna za otpočinjanje prvih reakcija, čist dobitak od glikolize su dva molekula ATP.

Energetski bilans glikolize �Pretvaranje glukoze u piruvat tokom glikolize nastaju dva molekula ATP-a �Glukoza + 2 Pi + 2 ADP + 2 NAD+ → 2 piruvat + 2 ATP + 2 NADH + 2 H+ + 2 H 2 O

Stvaranje redukovanog NADH �Pored proizvedenog ATP, glikoliza pretvara dva molekula koenzima NAD+ u NADH. � U toj reakciji NAD+ deluje kao oksidacijsko sredstvo koje prima elektrone od gliceraldehid-3 -fosfata. �NADH, nastali produkt te reakcije, obnavlja, i služi kao donor elektrona u drugim oksido-redukcijskim reakcijama u ćeliji. �U anaerobnim uslovima konverzijom piruvata u laktat ili etanol reoksidiše se NADH nastao glikolizom u NAD+. �U aerobnim organizmima NADH služi kao dodatni izvor energije dajući svoje elektrone transportnom lancu elektrona putem kojeg će na kraju poslužiti za redukciju O 2 u H 2 O uz povezano stvaranje dodatnog ATP.

Sledeći korak u metabolizmu �Sledeći korak u metabolizmu pirogrožđane kiseline njegova oksidativna dekarboksilacija u prisutnosti koenzima A (Co. A) koji služi kao nosač acilnih grupa u različitim metaboličkim reakcijama. �Jedan se ugljenik piruvata oslobodi kao CO 2, a preostala dva ugljenika predaju se koenzimu A pa nastaje acetil-Co. A. � U tom se procesu redukuju molekuli NAD+ u NADH. �Acetil-Co. A nastao ovom reakcijom ulazi u ciklus limunske kiseline ili Krebsov ciklus koji je središnji put oksidativnog metabolizma.
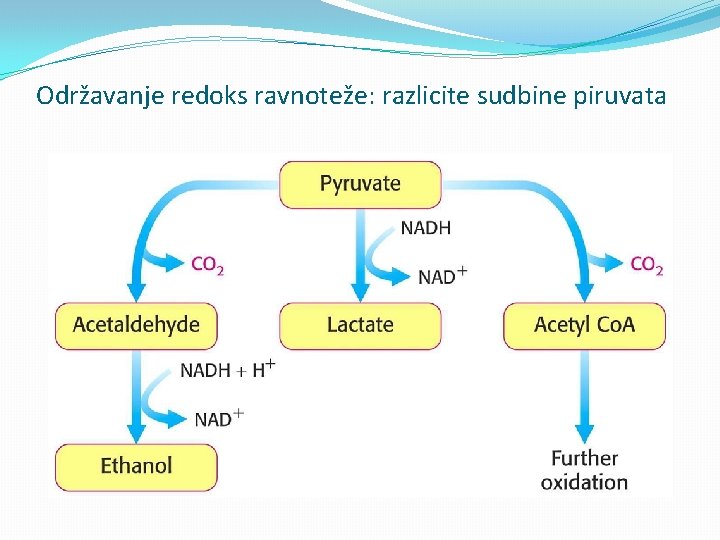
Održavanje redoks ravnoteže: razlicite sudbine piruvata


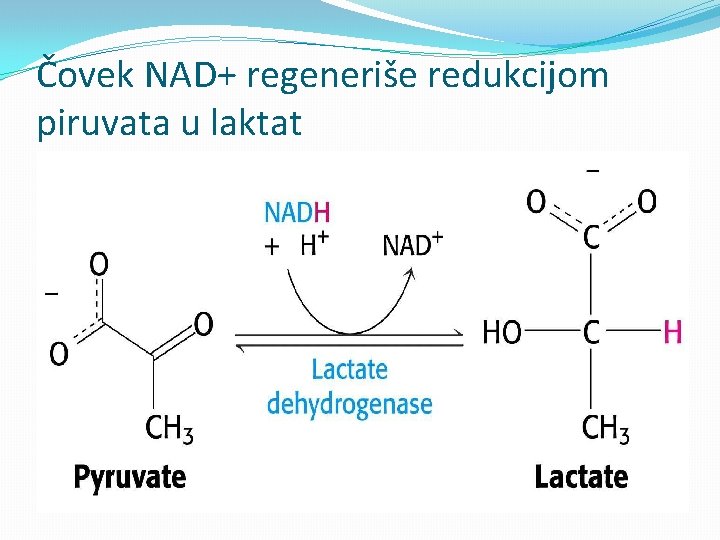
Čovek NAD+ regeneriše redukcijom piruvata u laktat

Kontrola glikolize �Kvasci i neki drugi mikroorganizmi regeneriraju NAD+ oksidacijom piruvata u etanol �Glikoliza je strogo kontrolisana � Fosfofruktokinaza je kljucni enzim kontrole glikolize


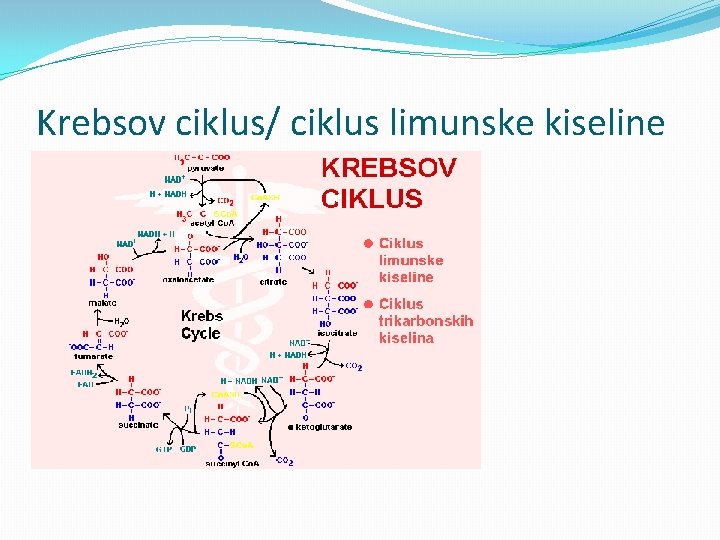
Krebsov ciklus/ ciklus limunske kiseline

CIKLUS LIMUNSKE KISELINE �Faza aerobnog metabolizma usmerena je na potpunu oksidaciju piruvata do krajnjih proizvoda ugljen dioksida i vode. �Ciklus razgradnje piruvata u aerobnim uslovima detaljno je objasnio biohemičar Hans Krebs po kome je ovaj ciklus dobio naziv Krebsov ciklus. Ovaj ciklus naziva se i ciklus trikarbonskih kiselina, jer u toku njegovog odvijanja stvaraju se molekuli kiselina sa tri karboksilne grupe, kao i ciklus limunske kiseline (citratni ciklus, CLK) zbog veoma bitne uloge koju ima citrat u njemu.

CLK � Sam ciklus limunske kiseline ima dvostruku ulogu (amfibolična uloga), jer se u njemu susreću reakcije razgradnje (katobolizam) i reakcije sinteze (anabolizam). � Oksidativnom dekarboksilacijom piruvata uz učešće multienzimskog (PDH) kompleksa sastavljenog od tri enzima i prisutnog Co. A-SH nastaje acetil-S-Co. A. � Nastali acetil-S-Co. A predstavlja “aktivirani acetat”, koji se uključivanjem u ciklus limunske kiseline, razgrađuje do krajnjih proizvoda CO 2 i H 2 O. � CLK praktično predstavlja stecište krajnjeg metabolizma i drugih organskih jedinjenja, a to su pre svih, pored ugljenih hidrata, aminokiseline i masne kiseline. � U ciklusu limunske kiseline na svaki uključeni molekul acetil-S-Co. A nastaju 2 molekula CO 2 uz oslobadjanje elektrona i H+. Akceptori elektrona i H+ u toku skoro svih reakcionih faza CLK su NAD+ i FAD , koji prelaze u NADH i FADH 2.

CLK �Tokom svakog ciklusa limunske kiseline nastaju: 2 molekula GTP, 6 molekula NADH i 2 molekula FADH 2 � Sa uključenjem 2 molekula acetil-S-Co. A (jedan molekul glukoze daje 2 molekula acetil-S-Co. A). �Oksidacijom svakog molekula NADH nastaju 3 molekula energijom bogatog ATP, i još dva molekula ATP pri formiranju svakog FADH 2. �Na ovaj način svaki razgradjeni molekul glukoze daje ukupno 36 molekula ATP. (GTP je ekvivalentan ATP).




Aktivacija piruvata � Pirogroždjana kiselina - (odn. piruvat) dobijen glikolizom u citosolu transportuje se u mitohondrije gde se razlaže do CO 2 i H 2 O u CTK. � Piruvat ne ulazi direktno u ciklus već se prvo oksidativno dekarboksiluje uz učešće enzimskog kompleksa piruvatdehidrogenaze(PDH-kompleks) do stvaranja energijom bogatog tioestarskog jedinjenja acetil-S῀Co. A uz oslobadjanje CO 2 i redukovanog NADH. � Piruvat + NAD+ + Co. A -SH ------> acetil-Co. A + NADH + CO 2 � CH 3 COCOO- +NAD++ Co. A-SH CH 3 CO-S-Co. A + NADH +CO 2

Faze CLK � Ciklus se sastoji iz osam faza: � 1. Formiranje citrata, kondenzacijom Acetil Co. A i oksaloacetata. � 2. Pretvaranje citrata u izocitrat preko cis-akonitata. � 3. Dehidrogenizacija izocitrata i dobijanje α-ketoglutarata i CO 2 � 4. Oksidacija α-ketoglutarata do sukcinil-Co. A i CO 2 � 5. Pretvaranje sukcinil Co. A u sukcinat. � 6. Dehidrogenacija sukcinata u fumarat. � 7. Hidratacija fumarata i formiranje maleata. � 8. Dehidrogenacija maleata i formiranje oksalacetata.

Faza 1 � 1. Formiranje citrata, kondenzacijom Acetil Co. A i okaloacetata. �Proces katališe i reguliše enzim citrat sintaza. U reakciji metilni ugljenik, acetilne grupe iz Acetil-Co. A se kondenzuje sa karbonilnom grupom oksaloacetata; istovremeno tioestarska veza se cepa i oslobađa se slobodni koenzim A. citrat sintaza � Acetil-Co. A + oksaloacetat +H 2 O------->citrat + Co. A-SH + H+ � Co. A-SH dobijen u ovoj reakciji je slobodan i u mogućnosti je da dalje učestvuje u oksidativnoj dekarboksilaciji naredne molekule piruvata da bi se dobio sljedeći molekul acetil Co. A koji ulazi u ciklus.

Faza 2 � 2. Pretvaranje citrata u izocitrat preko cis-akonitata. � Enzim akonitaza katalizira reverzibilno pretvaranje citrata u izoctirat preko intermedijerne formacije trikarboksilnog cis akonitata. � -Obzirom da se izocitrat stalno transformiše u metabolite naredne faze cilkusa, reakcija se u ćelija stalno odvija udesno. Akonitaza je kompleksan enzim koji sadrži gvožđe


Faza 3 � 3. Dehidrogenizacija izocitrata i dobijanje α-ketoglutarata i CO 2 � Uz pomoć enzima izocitrat dehidrogenaze izocitrat dehirogenizira u α-ketogulrat. izocitrat dehidrogenaza � Izocitrat + NAD+ ----> α-ketoglutarat+ CO 2+ NADH + H+ � Enzim treba jone Mg 2+ i Mn 2+.


Faza 4 � 4. Oksidacija α-ketoglutarata do sukcinil-Co. A i CO 2 �U ovoj fazi a-ketoglutarat prolazi oksidatovnu dekarboksilaciju i formira Sukcinil-Co. A i CO 2. Proces katalizira enzimski kompleks a-ketoglutarat dehidrogenaza


Faza 5 � 5. Pretvaranje sukcinil-Co. A u sukcinat. � Sukcinil-Co. A je visokoenergetski metabolit. Velika količina energije se oslobađa pri hidrolizi tioesterske veze. �Sukcinil-S- Co. A + H 2 O ----> Sukcinat+ Co. A-SH + H+ �U ćelijama sukcinil-Co. A ne gubi Co. A grupu prostom hidrolizom tokom koje se troši energija. Umesto toga, podleže vezanoj duploj reakciji, kojom se konzervira energija, a tokom kojih je cepanje tioestarske veze praćeno fosforilacijom guanozin difosfata (GDP) u guanozin trifosfata (GTP).


Faza 6 � 6. Dehidrogenacija sukcinata u fumarat. � Sukcinat, nastao u predhodnom stadijumu iz sukcinil. Co. A, se dehidrogenizuje u fumarat. Proces se katališe uz pomoć enzima sukcinat dehidrogenaze, koji je u kovalentnoj vezi sa FAD, koji ima ulogu akceptora vodonikovog atoma, �Sukcinat + Sukcinatdehidrogenaza-FAD ----> Fumarat + Sukcinatdehidrogen. -FADH 2 �Sukcinat dehidrogenaza je inhibirana od strane malonata, što ima važnu ulogu u regulaciji samog ciklusa.


Faza 7 � 7. Hidratacija fumarata i formiranje maleata. � Reverzibilna reakcija hidratacije fumarata u L-maleat, katalizirana je enzimom fumarat hidratazom, nazvan i fumaraza. Enzim je molekulske težine oko 200. 000 sa četiri polipeptidne subjedinice, bez koenzima i jako je specifičan. Hidratizuje dvostruku trans vezu fumarata, fumaraza i Mg 2+ Fumarat + H 2 O ---->L-maleat <----

Faza 8 � 8. Dehidrogenacija maleata i formiranje oksalacetata. � Enzim L-maleat dehidrogenaza vezana je za NAD i prisutna je u mitohondrijama, katališe dehidrogenaciju maleata do oksalacetata u zadnjoj reakciji ciklusa limunkse kiseline. L-malat + NAD+ ----> Oxaloacetat + NADH + H+ � Reakcija je reverzibilna, međutim u standardnim uslovima je usmjerena udesno, obzirom da se oksaloacetat, kao produkt ove reakcije, brzo uklanja reakcijom citratne sintaze, te je njegova koncentracija u ćeliji jako mala.


Energetski bilans CLK �Pošto je svaki NADH ekvivalentan 3 ATP, FAD je ekvivalent 2 ATP, a GTP je ekvivalent 1 ATP imamo sledeći ukupan energetski bilans po jednom molekulu glukoze: reakcija Glukoza 2 piruvata CO 2 + H 2 O 2 NADH+ H+ 2 NAD+ Ukupno ATP 2 ATP 30 ATP 4 ATP 36 ATP
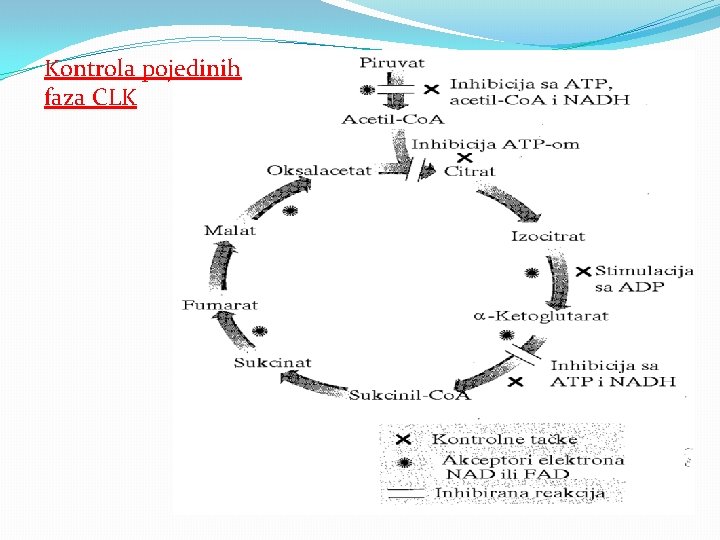
Kontrola pojedinih faza CLK
- Slides: 51