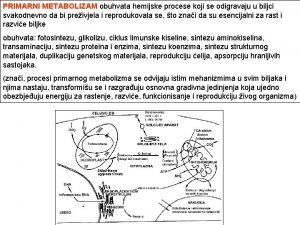
MAVANSKA SREDNJA KOLA METABOLIZAM AMINOKISELINA DEAMINACIJA DEKARBOKSILACIJA TRANSAMINACIJA

MAČVANSKA SREDNJA ŠKOLA METABOLIZAM AMINOKISELINA DEAMINACIJA DEKARBOKSILACIJA TRANSAMINACIJA KLARA KAKUČKA, prof. hemije

PROTEINI • U ishrani životinja, proteini zauzimaju veoma značajno mesto. • Proteolitičkom razgradnjom hranom unetih složenih peptidnih i proteinskih struktura nastaju aminokiseline, koje nakon resorpcije u probavnom traktu, služe za izgradnju mnogih, organizmu neophodnih strukturnih proteina, kao i nekih drugih biološki važnih molekula, kao što su enzimi, hormoni itd

Nastajanja slobodnih aminokiselina • Drugi proces nastajanja slobodnih aminokiselina odvija se kroz razgradnju tkivnih proteina unutar organizma životinja. • Aminokiseline nastale na ovaj način takodje imaju ulogu gradivnih jedinica i učestvuju u biosintezi organizmu potrebnih proteina. • U organizmu su praktično prisutna dva dimanički uravnotežena procesa: proces katabolizma i proces anabolizma.

Razgradnja proteina • Razgradnja proteina vrši se uz katalitičko delovanje enzima proteaza , koje se, prema mestu nalaženja u organizmu životinja, dele na: • - proteaze probavnog trakta, • - ekstracelularne proteaze (nalaze se u krvi i ekstracelularnim tečnostima) i • - intracelularne proteaze (većinom se nalaze u lisozomima).

Proteaze • Prema mestu aktivnog napada na polipeptidnom lancu proteaze se dele na: • - endopeptidaze (cepaju proteine na tačno odredjenim mestima u sredini lanca) i • - egzopeptidaze (cepaju proteinske lance od kraja i to kar boksipep tidaze (deluju na karboksilni kraj) i aminopeptidaze (deluje na N -terminalni deo lanca).

Proteaze • Za razliku od mnogih drugih enzima, proteaze nisu strogo supstrat specifične i ne deluju specifično na odredjene proteine, već su usmerene na odredjene veze i strukturne karakteristike polipeptidnog lanca. • Tako na primer proteaze pepsin) i tripsin katalitički deluju na sve proteine, što je izuzetno značajno u procesima varenja, jer njihovim delovanjem dolazi do denaturacije proteina, koji se lakše hidrolizuju do aminokiselinskih jedinica.



Proteolitički enzimi • • • Peptidaze • Endopeptidaze i egzopeptidaze • Endopeptidaze ili proteaze – Serin proteaze – Cistein proteaze – Aspartat proteaze – Metalo-proteaze • Egzopeptidaze – Karboksipeptidaze – Aminopeptidaze – Dipeptidaze

Uloga proteolitičkih enzima u varenju proteina • • • Varenje u želucu Pepsin Varenje u duodenumu Tripsin Himotripsin Elastaza Karboksipeptidaze A i B Varenje u tankom crevu Endopeptidaze Aminopeptidaze Dipeptidaze Tripsin Himotripsin Elastaza

Varenje u želucu: Pepsini • • Enzim: Pepsin A (karboksil-proteaza) • Proenzim: Pepsinogen A • Aktivatori: – Autoaktivacija (pepsinogen, p. H < 5) – Autokataliza (pepsin) • Specifičnost (R): R 1 R 2 – Phe CO NHCHCO – Tyr
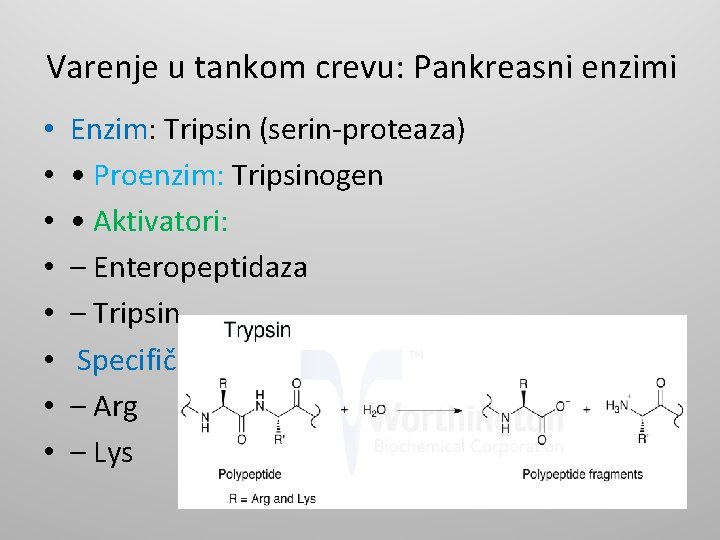
Varenje u tankom crevu: Pankreasni enzimi • • Enzim: Tripsin (serin-proteaza) • Proenzim: Tripsinogen • Aktivatori: – Enteropeptidaza – Tripsin Specifičnost (R): – Arg – Lys

Varenje u tankom crevu • • • Enzim: Himotripsin (serin-proteaza) • Proenzim: Himotripsinogen • Aktivator: – Tripsin • Specifičnost (R): – Tyr, Trp, Phe, Met, Leu • Enzim: Elastaza (serin-proteaza) • Proenzim: Proelastaza • Aktivator: – Tripsin • Specifičnost (R): – Ala, Gly, Ser

Varenje u tankom crevu • • • • Enzim: Karboksipeptidaza A Proenzim: Prokarboksipeptidaza A Aktivator: – Tripsin Specifičnost (R): – Val, Leu, Ile, Ala Enzim: Karboksipeptidaza B Proenzim: Prokarboksipeptidaza B Aktivator: – Tripsin Specifičnost (R): – Arg, Lys

Varenje u tankom crevu • Endopeptidaze • – Endopeptidaza 24. 11 (hidrofobne aminokiseline) • Aminopeptidaze • – Aminopeptidaza A (kisele aminokiseline) • – Aminopeptidaza N (neutralne aminokiseline) • – Leucin-aminopeptidaza • Dipeptidaze

Neaktivni prekursor- zimogen • Veći broj proteolitičkih enzima probavnog trakta nastaje u ćelijama želuca ili pankreasa i to prvo u vidu neaktivnih prekursora zimogena. • Zimogeni imaju duži proteinski lanac od enzima, pa se tek proteolitičkim cepanjem tog lanca na tačno odredjenom mestu stvara mogućnost formiranja aktivnog enzimskog centra, odnosno nastajanje aktivnih proteaza. • Na ovaj način od pepsinogena nastaje pepsin , od tripsinogena tripsin , od himotripsinogena himotripsin itd.

Metabolički putevi AK • Aminokiseline nastale proteolitičkom razgradnjom proteinskih i peptidnih lanaca imaju različite metaboličke puteve. • Tako na primer aminokiseline učestvuju : • - u izgradnji novih proteinskih struktura u tkivima životinja , • - kao metabolički intermedijeri u biosintetskim reakcijama , pri stvaranju razgradnih aminokiselinskih medjuproizvoda , itd.

Metabolički putevi AK • Ovako nastale jedinice učestvuju u biosintezi ugljenih hidrata (glukoze i glikogena ako potiču iz glukogenih aminokiselina) i masnih kiselina preko aceto S - Co. A i acetoacetil - S - Co. A (ako potiču iz ketogenih aminokiselina). • Aminogrupa, odnosno amonijak izdvojen iz aminokiselina, praktično se prevodi u oblik uree (kod sisara), mokraćne kiseline, odnosno njenih soli urata (kod ptica, gmizavca i vodozemaca) ili glutaminsku i alaninsku formu, koje predstavljaju transportni oblik amonijaka putem krvotoka.

Razgradnja aminokiselina • Aminokiseline se u organizmu životinja uglavnom razgrađuju reakcijama deaminacije i dekarboksilacije, kao i procesom konačne razgradnje tako nastalih medjuproizvoda, do CO 2 i H 2 O. • Treći tip reakcija, koje su prisutne u pojedinim fazama razgradnje aminokiselina, su reakcije transaminacije. • U toku odvijanja ovih reakcija dolazi do prenošenja aminogrupe sa jedne aminokiseline (npr. alanina) na ketokiselinu (npr. -ketoglutarat) pri čemu nastaje druga aminokiselina (glutamat).

Deaminacija aminokiselina • U reakcijama deaminacije azot, koji je vezan u obliku -aminogrupe, se oslobađa u obliku amonijaka. • Imajući u vidu da je amonijak i u malim koncentracijama veoma jak ćelijski otrov, organizam ga posebnim metaboličkim procesima prevodi u oblik koji se potom jednostavno uklanja, pri čemu se na ovaj način detoksikuje.

Deaminacija aminokiselina • Oksidativna deaminacija - odvija se uz katalitičko delovanje dehidrogenaza, koje najčešće sadrže kao koenzimsku grupu FAD. • Proces deaminacije počinje dehidrogenovanjem pri čemu nastaje iminokiselina, koja u sledećoj reakcionoj fazi daje -ketokiselinu i amonijak. • Vodonik koji se izdvaja iz aminokiseline završava u respiratornom lancu gde sa kiseonikom daje konačan proizvod vodu. • U mitohondrijama svih tkiva nalazi se enzim glutamat dehidrogenaza (GDH), koja prenosi vodonik na NAD+ prema reakciji : • Glutamat + NAD+ GDH α-ketoglutarat + NADH + NH 4+

Dekarboksilacija • Drugi reakcioni put razgradnje aminokiselina predstavlja dekarboksilacija pri kojoj uz izdvajanje ugljendioksida iz aminokiseline nastaje primarni amin, čija se strukturna formula izvodi iz formule dekarboksilovane aminokiseline. • Ovako nastali amini nazivaju se biogeni amini i imaju izrazito farmakološko delovanje, a učestvuju i kao značajni prekursori hormona, koenzima i drugih biološki važnih molekula. • Histamin koji nastaje dekarboksilacijom histidina, u prisustvu enzima histidin dekarboksilaze pored ostalih efekata, utiče stimulatorno na lučenje želudačnog soka

Transaminacija aminokiselina • Transaminacija predstavlja reakcioni put u toku koga dolazi do prenosa aminogrupe sa jedne aminokiseline na ketokiselinu pri čemu dolazi do nastajanja neesencijalne aminokiseline. • Samim tim ne dolazi do izdvajanja slobodnog amonijaka Ovim procesom praktično se povećava količina neesencijalnih aminokiselina u organizmu koje intenziviraju biosintezu proteina. • U procesu transaminacije glutamat predstavlja osnovnog donora aminogrupe, dok se ketoglutarat pojavljuje kao glavni akceptor amino grupe. • Enzimi koji katalizuju reakcije transaminacije najčešće imaju kao koenzimsku grupu piridoksalfosfat čija aldehidna grupa ima veoma bitnu ulogu u procesu prenosa aminogrupe.
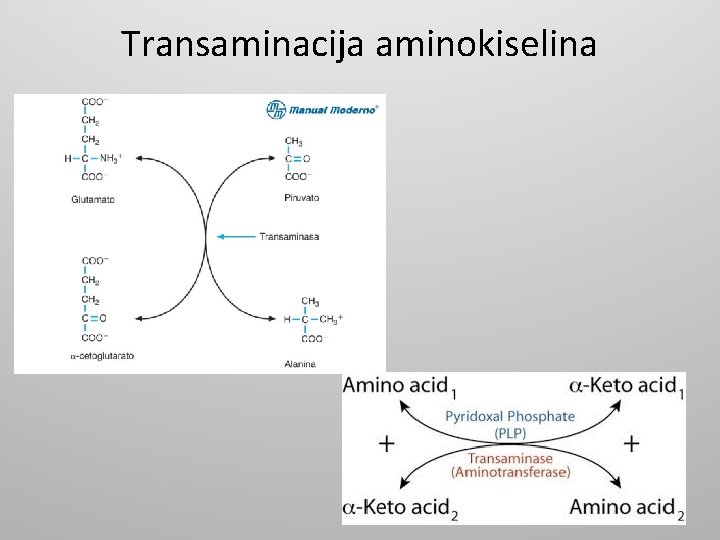
Transaminacija aminokiselina
- Slides: 24