Lenergia laltra faccia della materia Energia Attitudine a
























- Slides: 26

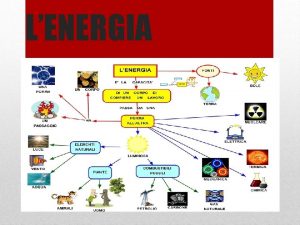
L’energia: l’altra faccia della materia

Energia Ø Ø Attitudine a compiere un lavoro Lavoro – ciò che determina cambiamento o movimento di un oggetto.

Energia l L'energia è la proprietà fondamentale della materia che si esprime ogni volta che: l una forza "entra in azione", o , come si dice in termini fisici, l ogni volta che si compie un lavoro; Ø Ogni trasformazione chimica o fisica richiede energia. Ø L’Energia fa si che le cose avvengano. Ø Si trova dappertutto intorno a noi, nei mezzi di trasporto, nell'industria, nelle case e anche nel nostro corpo.

Può assumere due forme fondamentali : Cinetica - posseduta da un corpo in movimento Potenziale – (energia di accumulo) dipende dalla posizione di un corpo in un campo di forze

En. Cinetica e potenziale

Tipi di energia l l Calore - energia che si trasferisce tra due corpi a differente temperatura. Energia chimica - en. rilasciata o assorbita nelle trasformazioni chimiche (es. Combustione). l En. Elettrica - energia dovuta al movimento di cariche elettriche l Energia Radiante - en. che viaggia nello spazio vuoto (luce, UV, Radiazioni infrarosse, onde radio)

L'energia elettrica l è quella che accende le lampadine e fa funzionare i nostri elettrodomestici

Energia chimica l Definiamo energia chimica quella contenuta nei cibi e nei combustibili e quella che fa funzionare una batteria. l L’energia chimica è contenuta nei legami chimici

Energia termica l L'energia termica o calore è data dal movimento delle molecole all'interno dei corpi che aumenta con l'innalzamento della temperatura.

Energia radiante l L'energia radiante si trasmette nello spazio attraverso le onde elettromagnetiche. Un esempio di questo tipo di energia è quella prodotta dal sole

Energia nucleare l L'energia nucleare è quella immagazzinata nel nucleo degli atomi

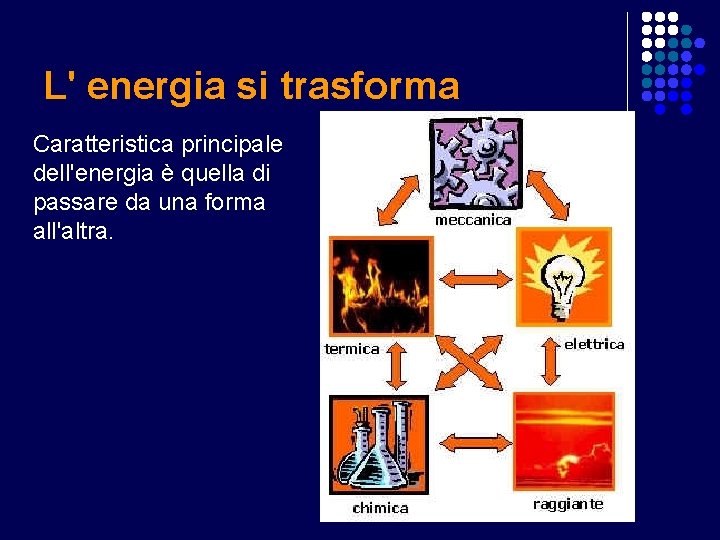
L' energia si trasforma Caratteristica principale dell'energia è quella di passare da una forma all'altra.

e si degrada. . . il passaggio da una forma di energia all'altra non è mai completo; c'è sempre una differenza tra la quantità di energia iniziale e la quantità di energia finale. Tale differenza si ritrova generalmente sotto forma di energia termica, che è una delle forme meno pregiate di energia.

Principio di conservazione dell’energia Ø l’energia non può essere creata né distrutta, Ø ma può solo essere trasformata da una all’altra delle diverse forme in cui si presenta. Nel 1905 Albert Einstein pubblicò la teoria della relatività, dimostrando l’equivalenza tra massa ed energia. E=mc 2

Il Calore l Il calore è un trasferimento di energia fra corpi che si trovano inizialmente a temperature diverse. l Il calore è energia in transito: fluisce sempre dai punti a temperatura maggiore a quelli a temperatura minore, finché non si raggiunge l'equilibrio termico.

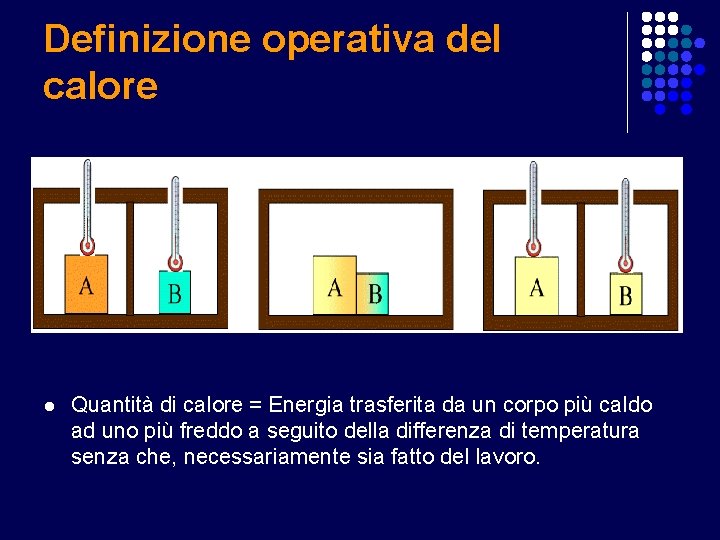
Definizione operativa del calore l Quantità di calore = Energia trasferita da un corpo più caldo ad uno più freddo a seguito della differenza di temperatura senza che, necessariamente sia fatto del lavoro.

La teoria cinetico molecolare Dalla metà dell’ 800 incomincia a svilupparsi la teoria cinetico molecolare, basata sui seguenti principi: l l I corpi materiali sono composti di minuscole particelle dotate di un movimento e quindi di energia cinetica. La temperatura è una misura dell’energia cinetica media delle particelle Modello di un gas

La conduzione del calore La conduzione di calore tra due corpi a contatto è un trasferimento dell'energia cinetica attraverso gli urti tra le particelle, le più veloci cedono parte del loro moto a quelle più lente. Alla fine si raggiunge un equilibrio e le energie cinetiche medie e le temperature dei due corpi sono uguali

Unità di misura l l In quanto energia, il calore si misura nel Sistema Internazionale in Joule. Nella pratica viene tuttavia ancora spesso usata come unità di misura la caloria. Alcune equivalenze: l l l 1 cal = 4, 186 Joule 1 Joule = 0, 2388 cal 1 CAL = 1 kcal = 1000 cal

Calore specifico l Si dice calore specifico di una sostanza: l la quantità di calore necessaria a innalzare di un grado la temperatura dell'unità di massa. l In relazione alle condizioni di riscaldamento si distinguono rispettivamente il calore specifico a volume e a pressione costante. In generale i due calori specifici dipendono dalla temperatura e nel caso dell'acqua e di tutte le sostanze praticamente incomprimibili hanno valori approssimativamente uguali.

Calorimetro Caloria l La caloria (o piccola caloria, simbolo cal) è un'unità di misura dell'energia. l Viene definita come la quantità di energia termica necessaria ad elevare da 14, 5 a 15, 5 °C la massa di un grammo di acqua distillata a livello del mare (pressione di 1 atm).

la temperatura l la temperatura è la proprietà fisica di un sistema corrispondente alle nozioni comuni di "caldo" e "freddo"; Esprime il livello termico di un corpo. I termini temperatura e calore sono quindi correlati, ma si riferiscono a concetti diversi: l la temperatura è una proprietà di un corpo, l mentre il calore è una forma di energia che fluisce da un corpo a un altro, per colmare una differenza di temperatura.

Scale di temperatura l L'unità base della temperatura nel Sistema Internazionale è il grado kelvin (simbolo: K) l In questa scala lo zero assoluto è collocato a -273, 15 °C l Una delle prime scale di temperatura fu ideata nel 1720 dal fisico tedesco Gabriel Daniel Fahrenheit. Nella scala Fahrenheit, alla pressione di 1 atm, la temperatura di congelamento dell'acqua corrisponde al valore di temperatura di 32 °F, mentre al suo punto di ebollizione si attribuisce il valore di 212 °F. Nella scala centigrada, o Celsius, introdotta dall'astronomo svedese Anders Celsius e impiegata nella maggior parte dei paesi, il punto di fusione dell’acqua corrisponde a 0 °C, quello di ebollizione a 100 °C. l l

Formule per convertire le temperature Conversione da a Formula Celsius Fahrenheit °F = °C × 1, 8 + 32 Fahrenheit Celsius °C = (°F − 32) / 1, 8 Celsius kelvin K = °C + 273, 15 kelvin Celsius °C = K − 273, 15

ZERO ASSOLUTO l l l Il valore più basso della scala Kelvin si chiama zero assoluto e corrisponde a -273° C. Secondo i fisici, lo zero assoluto corrisponde alla temperatura più bassa possibile, il limite al disotto del quale non si può scendere perché le molecole sono assolutamente immobili. Nella scala assoluta il ghiaccio fonde a 273 °K e l’acqua bolle a 373 °K.

Strumento di misura l Il termometro è lo strumento per la misura della temperatura, o delle variazioni di temperatura.
 Attitudine a ridursi in lamine sottili
Attitudine a ridursi in lamine sottili Enti primitivi
Enti primitivi E guardiamoci in faccia
E guardiamoci in faccia Si lanciano tre gettoni su una faccia dei quali
Si lanciano tre gettoni su una faccia dei quali Homeostasis
Homeostasis Niveles troficos
Niveles troficos Energia potentiala se poate defini numai pentru forte
Energia potentiala se poate defini numai pentru forte Pabs
Pabs Energia meccanica scuola primaria
Energia meccanica scuola primaria Proprietà macroscopiche della materia
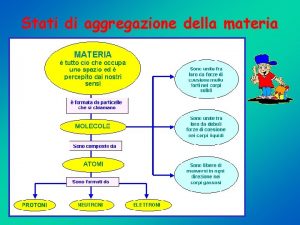
Proprietà macroscopiche della materia Gli stati di aggregazione della materia
Gli stati di aggregazione della materia Stati condensati della materia
Stati condensati della materia I passaggi di stato della materia
I passaggi di stato della materia Curve di riscaldamento e raffreddamento zanichelli
Curve di riscaldamento e raffreddamento zanichelli Teoria cinetico molecolare zanichelli
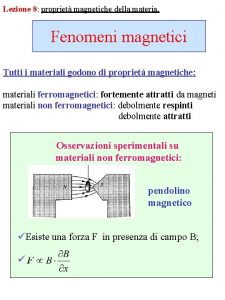
Teoria cinetico molecolare zanichelli Proprietà magnetiche della materia
Proprietà magnetiche della materia Teoria atomica della materia
Teoria atomica della materia Esperimento oersted zanichelli
Esperimento oersted zanichelli Il ciclo della materia
Il ciclo della materia I solidi
I solidi Principio della minima energia
Principio della minima energia Seta origini
Seta origini Il racconto della chimica e della terra soluzioni
Il racconto della chimica e della terra soluzioni Ritratto della mia bambina spiegazione
Ritratto della mia bambina spiegazione Prove della sfericità della terra
Prove della sfericità della terra Elena bettinelli
Elena bettinelli Simonetta klein il racconto della chimica
Simonetta klein il racconto della chimica