Stati della materia e passaggi di stato Prerequisiti













- Slides: 18

Stati della materia e passaggi di stato

Prerequisiti ßConoscere il S. I. ßSapere che la temperatura è una grandezza fondamentale del S. I. ßConoscere e comprendere i concetti di calore e temperatura ßConoscere le unità di misura utilizzate per esprimere il calore e la temperatura ßConoscere e il termometro 2

Obiettivi – Stati della materia ß Sapere e comprendere il significato dei termini “stato fisico” e “stato di aggregazione” della materia ß Conoscere e comprendere gli stati della materia dal punto di vista macroscopico ß Conoscere e comprendere i parametri caratterizzanti dei tre stati (pressione, temperatura, densità, volume, forma) ß Conoscere e comprendere i passaggi di stato, i parametri caratteristici e come li influenzano ß Conoscere l’evaporazione e i parametri che la caratterizzano anche in contrapposizione all’ebollizione ß Saper interpretare e costruire in laboratorio una curva di riscaldamento/raffreddamento 3

Obiettivi Trasformazioni ßConoscere e comprendere il significato di trasformazione in senso fisico e chimico, riuscire a fare esempi e saperle distinguere ßComprendere il concetto di sostanza pura, di componente, di elemento e di composto ßSaper interpretare e costruire in laboratorio una curva di riscaldamento/raffreddamento 4

Grandezze fisiche ß Sono tutte quelle grandezze che caratterizzano una sostanza e che possono essere modificate senza cambiare la natura intima di quella sostanza ß Le grandezze fisiche sono collegate alle proprietà fisiche o possono esserne un sinonimo ß La descrizione macroscopica di un corpo, di una sostanza o di un fenomeno passa attraverso le grandezze e/o proprietà fisiche ß Gli aspetti macroscopici di un corpo o di un fenomeno sono tutti quelli che possiamo percepire e osservare con i nostri sensi, direttamente o con uno strumento 5

Stati della materia ßLa materia può presentarsi in tre diversi stati di aggregazione ²Ciascuno stato presenta caratteristiche macroscopiche particolari ÌSolido ÌLiquido ÌAeriforme Stato Solido Liquido Aeriforme Forma Costante Variabile Volume Costante Variabile Densità Elevata/costante Media/costante Bassa/variabile 6

Aggregazione ßGli stati della materia sono chiamati anche di aggregazione perché ² Dipendono da come le particelle che compongono la materia si dispongono nello spazio e da come interagiscono ßLa teoria che descrive la materia come un insieme di piccolissime particelle invisibili riunite per formare un continuo apparente è chiamata ² Teoria particellare della materia ßTutte le descrizioni che parlano della materia sotto questo punto di vista sono definite ² Aspetti microscopici della materia 7

Descrizione particellare solido ßParticelle disposte in modo ordinato ßNon si allontanano l’una dall’altra ma possono vibrare ßCi sono legami stabili ² Ciascuna particella forma il massimo numero di interazioni con le sue vicine 8

Descrizione particellare liquido ßLe particelle si dispongono in modo disordinato ßSono legate ma i legami sono instabili ² Si formano e si spezzano in continuazione ßSi muovono costantemente ma non si possono allontanare le une dalle altre ² Possono solo scorrere 9

Descrizione particellare aeriforme ßLe particelle si muovono in modo disordinato e molto velocemente ² Ci sono urti continui tra particelle e sulle pareti del contenitore ßNon ci sono legami ßPossono allontanarsi le une dalle altre 10

Prova a rispondere ßDefinire la condizione in cui può trovarsi la materia (solido, liquido, aeriforme) ² Stato fisico o di aggregazione ßTipo di materia avente caratteristiche proprie che la differenziano da tutte le altre ² Sostanza pura ßQualunque sostanza che occupa un volume e possiede una massa ² materia 11

Passaggi di stato Temperatura Pressione 12

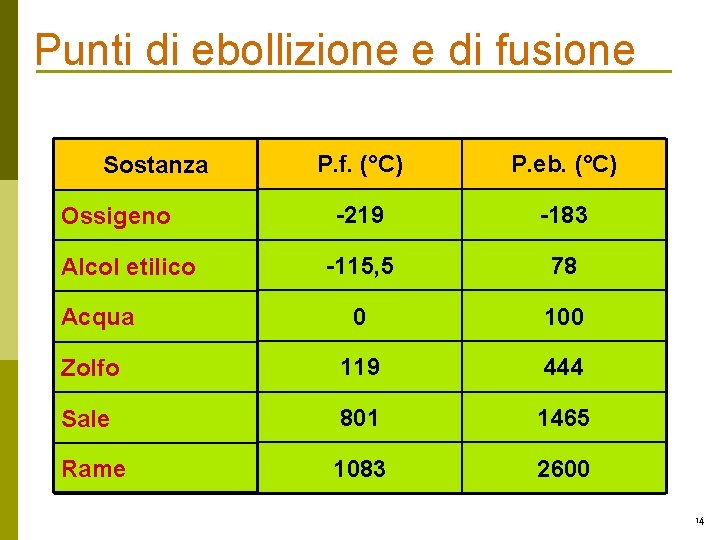
Proprietà fisiche ßLa temperatura dei passaggi di stato è una proprietà fisica di una sostanza ² È un parametro fisico caratterizzante ² Molte sostanze possono essere riconosciute attraverso la loro temperatura di ebollizione o di fusione ßSono denominate anche “Punti fissi” ßAltre proprietà fisiche possono essere ² Stato fisico ² Densità ² Colore ² Odore ² Durezza ² Sapore 13

Punti di ebollizione e di fusione Sostanza P. f. (°C) P. eb. (°C) -219 -183 -115, 5 78 0 100 Zolfo 119 444 Sale 801 1465 Rame 1083 2600 Ossigeno Alcol etilico Acqua 14

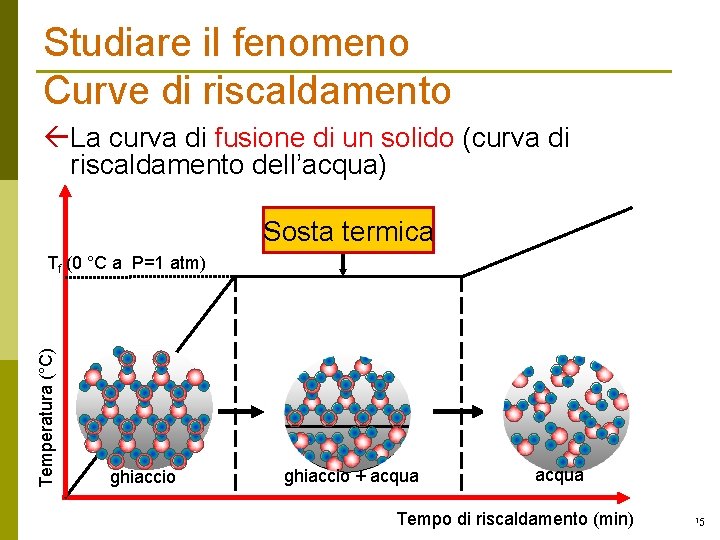
Studiare il fenomeno Curve di riscaldamento ßLa curva di fusione di un solido (curva di riscaldamento dell’acqua) Sosta termica Temperatura (°C) Tf (0 °C a P=1 atm) ghiaccio + acqua Tempo di riscaldamento (min) 15

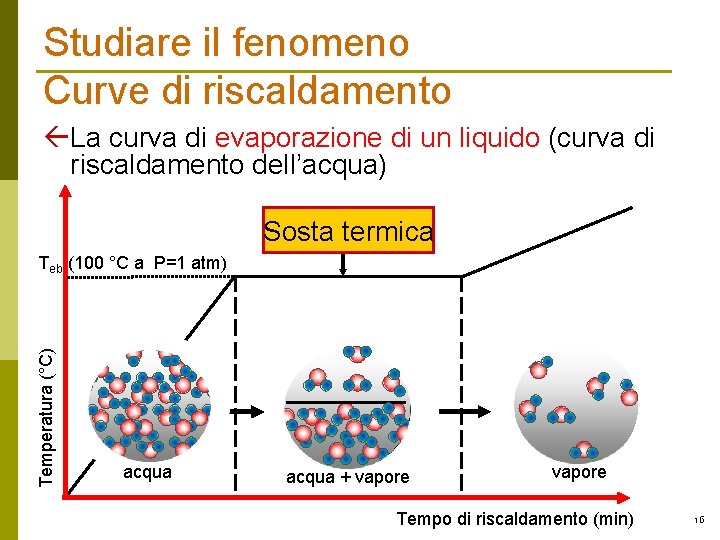
Studiare il fenomeno Curve di riscaldamento ßLa curva di evaporazione di un liquido (curva di riscaldamento dell’acqua) Sosta termica Temperatura (°C) Teb (100 °C a P=1 atm) acqua + vapore Tempo di riscaldamento (min) 16

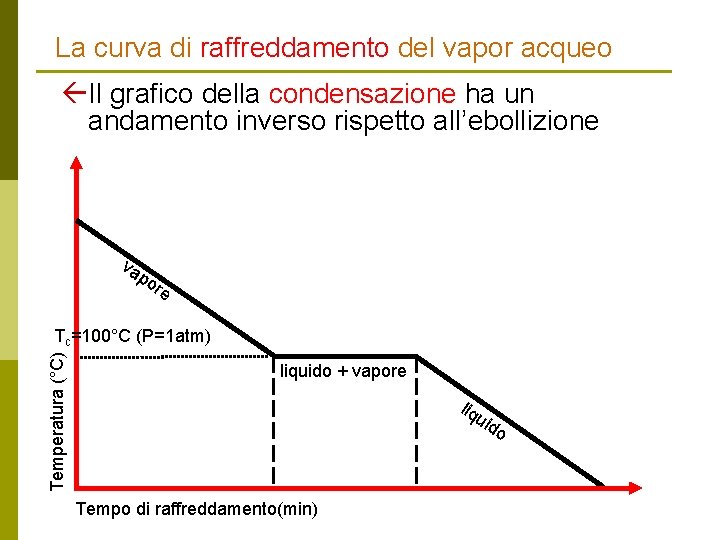
La curva di raffreddamento del vapor acqueo ßIl grafico della condensazione ha un andamento inverso rispetto all’ebollizione va po re Temperatura (°C) Tc=100°C (P=1 atm) liquido + vapore liq u ido Tempo di raffreddamento(min)

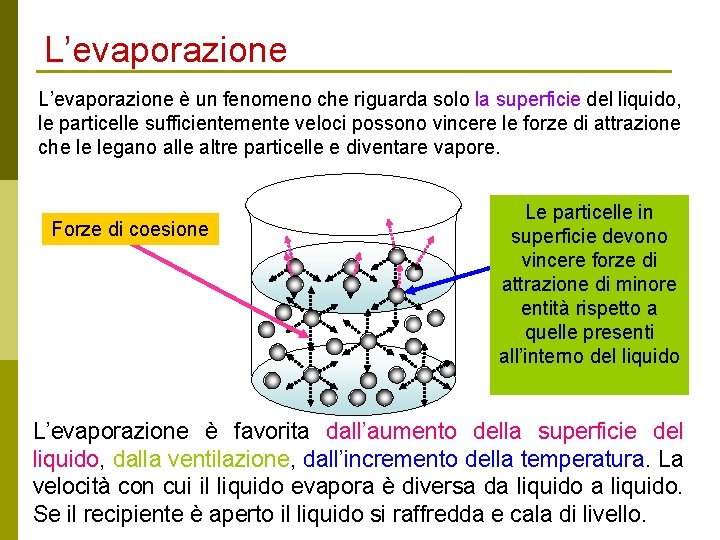
L’evaporazione è un fenomeno che riguarda solo la superficie del liquido, le particelle sufficientemente veloci possono vincere le forze di attrazione che le legano alle altre particelle e diventare vapore. Forze di coesione Le particelle in superficie devono vincere forze di attrazione di minore entità rispetto a quelle presenti all’interno del liquido L’evaporazione è favorita dall’aumento della superficie del liquido, dalla ventilazione, dall’incremento della temperatura. La velocità con cui il liquido evapora è diversa da liquido. Se il recipiente è aperto il liquido si raffredda e cala di livello.