Joanna Jagieo Badanie utleniania elektrody kobaltowej w roztworze

Joanna Jagiełło Badanie utleniania elektrody kobaltowej w roztworze zasadowym w obecności substancji przyspieszających i spowalniających korozję z wykorzystaniem elektrochemicznej wagi kwarcowej (EQCM) oraz wirującej elektrody dyskowej z pierścieniem (RRDE) Zakład Chemii Fizycznej Pracownia Elektrochemicznych Źródeł Energii Kierownik pracy: dr Michał Grdeń

Plan prezentacji 1. Właściwości i zastosowanie kobaltu 2. Korozja i pasywacja 3. Substancje przyspieszające i spowalniające korozję 4. Mechanizmy utleniania 5. Metody badawcze 6. Przykładowe wyniki i ich interpretacja

właściwości kobaltu → zastosowanie • Metal przejściowy, główne stopnie utlenienia +2, +3, nieszlachetny – ulega nieodwracalnym procesom utleniania • Duża wytrzymałość temperaturowa (t. topn. =14950 C) i mechaniczna – turbiny, składnik stellitów, noże • Zwiększa wytrzymałość na korozję – dodatek do stopów typu AB 5 , dodatek do elektrod niklowych, baterie(Ni/Cd, Ni/H 2 , litowo-jonowe), ogniwa paliwowe • Kataliza (może zastąpić Pt) – elektroliza wody, baterie metal-powietrze, ogniwa paliwowe; przykłady prac: elektrochemiczne utlenianie glukozy, dwufunkcyjność katalityczna- dysproporcjonowanie stopni utlenienia tlenu • Promieniotwórczość izotopu Co 60 - bomba kobaltowa (medycyna) • Kondensator chemiczny– efektywne gromadzenie ładunku w podwójnej warstwie elektrycznej i w procesie redoks (Co→Co 2+ +2 e) – odwracalne magazynowanie energii • Ferromagnetyk – materiały magnetyczne
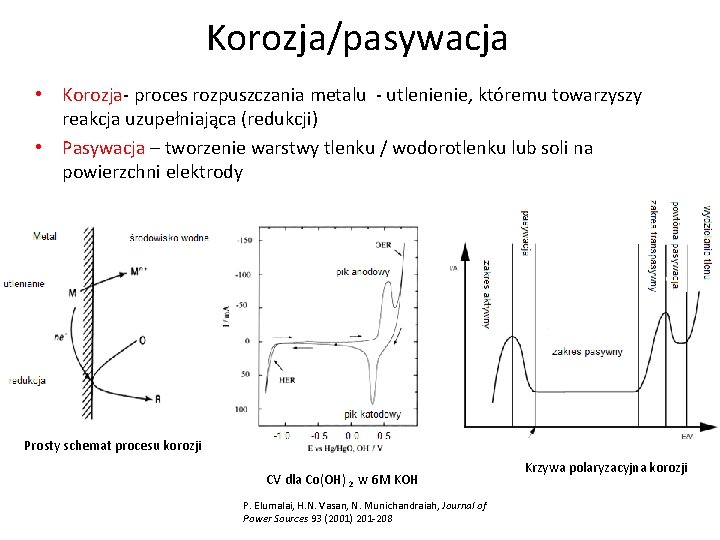
Korozja/pasywacja • Korozja- proces rozpuszczania metalu - utlenienie, któremu towarzyszy reakcja uzupełniająca (redukcji) • Pasywacja – tworzenie warstwy tlenku / wodorotlenku lub soli na powierzchni elektrody Prosty schemat procesu korozji CV dla Co(OH) 2 w 6 M KOH P. Elumalai, H. N. Vasan, N. Munichandraiah, Journal of Power Sources 93 (2001) 201 -208 Krzywa polaryzacyjna korozji
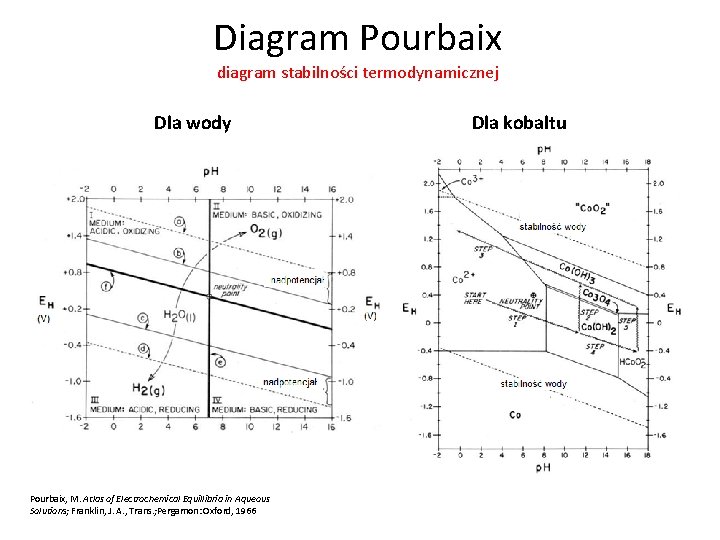
Diagram Pourbaix diagram stabilności termodynamicznej Dla wody Pourbaix, M. Atlas of Electrochemical Equillibria in Aqueous Solutions; Franklin, J. A. , Trans. ; Pergamon: Oxford, 1966 Dla kobaltu
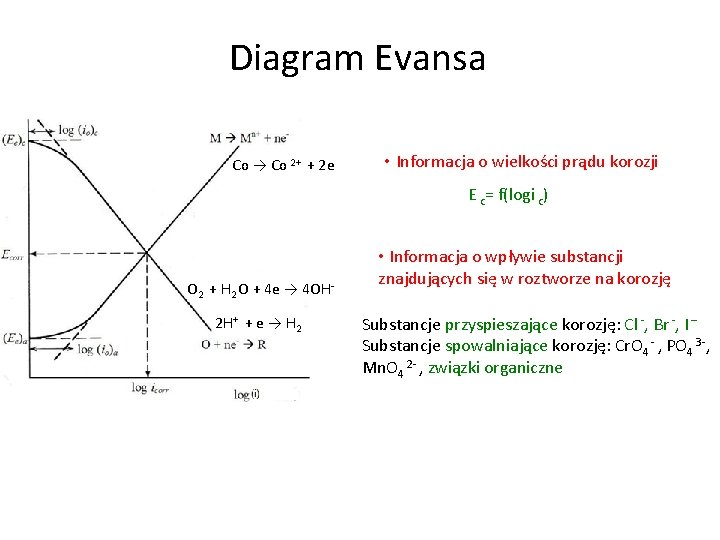
Diagram Evansa Co → Co 2+ + 2 e • Informacja o wielkości prądu korozji E c= f(logi c) O 2 + H 2 O + 4 e → 4 OH 2 H+ + e → H 2 • Informacja o wpływie substancji znajdujących się w roztworze na korozję Substancje przyspieszające korozję: Cl -, Br -, I – Substancje spowalniające korozję: Cr. O 4 - , PO 4 3 -, Mn. O 4 2 - , związki organiczne
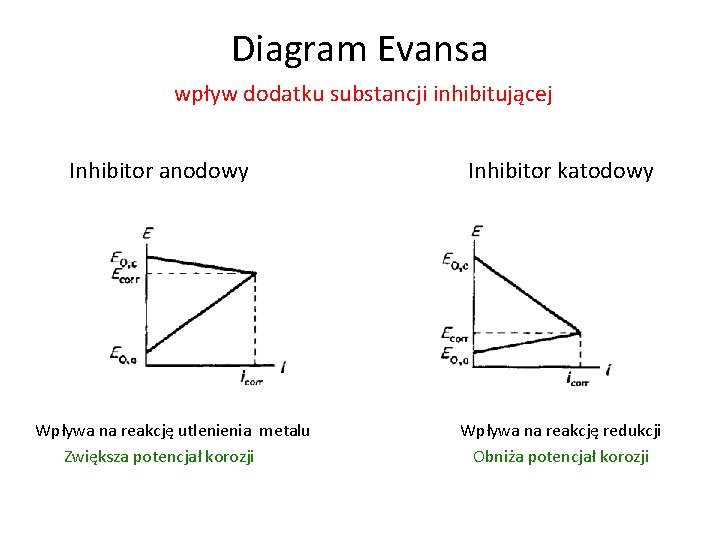
Diagram Evansa wpływ dodatku substancji inhibitującej Inhibitor anodowy Wpływa na reakcję utlenienia metalu Zwiększa potencjał korozji Inhibitor katodowy Wpływa na reakcję redukcji Obniża potencjał korozji

Mechanizmy utleniania • Nukleacja • Model „zamiany miejsc” • Zwykła adsorpcja
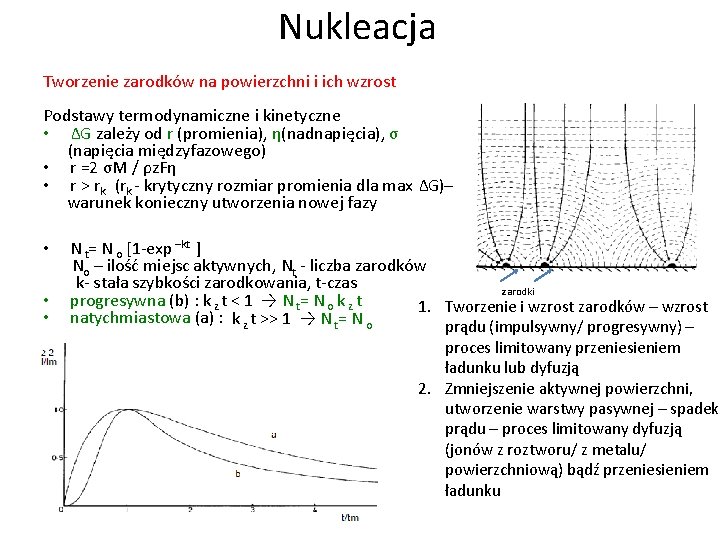
Nukleacja Tworzenie zarodków na powierzchni i ich wzrost Podstawy termodynamiczne i kinetyczne • ∆G zależy od r (promienia), η(nadnapięcia), σ (napięcia międzyfazowego) • r =2 σM / ρz. Fη • r > rk (rk - krytyczny rozmiar promienia dla max ∆G)– warunek konieczny utworzenia nowej fazy • • N t= N o [1 -exp –kt ] No – ilość miejsc aktywnych, Nt - liczba zarodków k- stała szybkości zarodkowania, t-czas zarodki progresywna (b) : k z t < 1 → N t= N o k z t 1. Tworzenie i wzrost zarodków – wzrost natychmiastowa (a) : k z t >> 1 → N t= N o prądu (impulsywny/ progresywny) – 1 D, 2 D, 3 D proces limitowany przeniesieniem ładunku lub dyfuzją 2. Zmniejszenie aktywnej powierzchni, utworzenie warstwy pasywnej – spadek prądu – proces limitowany dyfuzją (jonów z roztworu/ z metalu/ powierzchniową) bądź przeniesieniem ładunku
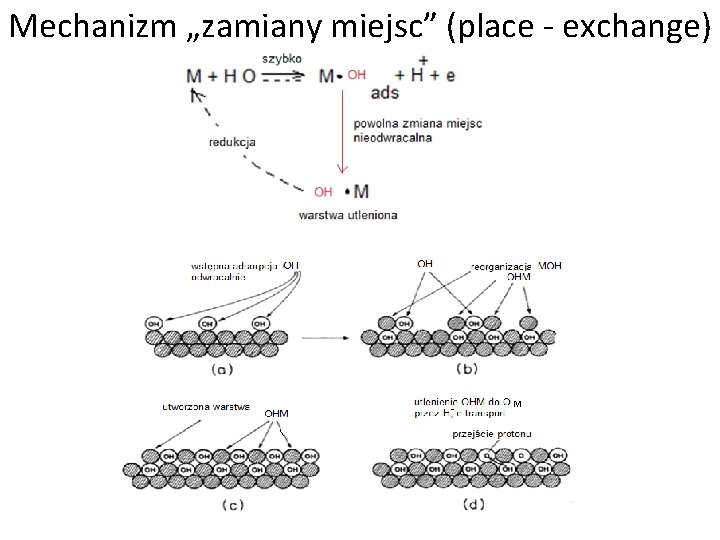
Mechanizm „zamiany miejsc” (place - exchange) M

Część eksperymentalna – metody badawcze Badanie wczesnych mechanizmów utleniania (korozja/pasywacja) kobaltu metalicznego do związków Co(II) – zakres aktywny + pasywacja na krzywej polaryzacyjnej korozji Określenie mechanizmu utleniania na podstawie: - Analizy zależności prąd-czas w trakcie procesu utleniania (pik prądowy dla modelu nukleacji) - Analizy zależności ładunek utleniania-czas (zależność logarytmiczna dla modelu „zamiany miejsc”) Konieczność określenia wkładu aktywnego rozpuszczania metalu do całkowitego prądu/ładunku przepływającego w trakcie utleniania -> specjalne techniki pomiarowe - Chronowoltamperometria i chronoamperometria - EQCM - RRDE Elektrody przygotowywane przez elektroosadzanie Co na dysku RRDE i elektrodach EQCM (z roztworu wodnego Co(NO 3)2 ). Pomiary w roztworach wodnych KOH, Na. OH z dodatkiem substancji mających wpływ na korozję/pasywację.

Elektrochemiczna waga kwarcowa EQCM • Zjawisko piezoelektryczne • Zmiana masy → zmiana częstotliwości drgań • Liniowe równanie Sauerbrey’a: ∆f=-∆m· 2·f 20 /(n·s·(√(μ·ρ)) ∆f – zmiana częstotliwości drgań ∆m – zmiana masy f 0 – podstawowa częstotliwość drgań kryształu (f 0 =4, 99[MHz]) n – tryb oscylacji (n=1) μ – moduł sprężystości poprzecznej kwarcu (μ =2, 947· 1011 g/(cm·s 2 )) ρ – gęstość kwarcu (ρ= 2, 648 g/cm 3 ) s- piezoelektryczna powierzchnia aktywna kwarcu (pokryta fragmentem elektrody mającej kontakt z roztworem) • Możliwość łączenia z innymi technikami elektrochemicznymi, np. CV – jednoczesna rejestracja sygnałów prądowych i zmian częstotliwości Informacje: Rozpuszczanie elektrody oraz skład warstwy pasywnej, zależność masa - czas → mechanizm utleniania
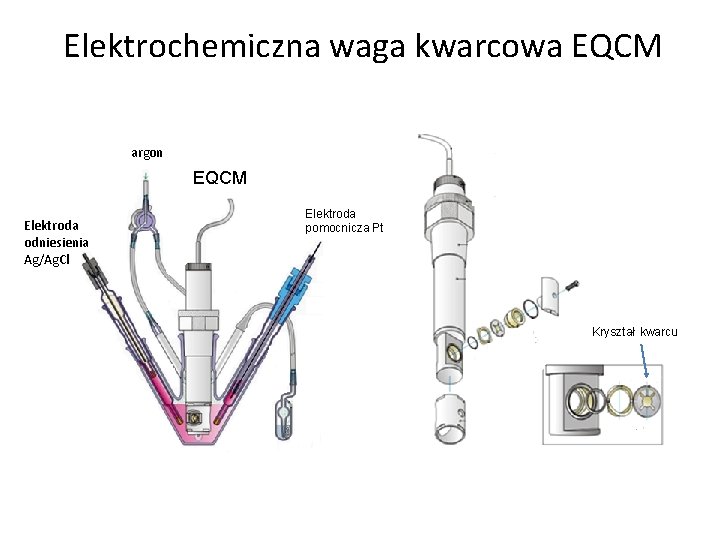
Elektrochemiczna waga kwarcowa EQCM argon EQCM Elektroda odniesienia Ag/Ag. Cl Elektroda pomocnicza Pt Kryształ kwarcu
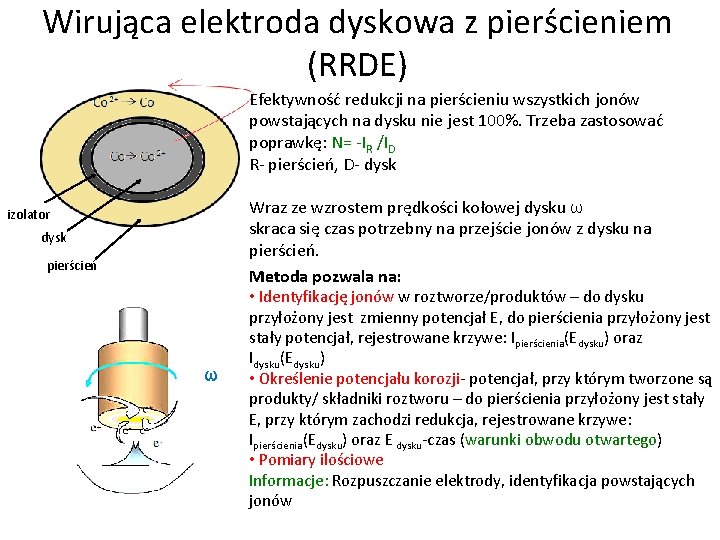
Wirująca elektroda dyskowa z pierścieniem (RRDE) Efektywność redukcji na pierścieniu wszystkich jonów powstających na dysku nie jest 100%. Trzeba zastosować poprawkę: N= -IR /ID R- pierścień, D- dysk Wraz ze wzrostem prędkości kołowej dysku ω skraca się czas potrzebny na przejście jonów z dysku na pierścień. Metoda pozwala na: • Identyfikację jonów w roztworze/produktów – do dysku izolator dysk pierścień ω przyłożony jest zmienny potencjał E, do pierścienia przyłożony jest stały potencjał, rejestrowane krzywe: Ipierścienia(Edysku) oraz Idysku(Edysku) • Określenie potencjału korozji- potencjał, przy którym tworzone są produkty/ składniki roztworu – do pierścienia przyłożony jest stały E, przy którym zachodzi redukcja, rejestrowane krzywe: Ipierścienia(Edysku) oraz E dysku-czas (warunki obwodu otwartego) • Pomiary ilościowe Informacje: Rozpuszczanie elektrody, identyfikacja powstających jonów

Wirująca elektroda dyskowa z pierścieniem (RRDE)
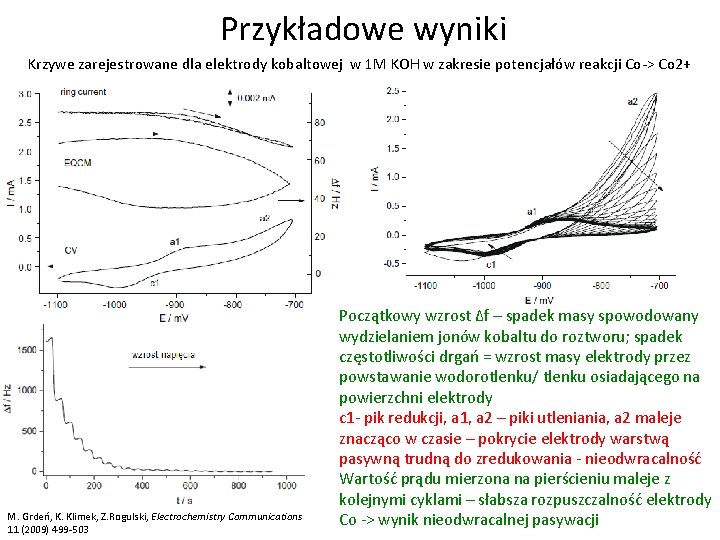
Przykładowe wyniki Krzywe zarejestrowane dla elektrody kobaltowej w 1 M KOH w zakresie potencjałów reakcji Co-> Co 2+ M. Grdeń, K. Klimek, Z. Rogulski, Electrochemistry Communications 11 (2009) 499 -503 Początkowy wzrost ∆f – spadek masy spowodowany wydzielaniem jonów kobaltu do roztworu; spadek częstotliwości drgań = wzrost masy elektrody przez powstawanie wodorotlenku/ tlenku osiadającego na powierzchni elektrody c 1 - pik redukcji, a 1, a 2 – piki utleniania, a 2 maleje znacząco w czasie – pokrycie elektrody warstwą pasywną trudną do zredukowania - nieodwracalność Wartość prądu mierzona na pierścieniu maleje z kolejnymi cyklami – słabsza rozpuszczalność elektrody Co -> wynik nieodwracalnej pasywacji

Dziękuję za uwagę
- Slides: 17
































