Imunohematologick vyeten v thotenstv a po porodu Dle












































- Slides: 47

Imunohematologická vyšetření v těhotenství a po porodu Dle „Doporučení TS ČLS JEP č. STL 2010 -06 ze dne 1. 3. 2010“ Eliška Rýznarová 1

Cílem doporučení je Prevence hemolytického onemocnění plodu a novorozence 2

Těžkým průběhem HON se rozumí • • Úmrtí plodu Provedení intrauterinní transfuze plodu (IUT) Výměnná transfuze novorozence Transfuze erys během 1. týdne života z důvodu anémie způsobené HON • V ČR je cca 25 takových těžkých případů za rok 3

Odběr a značení vzorku krve • Vzorek matky, otce: sražený nebo odebraný do citrátu, EDTA, CPD-A • Vzorek plodu: je krev z umbilikální žíly • Vzorek novorozence: pupečníková nebo kapilární krev • Zkumavku označit před odběrem krve ! • Na štítku: jméno příjmení číslo pojištěnce (rodné číslo) datum odběru vzorku • Na štítku plodu: údaje těhotné + označení „plod“ • Na štítku novorozence: jméno nemusí být známo příjmení číslo pojištěnce vygenerované – unikátní • Po nalepení štítku ověřit identifikaci dotazem, ze zdrav. dokumentace 4

Žádanka • • • Jméno a příjmení Číslo pojištěnce (rodné číslo) Datum požadavku Diagnóza Zdravotní pojišťovna Pořadí a týden gravidity Transfuzní anamnéza Informace o zjištěných protilátkách, specifita, HON Informace o provedené Rh. D profylaxi Identifikace žadatele Identifikace osoby, která vzorek odebrala Bez správného odběru, značení zkumavky a žádanky nelze provést vyšetření ! 5

Klinická významnost protilátek proti ery • Klinicky významné: anti-D, -c, -K, -E, -C, -e, -G, -Ce, -c. E, -Fya, Jka, anti-A, -B, -AB • Klinický význam zvažovat individuálně: anti-S, -s, - M, -Cw, -ce, - Cx, -Ew, Fyb, - k, -Kpa, b, - Jsa, b, PP 1 Pk, -U, - Jkb, -Tja, -Yta, -LW, -Diego, -Jra, proti Ag s vysokou četností: např. anti-Ena, - Gerbich, proti Ag s nízkou frekvencí: např. anti-Wra • Klinicky nevýznamné: anti-P 1, - Lea, -Leb, -H, I, -HI, -N, -Lutheran, panspecifické protilátky (reagují se všemi panelovými diagn. ery i s ery vlastními), chladové protilátky, protilátky reagující pouze v enzymovém prostředí 6

Protilátky jako příčina HON • HON mohou teoreticky způsobovat jakékoliv alogenní protilátky třídy Ig. G • Nejčastější příčinou těžkého HON jsou: anti-D (85%) anti-c (3, 5%) – mohou způsobit i opožděnou anemii novorozence anti-K (10%) anti-E (2 -7%) • Protilátky stejné specifity a síly se in vivo nechovají stejně • Nejčastěji se vyskytující protilátky jako následek předchozí transfuze jsou: anti-c, -K, Fya • Z hlediska těžkého HON vyžadují „přísné“ sledování: anti-D, - c, -K, -E 7

Vstupní vyšetření každé těhotné ve 12. týdnu (10. -16. ) minimální požadavky • ABO : monoklonální anti-A, -B, erys A 1, B, u dalších těhotenství anti-A, -B, shoda se záznamem ! • D: 2 x anti-D Ig. M, DVI-, různé klony, Rh kontrola, Dw NE u dalších těhotenství 1 x anti-D Ig. M, DVI-, Rh kontrola, shoda se zázn. ! • Screening protilátek minimálně se 3 typy diagn. erys LISS NAT s polyspecifickým AGH anti-Ig. G + C 3 d, enzymový test u zkumavkových testů V případě pozitivity identifikace protilátek • Identifikace protilátek minimálně s 8 typy dg. erys LISS NAT s polyspecifickým AGH anti-Ig. G + C 3 d, enzymový test doplňující, ověření specif. protilátky typizací antigenu • Titrace protilátky zkumavkovým NAT bez potenciátoru, AGH anti. Ig. G, nebo -Ig. G-C 3 d nebo sloupcovou aglutinací LISS NAT První zkumavka, sloupec: titr 1 (neředěné sérum/plazma + erys) Sérum/plazmu ředit fyziologickým roztokem 8

Klinicky významný titru protilátek u těhotných • Zkumavkovým NAT: . Sloupcovou aglutinací LISS NAT: anti-D, - C, -E: ≥ 32 anti-D, - C, -E: ≥ 128 anti-K: ≥ 4 anti-K: ≥ 8 ostatní protilátky: ≥ 64 ostatní protilátky: ≥ 128 (nejsou data) • Individuálně klinicky významný může být i nižší titr • U protilátky anti-K je význam titru omezený - způsobují efekt imunitní suprese erytropoézy • Je důležité i stanovení titru protilátek ve směsi • Při titrování je nutná srovnávací titrace s předchozím vzorkem (používají se vždy jiné dg. erys) • Titrují se pouze klinicky významné Ig. G a přednostně s heterozygotními dg. ery • Změna titru o více než 2 stupně je signifikantní • Náhlý pokles titru o více než 3 stupně může být známkou těžkého postižení nebo i exitu plodu 9

Titrování je screeningový test • Titrování se uplatňuje jako screeningový test pro rozhodování o tom kdy je třeba začít monitorovat HON jinou metodou než imunohematologickou. • Titrování se provádí jen do dosažení klinicky významného titru. • Pokud je v anamnéze HON je vhodné určit genotyp plodu, pokud není otec homozygot pro daný antigen. Antigen-pozitivní plod sledovat jinými metodami než imunohematologickými. Zde není užitečné pro stanovení tíže fetální anémie stanovení titru klinicky významných protilátek. 10

Opakované vyšetření těhotné ve 28. týdnu (26. – 30. ) Všechny ženy D+ a D- bez protilátek nebo s klinicky nevýznamnými. Minimální požadavky: • ABO : pokud jsou záznamy !! pak pouze kontrolní vyšetření s monoklonálním anti-A, -B a u dalších těhotenství se neprovádí • D: pokud jsou záznamy !! 1 x anti-D Ig. M, DVI-, Rh kontrola, Dw NE u dalších těhotenství se neprovádí • Screening protilátek jako u vstupního vyšetření Odběr vzorku před aplikací Ig anti-D ! minimálně se 3 typy diagn. erys LISS NAT s polyspecifickým AGH anti -Ig. G + C 3 d, enzymový test u zkumavkových testů v případě pozitivity identifikace protilátek • Identifikace protilátek jako u vstupního vyšetření minimálně s 8 typy dg. erys LISS NAT s polyspecifickým AGH anti-Ig. G + C 3 d, enzymový test doplňující, ověření specif. protilátky typizací antigenu • Titrace protilátky jako u vstupního vyšetření zkumavkovým NAT bez potenciátoru, AGH anti-Ig. G, nebo -Ig. G-C 3 d nebo Sloupcovou aglutinací LISS NAT 11

Požadavky na diagnostické erytrocyty • Zastoupení antigenů u screeningových diagnostických erys: C, Cw, c, D, E, e, K, k, Fya, Fyb, Jka, Jkb, S, s, M, N, Lea 1 x s fenotypem: DCe / DCe (R 1 R 1) 1 x s fenotypem: Dc. E / Dc. E (R 2 R 2) Homozygotní zastoupení antigenů: Fya, Fyb, Jka, Jkb, S, s. Poznámka: antigeny Fyb, N a Lea jsou uvedeny spíše z důvodu možné transfuze krve. • Zastoupení antigenů u panelových diagnostických erys: ≥ 1 x fenotyp DCe/DCe (R 1 R 1) a DCe/DCe Cw+ (R 1 w R 1) a zároveň oboje exprimovat: K, k, Fya, Fyb, Jka, Jkb, M, S, s ≥ 1 x fenotyp Dc. E/Dc. E (R 2 R 2) ≥ 1 x fenotyp D- Ccee (r´r) ≥ 1 x fenotyp D- cc. Ee (r´´r) ≥ 2 x fenotyp D- ccee (rr) a s fenotypy K+, K-, Jk(a+b-), Jk(a-b+), S+s-, S-s+, Fy(a+b-), Fy(a-b+) 12

Požadavek na monoklonální anti-B • Diagnostikum anti-B nesmí reagovat se získanou krevní skupinou B. • Co to je „získaná“ krevní skupina B ? Bakteriální enzymy (deacetylázy) mění imunodominatní cukr krevních skupin A (acetyl-galaktosamin) na imunodominantní cukr krevní skupiny B (na galaktosamin který je základní strukturou galaktósy a některá monoklonální nebo i polyklonální anti-B pak mohou s galaktosaminem reagovat. V tomto případě pak erys A 1 reagují jako by nesly B antigen a krevní skupina se jeví jako AB. 13

Kdy vyšetřovat slabý antigen D u těhotné • Slabé D je třeba vyšetřit vždy v případě genotypování plodu z plazmy matky. U žen se slabým D nelze genotypizaci plodu z plazmy matky provést nebo jen po konzultaci s RL • Na slabý antigen D nebo variantu D je vhodné myslet v případě: - Pozorování slabší reakce než na 2+ s oběma anti-D - Při zjištění zcela diskrepantních reakcí: negativní a pozitivní - Při rozdílu v síle reakcí obou anti-D o 2+ - V případě nečekaného nálezu protilátky anti-D u osoby „ se zdánlivě normálním D“ (a vyloučenou autoreakcí) - Zjistíme-li diskrepance mezi anamnestickým údajem a současným vyšetřením - V tomto případě stanovíme nebo vyloučíme variantu antigenu D - Do té doby a také ve sporných případech klasifikujeme těhotnou jako D- - A laboratoř doporučí anti-D profylaxi • Vyšetřením antigenu D určíme D- ženy profylaxi anti-D (Profylaxe anti-D viz dále samostatná kapitola). 14

Sledování těhotných s klinicky významnými protilátkami anti-D, -c, K, - E a protilátkami zodpovědnými za těžké HON v anamnéze Testování 4 týdny po vstupním vyšetření: • kontrolní vyšetření AB 0 D stačí, pokud jsou záznamy!! anti-A, -B, 1 x anti-D, Rh kontrola • Identifikace protilátek • Stanovení titru protilátek paralelně s předchozím vzorkem Je nutné testovat každé další 4 týdny, 28. týden a pak 1 x za 14 dnů: • • • Identifikace protilátek Stanovení titru protilátek paralelně s předchozím vzorkem Titrování se provádí pokud není jednoznačně prokázáno, že je otec pro daný antigen negativní (otec nejistý) • Po dosažení klinicky významného titru další titrování neprovádět. Pokračovat ve sledování plodu jinými metodami (např. Dopplerova metoda pro měření krevního průtoku arteria cerebri media). • V identifikaci protilátek pokračujeme protože je možná tvorba další protilátky, pak se postupuje podle klinické závažnosti protilátky a význam pro transfuzi krve 15

Sledování těhotných s klinicky významnými protilátkami jinými než již zmíněnými (anti-D, -c, -K, -E) Kontrolní vyšetření se provádí po vstupním vyšetření až ve 28. týdnu těhotenství: • kontrolní vyšetření AB 0 D stačí, pokud jsou záznamy!! anti-A, -B, 1 x anti-D, Rh kontrola • Identifikace protilátek • Stanovení titru protilátek paralelně s předchozím vzorkem z 12. týdne Po 28. týdnu pak vyšetřovat každé 4 týdny (může se objevit další specifická protilátka): • Identifikaci protilátek • Stanovení titru protilátek paralelně s předchozím vzorkem • Titrování se provádí pokud není jednoznačně prokázáno, že je otec pro daný antigen negativní (otec nejistý) • Po dosažení klinicky významného titru další titrování neprovádět. Pokračovat ve sledování plodu jinými metodami (např. Dopplerova metoda pro měření krevního průtoku arteria cerebri media). • V identifikaci protilátek pokračujeme, je možná tvorba další protilátky 16

Specifické postupy V případě výskytu protilátky Anti-K • Klinicky významný titr je zkumavkově ≥ 4, sloupcovou aglutinací ≥ 8 • Význam titru omezený – uplatňuje se efekt imunitní suprese erytropoézy • Vyšetřit otce, je-li heterozygot a vyšetřit plod genotypováním z plazmy matky poprvé 20. týden. Je-li vyšetření negativní opakovat 28. týden. Popřípadě provést genotypizaci ze vzorku získaného kordocentézou. To však přináší vysoké riziko FMH, další aloimunizace matky (30%), riziko potratu (1 -3%). • V případě K pozitivity plodu monitorovat plod pomocí ultrazvuku. • Většina případů tvorby anti-K je způsobena předchozí transfuzí Kell pozitivních ery • Dívkám a ženám ve fertilním věku se doporučuje v případě transfuze aplikace Kell negativních ery 17

Další specifické postupy • V případě zjištění anti-C+D: Je třeba odlišit, zda se nejedná o protilátku anti-C+G, resp. Anti-G. V tomto případě by těhotné měly podstoupit Rh profylaxi • AB 0 inkompatibilita: U AB 0 inkompatibility neexistuje dostupný test k přesné prenatální předpovědi HON Nemá smysl identifikovat těhotné s vysokými titry anti-A, -B ani sledování dynamiky titrů imunních Ig. G protilátek anti-A, anti-B titrováním NAT s erys A 1 nebo B 18

Anti-D profylaxe • Především je žádoucí monitorovat situaci před podáním Ig anti-D. Odebrat vzorek těhotné a vyšetřit protilátky. 19

Poznámka k Anti-D profylaxi • Fetal Bleed Screening Kit slouží k průkazu fetomaternálního krvácení při proniknutí 30 ml a více AB 0 kompatibilní D pozitivní fetální krve do krevního oběhu D negativní ženy. • Test je sestaven tak, aby dal negativní výsledek při nejobvyklejším rozsahu fetálního krvácení, což je méně než 2 ml plné krve. • Pozitivita screeningového testu ukazuje na zvýšené fetomaternální krvácení. Je nutné kvantitativní stanovení a určit profylaktickou dávku Rh imunoglobulinu a aplikovat do 72 hod po porodu. 20

Poznámka: Standardní dávka pro potlačení Rh imunizace: • Je 1 ml Rh-imunního globulinu o obsahu asi 300 µg protilátky na maximálně 15 ml erytrocytů plodu, což odpovídá asi 30 ml plné krve. • Negativita screeningového vyšetření fetomaternálního krvácení v indikovaných případech znamená, že k ochraně před tvorbou anti-D u ženy postačí pouze standardní dávka Rh -imunního globulinu o objemu 1 ml. 21

Poznámka: Fetal Bleed Screening Test pro průkaz fetomaternálního krvácení před aplikací Ig anti-D kapka mateřských erys + 1 kapka Anti-D modif. (senzibilizace D pozitivních ery) 15 min 37°C a pak 3 – 4 x proprat v 0, 9% Na. Cl + 1 kapka indikátorových erys, centrifugace, mikroskopování < 1 rozeta / 3 zorná pole = 1 dávka Rh imunního globulinu > 1 rozeta / 3 zorná pole = nutné kvantitativní stanovení 22

Fetal Bleed Screening Test využití ke stanovení slabého D z pupečníkové krve Poznámka: případě, že je PAT pozitivní v souvislosti s protilátkami ABO systému a nelze testovat slabé D metodou NAT jednotné aglutinační pole = pozitivní výsledek 23

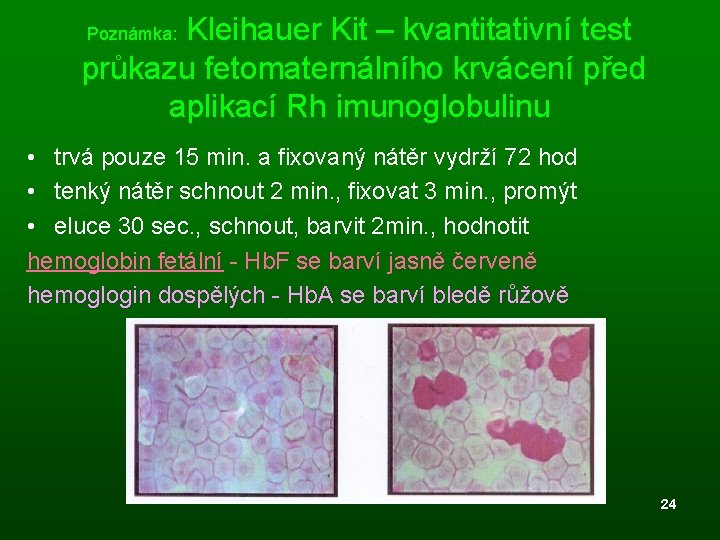
Kleihauer Kit – kvantitativní test průkazu fetomaternálního krvácení před aplikací Rh imunoglobulinu Poznámka: • trvá pouze 15 min. a fixovaný nátěr vydrží 72 hod • tenký nátěr schnout 2 min. , fixovat 3 min. , promýt • eluce 30 sec. , schnout, barvit 2 min. , hodnotit hemoglobin fetální - Hb. F se barví jasně červeně hemoglogin dospělých - Hb. A se barví bledě růžově 24

Testování po anti-D profylaxi Postup v případě, že existuje záznam o podání Ig anti-D: • Je-li záznam o podání v posledních 8 týdnech a titr nízký, stačí kontrola titru každé 4 týdny • Pokud je titr anti-D stále stejný nebo klesá nebo protilátka není detekovatelná – kontroly neprovádět Poznámka: • Anti-D protilátky po profylaxi často reagují pouze v enzymovém testu a často nereagují se všemi D+ erys • Jejich titry jsou obvykle nízké: (2 zkumavkově, 8 sloupcovou aglutinací, do 1 UI/ml) 25

Testování v případě nejasností o anti-D profylaxi Postup v případě, že neexistuje záznam o podání Ig anti-D nebo je titr zkumavkově 4 nebo sloupcovou aglutinací 16: • Stanovit titr anti-D každé 4 týdny až do 28. týdne • Po 28. týdnu stanovit titr 1 x za 14 dnů • Odhalit případnou „maskovanou“ klinicky významnou protilátku testováním s panelem D- diagnostických erys (pro případ transfuze krve) Poznámka: Odlišení aktivní a pasivní imunizace: • Při aktivní imunizaci – výskytu imunní anti-D je titr obvykle stabilní nebo se zvyšuje • Při pasivní imunizaci - po anti-D profylaxi titr protilátky klesá nebo je nedetekovatelná (po potvrzení již není nutné provádět titraci) 26

Tvorba anti-D po aktivní a pasivní imunizaci V případě aktivní imunizace: • Dochází ke tvorbě anti-D cca 4 týdny po expozici antigenem D • Vrchol sérologické detekce protilátky je po 6 -10 týdnech • Titry imunní protilátky zůstávají obvykle stabilní a zvyšují se po další stimulaci cizorodým antigenem V případě pasivní imunizace po podání anti-D profylaxe: • Můžeme pasivní anti-D detekovat NAT po dobu 8 i více týdnů • Citlivější metodou až 12 týdnů, vyjímečně několik měsíců • Vrchol sérologické detekce protilátky je cca 3 -7 dnů po podání Ig anti-D 27

Laboratorní testování „otce“ 28

Laboratorní testování otce 29

Laboratorní testování otce „pokračování“ • Vyšetřením otce se určuje riziko imunizace mezi matkou a plodem • Pokud jsou v séru/plazmě těhotné především anti-D, -c, -K, -E, pak je nutné zjistit, zda je otec pro daný antigen homozygot nebo heterozygot (pravděpodobnost pro plod) • Genotypování otce se provádí vyjímečně (například nejasné výsledky v případě těžkého HON či nedostupné genotypování plodu) • Je-li otec v daném antigenu negativní – lze sledovat těhotnou v režimu jako kdyby protilátky neměla (pozor otec nejistý !) • Testování séra/plazmy matky + ery otce se provádí k vyloučení imunologické reakce proti vzácně se vyskytujícímu antigenu V případě, kdy u matky nebyly zjištěny protilátky ale bylo zjištěno těžké HON (Při neshodě v AB 0 je třeba předem vysytit aglutininy v séru/plazmě matky opakovanou absorpcí při 4°C a 37°C na příslušné ery dárce. ) 30

Laboratorní testování plodu Testování AB 0 D se provádí vyjímečně jen v případě kordocentézy u suspektní anémie způsobené HON před IUT: • aglutinogeny 2 x, anti-D Ig. M DVI- 2 x různé klony, Dw NE • PAT (význam sporný, eluce a identifikace protilátky nepřináší nové informace) Genotypování plodu se provádí pokud je reálně dostupné: • Přednostně z plazmy matky PCR metodou • A to v případě klinicky významného titru protilátek u těhotné a je-li otec heterozygot v daném antigenu • RHD a RHCE genotypizace je možná poprvé v 15. -18. týdnu (gen RHD produkuje antigen D, gen RHCE antigeny C, c, E, e) • Genotypování Kell je možné poprvé ve 20. týdnu a je-li negativní, opakovat ve 28. týdnu. • V případě K pozitivity monitorovat plod 31

Poznámka: PCR (polymerase chain reaction) PCR-SSP s použitím sekvenčně specifických primerů (alelově skupinově specifických) PCR-SSOP využití hybridizace se sekvenčně specifickými oligonukleotidovými sondami PCR-RFLP stanovení polymorfismu v délce restrikčních fragmentů (za pomoci panelu restrikčních endonukleáz, vyhodnocení délky fragmentů DNA) 32

Poznámka: Jak probíhá PCR-SSP 1. Extrakce – izolace DNA z jádra leukocytů natrávením proteinázou K, precipitace DNA etanolem, rozpuštění DNA v d. H 2 O nebo TRISu. 2. Amplifikace DNA – PCR - polymerázová řetězová reakce je napodobení procesu replikace. Namnožení DNA vzorku. Amplifikují se specifické sekvence DNA za pomoci vždy 1 známého páru primerů, charakteristického pro daný antigen. Pokud se primery nenavážou, pak neodpovídají danému antigenu a k amplifikaci nedojde. Do reakce: DNA matrice (vyšetřovaný vzorek) + nukleotidy, stavební kameny DNA adenin (A), thymin (T), cytosin C, guanin(G) + Tag polymeráza syntetizující novou DNA. PCR probíhá ve 3 krocích, které se opakují až 40 x v cykléru aby se namnožil dostatek vyšetřované DNA: Denaturace: rozplétá se dvouřetězová DNA při 92 -96°C 1 min. Annealing (primerování): dané primery se vážou na rozpletenou DNA při 45 -72°C 2 min. Extenze (syntéza): vkládání nukleotidů A-T, C-G 3. Detekce DNA elektroforézou v agarovém gelu (+ vizualizace ethidium bromidem, vyzařuje v UV světle oranžové světlo) 4. Vyhodnocení 33

Vyšetření matky po porodu Rutinní testování po porodu nepřináší žádnou užitečnou informaci • Ani u matek s klinicky významnými protilátkami • Stanovení titru po porodu také nemá význam. Testování matky po porodu má význam v případě: • Že během těhotenství nebyla vůbec testována • Nebo protilátky u ní zjištěny nebyly ale přesto má novorozenec známky HON. V tomto případě se testuje sérum/plazma matky + erys otce za účelem odhalení reakce proti antigenu s nízkou frekvencí výskytu (AB 0 kompatibilita pro testování nutná, nebo je nutná absorpce aglutininů) • V případě předtransfuzního testování pro výběr krve k transfuzi matky nebo novorozence. Zkouška kompatibility u novorozence se přednostně provádí ze séra/plazmy matky, kde jsou také jediné protilátky, které se mohou vyskytnout i v séru/plazmě novorozence. 34

Vyšetření novorozence – AB 0 Rutinní vyšetření AB 0 všech novorozenců se nedoporučuje ani pokud je matka KS 0 (u všech novorozenců je ikterus monitorován) Vyšetření AB 0 se provádí pro případ transfuze: • U suspektního HON nebo AB 0 HON • Při výskytu klinicky významných protilátek u matky • Upřednostňuje se vyšetření z pupečníkové krve • Testují se aglutinogeny 2 x 35

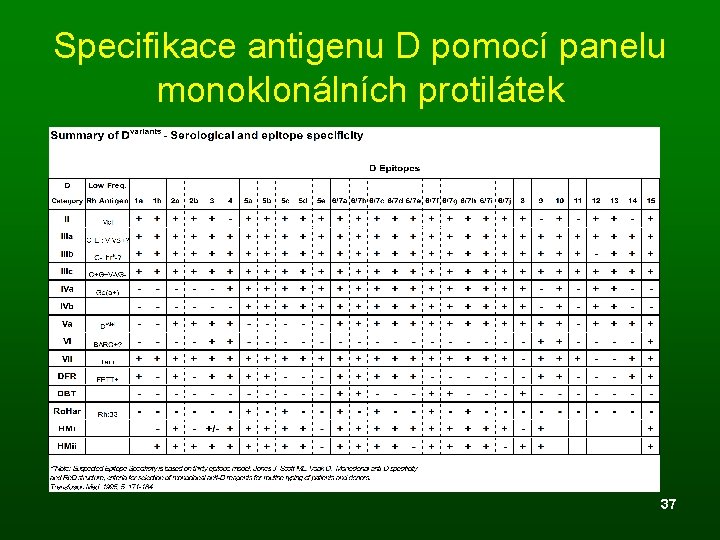
Vyšetření antigenu D Rh D pozitivní Rh D negativní Rh Dw/v (weak / variant) se stanoví nepřímým antiglobulinovým testem (NAT) Klasifikace variantních D antigenů pomocí panelu specifických monoklonálních diagnostik 36

Specifikace antigenu D pomocí panelu monoklonálních protilátek 37

Vyšetření antigenu D u novorozence Se provádí: • Z důvodu zajištění anti-D profylaxe u D- matek: (2 x anti-D Ig. M DVI-, Rh kontrola) • Pro případ transfuze krve u suspektního HON: - Kdy u matky jsou přítomny klinicky významné protilátky - Nebo je matka bez protilátek, ale novorozenec má známky HON Poznámka: • Testování Dw ani variantního D se nedoporučuje: protože není dokázáno, že by ery DVI+ senzibilizovaly matku (je znám 1 případ za 40 let a možná je spíše otázkou diagnostik) a navíc při pozitivitě PAT je testování nespolehlivé • Při nálezu slabých reakcí s anti-D diagnostiky a zjištění slabého D je třeba se po konzultaci vyjádřit k profylaxi anti-D 38

Screening nepravidelných protilátek u novorozence Screening protilátek u novorozence se provádí: • Pokud nebyl proveden u matky nebo není výsledek znám: provádí se běžným způsobem se 3 typy diagnostických erys LISS NAT Dále se provádí speciální testování v případě: • Kdy novorozenec má známky HON ale matka je bez protilátek • Je vhodné hledat protilátku proti antigenu s nízkou frekvencí výskytu Nejlépe již zmíněným testováním séra/plazmy matky a erys otce. V případě ABO inkompatibility mezi matkou a otcem se někdy provádí testování: Mezi sérem/plazmou novorozence a erys otce LISS NAT 39

PAT u novorozence • Se nedoporučuje provádět jako rutinní vyšetření ani u D+ ani D- matek • Zvláště ne po prenatální anti-D profylaxi Z tohoto důvodu může být u novorozenců PAT+ až v 3 -6% avšak bez klinického významu • Profylaktické podání anti-D Ig. G nezpůsobuje destrukci fetálních nebo novorozeneckých D+ ery 40

Vyšetření PAT u novorozence se provádí: • Pokud byla u matky prokázána potenciálně klinicky významná protilátka • Pokud u matky protilátky neprokázány nebyly ale novorozenec má klinické známky HON • V případě suspektního AB 0 HON • V případě, že u matky nebyl proveden screening protilátek ani během těhotenství a ni po porodu nebo není výsledek znám Poznámky: • Provádí se přednostně z pupečníkové krve sloupcovou aglutinací • PAT falešně negativní – technické chyby • PAT falešně pozitivní – silné chladové autoaglutininy 41

Vypovídající hodnota PAT u novorozence • Pozitivita PAT nepotvrzuje diagnózu HON U novorozence je nutné vyšetření Hb a sérového bilirubinu • Prediktivní hodnota pozitivity PAT je cca 23% • Naopak u PAT negativního mohou být příznaky těžkého HON a nejenom u AB 0 inkompatibility 42

Eluční test u novorozence s PAT + Eluce není nutná: • Pokud je protilátka u matky jednoznačně identifikována • U AB 0 HON kde je dostatečné vyšetření imunních protilátek anti-A, anti-B třídy Ig. G s erys A 1, B LISS NAT Eluce je vhodná: • V případě výskytu směsi protilátek k určení toho, která protilátka se podílí na HON. Ostatní Ig. G protilátky přenesené pasivně se neuplatňují, protože novorozenec korespondující antigen nemá. Způsobují však problémy při výběru kompatibilní krve v případě transfuze. • V případě suspektní reakce proti antigenu s nízkou frekvencí výskytu, kdy nejsou k dispozici výsledky vyšetření matky. Testuje se eluát proti erys otce LISS NAT. Metoda: Eluce kyselá, tepelná. Testuje se eluát LISS NAT s dg. ery nesoucími korespondující antigen 43

Vyšetření imunních protilátek anti-A, - B třídy Ig. G u novorozence • Je základním vyšetřením při podezření na AB 0 HON • Vyšetření metodou LISS NAT např. sloupcovou aglutinací s ery krevní skupiny A 1, B a jako kontrolní se používají ery 0 44

Test kompatibility u novorozence Provádí se v případě: • Transfuze erytrocytů • Výměnné transfuze modifikované kompatibilní plné krve Přednostně se provádí ze séra/plazmy matky, není-li k dispozici, lze použít vzorek novorozence (krev kompatibilní pro matku i novorozence) 45

Závěrem důležitá informace: • Při podezření na HON zaslat do laboratoře i vzorek matky ! • Myslet na odebrání vzorku matky a jeho transport současně při transportu novorozence do jiného zdravotnického zařízení ! 46

Děkuji za pozornost 47