Fyzika kondenzovanho stavu 2018 19 1 prezentace SLOUPY





















- Slides: 54

Fyzika kondenzovaného stavu (2018 -19) 1. prezentace

SLOUPY PODPÍRAJÍCÍ LIDSKOU CIVILIZACI - materiály - komunikace - informace

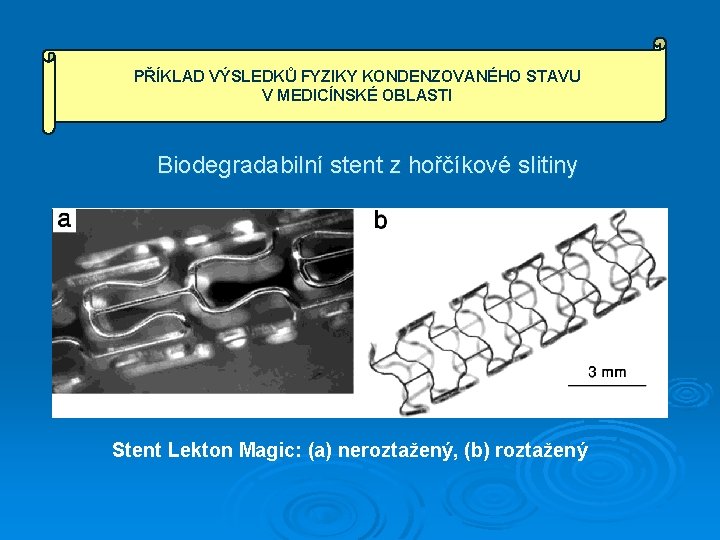
PŘÍKLAD VÝSLEDKŮ FYZIKY KONDENZOVANÉHO STAVU V MEDICÍNSKÉ OBLASTI Biodegradabilní stent z hořčíkové slitiny Stent Lekton Magic: (a) neroztažený, (b) roztažený

Čokoláda a její krystaly - atraktivní oblast výzkumu… kakaový tuk - krystaly triglyceridu

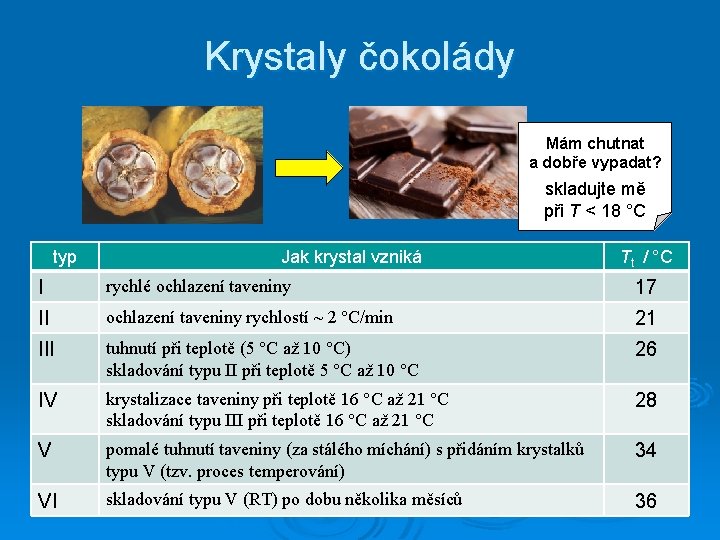
Krystaly čokolády Mám chutnat a dobře vypadat? skladujte mě při T < 18 °C typ Jak krystal vzniká Tt / °C I rychlé ochlazení taveniny 17 II ochlazení taveniny rychlostí ~ 2 °C/min 21 III tuhnutí při teplotě (5 °C až 10 °C) skladování typu II při teplotě 5 °C až 10 °C 26 IV krystalizace taveniny při teplotě 16 °C až 21 °C skladování typu III při teplotě 16 °C až 21 °C 28 V pomalé tuhnutí taveniny (za stálého míchání) s přidáním krystalků typu V (tzv. proces temperování) 34 VI skladování typu V (RT) po dobu několika měsíců 36

Co jsou a jak vznikají kondenzované látky ?

Kondenzace a tuhnutí Ø vysoká teplota - zanedbatelný vliv přitažlivých sil - Ek (energie tepelného pohybu částic) převažuje Ø snižování teploty - přitažlivé síly začínají nabývat na důležitosti - molekulární páry (dvojice) zůstávají déle pohromadě - korelace v pohybu molekul - krátkodobě existující klastry molekul

Kondenzace a tuhnutí Ø kondenzační teplota - významná korelace pohybu molekul (vznik kapaliny) - energie přitažlivé interakce Ek - vliv energie odpudivých sil - krátkodosahové uspořádávání molekul (přeuspořádání po uplynutí relaxační doby) - přitažlivé interakce co nejvíce „stěsnávají“ molekuly - odpudivé interakce zajišťují minimální separaci Ø další snižování teploty - uspořádávání molekul (resp. atomů, iontů) - tuhnutí vznik pevné látky (PL)

Dva typy tuhnutí kapalin Ø krystalizace (Tt) Ø tuhnutí v důsledku rychlého zvýšení viskozity při jejím ochlazení - amorfní látky (vosk, asfalt, . . . ) - sklo (má schopnost krystalizace, ale viskozita roste s poklesem teploty tak rychle, že látka ztuhne dříve, než stačí zkrystalizovat)

Kondenzované látky dělení na kapalné a pevné látky Ø kapalné - newtonovské kapaliny - nenewtonowské kapaliny Ø pevné (hookovské, nehookovské) - krystalické - amorfní - polymery Ø skla

Kondenzované látky dělení na pevné a měkké látky Ø pevné látky (hookovské, nehookovské) - krystalické - amorfní Ø měkké látky (MKL) - mýdlo, kečup, tvaroh, barvy. . . ) - polymery - kapalné krystaly - kapaliny (newtonovské, nenewtonovské)

Krystalické látky

Struktura krystalických látek

Johannes Kepler (1611) O šestiúhelné sněhové vločce poutavé čtení o „ničem“ -v jistém smyslu první krystalografická práce - napsáno roku 1610 v Praze - vyšlo 1611 ve Frankfurtu nad Mohanem

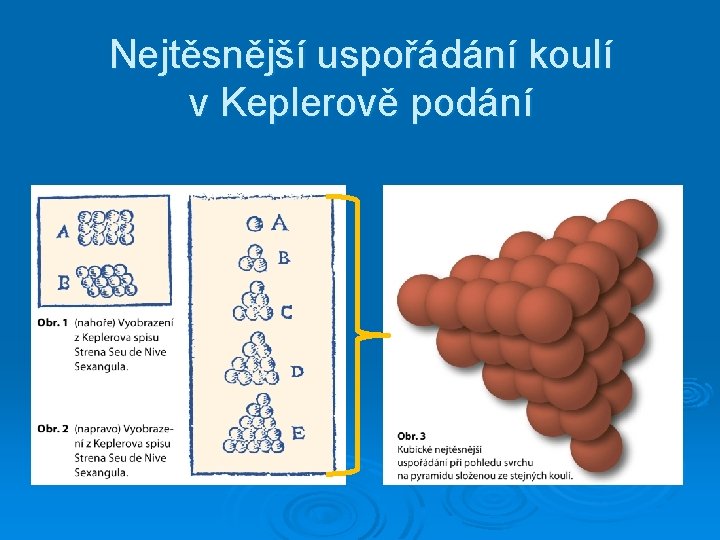
Nejtěsnější uspořádání koulí v Keplerově podání

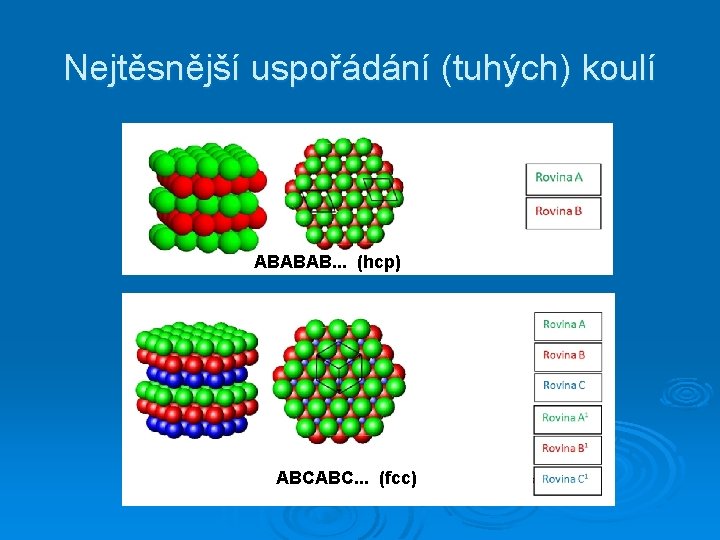
Nejtěsnější uspořádání (tuhých) koulí ABABAB. . . (hcp) ABCABC. . . (fcc)

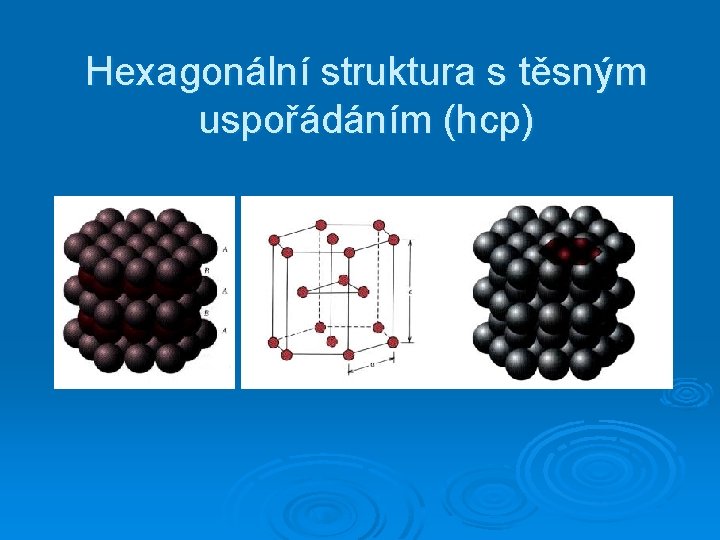
Hexagonální struktura s těsným uspořádáním (hcp)

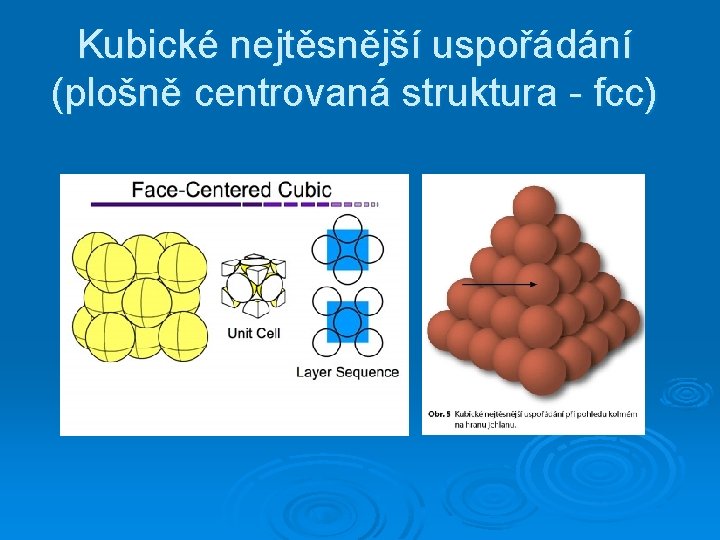
Kubické nejtěsnější uspořádání (plošně centrovaná struktura - fcc)

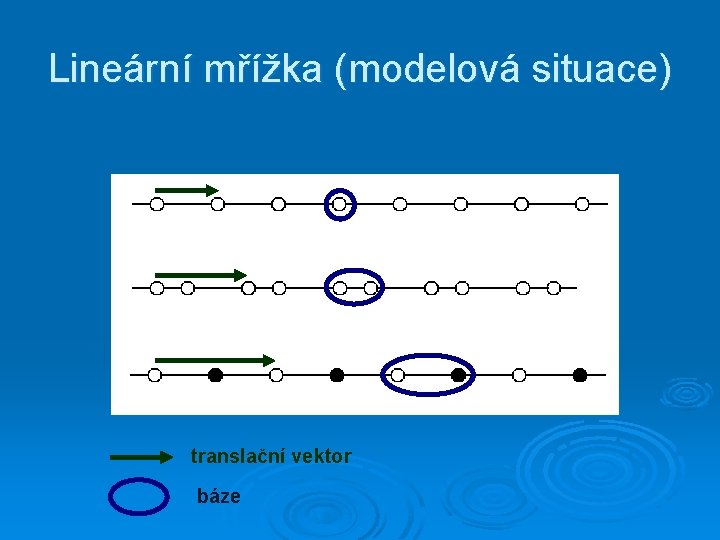
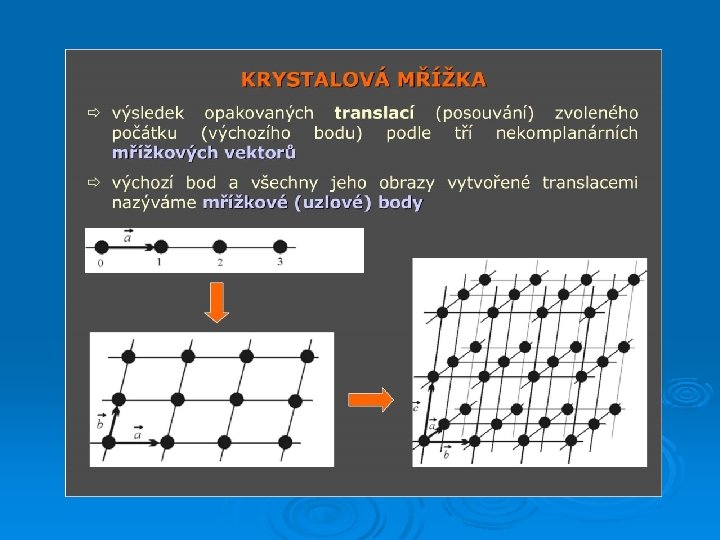
Lineární mřížka (modelová situace) translační vektor báze


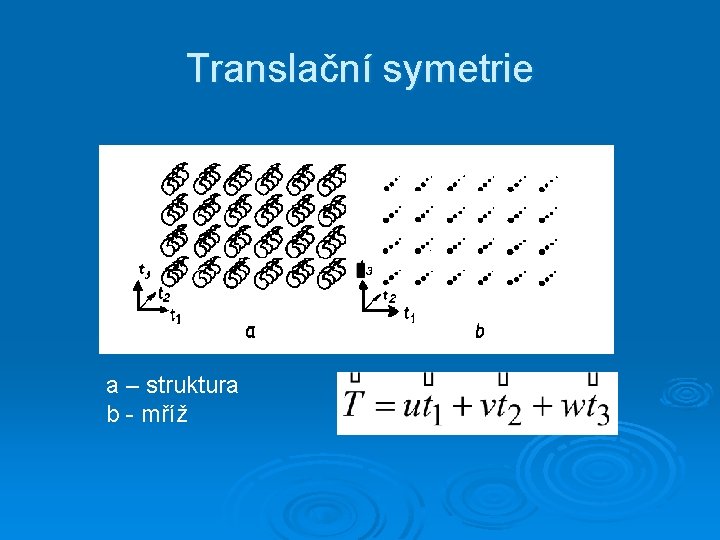
Translační symetrie a – struktura b - mříž

Základní prvky symetrie krystalů Ø střed inverze Ø rovina souměrnosti (zrcadlení) Ø n-četná rotační osa symetrie Ø n-četná inverzní osa rotace Ø n-četná šroubová rotační osa symetrie Ø translační rovina souměrnosti (skluzová rovina)

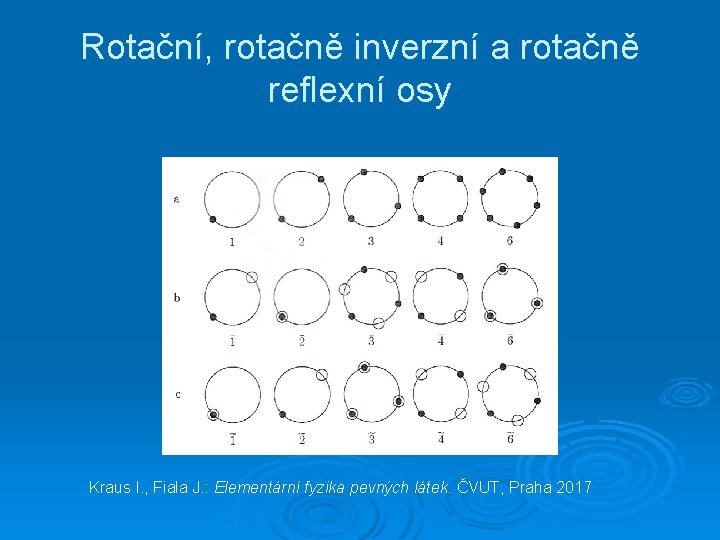
Rotační, rotačně inverzní a rotačně reflexní osy Kraus I. , Fiala J. : Elementární fyzika pevných látek. ČVUT, Praha 2017

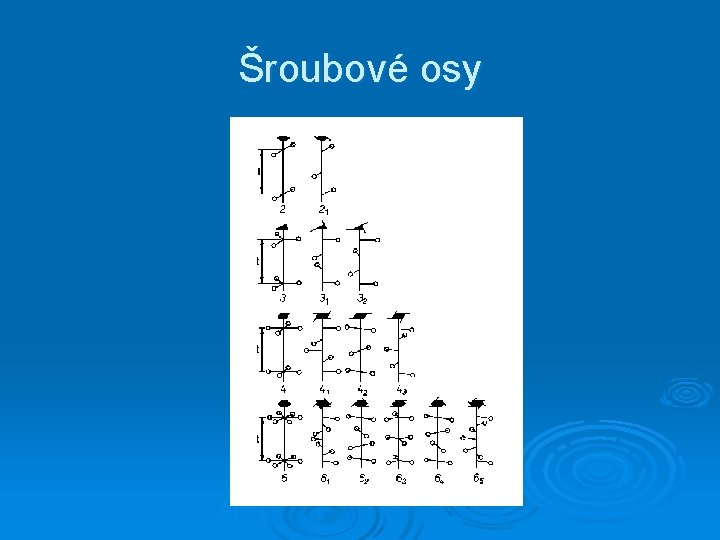
Šroubové osy

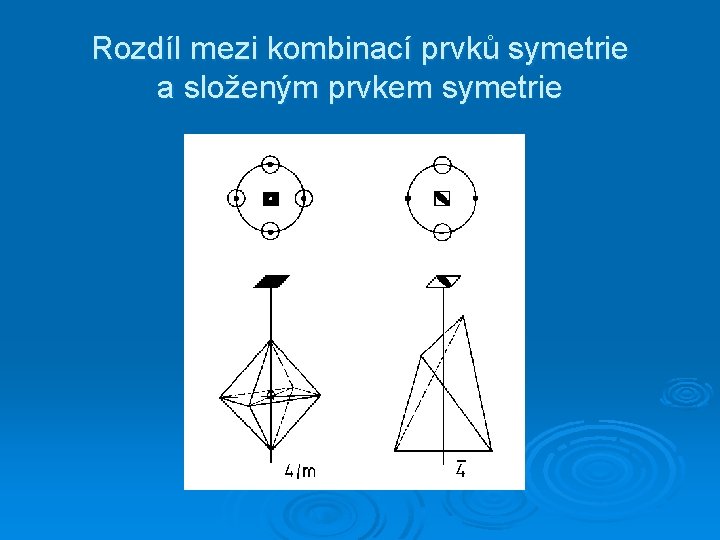
Rozdíl mezi kombinací prvků symetrie a složeným prvkem symetrie

Značení prvků souměrnosti Hermannova – Mauguinova symbolika a grafické značky prvků souměrnosti ve směru kolmém k nákresně. Kraus I. , Fiala J. : Elementární fyzika pevných látek. ČVUT, Praha 2017

Rozdělení operací symetrie prvního druhu druhého druhu zavřené otevřené rotace zrcadlení translace inverze rotace skluzný pohyb šroubový pohyb rotační inverze šroubový pohyb skluzný pohyb rotační inverze kongruentní L L, P P enantiomorfní L P, P L několikrát aplikováno návrat k výchozímu bodu nevrátíme se k výchozímu bodu

K čemu přítomnost určitých prvků symetrie používáme? Ø klasifikační kritérium pro rozdělení krystalových tvarů, krystalových struktur a prostorových mřížek do určitých kategorií 14 Bravaisových mřížek 7 krystalografických soustav 32 bodových grup (oddělení souměrnosti) 230 prostorových grup

Prvky symetrie neobsahující translaci střed inverze - ke každému atomu s průvodičem R existuje identický atom s průvodičem –R rovina souměrnosti (m) - rovina vůči níž jsou obě části krystalové struktury vzájemným zrcadlovým obrazem n-četná rotační osa - otočením o úhel 2 /n se krystal ztotožní sám se sebou n-četná inverzní osa rotace - po rotaci o úhel 2 /n kolem této osy a po následující inverzi splyne krystal sám se sebou

Prvky symetrie obsahující translaci n-četná šroubová osa - otočení o 2 /n a následující translace o c/n (kde c je nejmenší vzdálenost mezi uzlovými body ve směru osy) translační rovina souměrnosti (skluzová rovina) - krystalová struktura přechází sama v sebe operací zrcadlení a s ní spojenou translací ve směru rovnoběžném s touto rovinou zrcadlení

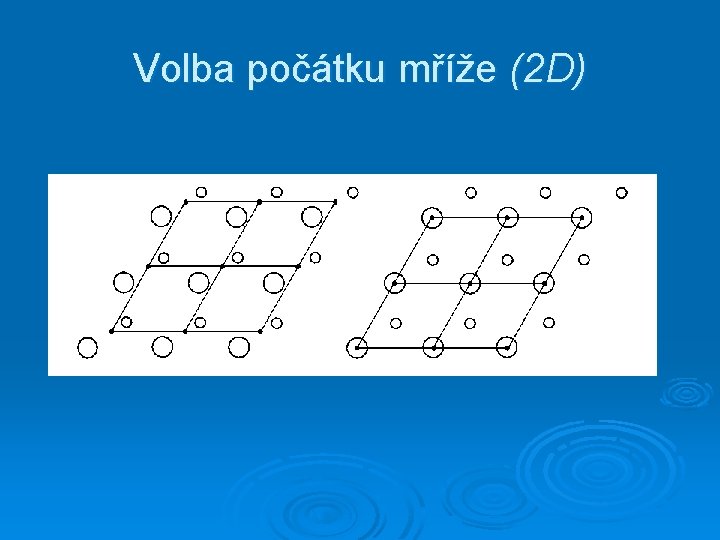
Volba počátku mříže (2 D)

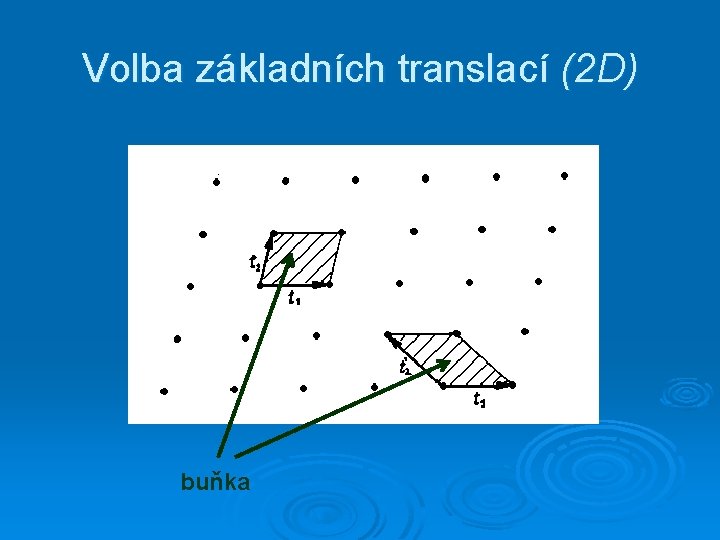
Volba základních translací (2 D) buňka

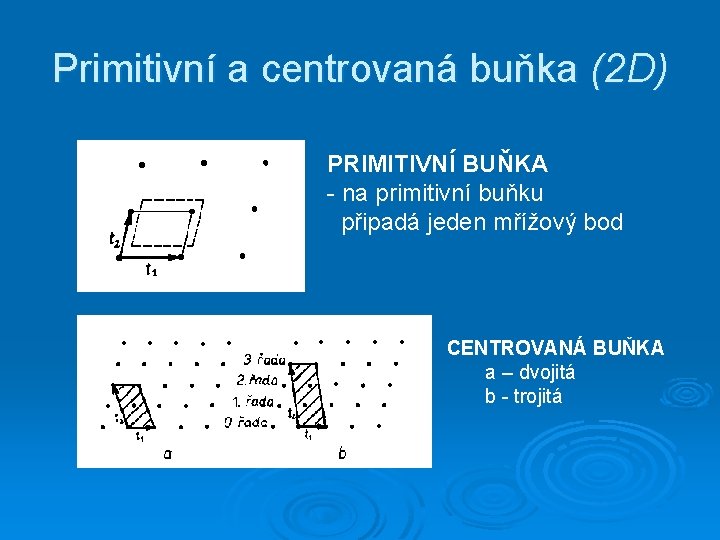
Primitivní a centrovaná buňka (2 D) PRIMITIVNÍ BUŇKA - na primitivní buňku připadá jeden mřížový bod CENTROVANÁ BUŇKA a – dvojitá b - trojitá

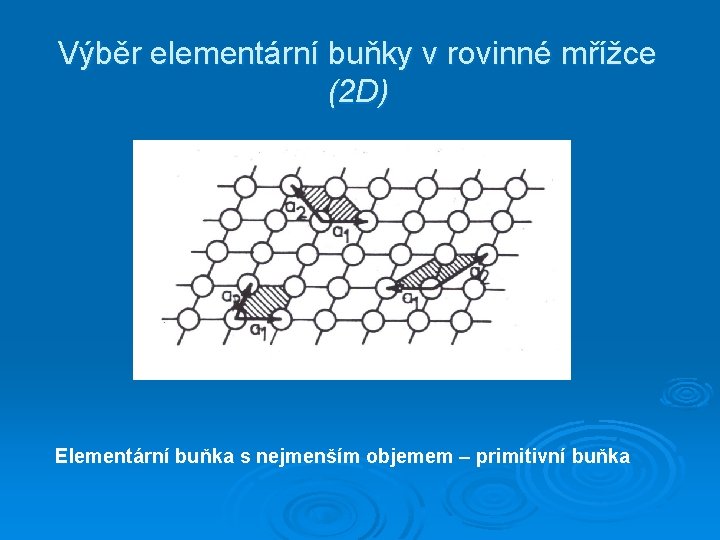
Výběr elementární buňky v rovinné mřížce (2 D) Elementární buňka s nejmenším objemem – primitivní buňka

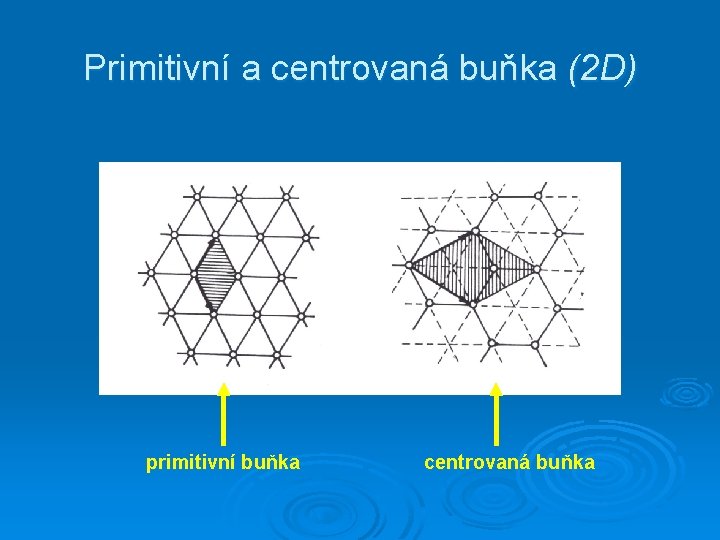
Primitivní a centrovaná buňka (2 D) primitivní buňka centrovaná buňka

Rovinné (Bravaisovy) mřížky Blakemore J. S. : Solid State Physics. Cambridge University Press 1985.

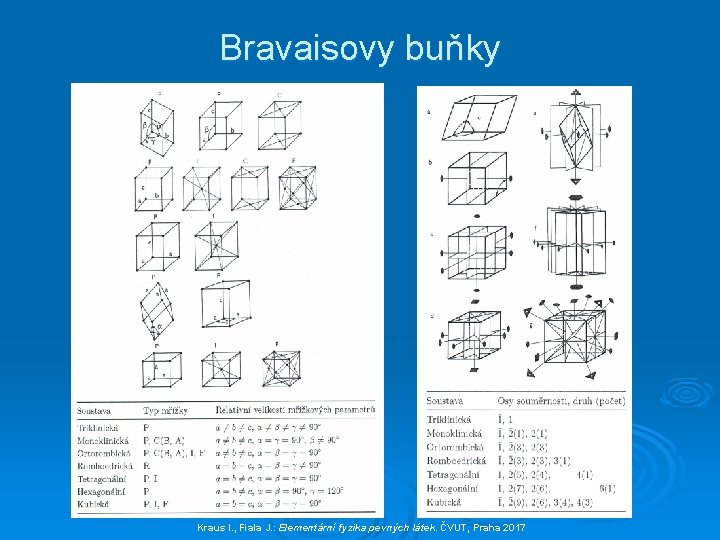
Bravaisovy buňky (3 D) Bravaisova pravidla pro výběr základní buňky 1. Počet pravých úhlů v základní buňce musí být maximální. 2. Symetrie základní buňky musí být shodná se symetrií celé mřížky. 3. Při dodržení předchozích podmínek musí být objem základní buňky minimální. 4. V případě, kdy symetrie nemůže rozhodnout, vybírá se základní buňka, tak aby její hrany byly co nejkratší.

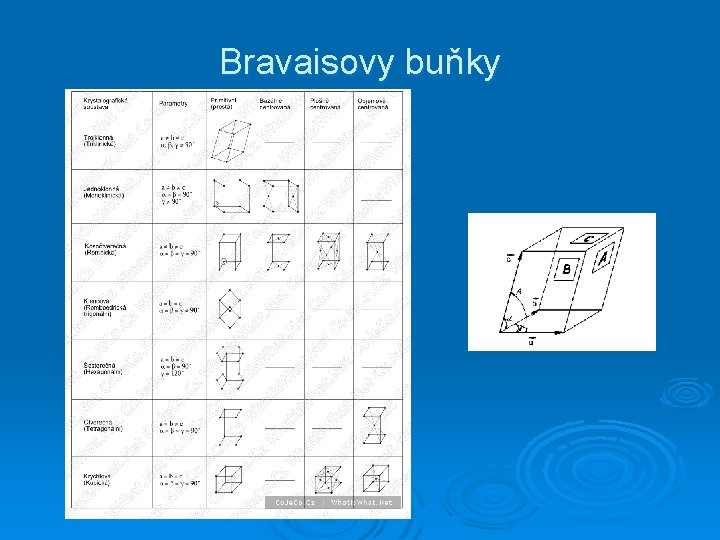
Bravaisovy buňky

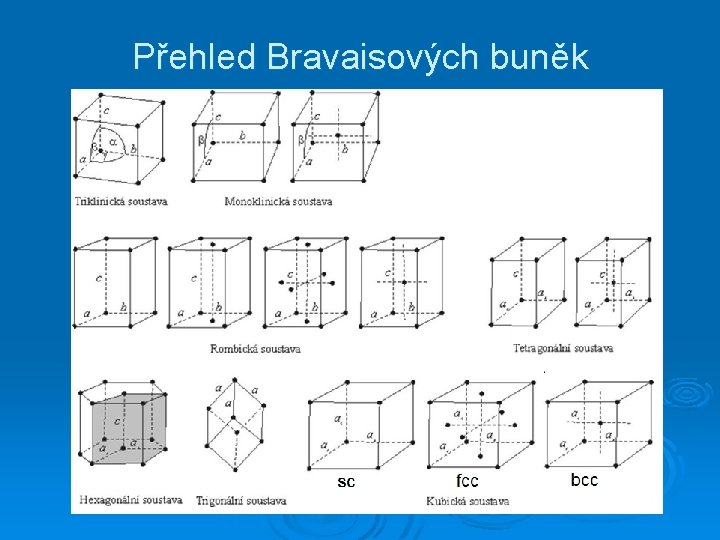
Přehled Bravaisových buněk

Bravaisovy buňky Kraus I. , Fiala J. : Elementární fyzika pevných látek. ČVUT, Praha 2017

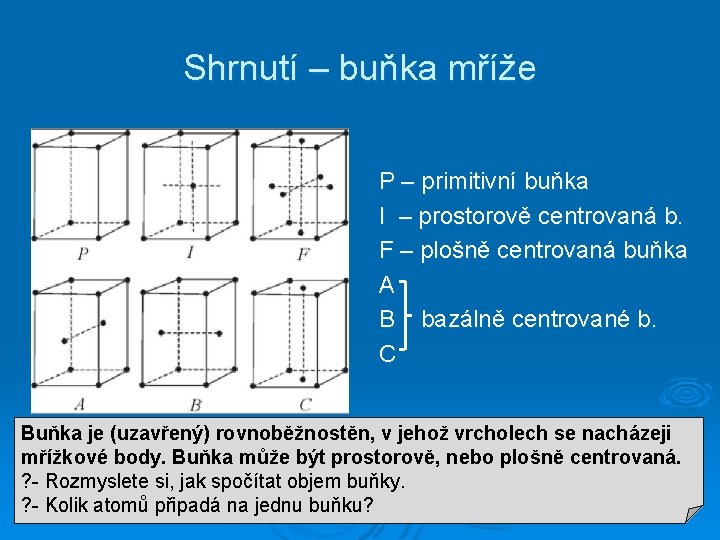
Shrnutí – buňka mříže P – primitivní buňka I – prostorově centrovaná b. F – plošně centrovaná buňka A B bazálně centrované b. C Buňka je (uzavřený) rovnoběžnostěn, v jehož vrcholech se nacházeji mřížkové body. Buňka může být prostorově, nebo plošně centrovaná. ? - Rozmyslete si, jak spočítat objem buňky. ? - Kolik atomů připadá na jednu buňku?

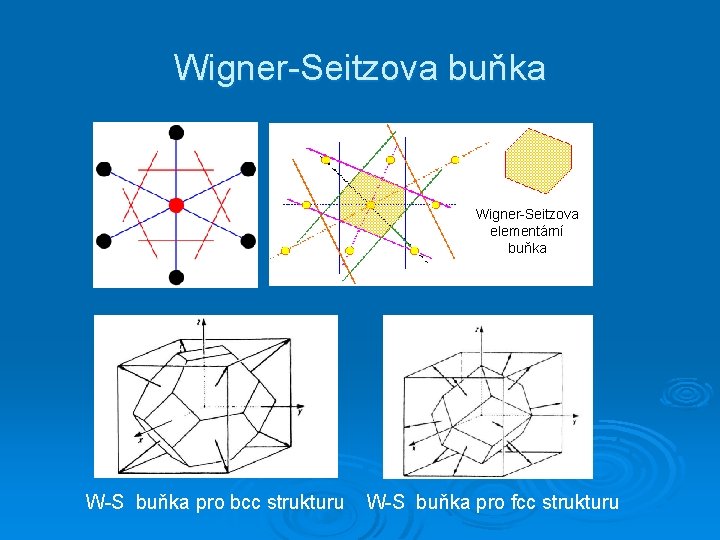
Wigner-Seitzova buňka Wigner-Seitzova elementární buňka W-S buňka pro bcc strukturu W-S buňka pro fcc strukturu

Symetrie Bravaisových buněk krystalová soustava minimální symetrie triklinická (trojklonná) žádná monoklinická (jednoklonná) jedna 2 -četná osa podél c ortorombická (rombická, kosočtverečná) tři 2 -četné osy podél a, b , c tetragonální (čtverečná) jedna 4 -četná osa podél c kubická (izometrická) čtyři 3 -četné osy podél tělesových úhlopříček krychle hexagonální (šesterečná) jedna 6 -četná osa podél c trigonální (romboedrická, klencová) jedna 3 -četná osa podél hexagon. buňky

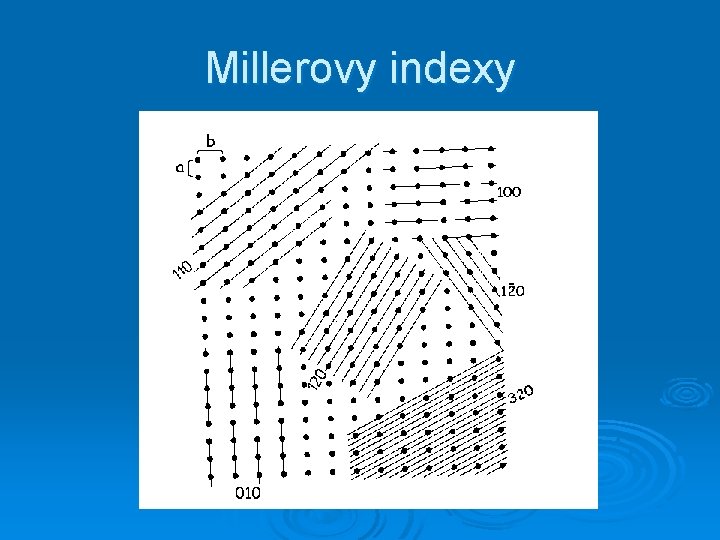
Millerovy indexy

Millerovy indexy mřížových rovin

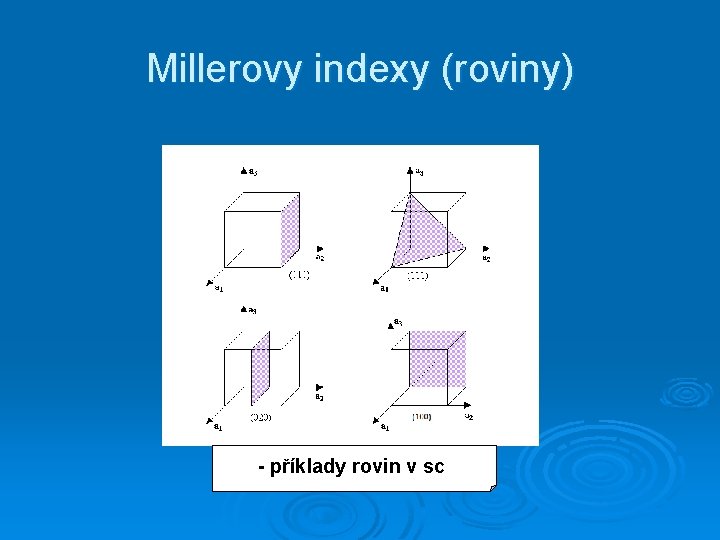
Millerovy indexy (roviny) - příklady rovin v sc

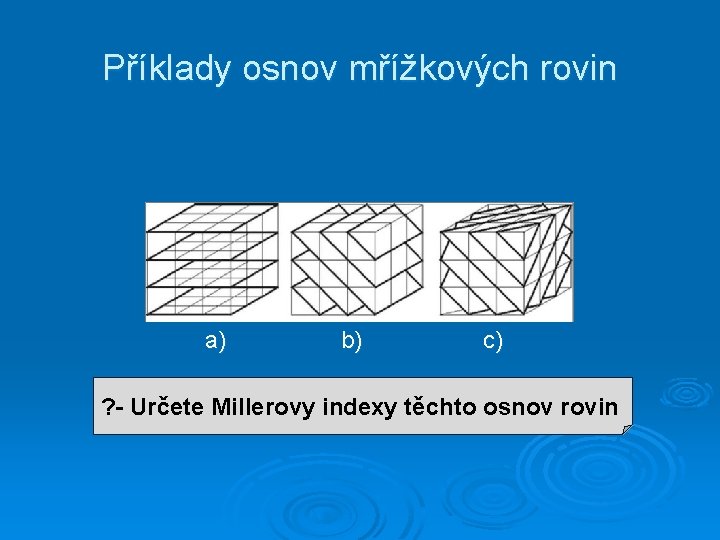
Příklady osnov mřížkových rovin a) b) c) ? - Určete Millerovy indexy těchto osnov rovin

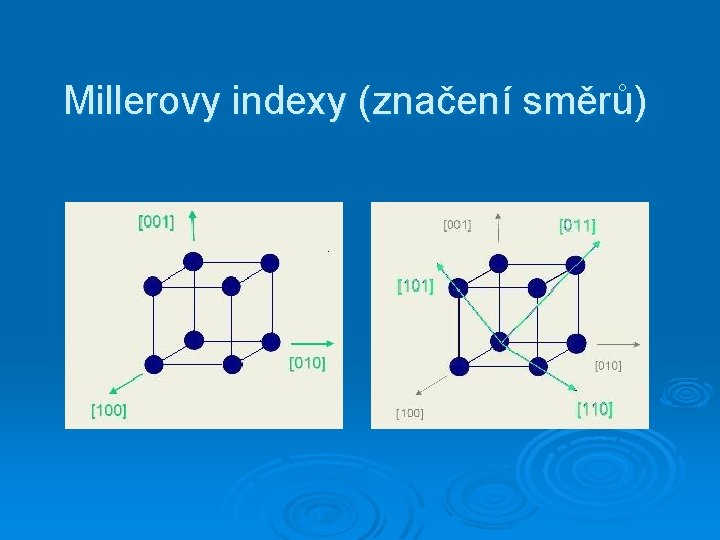
Millerovy indexy (značení směrů)

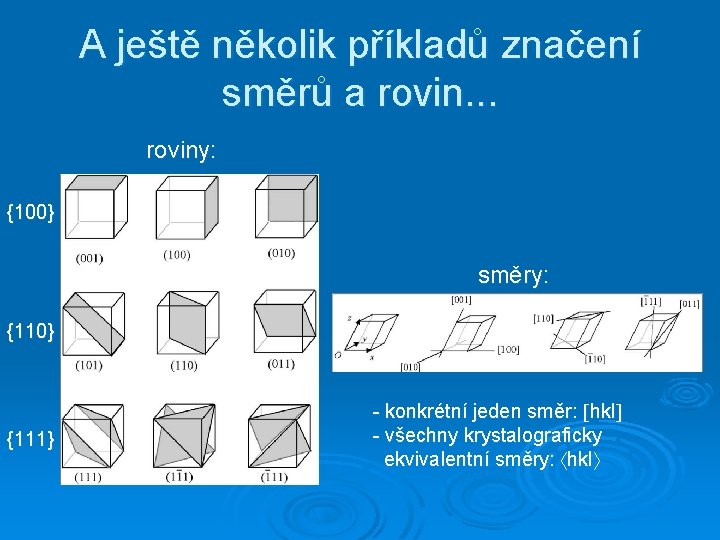
A ještě několik příkladů značení směrů a rovin. . . roviny: {100} směry: {110} {111} - konkrétní jeden směr: hkl - všechny krystalograficky ekvivalentní směry: hkl

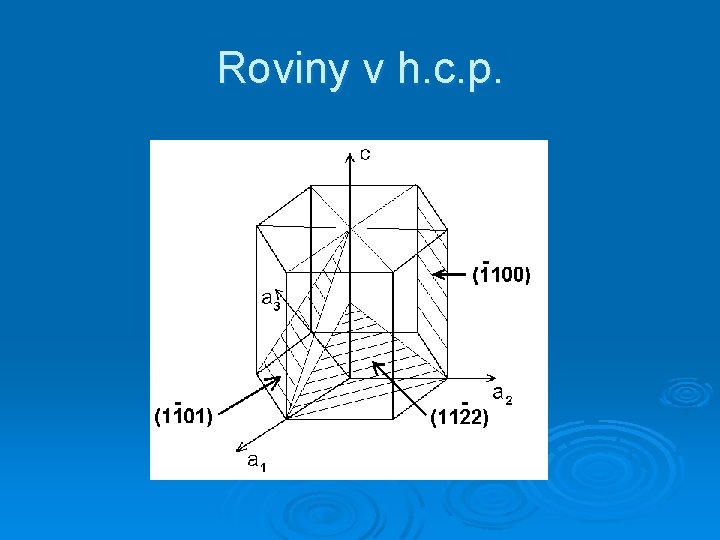
Roviny v h. c. p.

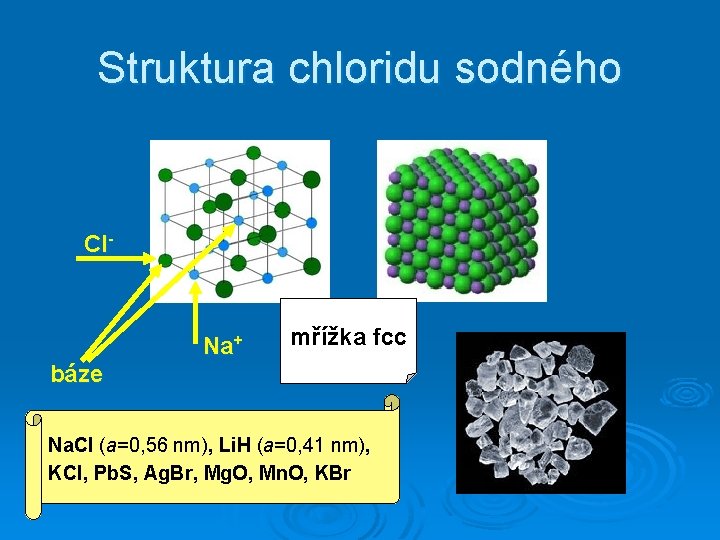
Struktura chloridu sodného Cl- Na+ mřížka fcc báze Na. Cl (a=0, 56 nm), Li. H (a=0, 41 nm), KCl, Pb. S, Ag. Br, Mg. O, Mn. O, KBr

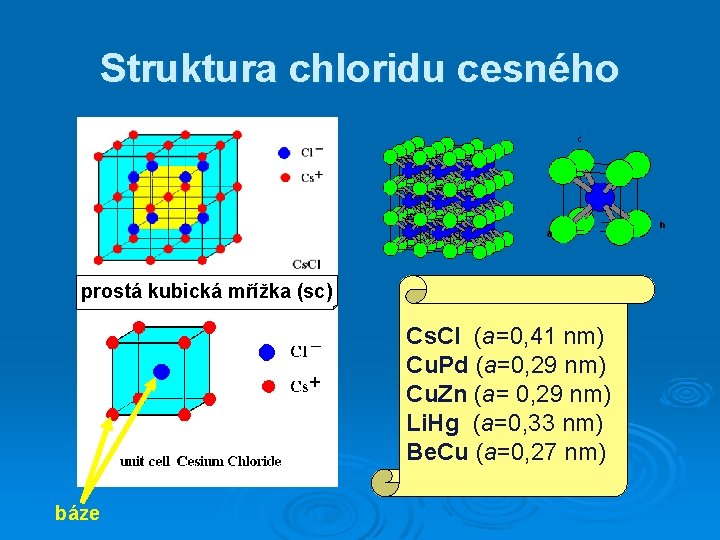
Struktura chloridu cesného prostá kubická mřížka (sc) Cs. Cl (a=0, 41 nm) Cu. Pd (a=0, 29 nm) Cu. Zn (a= 0, 29 nm) Li. Hg (a=0, 33 nm) Be. Cu (a=0, 27 nm) báze

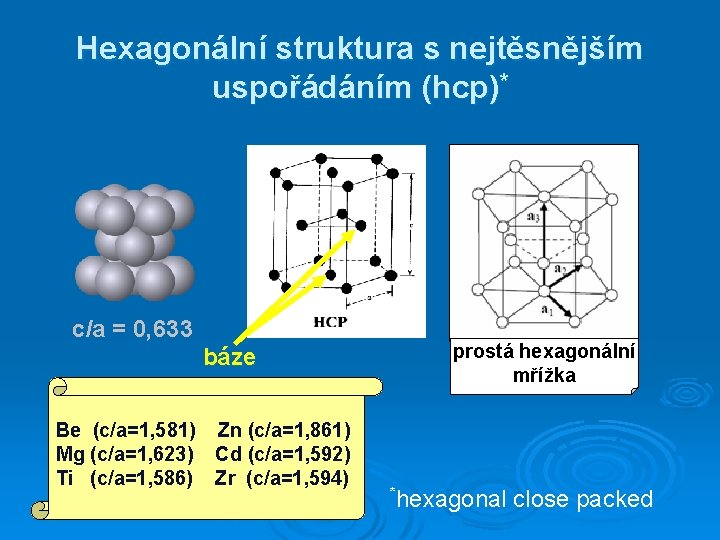
Hexagonální struktura s nejtěsnějším uspořádáním (hcp)* c/a = 0, 633 báze Be (c/a=1, 581) Zn (c/a=1, 861) Mg (c/a=1, 623) Cd (c/a=1, 592) Ti (c/a=1, 586) Zr (c/a=1, 594) prostá hexagonální mřížka *hexagonal close packed

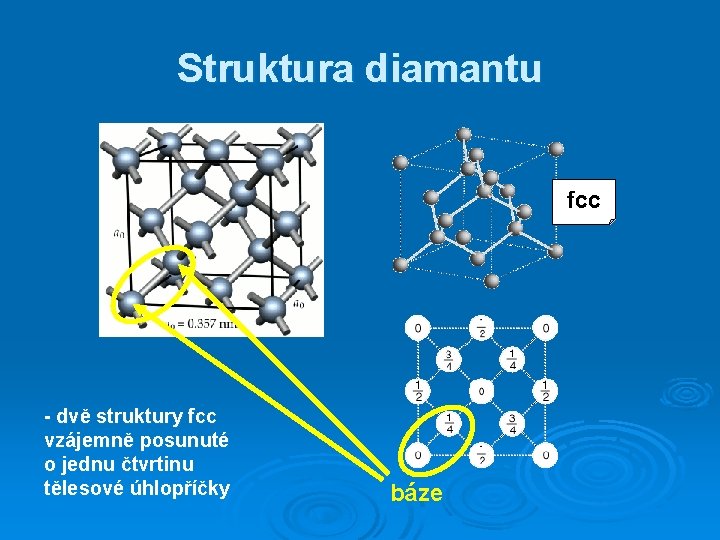
Struktura diamantu fcc - dvě struktury fcc vzájemně posunuté o jednu čtvrtinu tělesové úhlopříčky báze