FIZYKA III MEL Fizyka jdrowa i czstek elementarnych
















![Energia wiązania EB/A [Me. V] 10 8 6 4 2 50 100 150 200 Energia wiązania EB/A [Me. V] 10 8 6 4 2 50 100 150 200](https://slidetodoc.com/presentation_image_h/ab24dc06aa6574f2cc14e7b46c54f6c2/image-30.jpg)
![liczby magiczne EB/A [Me. V] 2 8 20 28 50 82 126 10 8 liczby magiczne EB/A [Me. V] 2 8 20 28 50 82 126 10 8](https://slidetodoc.com/presentation_image_h/ab24dc06aa6574f2cc14e7b46c54f6c2/image-32.jpg)
- Slides: 32

FIZYKA III MEL Fizyka jądrowa i cząstek elementarnych Wykład 1 – własności jąder atomowych


Odkrycie jądra atomowego Rutherford (1911) Ernest Rutherford (1871 -1937) R 10 fm 1908

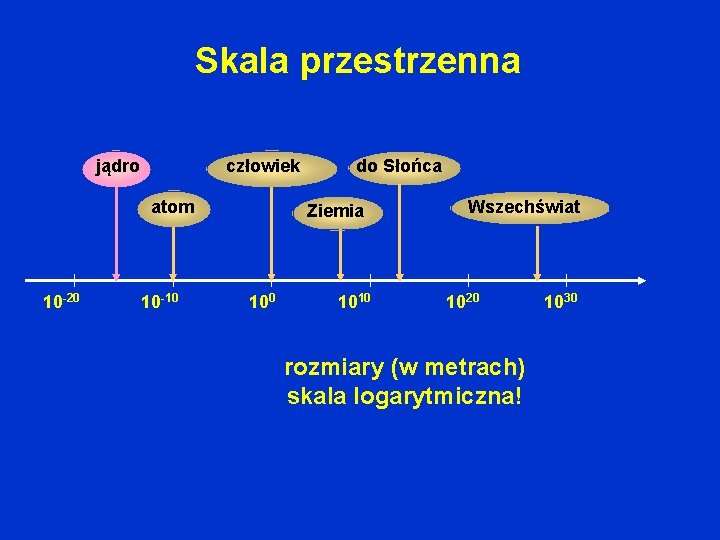
Skala przestrzenna jądro człowiek atom 10 -20 10 -10 do Słońca Ziemia 100 1010 Wszechświat 1020 rozmiary (w metrach) skala logarytmiczna! 1030

Cząstki i oddziaływania • jądra atomowe • składniki jąder: protony i neutrony (nukleony) • liczne cząstki produkowane w wyniku procesów , w których uczestniczą nukleony lub jądra Oddziaływania: • grawitacyjne • słabe • elektromagnetyczne • silne

Trzy grupy cząstek elementarnych Nośniki oddziaływań: • fotony (oddz. elektromagn. ) • bozony W i Z (oddz. słabe) • gluony (oddz. silne) • grawitony? (oddz. grawitacyjne) Leptony: Hadrony: • elektrony i neutrina elektronowe • nukleony • miony i neutrina mionowe • mezony • taony i neutrina taonowe • …. (kilkaset cząstek)

Masy obiektów subatomowych Masy wyrażamy w jednostkach energii: Jednostka energii – elektronowolt: 1 e. V = 1, 602 10 -19 C V = 1, 602 10 -19 J Jednostka masy: Me. V/c 2 lub Me. V (c = 1) Masy nuklidów wyrażamy w atomowych jednostkach masy u: 1 u= masy obojętnego atomu węgla

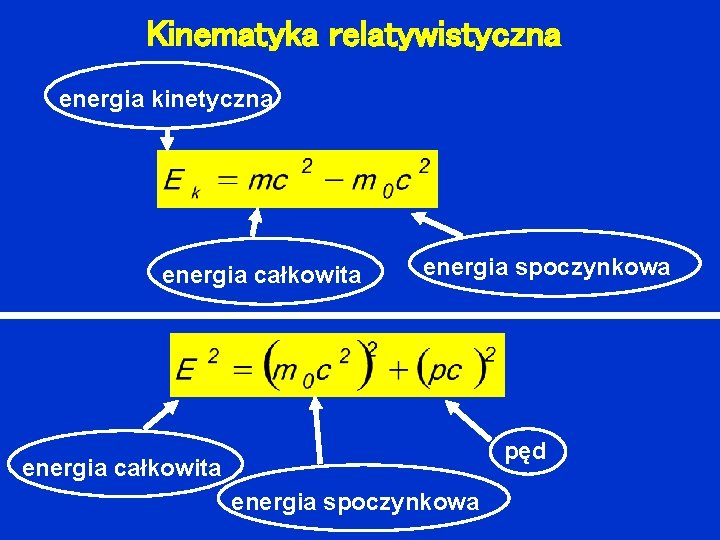
Kinematyka relatywistyczna energia kinetyczna energia całkowita energia spoczynkowa pęd energia całkowita energia spoczynkowa

Falowe własności materii Długość fali de Broglie’a: Zasada nieoznaczności:

Pustka materii Xe tylko tu. . . _ _ _ ośrodek ciągły (tu ciekły ksenon) jest prawie pusty!

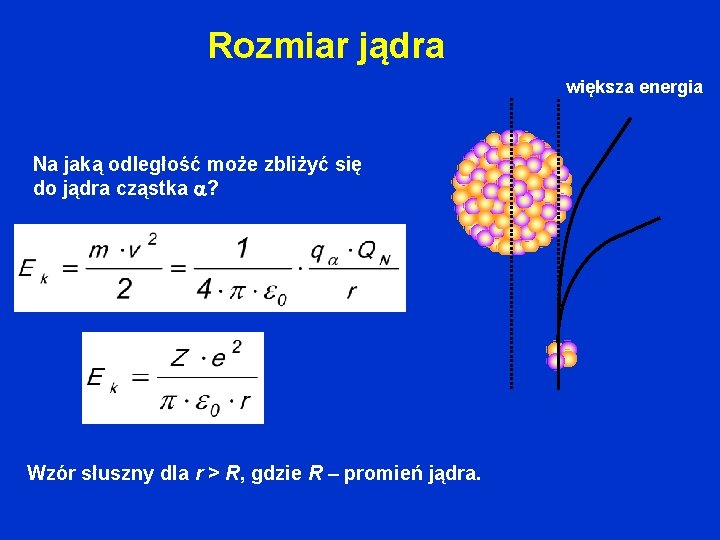
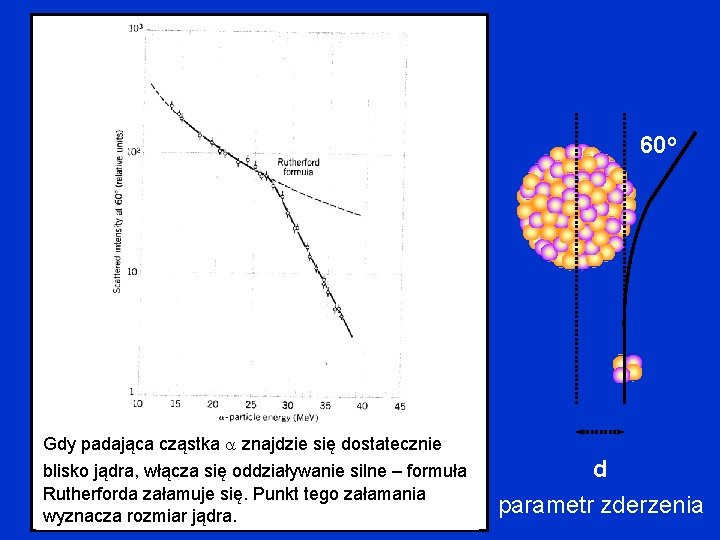
Rozmiar jądra większa energia Na jaką odległość może zbliżyć się do jądra cząstka ? Wzór słuszny dla r > R, gdzie R – promień jądra.

60 o Gdy padająca cząstka znajdzie się dostatecznie blisko jądra, włącza się oddziaływanie silne – formuła Rutherforda załamuje się. Punkt tego załamania wyznacza rozmiar jądra. d parametr zderzenia

Rozmiar jądra Dla jądra węgla: Ek = 5, 1 Me. V R = 3, 4 10 -15 m Dla jądra aluminium: Ek = 9, 0 Me. V R = 4, 1 10 -15 m Rozmiar jądra: 10 -15 m Rozmiar atomu: 10 -10 m

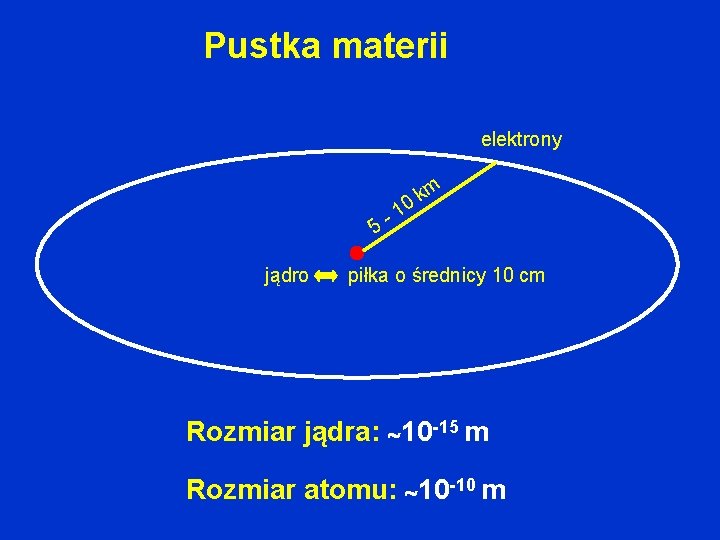
Pustka materii elektrony m k 0 1 5 jądro piłka o średnicy 10 cm Rozmiar jądra: 10 -15 m Rozmiar atomu: 10 -10 m

Świat jądrowy ładunek: q = Ze e = 1. 6 · 10 -19 C energia jonizacji atomu wodoru – 13. 6 e. V energia separacji nukleonu z jądra – 8. 5 Me. V Skala gęstości w mikro- i makroświecie: materia jądrowa biały gwiazda ciało stałe karzeł neutronowa 10 -5 100 105 1010 gęstość [g/cm 3] czarna dziura 1015 1020

Składniki jądra Ładunek jądra = n·e+ Masa jądra około dwukrotnie większa niż masa protonów. Nukleony – protony i neutrony

Elektrony w jądrze? Hipoteza: jądro zawiera A protonów i A – Z elektronów zasada nieoznaczoności (masa elektronu 0. 5 Me. V) więc nie! oraz analiza spinów jąder… np: spin jądra 147 N jest całkowity (eksperyment) podczas, gdy suma spinów (połówkowych) 14 protonów i 7 elektronów byłaby połówkowa!

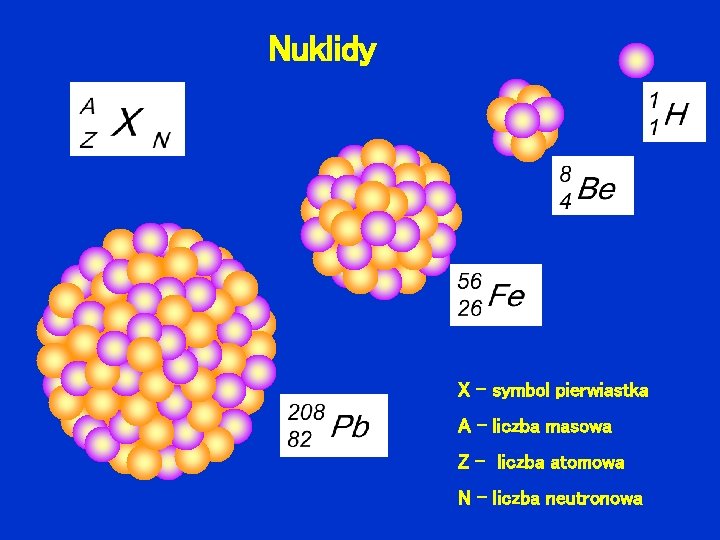
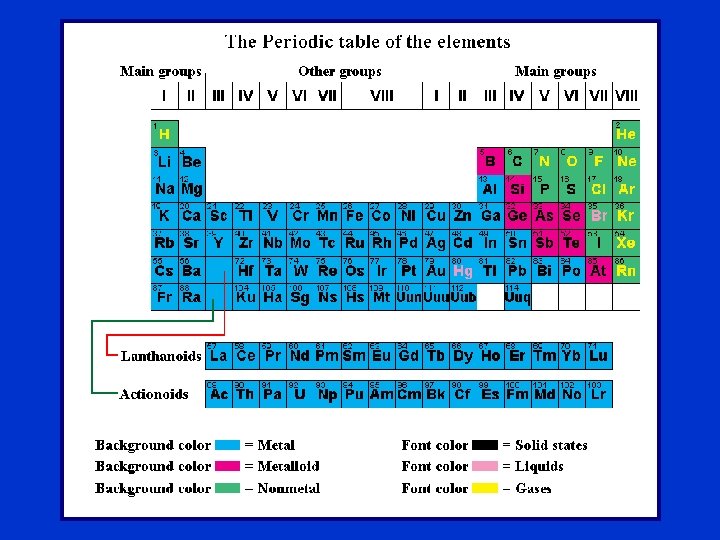
Nuklidy X - symbol pierwiastka A - liczba masowa Z - liczba atomowa N - liczba neutronowa

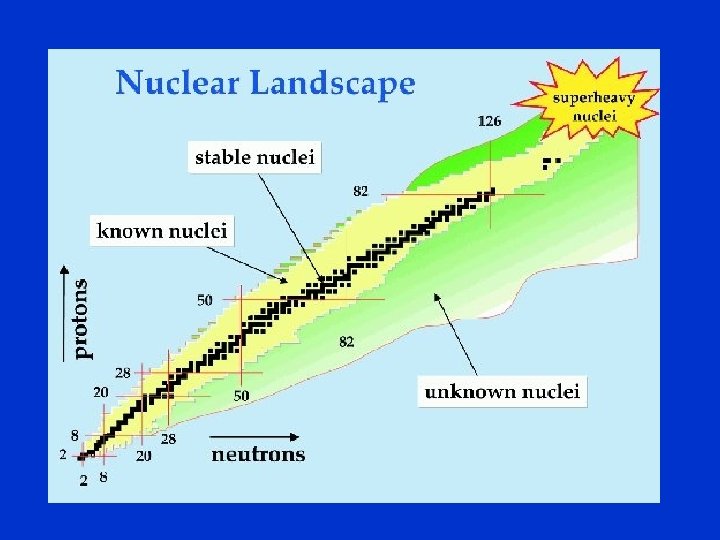
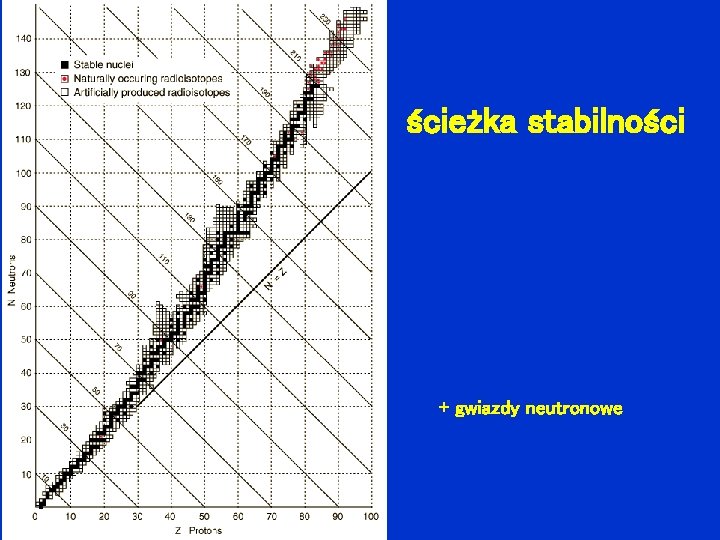
ścieżka stabilności + gwiazdy neutronowe


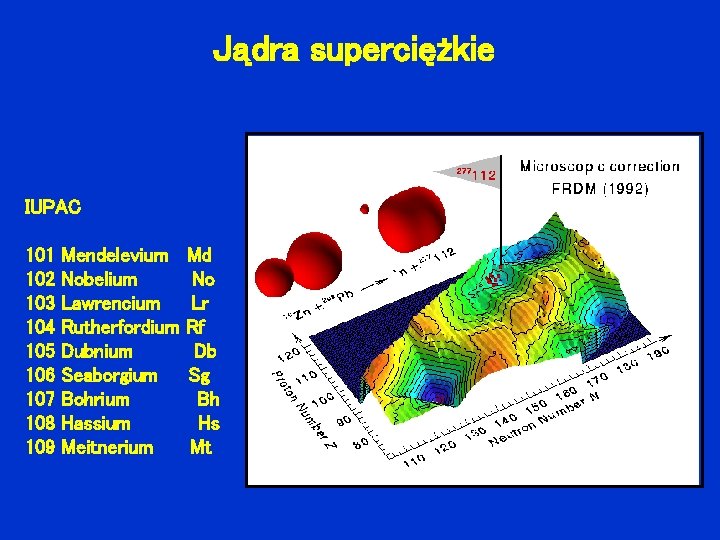
Jądra superciężkie IUPAC 101 102 103 104 105 106 107 108 109 Mendelevium Nobelium Lawrencium Rutherfordium Dubnium Seaborgium Bohrium Hassium Meitnerium Md No Lr Rf Db Sg Bh Hs Mt

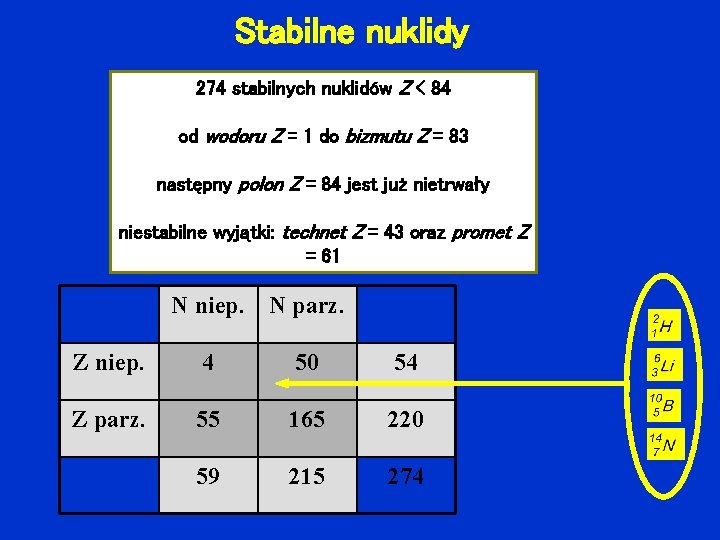
Stabilne nuklidy 274 stabilnych nuklidów Z < 84 od wodoru Z = 1 do bizmutu Z = 83 następny polon Z = 84 jest już nietrwały niestabilne wyjątki: technet Z = 43 oraz promet Z = 61 N niep. N parz. Z niep. 4 50 54 Z parz. 55 165 220 59 215 274

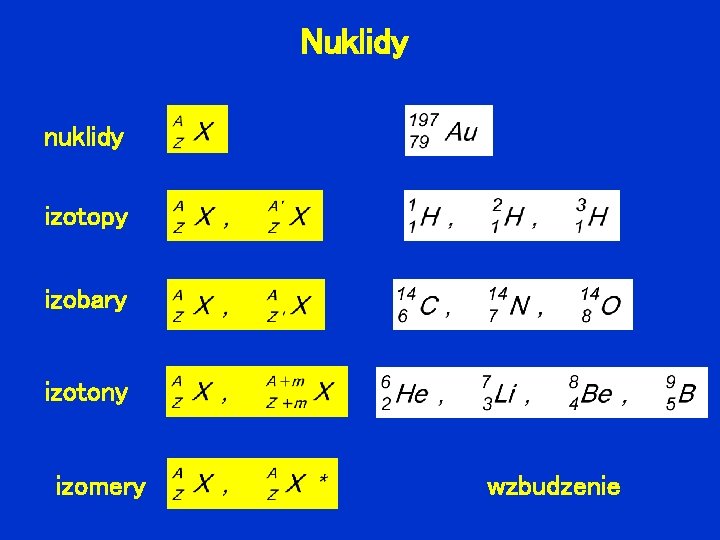
Nuklidy nuklidy izotopy izobary izotony izomery wzbudzenie

Masy jąder

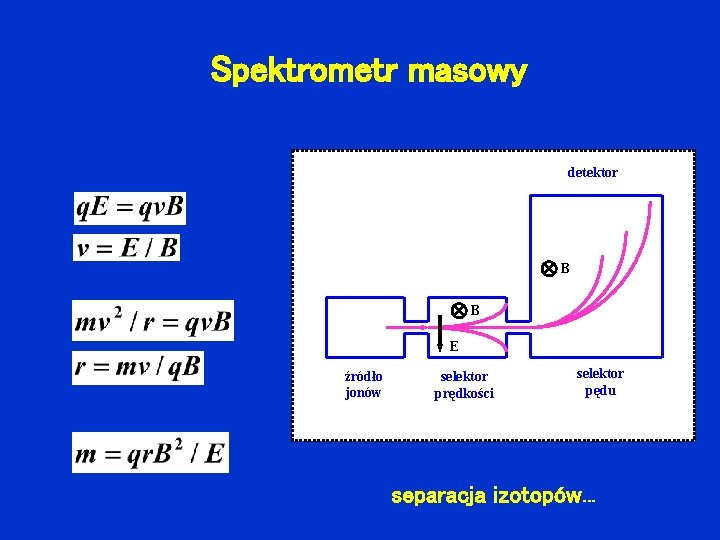
Spektrometr masowy detektor B B E źródło jonów selektor prędkości selektor pędu separacja izotopów. . .

Aston 1919 Francis Aston 1877 - 1945 1922 od 1919 zidentyfikował i zmierzył masy 212 izotopów. . .

Defekt masy m – masa jądra mp – masa protonu (938. 3 Me. V) mn – masa neutronu (939. 6 Me. V) defekt masy: m c 2 = [Z · mp + (A – Z) · mn – m] c 2 > 0 energia wiązania: EB = m c 2 EB / A 8. 5 Me. V

Defekt masy (cd) kolaps jądrowy. . .

deuter 1 H 1 - wodór 2 H 1 - deuter 3 H 1 - tryt md = 1875 Me. V < mp + mp = 1878 Me. V m 3 Me. V słabo związany układ dwóch nukleonów
![Energia wiązania EBA Me V 10 8 6 4 2 50 100 150 200 Energia wiązania EB/A [Me. V] 10 8 6 4 2 50 100 150 200](https://slidetodoc.com/presentation_image_h/ab24dc06aa6574f2cc14e7b46c54f6c2/image-30.jpg)
Energia wiązania EB/A [Me. V] 10 8 6 4 2 50 100 150 200 250 A Energia potencjalna układu związanego jest ujemna

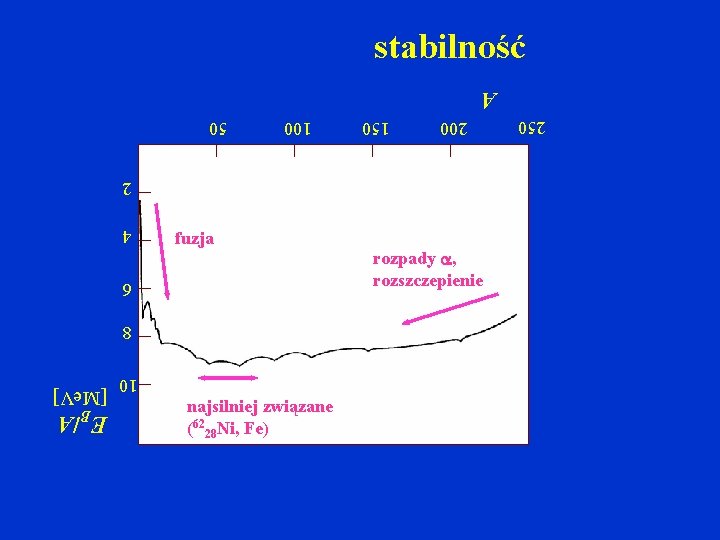
stabilność A 200 150 100 50 2 4 6 8 10 najsilniej związane (6228 Ni, Fe) rozpady , rozszczepienie 250 fuzja [Me. V] EB/A
![liczby magiczne EBA Me V 2 8 20 28 50 82 126 10 8 liczby magiczne EB/A [Me. V] 2 8 20 28 50 82 126 10 8](https://slidetodoc.com/presentation_image_h/ab24dc06aa6574f2cc14e7b46c54f6c2/image-32.jpg)
liczby magiczne EB/A [Me. V] 2 8 20 28 50 82 126 10 8 6 4 2 N=28 Z=8 N=8 Z=28 N=50 N=82 Z=50 Z=82 N=126 Z=20 N=20 Z=2 N=2 50 100 150 200 250 A