Dzia II Fizyka atomowa e Temat Efekt fotoelektryczny




















![n Energie elektronu na kolejnych orbitach oraz serie widmowe. E [e. V] n 4 n Energie elektronu na kolejnych orbitach oraz serie widmowe. E [e. V] n 4](https://slidetodoc.com/presentation_image_h/b69aba6b53ae1e73a63fcf0550f50443/image-27.jpg)



- Slides: 30

Dział II Fizyka atomowa. e

Temat: Efekt fotoelektryczny n Widmo światła 760 nm c - prędkość światła - długość fali - częstotliwość 380 nm

ZJAWISKO FOTOELEKTRYCZNE polega na tym, że w wyniku oświetlania określonym promieniowaniem elektromagnetycznym z powierzchni metalu wybijane są elektrony. n WA !! ! E N Ż e

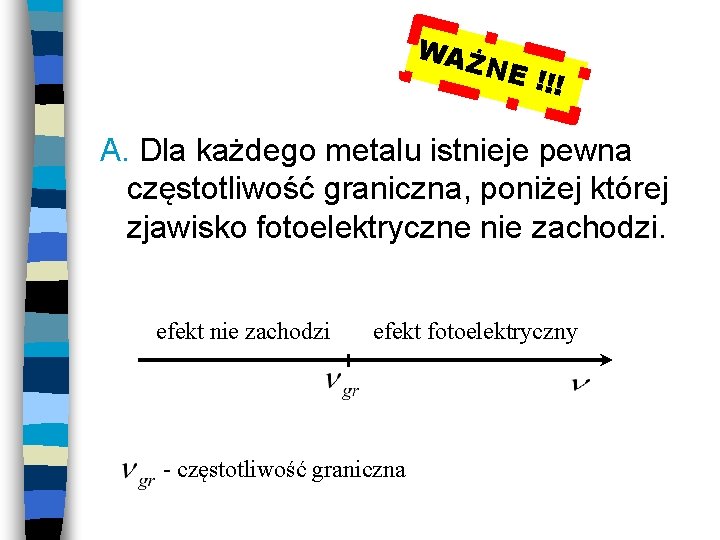
WAŻ N E !!! A. Dla każdego metalu istnieje pewna częstotliwość graniczna, poniżej której zjawisko fotoelektryczne nie zachodzi. efekt nie zachodzi efekt fotoelektryczny - częstotliwość graniczna

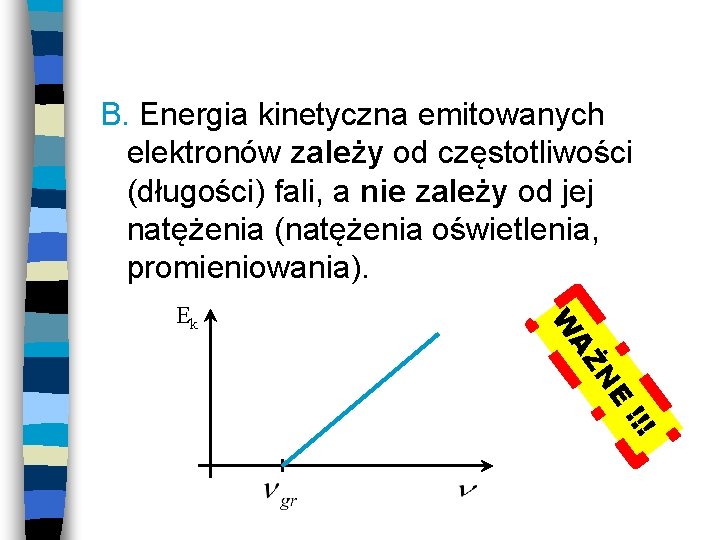
B. Energia kinetyczna emitowanych elektronów zależy od częstotliwości (długości) fali, a nie zależy od jej natężenia (natężenia oświetlenia, promieniowania). N AŻ W Ek E !!!

C. Natężenie prądu, który pojawia się w obwodzie, jest proporcjonalne do natężenia promieniowania (światła) padającego na katodę. Im większe jest natężenie promieniowania (światła), tym większe jest natężenie prądu. W !! ! E AŻN

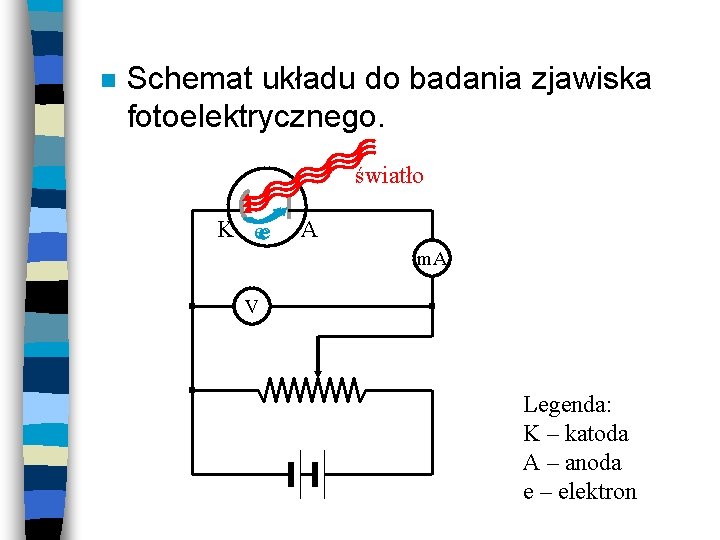
n Schemat układu do badania zjawiska fotoelektrycznego. światło K eee A m. A V Legenda: K – katoda A – anoda e – elektron

n Potencjał hamujący (napięcie hamowania) - praca pola elektrycznego, gdzie to potencjał (napięcie) między elektrodami - aby zatrzymać efekt fotoelektryczny: to praca pola elektrycznego musi być równa maksymalnej energii kinetycznej

Temat: Efekt fotoelektryczny - foton. n Planck przyjął, że światło emitowane jest w postaci porcji energii - kwantów energii, nazwanych fotonami. Max Planck 1858 -1947 1889 odkrył stałą fizyczną następnie nazwaną jego nazwiskiem http: //pl. wikipedia. org/wiki/Max_Planck

n ε Wartość kwantu energii zależy od częstotliwości promieniowania i jest równa: ε gdzie h to stała Plancka WA !! ! E N Ż

n Charakterystyka fotonu: – nie posiada masy spoczynkowej, czyli istnieje gdy się porusza, – w próżni ma stałą prędkość c = 300000 km/s , w ośrodku prędkość fotonu zależy od współczynnika załamania, – gdy przechodzi przez ośrodek częstotliwość nie zmienia się, zmienia się długość fali z nim stowarzyszonej. WAŻNE !!!

n Einstein zinterpretował zjawisko fotoelektryczne jako zderzenie dwóch cząstek: fotonu i elektronu. Albert Einstein 1879 -1955 Nagroda Nobla 1921 za interpretację zjawiska fotoelektrycznego http: //pl. wikipedia. org/wiki/Albert_Einstein

n Energia fotonu ε jest spożytkowana na: - wybicie elektronu z sieci krystalicznej metalu, pracę wyjścia W, - nadanie prędkości, dostarczenie energii kinetycznej Ek. n Co zapisujemy symbolicznie: ε = W+ E k

n Wzór Millikana-Einsteina powstaje po podstawieniu energii kwantu i energii kinetycznej do wzoru: = W+ Ek ε Robert Millikan 1868 -1953 Nagroda Nobla 1923 za wyznaczenie ładunku elementarnego i prace nad zjawiska fotoelektrycznego http: //pl. wikipedia. org/wiki/Robert_Millikan

n Pamiętając, że praca wyjścia oraz energia kinetyczna otrzymujemy inną postać wzoru Millikana -Einsteina:

Zad. 1 n Obliczyć graniczną częstotliwość fali νgr zjawiska fotoelektrycznego dla srebra, dla którego praca wyjścia W = 4, 7 e. V.

Zad. 2 n Obliczyć pracę wyjścia W elektronów wybijanych z powierzchni cezu, dla których graniczna długość fali zjawiska fotoelektrycznego wynosi λg = 660 nm. Wynik podać w dżulach i elektronowoltach.

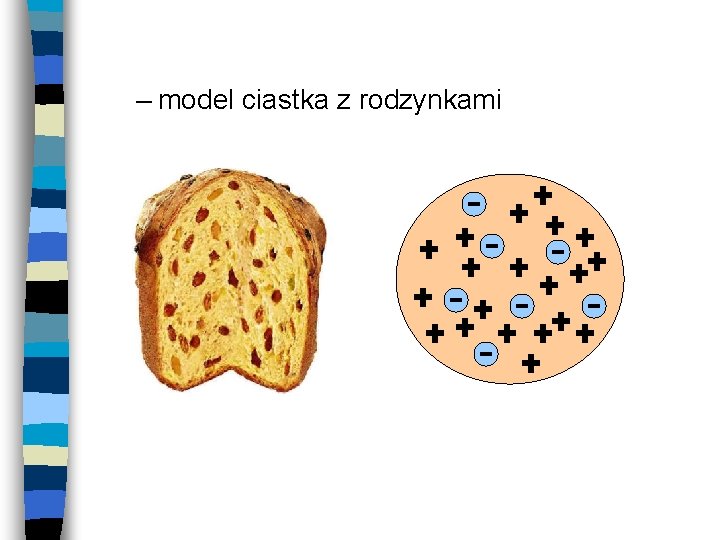
Temat: Atom wodoru. n Model atomu według Thomsona – 1898 odkrycie elektronu Joseph Thomson 1856 -1940 Nagroda Nobla 1906 za prace nad przewodnictwem prądu elektrycznego w gazach http: //pl. wikipedia. org/wiki/Joseph_John_Thomson

– model ciastka z rodzynkami

n Doświadczenie Rutherforda ekran cząstki α źródło promieniowania folia złota Ernst Rutherford 1871 -1936 http: //pl. wikipedia. org/wiki/Ernest_Rutherford

n Przewidywania teoretyczne (cząstki alfa przelatują przez folię): – istnieją jedynie niewielkie odchylenia od pierwotnego ruchu cząstek. n Interpretacja doświadczenia (cząstki napotykając folię są odchylane pod różnymi kątami a nawet zawracane): – ładunek dodatni jest skupiony w małym jądrze atomowym, – elektrony krążą w dużej odległości od jądra.

n Widma atomowe różnych gazów. wodór hel neon pary rtęci niewidoczne prążki fioletowe

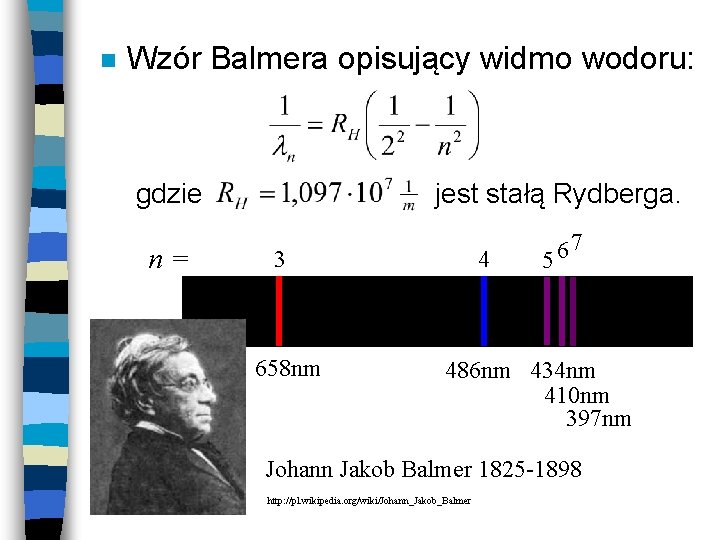
n Wzór Balmera opisujący widmo wodoru: gdzie jest stałą Rydberga. n= 7 6 5 3 658 nm 4 486 nm 434 nm 410 nm 397 nm Johann Jakob Balmer 1825 -1898 http: //pl. wikipedia. org/wiki/Johann_Jakob_Balmer

n Model atomu wodoru wg Bohra. WAŻNE !!! Postulaty Bohra: 1. Elektron w atomie wodoru porusza się po kołowej orbicie dookoła jądra pod wpływem siły coulombowskiej i zgodnie z prawami Newtona. 2. Elektron może poruszać się po takiej orbicie dla której moment pędu jest równy wielokrotności stałej Plancka.

3. Elektron poruszający się po orbicie stacjonarnej nie wypromieniowuje energii elektromagnetycznej. 4. Atom przechodząc ze stanu En do stanu Ek wypromieniowuje kwant energii WA ŻN Niels Bohr 1885 -1962 http: //pl. wikipedia. org/wiki/Niels_Bohr E! !!

Stan podstawowy elektronu - stan, w którym energia elektronu jest najniższa. n Stan wzbudzony elektronu - stan, w którym energia elektronu jest wyższa, znajduje się on na wyższej orbicie. n
![n Energie elektronu na kolejnych orbitach oraz serie widmowe E e V n 4 n Energie elektronu na kolejnych orbitach oraz serie widmowe. E [e. V] n 4](https://slidetodoc.com/presentation_image_h/b69aba6b53ae1e73a63fcf0550f50443/image-27.jpg)
n Energie elektronu na kolejnych orbitach oraz serie widmowe. E [e. V] n 4 -0, 85 3 -1, 51 2 seria Balmera seria Paschena -3, 4 seria Lymana 1 -13, 6

Zad. 1 Oblicz energię kwantu pochłanianego przez elektron przeskakujący z orbity pierwszej na trzecią. Wyraź ją w elektronowoltach i dżulach.

Zad. 2 Oblicz energię kwantu emitowanego przy przejściu elektronu z orbity trzeciej na drugą i wyraź ją w dżulach. Podaj częstotliwość oraz długość fali emitowanej podczas tego przejścia elektronu. Jeśli to możliwe podaj barwę światła.

i Z Y k WAŻN E !!! w w w y z i. f s i. ka o c s. l p. m B a r t o s o z n e J c a k b i
 Wzór einsteina millikana
Wzór einsteina millikana Fizyka atomowa
Fizyka atomowa Miernik rychlosti
Miernik rychlosti Atomowa spektrometria absorpcyjna
Atomowa spektrometria absorpcyjna Typy rymów
Typy rymów Funkcje łodygi
Funkcje łodygi Bernadetta izydorczyk
Bernadetta izydorczyk Boisko wymiary
Boisko wymiary Esej na temat
Esej na temat Stefan wyszyński ciekawostki
Stefan wyszyński ciekawostki Esej na temat
Esej na temat Struktura administracji publicznej w polsce
Struktura administracji publicznej w polsce Opowiadanie ćwiczenia redakcyjne
Opowiadanie ćwiczenia redakcyjne Moc fizyka
Moc fizyka N energia praca
N energia praca Podstawa programowa fizyka
Podstawa programowa fizyka Jednostka kąta bryłowego
Jednostka kąta bryłowego Fizyka pęd
Fizyka pęd Fizyka
Fizyka Soczewki rozpraszające
Soczewki rozpraszające Masa w układzie si
Masa w układzie si Studnia potencjału
Studnia potencjału I zasada termodynamiki
I zasada termodynamiki Dziekuje za uwage fizyka
Dziekuje za uwage fizyka Silnik carnota budowa
Silnik carnota budowa Zachodzące w powietrzu otaczającym kulę ziemską
Zachodzące w powietrzu otaczającym kulę ziemską Zasada zachowania pędu
Zasada zachowania pędu Soczewki skupiające
Soczewki skupiające Umk fizyka
Umk fizyka Budowa mikrofonu fizyka
Budowa mikrofonu fizyka Zastosowanie zjawiska fotoelektrycznego
Zastosowanie zjawiska fotoelektrycznego