Die Redoxreaktion Gleichungen komplexer Redoxreaktionen Aufstellung der Gleichungen















- Slides: 15

Die Redoxreaktion Gleichungen komplexer Redoxreaktionen: Aufstellung der Gleichungen (Regeln) ü Übungen zur Redoxzahl und Redoxgleichung ü Beispiele für Redoxreaktionen ü

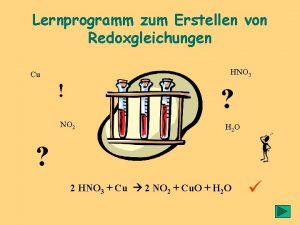
Regeln zur Aufstellung von Gleichungen für Redoxvorgänge Beispiel: Kohlenstoff wird in konz. Schwefelsäure erhitzt. Dabei entsteht CO 2 + SO 2

Versuch Zucker und Schwefelsäure (konz. ) Taste = weiter 04. 08. 2001 Hans Sturm Die Schwefelsäure verkohlt den Zucker. Es entsteht Zuckerkohle, die mit heißer Schwefelsäure zu Kohlendioxid und Schwefeldioxid weiterreagiert (=> Aufblähen des Gemisches).

Die Redox-Gleichung Die Reaktion von Kohlenstoff mit Schwefelsäure ist eine Redox-Reaktion. Im Folgenden wird erklärt, wie die Gleichung für eine derartige Reaktion aufgestellt wird. 04. 08. 2001 Hans Sturm

Die Redoxgleichung 1. Regel: Beispiel: Edukte => Produkte C CO 2 + SO 2 (unvollständige Gleichung) Erklärungen 04. 08. 2001 + H 2 SO 4 => Hans Sturm

Die Redox-Gleichung Regel: Bestimmung der Oxidationszahlen, die sich während der Reaktion ändern Beispiel: 0 C + +6 H 2 SO 4 +4 +4 CO 2 + SO 2 Erklärungen 04. 08. 2001 2. Hans Sturm =>

Die Redox-Gleichung Regel: Aufstellen der Teilgleichungen (unvollständig) Beispiel: Oxidation: 0 +4 C => CO 2 Reduktion: +6 +4 H 2 SO 4 => SO 2 Erklärungen 04. 08. 2001 3. Hans Sturm

Die Redox-Gleichung Regel: Oxidations. Zahlen mit Elektronen ausgleichen 04. 08. 2001 4. Beispiel: Oxidation: 0 +4 C => CO 2 + 4 e- Reduktion: +6 +4 H 2 SO 4 + 2 e - => SO 2 Hans Sturm

Die Redox-Gleichung Regel: Ladungsausgleich durch H 3 O + ín saurer Lösung (in alkalischer Lösung durch Hydroxidionen) 04. 08. 2001 5. Beispiel: Oxidation: C => CO 2 + 4 e- + 4 H 3 O+ Reduktion: H 2 SO 4 + 2 e - + 2 H 3 O+ => SO 2 Hans Sturm

Die Redox-Gleichung Regel: Ausgleich der Stoffbilanz mit Wasser 6. Beispiel: Oxidation: C + 6 H 2 O => CO 2 + 4 e- + 4 H 3 O+ Reduktion: H 2 SO 4 + 2 e - + 2 H 3 O+ => SO 2 + 4 H 2 O 04. 08. 2001 Hans Sturm

Die Redox-Gleichung Regel: Anpassung der e--Zahlen in beiden Teilgleichungen 7. Beispiel: Oxidation: C + 6 H 2 O => CO 2 + 4 e- + 4 H 3 O+ Reduktion: H 2 SO 4 + 2 e - + 4 H 3 O+ => SO 2 + 4 H 2 O / * 2 Red: 2 H 2 SO 4 + 4 e - + 8 H 3 O+ => 2 SO 2 + 8 H 2 O 04. 08. 2001 Hans Sturm

Die Redox-Gleichung Regel: 8. Beispiel: Addition der Teilgleichungen C + 6 H 2 O + 2 H 2 SO 4 + 4 e- + 4 H 3 O+ ====> CO 2 + 4 e- + 4 H 3 O+ + 2 SO 2 + 8 H 2 O C + 2 H 2 SO 4 => CO 2 2 SO 2 + 2 H 2 O 04. 08. 2001 Hans Sturm

Redox-Reaktionen in der Technik n Das Galvanische Element (Die Elektrische Zelle) n Die Taschenlampenbatterie (Primärelement) n Die Autobatterie Bleiakkumulator (Sekundärelement) n Die 04. 08. 2001 Brennstoffzelle Hans Sturm

Übung macht den Meister n Übungen mit dem Computer (Oxidationszahlen, Teilgleichungen) n Übungsblatt (Aufgaben - Word) n Oxidationszahlen (Übungen mit Excel) n Informationen (Redox -Reaktionen Definition „Microsoft. Encarta“ - Word) 04. 08. 2001 Hans Sturm

Ende der Präsentation 04. 08. 2001 Hans Sturm
 Redoxreaktion übungen
Redoxreaktion übungen Läufersystem
Läufersystem Komplexer spannungsteiler
Komplexer spannungsteiler Spannungsteiler erklärung
Spannungsteiler erklärung Hallenhockey aufstellung
Hallenhockey aufstellung Redoxgleichungen übungen mit lösung
Redoxgleichungen übungen mit lösung Die mier en die sprinkaan fabel
Die mier en die sprinkaan fabel Das ist der daumen der pflückt die pflaumen
Das ist der daumen der pflückt die pflaumen Syra bas reaktion
Syra bas reaktion Spændingsrækken metaller
Spændingsrækken metaller Redoxamphoterie beispiele
Redoxamphoterie beispiele Atp aquaristik
Atp aquaristik Primrer
Primrer Realmath gleichungen
Realmath gleichungen Wofür braucht man gleichungen im leben
Wofür braucht man gleichungen im leben Waagemodell gleichungen
Waagemodell gleichungen