Soluo Ideal Uma soluo ideal aquela onde no










- Slides: 17

Solução Ideal Uma solução ideal é aquela onde não há efeitos importantes pela mudanças nas interações atômicas/moleculares na formação da solução Uma solução real se aproxima do comportamento ideal quando os components são quimicamente idênticos. Ex. (Ag, Au) Potencial químico do componente i relativo àquele do componente puro na pressão pi*

Em soluções líquidas e sólidas, estamos interessados efetivamente em situações onde p = 1 atm. Assim, eliminamos a dependência com a pressão. Comparação com a equação anterior conduz a uma definição de uma solução ideal para fases condensadas:

A equação anterior pode ser escrita na forma: O subescrito mix é usado quando o estado de referência para os components puros corresponde ao mesmo estado de agregação da solução Soluções que seguem a equação acima são chamadas Raoultianas

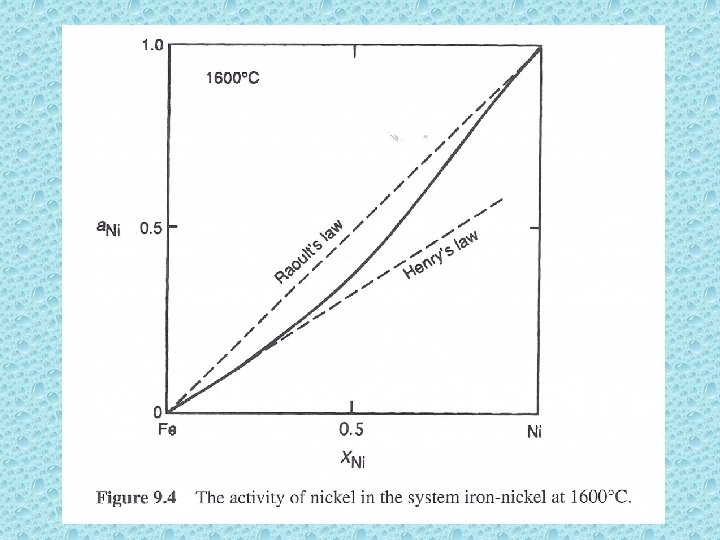
A partir das expressões apresentadas anteriormente, vê- se que, para uma solução ideal: Onde: ai é a atividade do componente i na solução e xi a fração molar do componente na solução condensada. Lei de Raoult

As seguintes expressões para grandezas parciais de mistura, a xi constante, se aplicam a soluções ideiais:

As quantidade integrais de mistura podem ser obtida a partir das quantidades parciais molares de mistura, para qualquer propriedade Y, através da expressão:



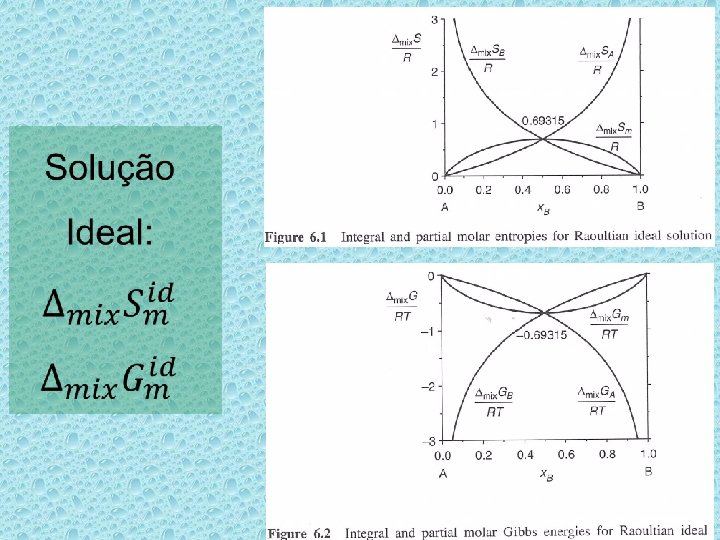
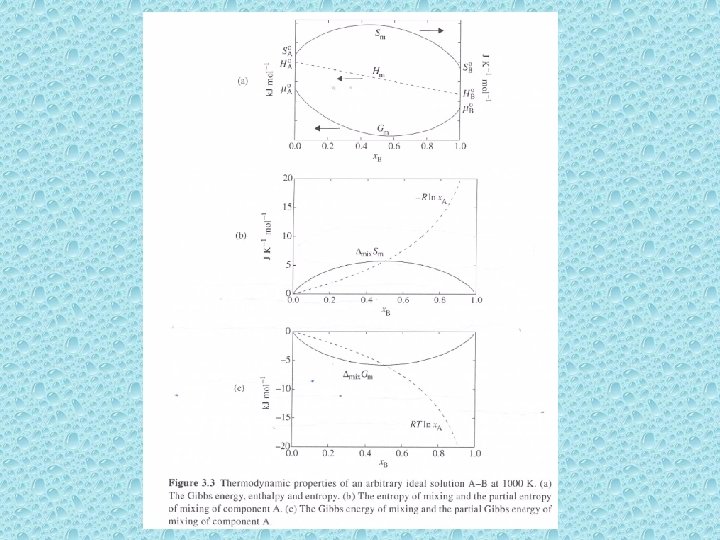
Como pode ser visto em uma das figuras anteriores, a energia de Gibbs de mistura para a solução ideal é simétrica com relação à composição. Ela atinge um valor mínimo de – 0, 69315 RT para a composição equiatômica e aproxima-se de zero para os elementos puros. As quantidades parciais de mistura mudam de maneira muito mais marcante com a composição, devido ao termo logarítmico da expressão. 1 0

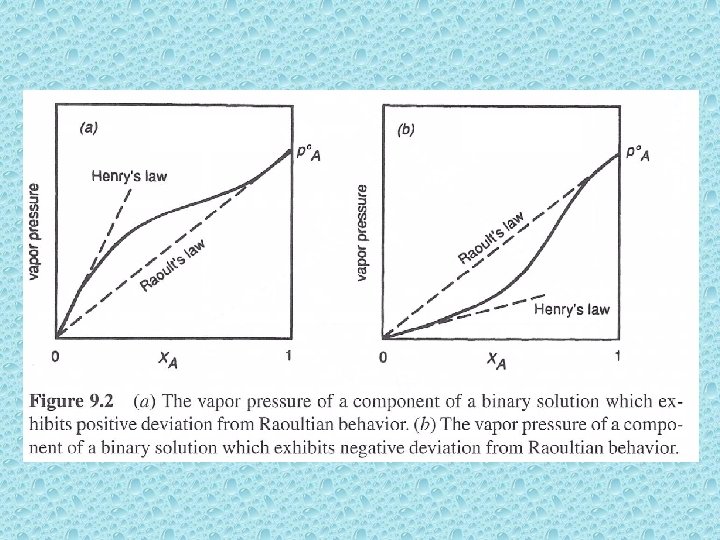
Solução Real Os resultados experimentais para vários sistemas reais indicam desvio em relação ao comportamento ideal.

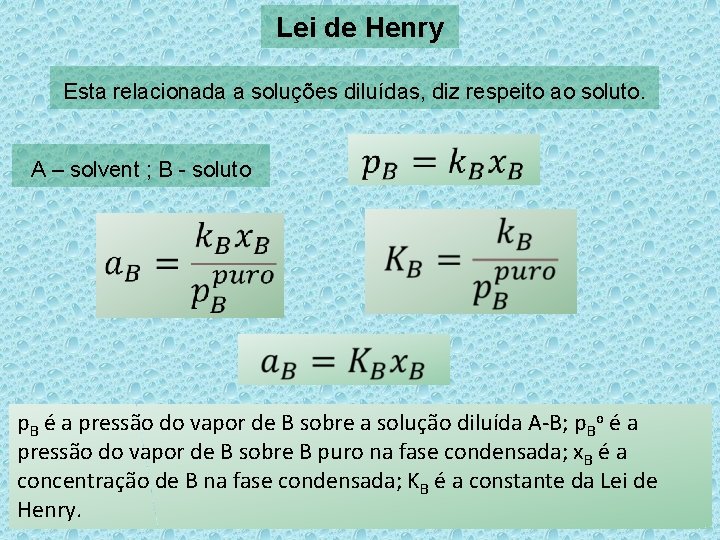
Lei de Henry Esta relacionada a soluções diluídas, diz respeito ao soluto. A – solvent ; B - soluto p. B é a pressão do vapor de B sobre a solução diluída A-B; p. Bo é a pressão do vapor de B sobre B puro na fase condensada; x. B é a concentração de B na fase condensada; KB é a constante da Lei de Henry.



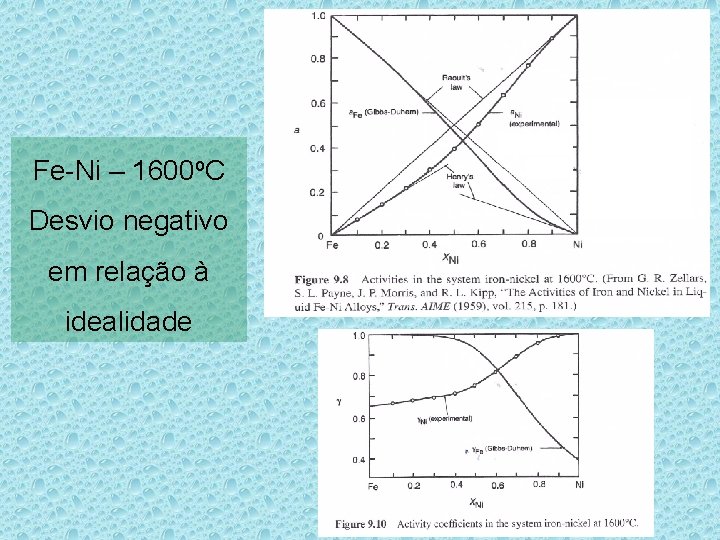
Fe-Ni – 1600 o. C Desvio negativo em relação à idealidade

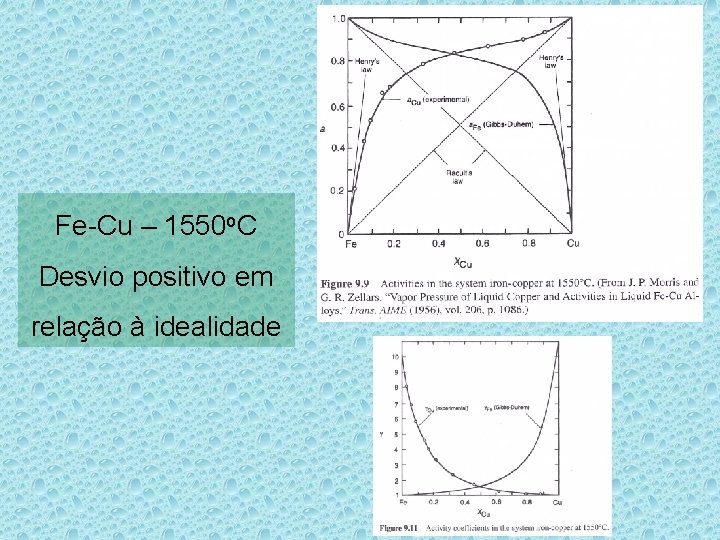
Fe-Cu – 1550 o. C Desvio positivo em relação à idealidade

Termos de excesso

Pode ser visto que o potencial químico de excesso é relacionado com o coeficiente de atividade através da relação: