Soli kyselin Soli kyselin Jak vznikaj soli HCl





- Slides: 14

Soli kyselin

Soli kyselin Jak vznikají soli? HCl → H+ + Cl- H 2 O H 2 SO 4 → 2 H++ SO 42 - NEUTRALIZACE KYSELINA HCl ZÁSADA Na. OH SŮL Na. Cl VODA H 2 O

Z čeho se skládají soli kyselin? Na. Cl kation KOV anion KYSELINY Soli kyseliny jsou sloučeniny složené z kationtu kovů a aniontu kyseliny.

Soli kyselin SOLI BEZKYSLÍKATÝCH KYSELIN halogenidy sulfidy SOLI KYSLÍKATÝCH KYSELIN vznikají náhradou vodíků kyslíkatých kyselin za kov

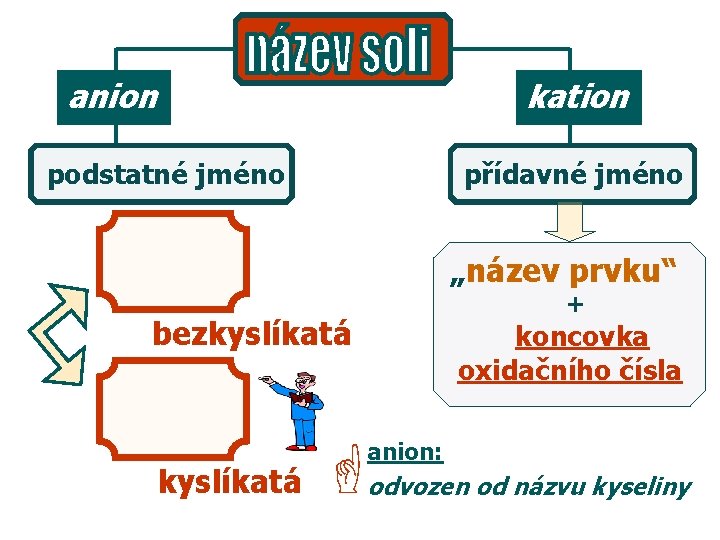
anion kation podstatné jméno přídavné jméno „název prvku“ + bezkyslíkatá anion: ☜ kyslíkatá koncovka oxidačního čísla odvozen od názvu kyseliny

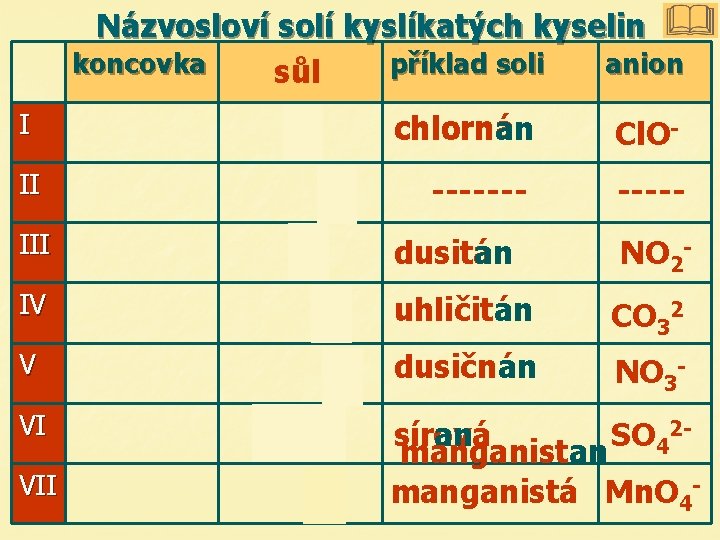
Názvosloví solí kyslíkatých kyselin koncovka kyselina příklad soli anion sůl I II chlorná chlornan Cl. O- ------- III dusitá dusitan NO 2 - IV uhličitá uhličitan CO 32 V dusičná dusičnan NO 3 - VI síran sírová SO 42 manganistan manganistá Mn. O 4 - VII

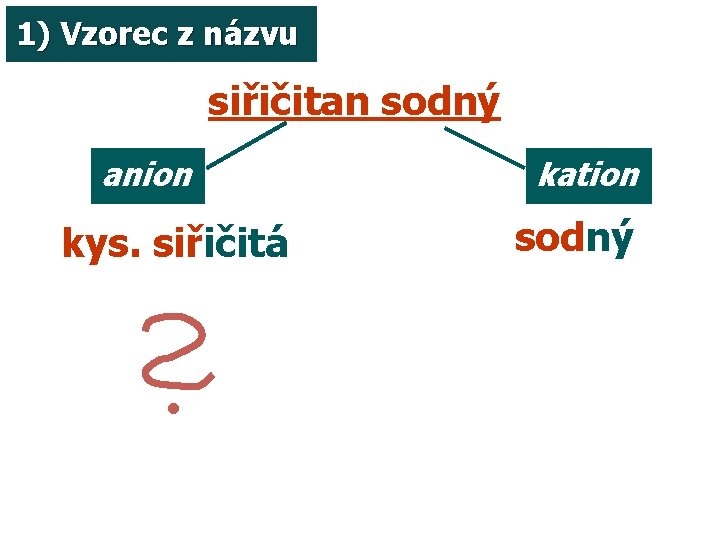
1) Vzorec z názvu siřičitan sodný anion kys. siřičitá kation sodný

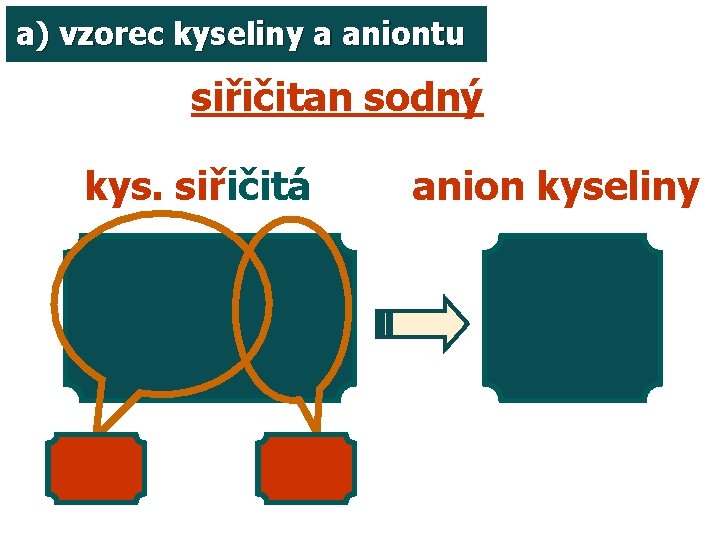
a) vzorec kyseliny a aniontu siřičitan sodný kys. siřičitá anion kyseliny

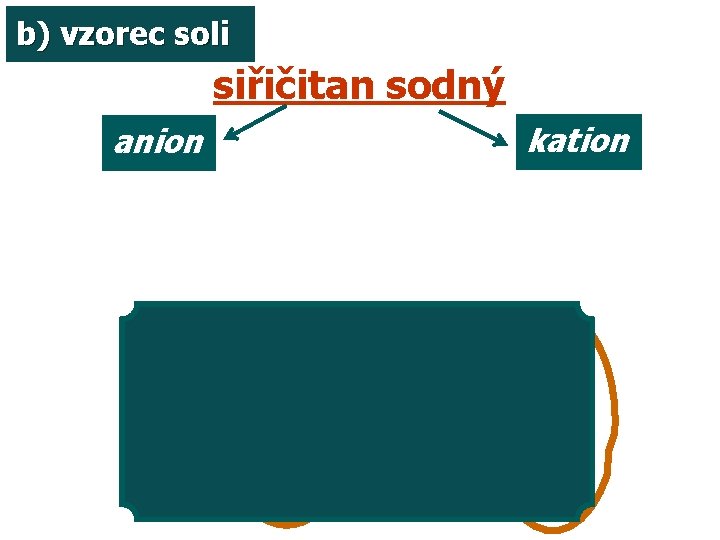
b) vzorec soli siřičitan sodný anion kation

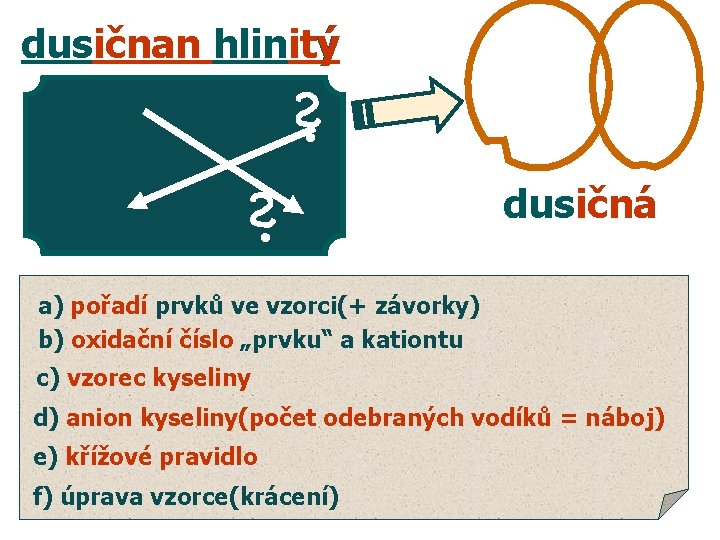
dusičnan hlinitý dusičná a) pořadí prvků ve vzorci(+ závorky) b) oxidační číslo „prvku“ a kationtu c) vzorec kyseliny d) anion kyseliny(počet odebraných vodíků = náboj) e) křížové pravidlo f) úprava vzorce(krácení)

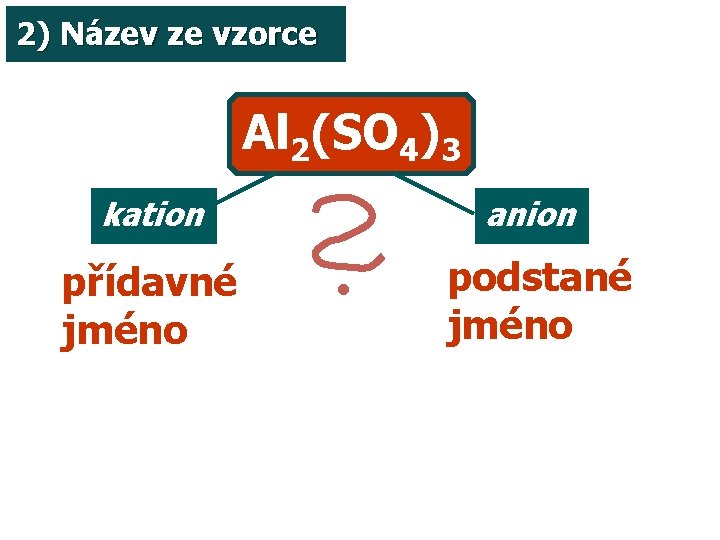
2) Název ze vzorce Al 2(SO 4)3 kation přídavné jméno anion podstané jméno


chloristá chloristan draselný a) „závorky“ a křížové pravidlo: b) náboj kationtu (PSP!) + koncovku c) náboj aniontu (počet odebraných vodíků v kyselině) d) vzorec kyseliny + oxidační číslo „prvku“ e) název aniontu = podstatné jméno(koncovka: – an ) f) název kationtu = koncovku přídavného jména

☜ uhličitá uhličitan vápenatý a) „závorky“ a křížové pravidlo: b) náboj kationtu (vápník má vždy +II – PSP) +koncovka c) náboj aniontu (počet odebraných vodíků v kyselině) d) vzorec kyseliny + oxidační číslo „prvku“ e) název aniontu = podstatné jméno(koncovka: – an ) f) název kationtu = koncovka přídavného jména