NZVOSLOV KYSELIN Nzvoslov kyselin Bezkyslkat Kyseliny Kyslkat Nzvoslov

NÁZVOSLOVÍ KYSELIN
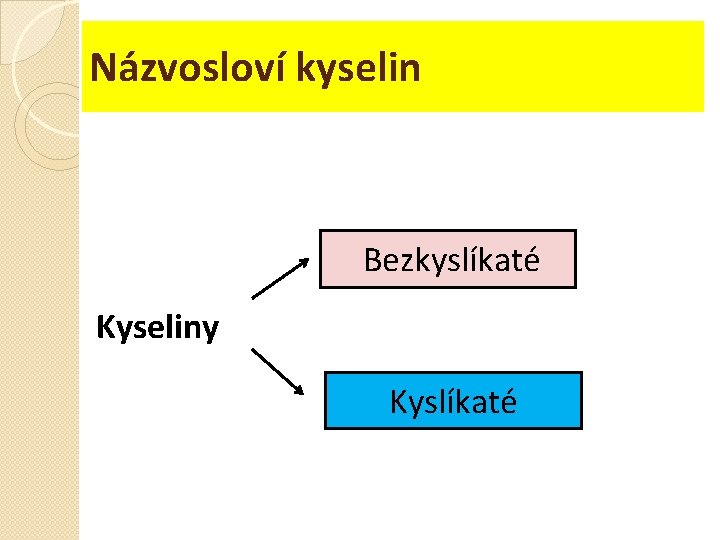
Názvosloví kyselin Bezkyslíkaté Kyseliny Kyslíkaté
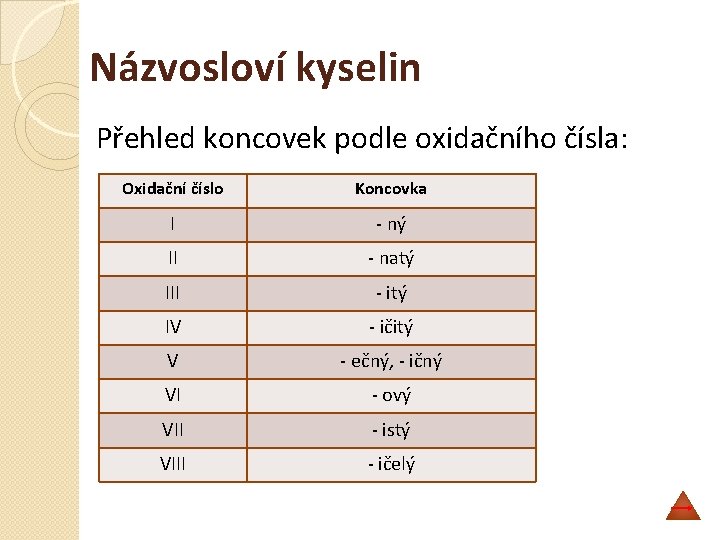
Názvosloví kyselin Přehled koncovek podle oxidačního čísla: Oxidační číslo Koncovka I - ný II - natý III - itý IV - ičitý V - ečný, - ičný VI - ový VII - istý VIII - ičelý

Názvosloví bezkyslíkatých kyselin Obecná charakteristika Obecný vzorec Obecný název

Názvosloví bezkyslíkatých kyselin Bezkyslíkaté kyseliny ve své struktuře neobsahují kyslík. Vznikají rozpuštěním některých plynných sloučenin vodíku ( HF, HCl, HBr, HI, H 2 S, HCN) ve vodě, jejich vzorce jsou totožné se vzorci původních sloučenin.

Názvosloví bezkyslíkatých kyselin 1)Obecný vzorec: Hm X H X m symbol atomu vodíku symbol kyselinotvorného prvku stechiometrický koeficient

Názvosloví bezkyslíkatých kyselin 2) Obecný název: podstatné jméno (kyselina) + přídavné jméno vytvořené z názvu odpovídající sloučeniny s vodíkem přidáním koncovky –ová Př. HCl chlorovodík- kyselina chlorovodíková

Názvosloví bezkyslíkatých kyselin 3) Příklady bezkyslíkatých kyselin HF kyselina fluorovodíková HCl kyselina chlorovodíková HBr kyselina bromovodíková HI kyselina jodovodíková H 2 S kyselina sulfanová HCN kyselina kyanovodíková

Kyslíkaté kyseliny Obecná charakteristika Obecný vzorec Obecný název Odvození názvu ze vzorce Odvození vzorce z názvu

Kyslíkaté kyseliny ve své molekule obsahují atomy vodíku, kyslíku a kyselinotvorného prvku. Př. kyselina sírová H 2 SO 4 Vznikají reakcí kyselinotvorných oxidů s vodou. SO 3 + H 2 O H 2 SO 4
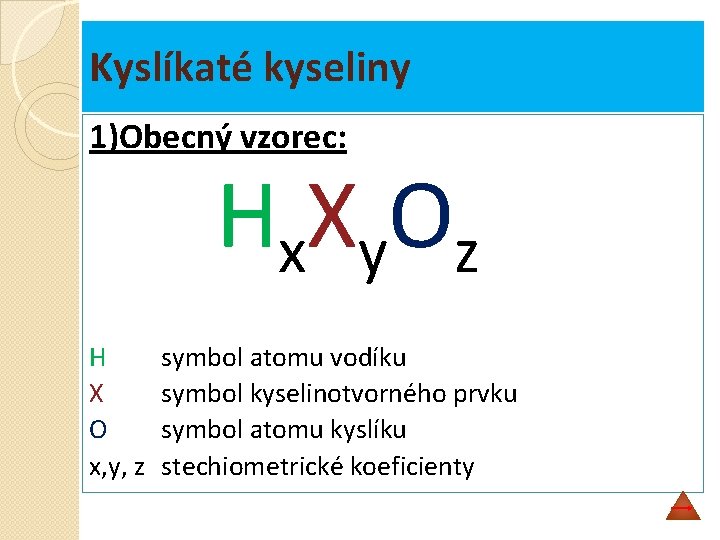
Kyslíkaté kyseliny 1)Obecný vzorec: Hx Xy O z H X O x, y, z symbol atomu vodíku symbol kyselinotvorného prvku symbol atomu kyslíku stechiometrické koeficienty

Kyslíkaté kyseliny 2) Obecný název : podstatné jméno kyselina + přídavné jméno odvozené od slovního základu kyselinotvorného prvku přidáním koncovky, která vyjadřuje hodnotu jeho oxidačního čísla Př. kyselina sírová H 2 SVIO 4

Kyslíkaté kyseliny 3) Tvorba názvu kyseliny: Př. Jaký název má kyselina o vzorci HNO 3? 1) Nejprve napíšeme oxidační čísla k vodíku a kyslíku. Vodík má oxidační číslo (I), kyslík (- II). HINz. O 3 -II 2) Dopočítání čísla z. Součet všech nábojů v sloučenině musí být vždy rovný 0. 1. 1+1. z+3. (-2) = 0 z = 5 H 1 IN 1 z. O 3 -II 3) HINVO 3 -II oxidační číslo dusíku je V → koncovka -ečný, -ičný 4) Název kyseliny je kyselina dusičná. K

Kyslíkaté kyselin 4)Tvorba vzorce z názvu: Př. Jaký vzorec má kyselina dusičná? 1) Vzorec kyseliny můžeme odvodit z oxidu, kde se kyselinotvorný prvek vyskytuje ve stejném oxidačním čísle jako v kyselině. kyselina dusičná→oxid dusičný N 2 O 5 2) K příslušnému oxidu přidáme vodu. N 2 O 5 + H 2 O → H 2 N 2 O 6 pokud je to možné, vykrátíme, v tomto případě 2 3)Výsledný vzorec kyseliny dusičné je HNO 3. K

Kyslíkaté kyseliny 5) Přehled některých kyslíkatých kyselin: HNO H 2 CO 3 HNO 3 H 2 SO 4 H 3 BO 3 H 3 PO 4 kyselina dusná kyselina uhličitá kyselina dusičná kyselina sírová kyselina trihydrogenboritá kyselina trigydrogenfosforečná
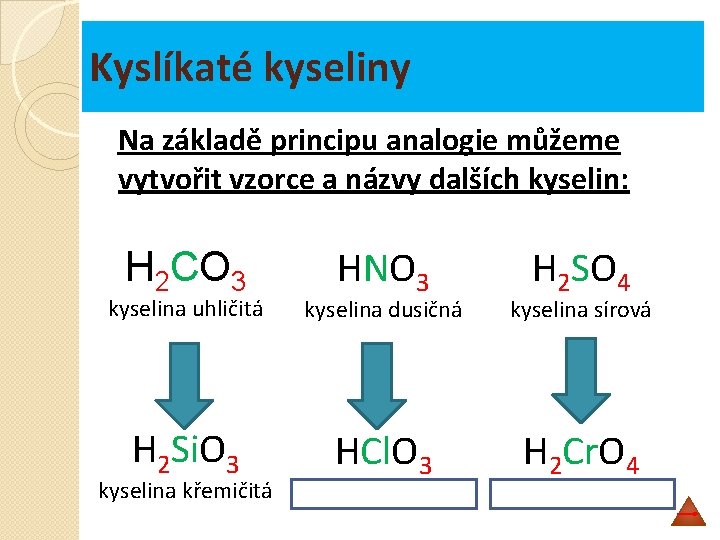
Kyslíkaté kyseliny Na základě principu analogie můžeme vytvořit vzorce a názvy dalších kyselin: H 2 CO 3 HNO 3 H 2 SO 4 kyselina uhličitá kyselina dusičná kyselina sírová H 2 Si. O 3 HCl. O 3 H 2 Cr. O 4 kyselina křemičitá kyselina chlorečná kyselina chromová
- Slides: 16