Rsistance au TAR et gestion de lchec thrapeuthique



































- Slides: 44

Résistance au TAR et gestion de l’échec thérapeuthique

Objectifs d'apprentissage • Comprendre quand il convient de passer à un traitement de deuxième intention • Connaître le traitement de deuxième intention à privilégier chez les adultes (y compris les femmes enceintes et allaitantes), les adolescents et les enfants • Décrire les mutations de résistance aux médicaments et comment elles influencent le choix d'un traitement de deuxième intention • Connaître les caractéristiques des médicaments généralement utilisés dans les traitements de deuxième intention

Gestion de l'échec thérapeutique. Quand passer à un traitement de deuxième intention ? • Améliorer les résultats cliniques • Prévenir la résistance aux médicaments • Réduire le risque de transmission • Éviter les changements inutiles

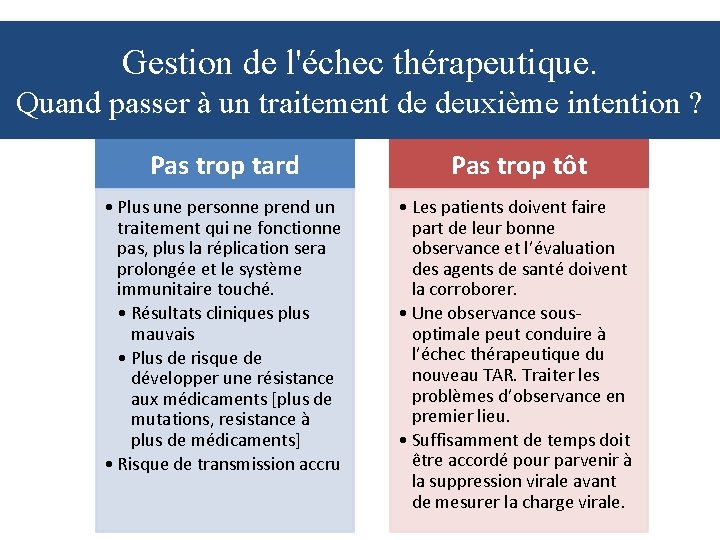
Gestion de l'échec thérapeutique. Quand passer à un traitement de deuxième intention ? Pas trop tard Pas trop tôt • Plus une personne prend un traitement qui ne fonctionne pas, plus la réplication sera prolongée et le système immunitaire touché. • Résultats cliniques plus mauvais • Plus de risque de développer une résistance aux médicaments [plus de mutations, resistance à plus de médicaments] • Risque de transmission accru • Les patients doivent faire part de leur bonne observance et l’évaluation des agents de santé doivent la corroborer. • Une observance sousoptimale peut conduire à l’échec thérapeutique du nouveau TAR. Traiter les problèmes d’observance en premier lieu. • Suffisamment de temps doit être accordé pour parvenir à la suppression virale avant de mesurer la charge virale.

Gestion de l'échec thérapeutique. Quand passer à un traitement de deuxième intention ? • En général, le fait de ne pas atteindre de charge virale faible dans les 1 à 3 mois après une bonne observance suggère que le virus est devenu résistant au TAR. – Se référer aux recommandations nationales définissant le seuil d’une charge virale « faible » . • Toutefois, il peut s'avérer utile d'utiliser l'échelle logarithmique pour évaluer la diminution de la charge virale. • Une diminution >1 log par mois avec une bonne observance peut suggérer que la suppression de la charge virale est possible en prolongeant le traitement actuel. • Poursuivre le traitement actuel et mesurer de nouveau la charge virale après quelques mois pour vérifier si elle a été supprimée.

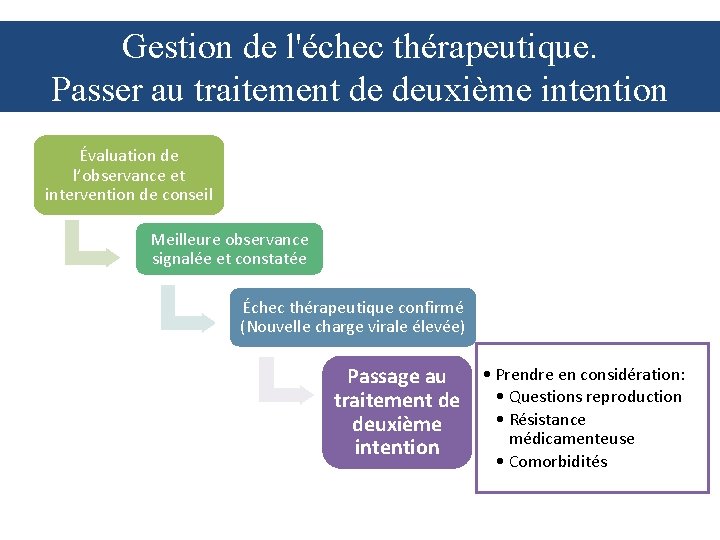
Gestion de l'échec thérapeutique. Passer au traitement de deuxième intention Évaluation de l’observance et intervention de conseil Meilleure observance signalée et constatée Échec thérapeutique confirmé (Nouvelle charge virale élevée) • Prendre en considération: Passage au • Questions reproduction traitement de • Résistance deuxième médicamenteuse intention • Comorbidités

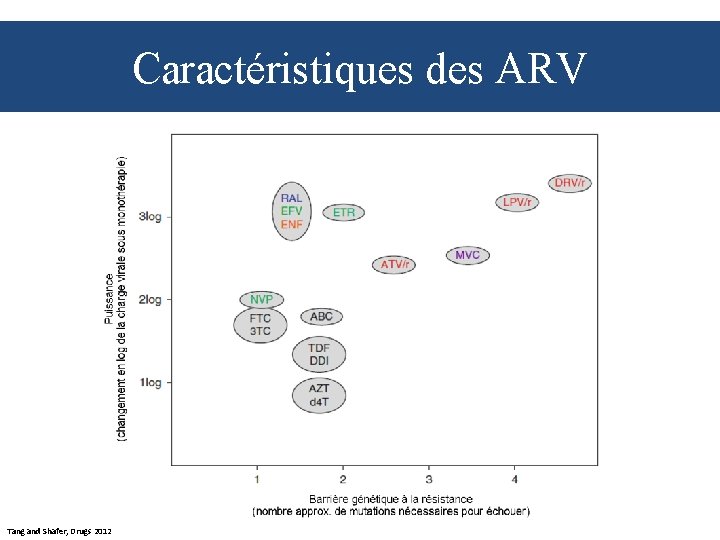
Caractéristiques des ARV Tang and Shafer, Drugs 2012

Caractéristiques des ARV (2) Tang and Shafer, Drugs 2012

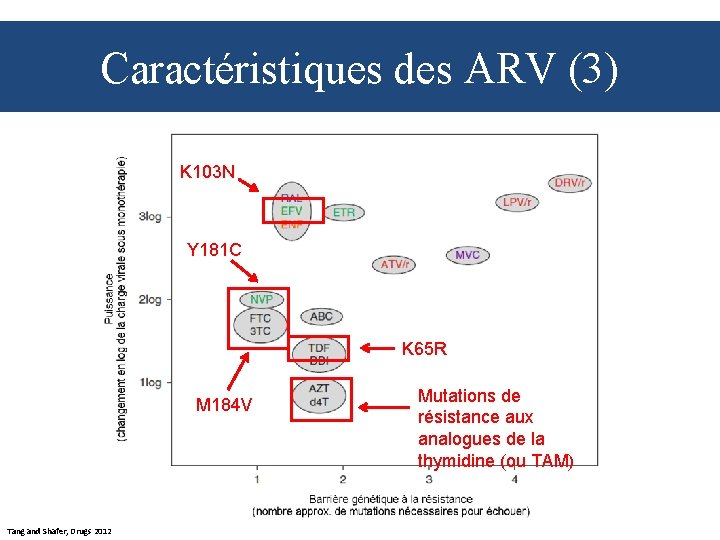
Caractéristiques des ARV (3) K 103 N Y 181 C K 65 R M 184 V Tang and Shafer, Drugs 2012 Mutations de résistance aux analogues de la thymidine (ou TAM)

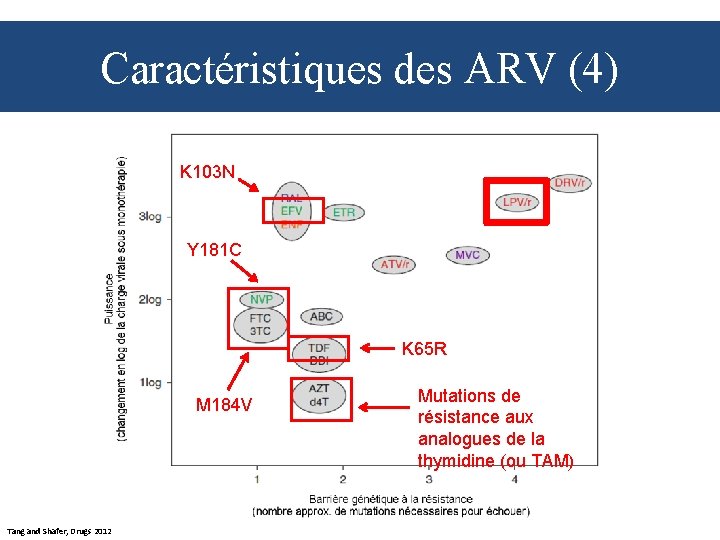
Caractéristiques des ARV (4) K 103 N Y 181 C K 65 R M 184 V Tang and Shafer, Drugs 2012 Mutations de résistance aux analogues de la thymidine (ou TAM)

Le risque de continuer à prendre un traitement inefficace…. . • Le virus peut avoir précocement développé une résistance à un seul médicament du traitement. • Plus le/la patient. e continue à prendre un traitement qui ne supprime pas complètement la réplication du virus, plus le risque de voir apparaître des mutations de résistance supplémentaires augmentera et plus le virus deviendra résistant à d’autres médicaments du TAR.

Prévalence des mutations de résistance en fonction de la fréquence de surveillance de la charge virale Gupta et al. , Lancet Infect Dis, 2009

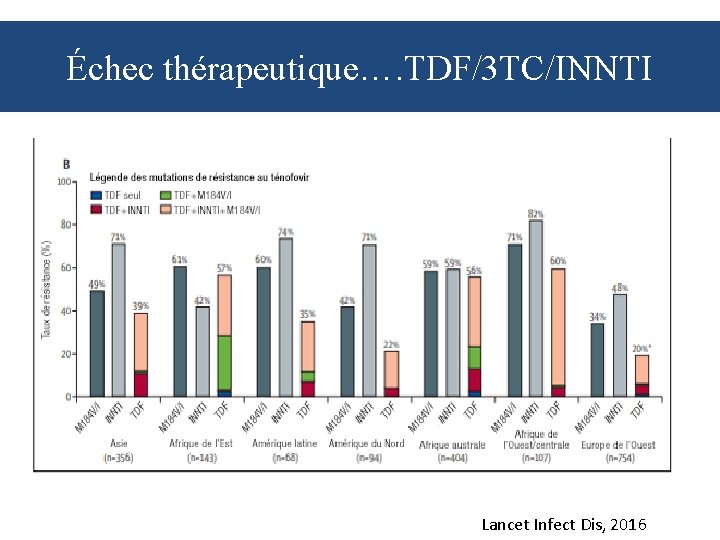
Échec thérapeutique…. TDF/3 TC/INNTI Lancet Infect Dis, 2016

Échec thérapeutique…. TDF/3 TC/INNTI (2) • Il s’agissait d’un TAR recommandé en première intention. • Le Teno. Res Study Group s’est intéressé aux mutations de résistance chez 1926 patients de 36 pays pour qui ces traitements avaient échoué entre 1998 et 2015. • Des différences marquées ont été mises en évidence en ce qui concerne la fréquence des mutations de résistance à plusieurs médicaments (particulièrement au TDF) selon la situation géographique du patient. – Cela était probablement dû à la moindre fréquence de la surveillance de la charge virale et à une plus longue période sous traitement inefficace dans les PRFI. Lancet Infect Dis, 2016

Échec thérapeutique d’un traitement de première intention…. . TDF/3 TC/INNTI • Tous les agents de ce traitement présentent une faible barrière à la résistance – Tous compromis par le changement d’un seul acide aminé • L’étude Teno. Res a mis en évidence que le risque de résistance au TDF était lié au schéma thérapeutique : NVP > EFV 3 TC > FTC

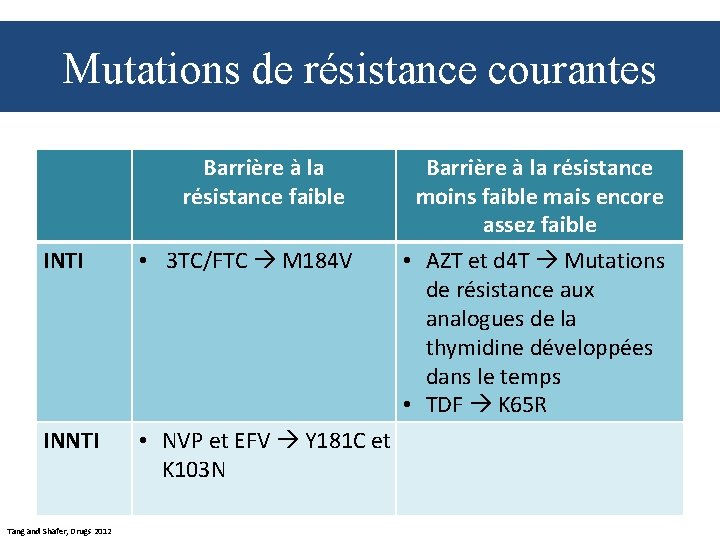
Mutations de résistance courantes Barrière à la résistance faible INTI • 3 TC/FTC M 184 V INNTI • NVP et EFV Y 181 C et K 103 N Tang and Shafer, Drugs 2012 Barrière à la résistance moins faible mais encore assez faible • AZT et d 4 T Mutations de résistance aux analogues de la thymidine développées dans le temps • TDF K 65 R

M 184 V • Sélectionnée par le 3 TC et le FTC, elle entraîne une résistance élevée au 3 TC et au FTC • Réduit la capacité réplicative du virus • Augmente la sensibilité à l'AZT et au TDF Tang and Shafer, Drugs 2012

Y 181 C et K 103 N • Y 181 C sélectionnée par la NVP, elle entraîne une résistance élevée à la NVP – Entraîne également une résistance à l'EFV • K 103 N sélectionnée par la NVP ou l'EFV, elle entraîne une résistance élevée aux deux Tang and Shafer, Drugs 2012; Stanford University, HIV Drug Resistance Database

K 65 R • Sélectionnée principalement par le TDF mais émerge aussi avec le d 4 T, l'ABC, la ddl • Entraîne une résistance moyenne au TDF, à l'ABC, à la ddl, au 3 TC/FTC et une faible résistance au d 4 T • Augmente la sensibilité à l'AZT Tang and Shafer, Drugs 2012

TAM • M 41 L, D 67 N, K 70 R, L 210 W, T 215 F/Y, et K 219 Q/E figurent parmi les TAM • Sélectionnées par l'AZT et le d 4 T • Entraînent une résistance croisée à plusieurs INTI • Les mutations émergent dans le temps selon deux schémas différents, mais peuvent se chevaucher Tang and Shafer, Drugs 2012; Marcelin et al. , Journal Medical Virology 2004

Inhibiteurs de l’intégrase (INI) • Le raltegravir (RAL) et l’elvitegravir (EVG) ont une plus faible barrière à la résistance • Le dolutégravir (DTG) a une barrière plus élevée – Pas d’échec thérapeutique dû à la résistance dans les essais comparatifs randomisés sur le dolutegravir avant mise sur le marché • RAL : comprimés 400 mg, comprimés sécables à croquer 100 mg, comprimés à croquer 25 mg, granulés (50 mg) pour suspension buvable • DTG : comprimés de 50 mg, 25 mg et 10 mg • Faibles interactions médicamenteuses • Peu d'effets indésirables mais une hypersensibilité allergique, des troubles du sommeil ou des vertiges peuvent être observés chez certains patients.

Le dolutégravir en 1ère intention - Avantages par rapport à l’éfavirenz ou la névirapine • Plus faible potentiel d’interaction médicamenteuse • Délai de suppression virale plus court • Barrière génétique plus élevée à la résistance médicamenteuse • Demi-vie longue • Comprimés de petite taille (plus faciles à avaler) • Actif contre l’infection à VIH-2, naturellement résistante à l’EFV • Disponible sous forme de générique à dose fixe • Possibilité de prix réduits dans les pays à revenu faible ou intermédiaire

Q 148 H/K/R/N • Il y a plusieurs substitutions possibles d’acide aminé en position 148 du gène de l’intégrase qui génèrent une résistance aux INI. • Cela arrive rarement lors qu’un INI puissant est utilisé dans un traitement composé de 2 ou 3 médicaments actifs. • Cela arrive plus souvent lorsque des INI de première génération moins puissants (RAL ou EVG) sont utilisés en première intention. Le patient change ensuite de traitement.

Recommandations de l’OMS

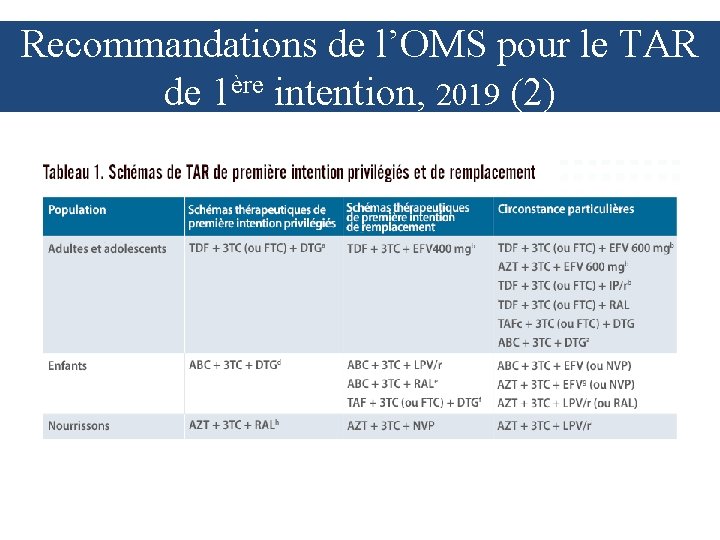
Recommandations de l’OMS pour le TAR de 1ère intention, 2019

Recommandations de l’OMS pour le TAR de 1ère intention, 2019 (2)

Traitement de 2ème intention • Pour le choix du traitement de 2ème intention, il convient de prendre en considération les médicaments que le/la patient. e a déjà pris auparavant et quelle résistance le virus a pu développer

Recommandations de l’OMS pour le TAR de 2ème intention, 2019 (2)

Recommandations de l’OMS pour le TAR de 2ème intention, 2019

Recommandations de l’OMS : traitements de 2ème intention (2) • Optimisation du traitement de fond à base d’INTI – Envisager le génotypage – Changements empiriques – utiliser AZT/3 TC si TDF/3 TC présents dans le traitement précédent et vice versa • Le dolutégravir associé à au moins un INTI actif (suggéré par le test de génotypage) constitue généralement un traitement approprié.

Traitements de deuxième intention dans le pays. Adultes • Renseigner conformément aux recommandations nationales

Traitements de deuxième intention dans le pays. Enfants • Renseigner conformément aux recommandations nationales

Anomalies du tube neural et DTG • La prévalence dans l’étude Tsepamo était de 5/1683 expositions au DTG en période périconceptionnelle • Trois fois supérieure à celle des femmes non exposées au DTG • 0, 30 % (1 sur 1000 expositions en période périconceptionnelle) • Le DTG semble sûr après fermeture du tube neural (~ 8 semaines de grossesse)

Inhibiteurs de la protéase • Acceptable chez les adolescentes et les femmes en âge de procréer • Barrière à la résistance élevée • DRV/r barrière à la resistance la plus élevée • Associations en doses fixes thermostables ATV/r et LPV/r disponibles • Interactions médicamenteuses, notamment avec les médicaments contre la tuberculose • Effets indésirables gastro-intestinaux (notamment nausées et diarrhée) courants Tang and Shafer, Drugs 2012; WHO Guidelines, 2013

Traitements de troisième intention • Incluent des médicaments sans résistance croisée aux traitements précédemment utilisés – Inhibiteurs de l'intégrase, IP de deuxième génération (darunavir/r) et INNTI (etravirine) • Adaptés en fonction de ce qui est disponible dans le pays • Le génotypage peut s’avérer utile, mais les mutations présentes dans l’ADNc mais non réplicatives peuvent être manquées – Plus utile pour le TAR récent ou en cours

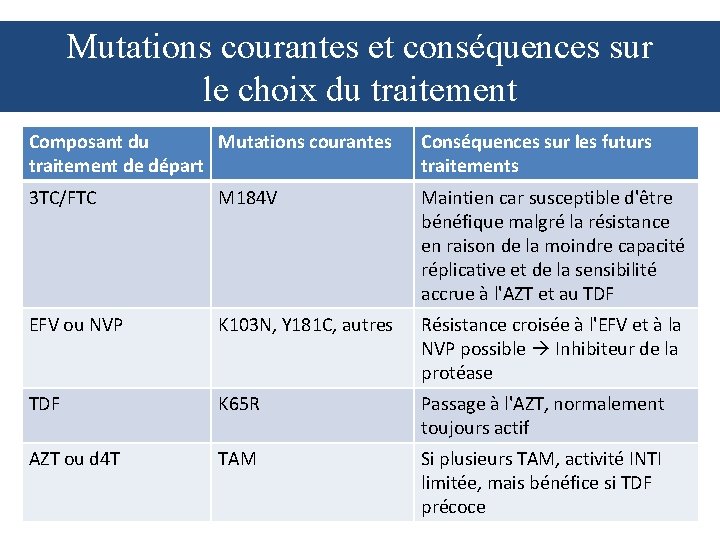
Mutations courantes et conséquences sur le choix du traitement Composant du Mutations courantes traitement de départ Conséquences sur les futurs traitements 3 TC/FTC M 184 V Maintien car susceptible d'être bénéfique malgré la résistance en raison de la moindre capacité réplicative et de la sensibilité accrue à l'AZT et au TDF EFV ou NVP K 103 N, Y 181 C, autres Résistance croisée à l'EFV et à la NVP possible Inhibiteur de la protéase TDF K 65 R Passage à l'AZT, normalement toujours actif AZT ou d 4 T TAM Si plusieurs TAM, activité INTI limitée, mais bénéfice si TDF précoce

Traitements de troisième intention dans le pays. Adultes • Renseigner conformément aux recommandations nationales

Traitements de troisième intention dans le pays. Enfants • Renseigner conformément aux recommandations nationales

Résumé • Éviter le changement précoce ou tardif de TAR. • En cas de changement motivé par un échec thérapeutique, éviter de remplacer un seul agent. • Il convient de tenir compte des mutations de résistance couramment associées aux agents des traitements précédents lors du choix d'un traitement de deuxième ou de troisième intention.

Cas 1 • Femme de 47 ans sous TDF/FTC/EFV depuis 2 ans avec des périodes de faible observance. • La surveillance systématique de la charge virale est mise en place et ses résultats font état d'une charge virale de 4 500 copies/ml. • Vous l'appelez pour lui donner rendez-vous au centre de soins et l'évaluation met en évidence une faible observance. • Elle assiste à cinq séances mensuelles de conseils pour une meilleure observance et parvient à une bonne observance pendant 3 mois. Le résultat de la nouvelle mesure de sa charge virale est de 3 300 copies/ml.

Cas 1 (2) • Quelles sont vos conclusions ? • Que faut-il faire ?

Cas 2 (3) • Homme de 28 ans récemment diagnostiqué séropositif au VIH en consultation externe. • Mis sous TDF/FTC/EFV et première mesure de la charge virale de 890 000 copies/ml. • Assiste à des séances de conseils pour une meilleure observance et parvient rapidement à une bonne observance. • Après trois mois de bonne observance constatée, le résultat de la nouvelle mesure de la charge virale est de 3 700 copies/ml.

Cas 2 (4) • Quelles sont vos conclusions ? • Que faut-il faire ?

Questions