RADSprocessen i reumatologien Ved Tove Lorenzen RADS Fagudvalg

















- Slides: 24

RADS-processen i reumatologien Ved Tove Lorenzen RADS Fagudvalg (Region Midts repræsentant)

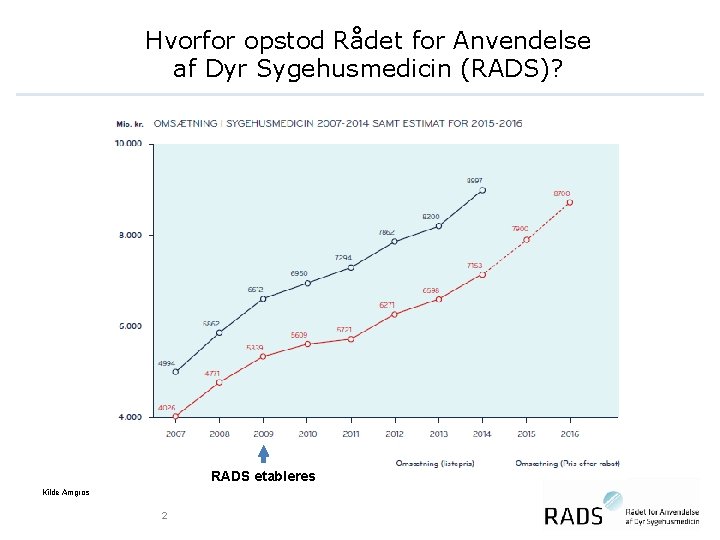
Hvorfor opstod Rådet for Anvendelse af Dyr Sygehusmedicin (RADS)? RADS etableres Kilde Amgros 2

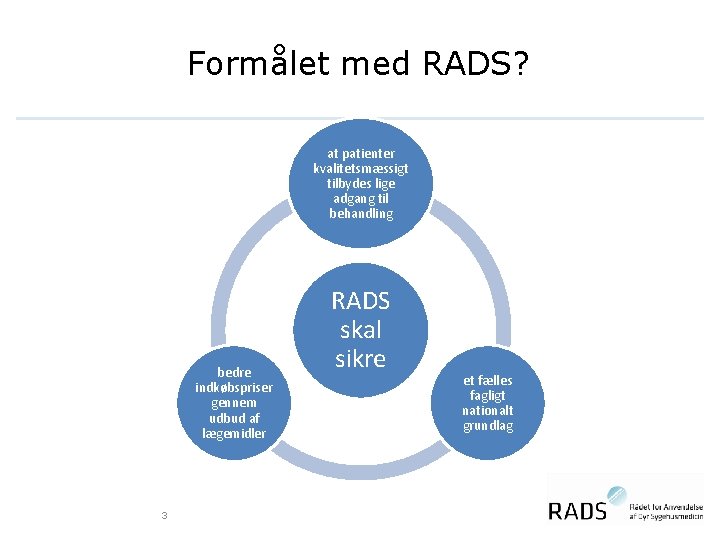
Formålet med RADS? at patienter kvalitetsmæssigt tilbydes lige adgang til behandling RADS skal sikre bedre indkøbspriser gennem udbud af lægemidler 3 RADS skal sikre et fælles fagligt nationalt grundlag

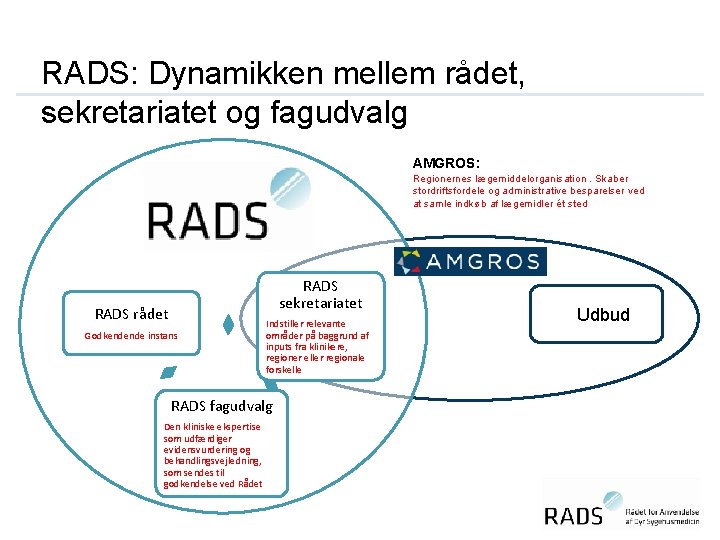
RADS: Dynamikken mellem rådet, sekretariatet og fagudvalg AMGROS: Regionernes lægemiddelorganisation. Skaber stordriftsfordele og administrative besparelser ved at samle indkøb af lægemidler ét sted RADS sekretariatet RADS rådet Godkendende instans Indstiller relevante områder på baggrund af inputs fra klinikere, regioner eller regionale forskelle RADS fagudvalg Den kliniske ekspertise som udfærdiger evidensvurdering og behandlingsvejledning, som sendes til godkendelse ved Rådet Udbud

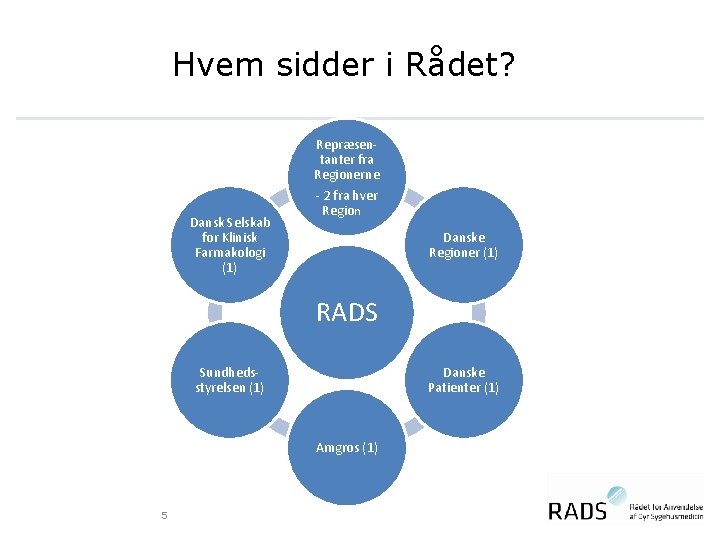
Hvem sidder i Rådet? Repræsentanter fra Regionerne Dansk Selskab for Klinisk Farmakologi (1) - 2 fra hver Region Danske Regioner (1) RADS Danske Patienter (1) Sundhedsstyrelsen (1) Amgros (1) 5

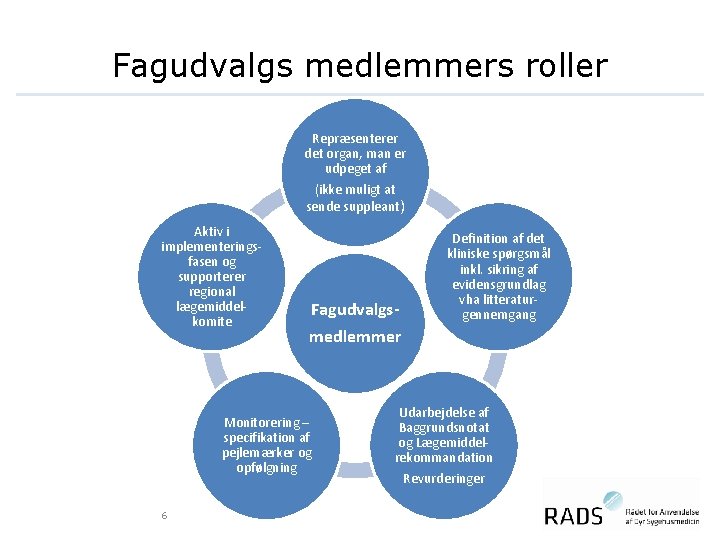
Fagudvalgs medlemmers roller Repræsenterer det organ, man er udpeget af (ikke muligt at sende suppleant) Aktiv i implementeringsfasen og supporterer regional lægemiddelkomite Fagudvalgsmedlemmer Monitorering – specifikation af pejlemærker og opfølgning 6 Definition af det kliniske spørgsmål inkl. sikring af evidensgrundlag vha litteraturgennemgang Udarbejdelse af Baggrundsnotat og Lægemiddelrekommandation Revurderinger

Det reumatologiske Fagudvalg Herunder 4 arbejds grupper (RA, Sp. A, Ps. A, JIA) • • • • • • Formand Hanne Merete Lindegaard, Overlæge, ph. d. , Dansk Medicinsk Selskab og Dansk Reumatologisk Selskab, samt Region Syddanmark Næstformand, Lis Smedegaard Andersen, ph. d. , speciallæge i intern medicin og reumatologi. Dansk Reumatologisk Selskab Tove Lorenzen, Specialeansvarlig overlæge, Region Midtjylland Marcin Szkudlarek, Overlæge, ph. d. , Region Sjælland Jesper Nørregaard, Klinikchef, ledende overlæge, dr. med. , Region Hovedstaden Vivian Kjær Hansen, Ledende overlæge, Region Nordjylland Birgitte Brock, Overlæge, lektor, ph. d. , sektionsleder. Dansk Selskab for Klinisk Farmakologi Camilla Munk Mikkelsen, Farmaceutisk sekretær, cand. pharm. Dansk Selskab for Sygehusapoteksledelse Dorte Vendelbo Jensen, Overlæge, DANBIO Lene Mandrup Thomsen, Fysioterapeut, Master i Rehabilitering. Gigtforeningen Troels Herlin, Overlæge, professor, dr. med. Inviteret af formanden Robin Christensen, Cand. scient. , Ph. D, Lektor i medicinsk statistik, seniorstatistiker. Inviteret af formanden. Lone Skov, Professor, overlæge, dr. med ph. d. , Hud- og allergi afdelingen, Gentofte Hospital.

Offentlige dokumenter Baggrundsnotat: Den videnskabelige og kliniske argumentation for Behandlings vejledning. Beskriver hvilke lægemidler der anses ligestillede, hvem der skal behandles med dem samt skifte- og seponerings kriterier Behandlings rekommandation: Konkretiserer vejledningen med de anbefalede lægemidler OG konkrete produkter, der skal anvendes efter udbud konkretiserer behandlingsvejledningen med de anbefalede lægemidler og konkrete produkter, der skal anvendes efter udbud Fra aktuelle runde (tredje) ny skabelon, hvori alle 3 dokumenter samles 8

Offentliggørelse på RADS hjemmeside http: //www. regioner. dk/radsdk Kan også tilgås via Danbio (Søg: RADS) 9

RADS-vejledninger status • Forpligtende vejledninger baseret på national klinisk konsensus • Skal kunne lægges til grund for regionernes fælles indkøb af sygehusmedicin (udbud) • De 5 regioner har givet hinanden håndslag på, at de vil efterleve RADS-vejledningerne • Vejledningerne er ikke juridisk bindende for den enkelte læge (gælder også NKR, vejledninger fra specialeselskaber mv. ) • Men den enkelte region kan pålægge deres ansatte (lægerne) at efterleve vejledningerne (den generelle patientpopulation) • Behandling af den individuelle patient er altid et lægefagligt skøn jf. den frie ordinationsret.

Fagudvalget fra start til slut 1. fase 6 -8 måneder 2. fase 3. fase 4. fase RADS møde • Det kliniske spørgsmål: Specifikation af opgaven ud fra også kommissorium • Introduktion til GRADE samt specifikation af PICO Se på • Krav og spørgsmål til leverandørpræsentationer skrivevejledningen. • Arbejdsgrupper/arbejdsdeling/roller Research (guidelines, • Introduktion til pejlemærker og forbrugstal metaanalyser) og litteratursøgning • Leverandørpræsentationer • Fremlæggelse af foreløbigt resultat af litteratursøgning, herunder søgestrategi, udvælgelseskriterier, søgeord, referencehåndtering Mødes i grupperne. • Opdeling af litteratur til dataekstraktion Gennemgang af • Lægemiddelhåndteringsanalyse litteratur Evidens vurdering • Evidenssyntese/GRADE profil* • Præsentation af opstartet baggrundsnotat Mødes i grupperne. • Sammenligningsgrundlag Udarbejde BGN • Estimering af pejlemærker og patientantal (Ex. Danbio) • Indhold af baggrundsnotat inkl. godkendelse • Præsentation af udarbejdede pejlemærker • Fra evidens til anbefaling • Præsentation v/formanden og/eller udvalgte medlemmer af fagudvalget 11 Udarbejde præsentation Monitorering

GRADE i RADS Fagudvalg Grades of Recommendation, Assessment, Development and Evaluation En metode til at vurdere evidens, kvaliteten heraf samt efterfølgende formulere anbefalinger, som er mere systematisk, transparent og omfattende end tidligere anvendte metoder Klar adskillelse mellem evidens-kvalitet og styrken af anbefaling

GRADE består af flere delelementer 1. Formulering af kliniske spørgsmål 2. Udledning af PICO’er 3. Systematisk litteratursøgning og -gennemgang 4. Evidensvurdering 5. Afdækning af værdier og præferencer 6. Graduering af rekommandationer 13

Klinisk spørgsmål Eksempel fra Reumatoid Artritis (RA) • Er der forskel på de biologiske lægemidler til behandling af patienter med reumatoid artritis som ikke tidligere har fået biologisk behandling? • Patienter hvor kombinationsbehandling med syntetiske Disease Modifying Anti Rheumatic Drugs (s. DMARDs) er mulig • Patienter hvor kombinationsbehandling ikke er en mulighed • Er der forskel på de biologiske lægemidler til behandling af patienter med reumatoid artritis som tidligere har været i behandling med biologisk behandling? • Patienter hvor kombinationsbehandling med s. DMARDs er mulig • Patienter hvor kombinationsbehandling ikke er en mulighed 14

PICOer fra RA Hver enkelt PICO danner baggrund for en metaanalyse P = patients P 1 : Patienter med RA, som har svigtet konventionel s. DMARD behandling, som ikke tidligere har været behandlet med biologiske lægemidler P 2: Patienter med RA, som har svigtet mindst et biologisk lægemiddel P 3: Patienter med RA, som er intolerante for s. DMARD behandling. P 4: Patienter med RA, som er intolerante for s. DMARD behandling og har svigtet på mindst 1 tidligere biologisk lægemiddel I = interventions I 1: etanercept + s. DMARD(s) I 2: I 3: I 4: I 5: I 6: I 7: I 8: I 9: infliximab 3 mg/kg + s. DMARD(s) infliximab 6 mg/kg + s. DMARD(s) adalimumab + s. DMARD(s) certolizumab + s. DMARD(s) golimumab + s. DMARD(s) abatacept + s. DMARD(s) anakinra + s. DMARD(s) tocilizumab + s. DMARD(s) C = comparators Interventionerne som angivet ovenfor (C 1 -9) O = outcomes O 1: ACR 50 4 -6 måneder O 2: withdrawals due to adverse events 4 -6 måneder O 3: total sharp score (TSS) ~12 måneder 15

Eksempel Forest plot for RA Biologisk vs DMARD (MTX)

Værdier og præferencer FU’s værdier og præferencer ift. de relevante behandlingsalternativer diskuteres – både fra et behandlerperspektiv og fra et organisatorisk perspektiv. Patientforeningerne opfordres til at sende deres input Fra 3. runde repr fra GF i FU Skal fremgå af baggrundsnotatet. 17

Graduering af rekommandationer Rekommandationer gradueres på baggrund af • Evidensens kvalitet • Variationen i værdier og præferencer • Forholdet mellem samlede fordele og ulemper 18

Graduering af rekommandationer Strong recommendation ”Fagudvalget/RADS rekommanderer” Anvendes i situationer, hvor det er helt tydeligt, at fordelene klart overstiger ulemperne. Weak recommendation ”Fagudvalget/RADS rekommanderer med forbehold. ” Anvendes i situationer, hvor det ikke er klart, om fordelene overstiger ulemperne, eller hvor der er tvivl om størrelsesordenen af fordele og ulemper. 19

Vejen til det vindende lægemiddel RADS • Fagudvalget ligestiller lægemidler, doser etc. • Lægemidlerne udbydes Udbud • Det vindende lægemiddel identificeres • Lægerne er forpligtede til - i udgangspunktet Klinik - at anvende det vindende lægemiddel 20

Klinik Lægerne er forpligtede til - i udgangspunktet - at anvende det vindende lægemiddel • Efterlevelsesmål kvantificerer i hvilken udstrækning det kan undlades at anvende 1. linje og eventuelt efterfølgende linjer. 21 • Afvigelse fra 1. linje skal altid begrundes særskilt i patientjournal. • I nogle regioner skal afvigelse tillige begrundes overfor stedligt sygehusapotek eller lægemiddel-kommite

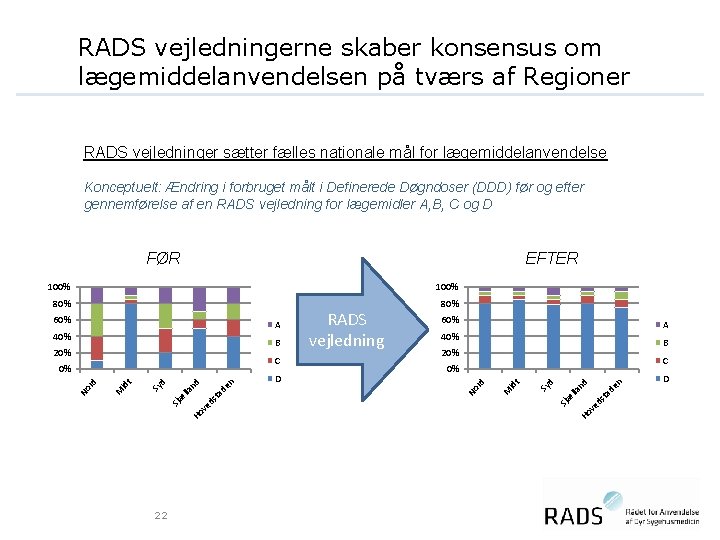
RADS vejledningerne skaber konsensus om lægemiddelanvendelsen på tværs af Regioner RADS vejledninger sætter fælles nationale mål for lægemiddelanvendelse Konceptuelt: Ændring i forbruget målt i Definerede Døgndoser (DDD) før og efter gennemførelse af en RADS vejledning for lægemidler A, B, C og D FØR EFTER 100% 80% C de n nd ve ds ta lla Ho Sy d 0% Sjæ ta ds ve Ho Sjæ lla de n nd d t id M rd No Sy 22 D B 20% t C 0% A 40% id B 20% 60% M 40% RADS vejledning rd A No 60% D

Fremadrettet og Nyhed • 1. januar 2017 afløser et nyt Medicinråd arbejdet i RADS • Alle RADS' fagudvalg afslutter inden da det arbejde, som er påbegyndt i år, så Medicinrådet kan begynde arbejdet fra bunden. • RADS’ anbefalinger gælder indtil Medicinrådet beslutter at ændre. • 24. august 2016 • Regionerne opretter fælles medicinforum, som skal sikre en mere ensartet og professionel sagsbehandling af nye lægemidler i regionerne. • Lægemidler, der ikke bliver sagsbehandlet i RADS/KRIS (Koordineringsrådet for ibrugtagning af sygehusmedicin) • Nye godkendte lægemidler, som godkendes i DK mellem 2 RADS runder – ex: Cosentyx

Biosimilære reumatologiske biologiske lægemidler Svarer til et velkendt biologisk lægemiddel, som allerede er godkendt, men er ikke kopipræparater som kendes fra syntetiske kemisk fremstillede lægemidler. Både originale biologiske og biosimilære biologiske lægemidler produceres af levende organismer, fx celler, gær og bakterier. Derfor forekommer små, men ubetydelige forskelle fra produktion til produktion af originallægemidlet. Gælder også for original lægemidlet. Biosimilært infliximab og Remicade® samt biosimilært etanercept og Enbrel® anses af EMA/CHMP (Committee for Human Medicinal Products) som fuldt ud biosimilære for så vidt angår fysisk/kemisk karakterisering samt den biologiske aktivitet af de to antistoffer. For biosimilært infliximab fandtes en mindre forskel i sammenligning med Remicade i en særlig form for glykosylering med sukker-stoffet afucose (kaldet afucosylering). Denne forskel kan have en mulig betydning for antistofafhængig cellulær cytotokcitet (ADCC – Antibodydependent cellular cytotoxicity), men har ikke kunnet påvises at have betydning for den kliniske effekt og sikkerhed af biosimilært infliximab. Udover denne omfattende karakterisering og sammenligning af de tilgængelige versioner af infliximab henholdsvis etanercept er effekt og sikkerhed ved anvendelse af disse biosimilære versioner undersøgt i kliniske studier uden påvisning af forskelle.
 Nis bank lorenzen
Nis bank lorenzen Dr mark lorenzen
Dr mark lorenzen Partially circumscribed mass
Partially circumscribed mass Cadrads
Cadrads Li rads
Li rads Hypointenz
Hypointenz Birads klasifikacija
Birads klasifikacija Birads staging
Birads staging Tove marquardsen
Tove marquardsen Tove valley broadband
Tove valley broadband Vitsord skala
Vitsord skala Verdensborger i danmark
Verdensborger i danmark Intrapersonell kommunikation
Intrapersonell kommunikation Tove engedal
Tove engedal Psykologi 1 tove phillips
Psykologi 1 tove phillips Dolken tove ditlevsen tema
Dolken tove ditlevsen tema 4 types of trust
4 types of trust Senmodernismen
Senmodernismen Abc ved matrix
Abc ved matrix Efterårslandskab. hankehøj ved vallekilde
Efterårslandskab. hankehøj ved vallekilde Malzeme yönetim fonksiyonları
Malzeme yönetim fonksiyonları Eksempler på fordybelsesområder
Eksempler på fordybelsesområder Personalpolitikk ved omstillingsprosesser
Personalpolitikk ved omstillingsprosesser Genhusning ved forsikringsskade
Genhusning ved forsikringsskade Have ved
Have ved













































