Radioactiviteit straling Rond 1900 onderzocht door echtpaar Curie
















- Slides: 21

Radioactiviteit

α, β, γ-straling Rond 1900 onderzocht door echtpaar Curie (Pierre en Marie). l Het betreft straling afkomstig uit de kern. l

Radioactiviteit l Radioactieve stoffen: stoffen die vanzelf straling uitzenden. Radio betekent stralend, en actieve betekend vanzelf. Een radioactieve stof zendt straling uit die niet zichtbaar is. Atomen met een instabiele kern zijn radioactief en zenden ioniserende straling uit: radioactief verval. l Waar straling uit radioactieve bronnen komt, veranderen moleculen in ionen. Daarom noemen we deze straling ook wel ioniserende straling. l

Besmetting of bestraling? l Radioactieve bron: het voorwerp waarin zich de radioactieve stof bevind. l Besmet: als je besmet bent, heb je zelf radioactieve stof op je huid gekregen of in geademd; je bent dan zelf ook een bron van straling. l Bestraalt: als je bestraalt bent, heb je zelf radioactieve stof geabsorbeerd. Je hebt zelf geen radioactieve stof binnen gekregen en je bent dus geen radioactieve bron geworden.

Atomen Een atoom: positief geladen kern waaromheen negatief geladen elektronen bewegen. De kern bestaat uit twee deeltjes; nucleonen: neutronen en protonen. Schrijfwijze: X: het chemisch symbool van het atoom (nuclide), A: het massagetal/massanummer/nucleongetal (het aantal kerndeeltjes) Z: het atoomnummer (het aantal protonen)

Atomen 235 -U: een uraniumatoom. Het atoom heeft atoomnummer 92 in het periodiek systeem. In de atoomkern zitten 92 protonen. Het massagetal is 235. Het aantal neutronen is dan 235 -92=143. Het aantal neutronen: N = A – Z. l Kernen van een gegeven type atoom hebben altijd hetzelfde aantal protonen, maar niet altijd hetzelfde aantal neutronen. Deze l kernen worden isotopen genoemd. l De atoomdeeltjes:

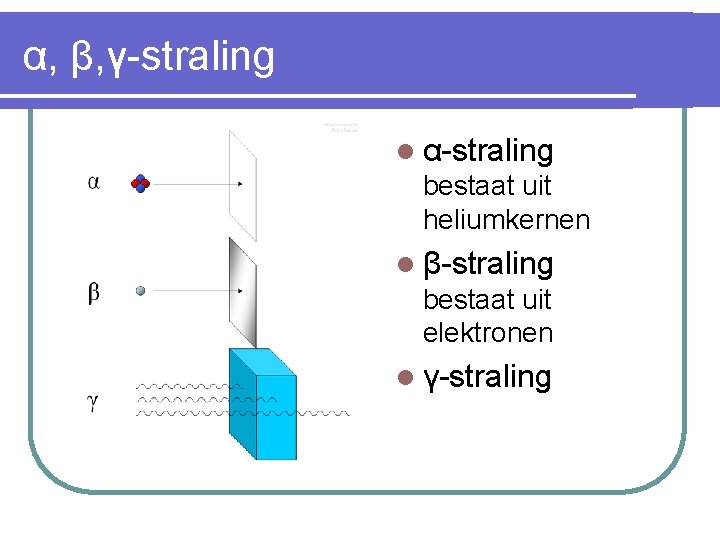
α, β, γ-straling l α-straling bestaat uit heliumkernen l β-straling bestaat uit elektronen l γ-straling

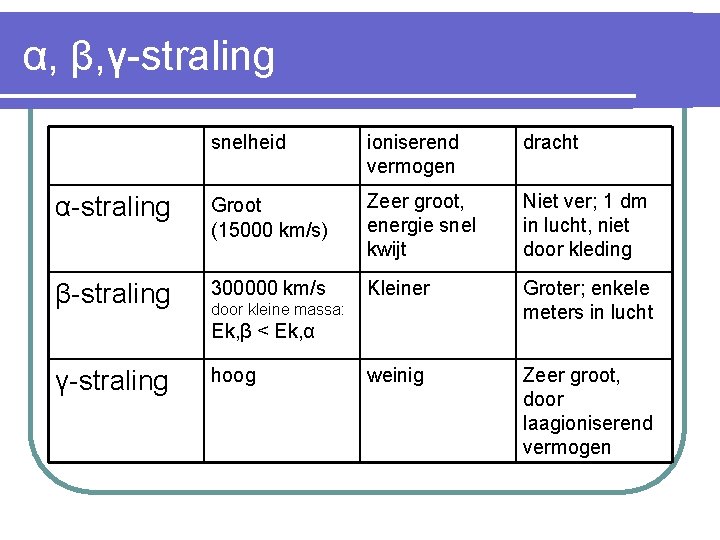
α, β, γ-straling snelheid ioniserend vermogen dracht α-straling Groot (15000 km/s) Zeer groot, energie snel kwijt Niet ver; 1 dm in lucht, niet door kleding β-straling 300000 km/s Kleiner Groter; enkele meters in lucht weinig Zeer groot, door laagioniserend vermogen door kleine massa: Ek, β < Ek, α γ-straling hoog

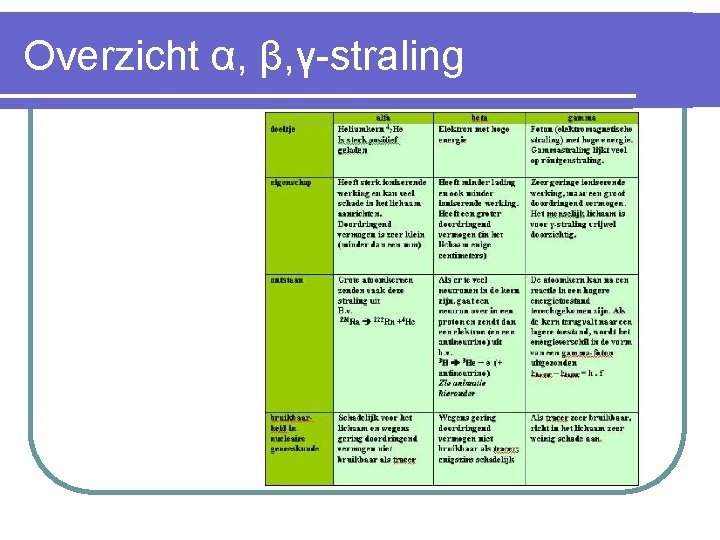
Overzicht α, β, γ-straling

Radioactief verval l α-straling een voorbeeld: l β-straling een voorbeeld: l γ-straling een voorbeeld: Let op: γ-straling komt meestal voor als bijproduct bij de andere radioactieve vervalreeksen l Op de site kun je hiermee oefenen: http: //www. emmauscollege. nl/nask/applets/vervalreeks. html

Vrijkomende energie l 1 e. V is de energie die een elektron opneemt als deze een spanningsverschil van 1 V doorloopt. l E = V · Q [J] = [J/C] · [C]

Activiteit l In een radioactieve stof vervallen er per seconde zeer veel atomen. Hoe meer atomen per seconde vervallen, hoe meer straling de stof zal uitzenden. Het aantal atomen dat per seconde vervalt, wordt de activiteit A genoemd. De eenheid is becquerel (Bq). l A(t) : de activiteit op tijdstip t in Bq (becquerel) ΔN(t) : het aantal actieve kernen Δt : tijd in s (seconden) Het min-teken geeft een afname aan.

Halveringstijd Een stof vervalt…. http: //www. emmauscollege. nl/nask/applets/vervalwet. html l De activiteit van een hoeveelheid stof wordt geleidelijk aan steeds minder. Er blijven namelijk steeds minder atomen over die nog moeten vervallen. De tijd t 1/2 wordt de halveringstijd genoemd. Dit is de tijd waarin de helft van de instabiele atomen van die stof vervalt. Na verloop van één halveringstijd is het aantal instabiele atomen dus met 50% afgenomen. l omdat A(t) ~ N(t), geldt ook : A(t)=A(0). l N(t) N(0) t t 1/2 : het aantal actieve kernen op tijdstip t = 0 : tijd in s (seconden) : de halveringstijd in s (seconden)

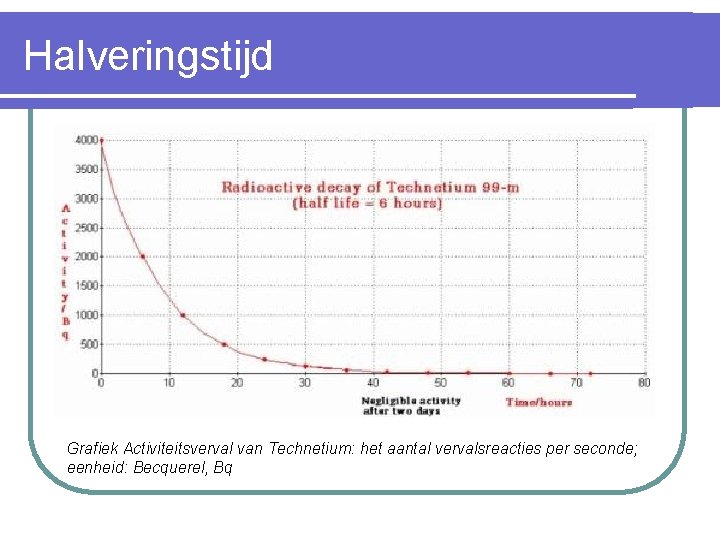
Halveringstijd Grafiek Activiteitsverval van Technetium: het aantal vervalsreacties per seconde; eenheid: Becquerel, Bq

Halveringsdikte l Als straling op een laag materiaal met een dikte d valt, wordt een deel ervan geabsorbeerd. De dikte waarbij de intensiteit wordt gehalveerd, noemt men de halveringsdikte d 1/2. N(d) N(0) d d 1/2 : het aantal actieve kernen na het doordringen van een dikte d : het aantal actieve kernen vóór het doordringen : dikte van het materiaal in m (meter) : de halveringsdikte in m (meter)

Risico’s l EL RSONE dt, E P D r EN t, wo , VLIEG k a R a O m O V t jn CO’S sche vluch wust te zi I S I R e ti INGS atlan hien van b dosis s STRAL n a r en ssc de en t neel o s Wie e er zich mi en verhoog r e e nd p r deren n a zonde steld aan ng. Vliege n da i ge méér n n a bloot ende stral a t g. Ee s n i l r ’ a e s r ionis ent flyer mische st s qu ‘fre an deze ko zaken. a an bloot and v t s e g huidi Het risico van ioniserende straling beschrijven we met de begrippen stralingsdosis en dosisequivalent.

Dosis l De stralingsdosis D is de hoeveelheid stralingsenergie die een bepaald volume heeft geabsorbeerd per kg bestraald materiaal. D E m : stralingsdosis in Gy (gray) : geabsorbeerde stralingsenergie in J (joule) : massa in kg (kilogram)

Dosisequivalent l De stralingsdosis heeft onvoldoende inzicht in het biologisch effect van de straling. Hierin speelt namelijk ook de soort straling een rol. Om dit effect beter te beschrijven gebruiken we het begrip dosisequivalent.

Dosisequivalent l Het dosisequivalent H is de stralingsdosis vermenigvuldigd met de weegfactor die het effect van de geabsorbeerde straling beschrijft. H : dosisequivalent in Sv (sievert) D : stralingsdosis in Gy (gray) Weegfactor: α-straling 20 β- en γ-straling 1

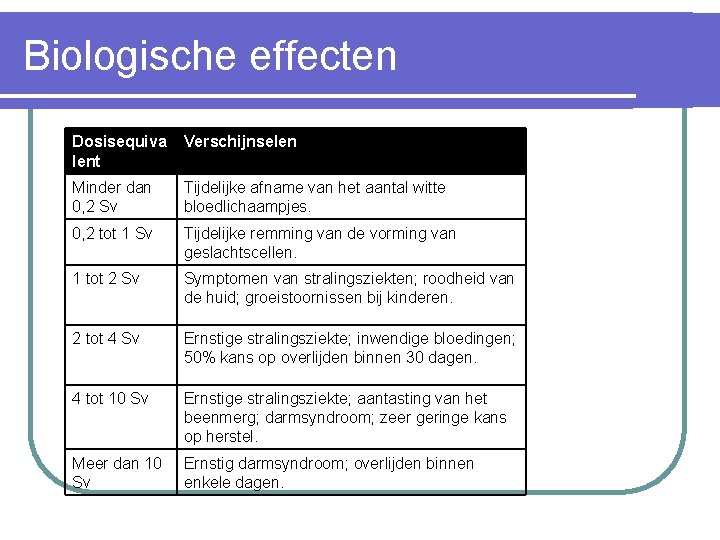
Biologische effecten Dosisequiva lent Verschijnselen Minder dan 0, 2 Sv Tijdelijke afname van het aantal witte bloedlichaampjes. 0, 2 tot 1 Sv Tijdelijke remming van de vorming van geslachtscellen. 1 tot 2 Sv Symptomen van stralingsziekten; roodheid van de huid; groeistoornissen bij kinderen. 2 tot 4 Sv Ernstige stralingsziekte; inwendige bloedingen; 50% kans op overlijden binnen 30 dagen. 4 tot 10 Sv Ernstige stralingsziekte; aantasting van het beenmerg; darmsyndroom; zeer geringe kans op herstel. Meer dan 10 Sv Ernstig darmsyndroom; overlijden binnen enkele dagen.

Einde l Samengevat: 140 -151