Organic Chemistry Second Edition Janice Gorzynski Smith University





![Reazioni di condensazione di composti carbonilici Reazioni aldoliche incrociate [2] Quando uno dei composti Reazioni di condensazione di composti carbonilici Reazioni aldoliche incrociate [2] Quando uno dei composti](https://slidetodoc.com/presentation_image_h/cb36519ce331d7f0f2160ae8b26a9439/image-14.jpg)
- Slides: 22

Organic Chemistry, Second Edition Janice Gorzynski Smith University of Hawai’i Chapter 24 Lecture Outline Prepared by Rabi Ann Musah State University of New York at Albany Copyright © The Mc. Graw-Hill Companies, Inc. Permission required for reproduction or display. 1

Reazioni di condensazione di composti carbonilici La reazione aldolica • Nella reazione aldolica, due molecole di un’aldeide o un chetone reagiscono l’una con l’altra in presenza di una base per formare un composto -idrossi carbonilico. 2

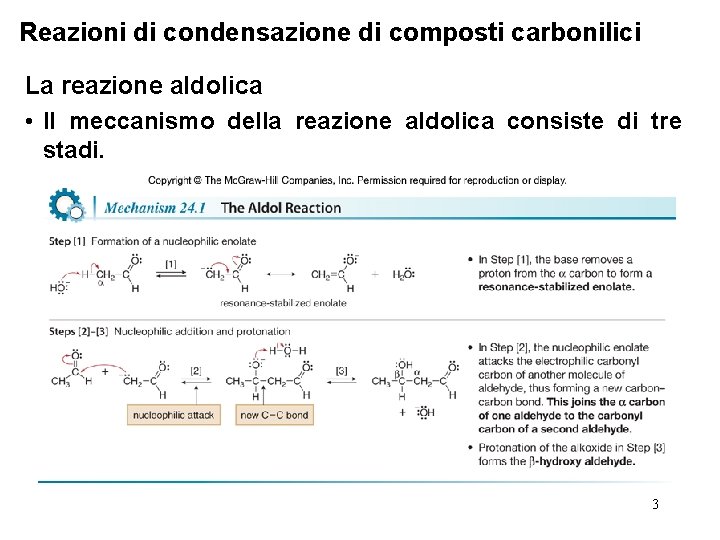
Reazioni di condensazione di composti carbonilici La reazione aldolica • Il meccanismo della reazione aldolica consiste di tre stadi. 3

Reazioni di condensazione di composti carbonilici La reazione aldolica • La reazione aldolica è una reazione reversibile di equilibrio, così che la posizione di equilibrio dipende dalla base utilizzata e dal composto carbonilico. • ¯OH è la base usata comunemente nelle reazioni di condensazione aldolica. Benchè con ¯OH si formi solo una piccola quantità di enolato, questo è appropriato perchè l’aldeide di partenza deve reagire con l’enolato nel secondo stadio della reazione. • La reazione di condensazione aldolica può essere eseguita sia con aldeidi che con chetoni. Con le aldeidi, di solito l’equilibrio favorisce il prodotto, ma con i chetoni l’equilibrio favorisce il composto di partenza. Comunque, ci sono modi per spostare l’equilibrio verso 4 destra.

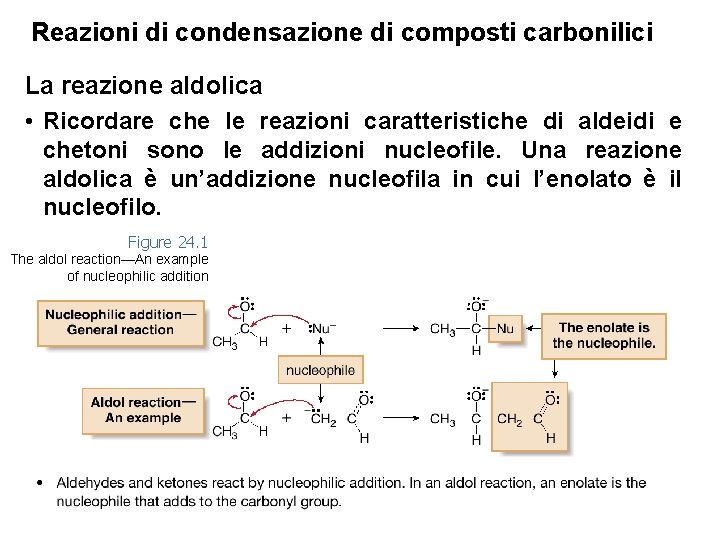
Reazioni di condensazione di composti carbonilici La reazione aldolica • Ricordare che le reazioni caratteristiche di aldeidi e chetoni sono le addizioni nucleofile. Una reazione aldolica è un’addizione nucleofila in cui l’enolato è il nucleofilo. Figure 24. 1 The aldol reaction—An example of nucleophilic addition 5

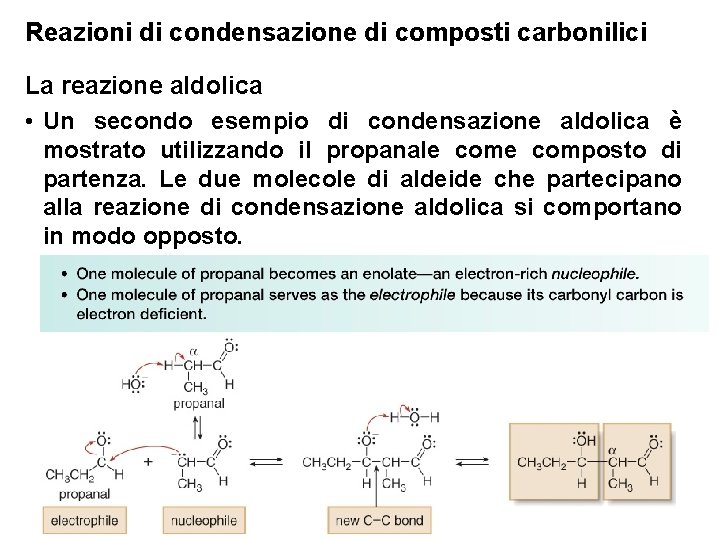
Reazioni di condensazione di composti carbonilici La reazione aldolica • Un secondo esempio di condensazione aldolica è mostrato utilizzando il propanale composto di partenza. Le due molecole di aldeide che partecipano alla reazione di condensazione aldolica si comportano in modo opposto. 6

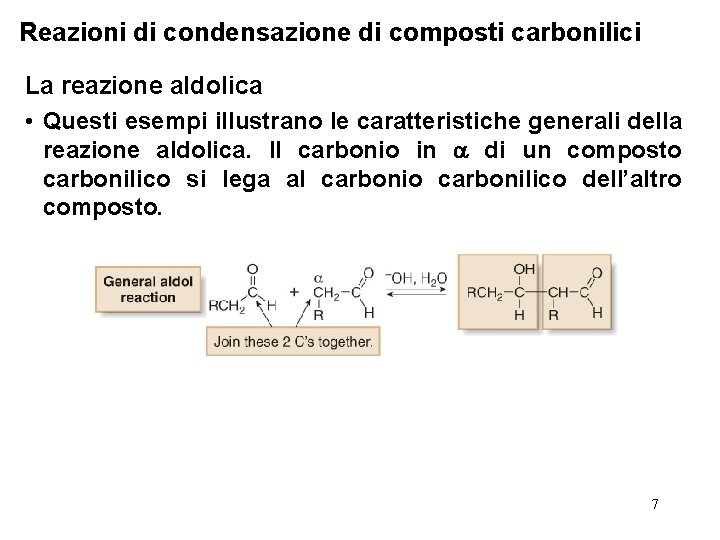
Reazioni di condensazione di composti carbonilici La reazione aldolica • Questi esempi illustrano le caratteristiche generali della reazione aldolica. Il carbonio in di un composto carbonilico si lega al carbonio carbonilico dell’altro composto. 7

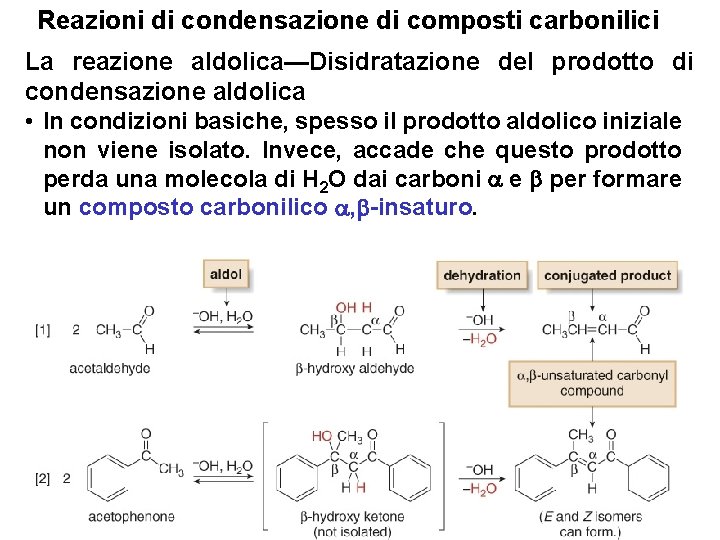
Reazioni di condensazione di composti carbonilici La reazione aldolica—Disidratazione del prodotto di condensazione aldolica • In condizioni basiche, spesso il prodotto aldolico iniziale non viene isolato. Invece, accade che questo prodotto perda una molecola di H 2 O dai carboni e per formare un composto carbonilico , -insaturo. 8

Reazioni di condensazione di composti carbonilici La reazione aldolica • Una reazione aldolica è spesso chiamata una condensazione aldolica, perchè i composti -idrossi carbonilici che si formano inizialmente perdono H 2 O per disidratazione. Una reazione di condensazione è una reazione in cui una piccola molecola, in questo caso H 2 O, è eliminata durante la reazione. • Può essere o non essere possibile isolare il composto idrossi carbonilico nelle condizioni di reazione della condensazione aldolica. Quando un composto carbonilico , -insaturo è ulteriormente coniugato con un doppio legame o un anello benzenico (come nel caso della reazione 2), l’eliminazione di H 2 O è spontanea e non si può isolare il composto -idrossi carbonilico. 9

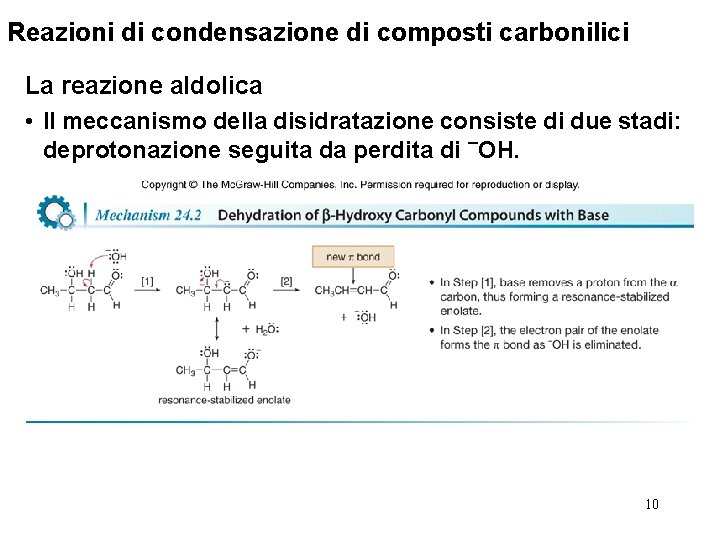
Reazioni di condensazione di composti carbonilici La reazione aldolica • Il meccanismo della disidratazione consiste di due stadi: deprotonazione seguita da perdita di ¯OH. 10

Reazioni di condensazione di composti carbonilici La reazione aldolica • La reazione di eliminazione che porta al processo di disidratazione procede attraverso un meccanismo E 1 c. B. • Il meccanismo E 1 c. B si differenzia dai meccanismi E 1 ed E 2. • Come l’eliminazione E 1, l’E 1 c. B coinvolge due stadi. Diversamente comunque dall’ E 1, l’intermedio nell’ E 1 c. B è un carbanione, non un carbocatione. • E 1 c. B è un acronimo per Eliminazione monomolecolare attraverso la Base Coniugata. • I normali alcoli disidratano solo in presenza di acidi, non di basi, poichè l’ idrossido è un gruppo uscente debole. Tuttavia, quando il gruppo OH si trova in posizione ad un carbonile, la perdita di un H e un OH dalle posizioni e forma un doppio legame coniugato, e la stabilità del sistema coniugato favorisce la reazione nonostante la presenza di un gruppo uscente molto debole. • La disidratazione del composto -idrossi carbonilico iniziale 11 sposta l’equilibrio della reazione aldolica verso destra, favorendo così la formazione dei prodotti.

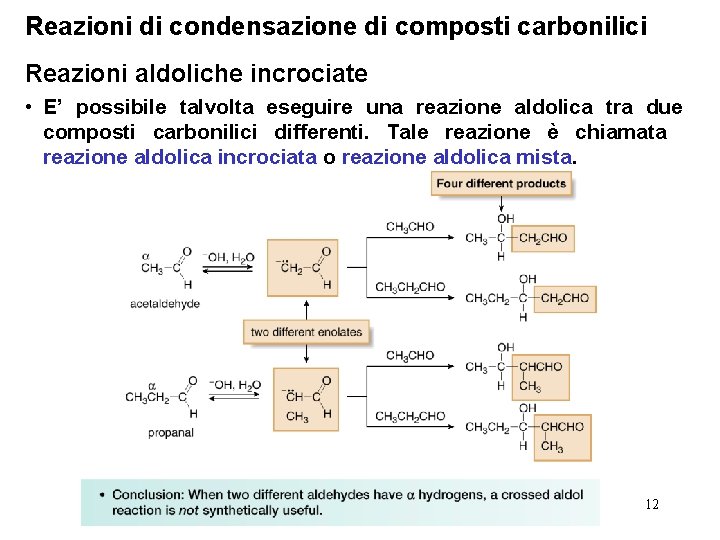
Reazioni di condensazione di composti carbonilici Reazioni aldoliche incrociate • E’ possibile talvolta eseguire una reazione aldolica tra due composti carbonilici differenti. Tale reazione è chiamata reazione aldolica incrociata o reazione aldolica mista. 12

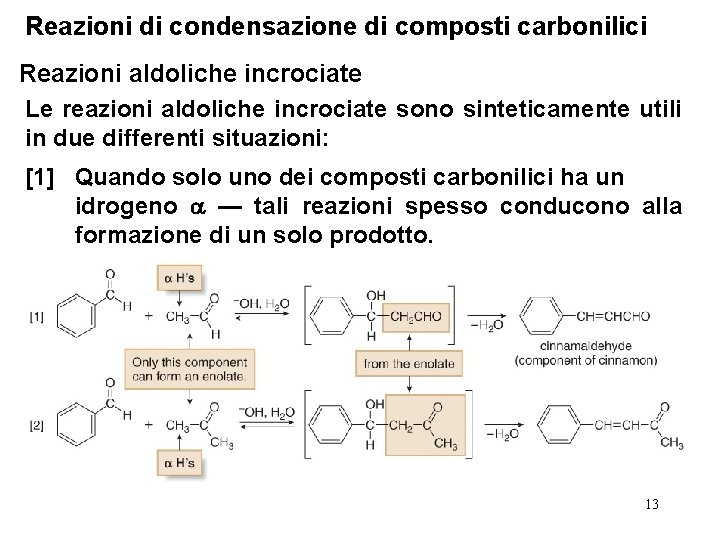
Reazioni di condensazione di composti carbonilici Reazioni aldoliche incrociate Le reazioni aldoliche incrociate sono sinteticamente utili in due differenti situazioni: [1] Quando solo uno dei composti carbonilici ha un idrogeno — tali reazioni spesso conducono alla formazione di un solo prodotto. 13
![Reazioni di condensazione di composti carbonilici Reazioni aldoliche incrociate 2 Quando uno dei composti Reazioni di condensazione di composti carbonilici Reazioni aldoliche incrociate [2] Quando uno dei composti](https://slidetodoc.com/presentation_image_h/cb36519ce331d7f0f2160ae8b26a9439/image-14.jpg)
Reazioni di condensazione di composti carbonilici Reazioni aldoliche incrociate [2] Quando uno dei composti carbonilici ha un protone in particolarmente acido, questi idrogeni sono rimossi più facilmente degli altri idrogeni . Come risultato, il composto -dicarbonilico sarà sempre il componente enolato della reazione aldolica. 14

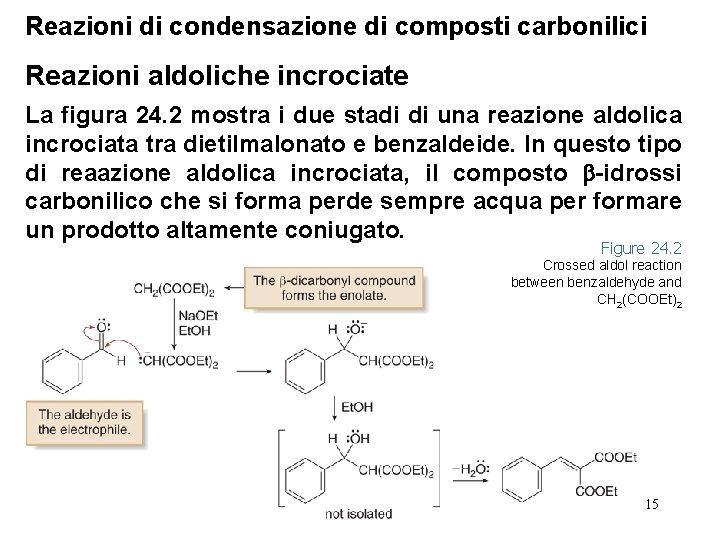
Reazioni di condensazione di composti carbonilici Reazioni aldoliche incrociate La figura 24. 2 mostra i due stadi di una reazione aldolica incrociata tra dietilmalonato e benzaldeide. In questo tipo di reaazione aldolica incrociata, il composto -idrossi carbonilico che si forma perde sempre acqua per formare un prodotto altamente coniugato. Figure 24. 2 Crossed aldol reaction between benzaldehyde and CH 2(COOEt)2 15

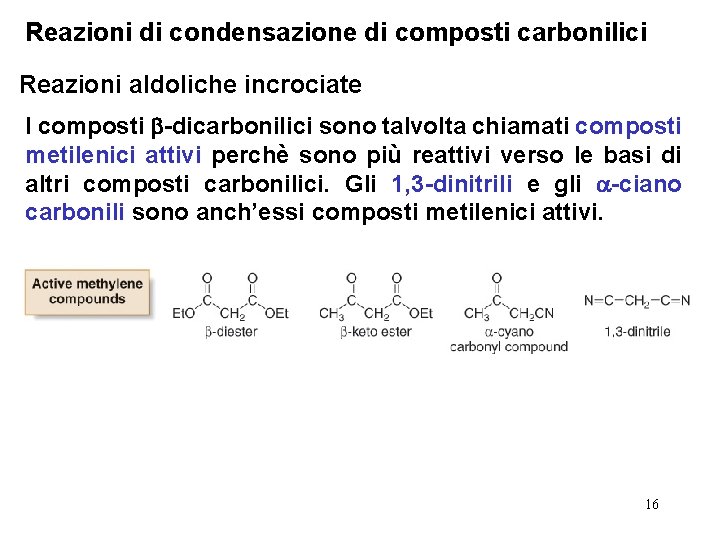
Reazioni di condensazione di composti carbonilici Reazioni aldoliche incrociate I composti -dicarbonilici sono talvolta chiamati composti metilenici attivi perchè sono più reattivi verso le basi di altri composti carbonilici. Gli 1, 3 -dinitrili e gli -ciano carbonili sono anch’essi composti metilenici attivi. 16

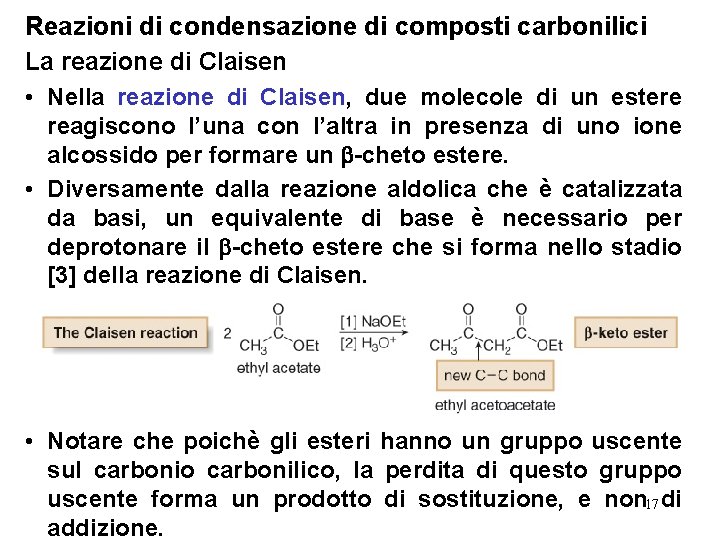
Reazioni di condensazione di composti carbonilici La reazione di Claisen • Nella reazione di Claisen, due molecole di un estere reagiscono l’una con l’altra in presenza di uno ione alcossido per formare un -cheto estere. • Diversamente dalla reazione aldolica che è catalizzata da basi, un equivalente di base è necessario per deprotonare il -cheto estere che si forma nello stadio [3] della reazione di Claisen. • Notare che poichè gli esteri hanno un gruppo uscente sul carbonio carbonilico, la perdita di questo gruppo uscente forma un prodotto di sostituzione, e non 17 di addizione.

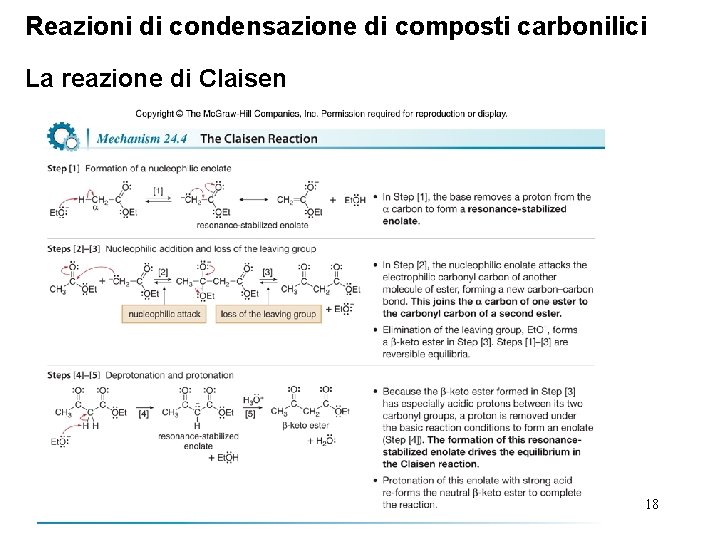
Reazioni di condensazione di composti carbonilici La reazione di Claisen 18

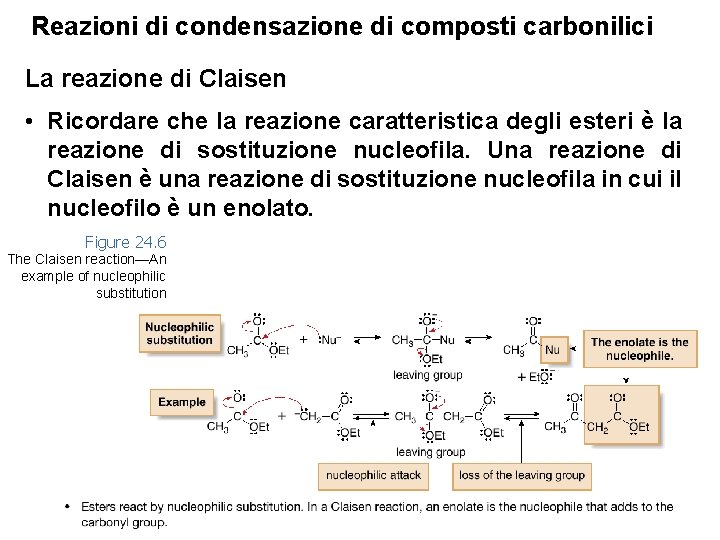
Reazioni di condensazione di composti carbonilici La reazione di Claisen • Ricordare che la reazione caratteristica degli esteri è la reazione di sostituzione nucleofila. Una reazione di Claisen è una reazione di sostituzione nucleofila in cui il nucleofilo è un enolato. Figure 24. 6 The Claisen reaction—An example of nucleophilic substitution 19

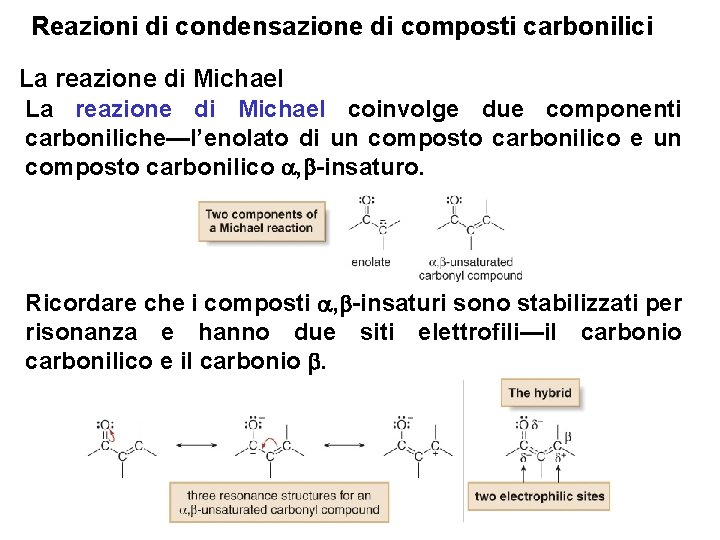
Reazioni di condensazione di composti carbonilici La reazione di Michael coinvolge due componenti carboniliche—l’enolato di un composto carbonilico e un composto carbonilico , -insaturo. Ricordare che i composti , -insaturi sono stabilizzati per risonanza e hanno due siti elettrofili—il carbonio carbonilico e il carbonio . 20

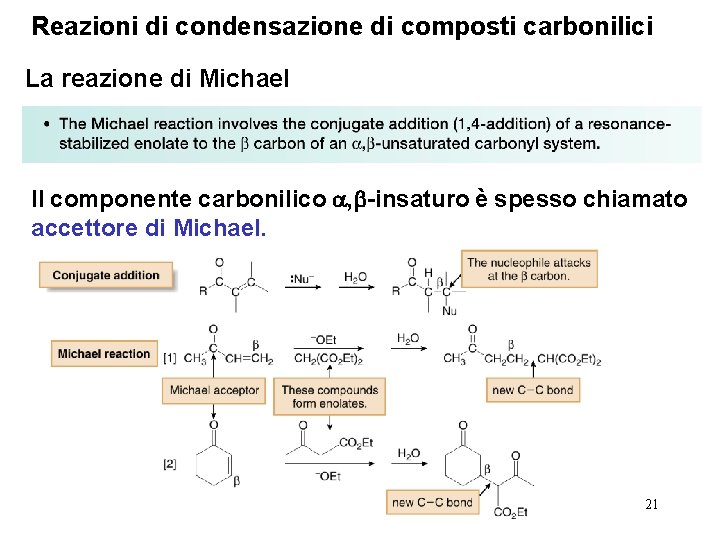
Reazioni di condensazione di composti carbonilici La reazione di Michael Il componente carbonilico , -insaturo è spesso chiamato accettore di Michael. 21

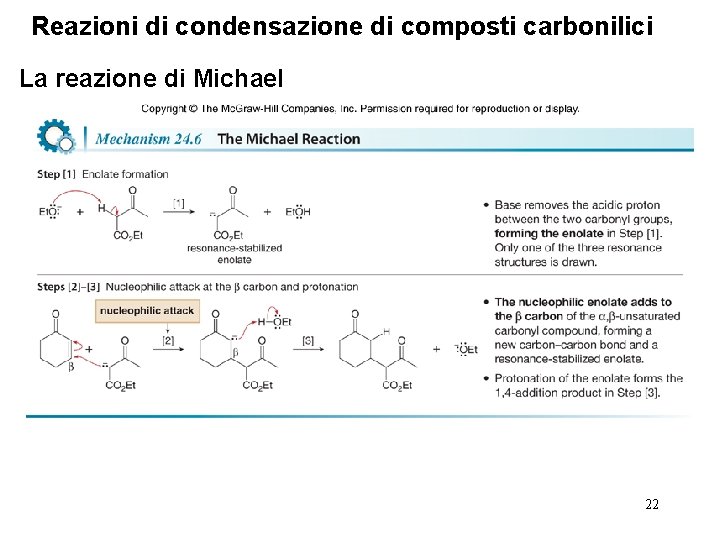
Reazioni di condensazione di composti carbonilici La reazione di Michael 22