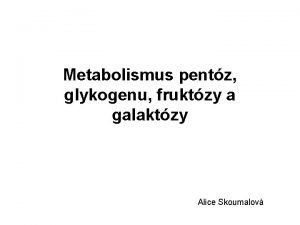Metabolismus erytrocyt Alice Skoumalov Erytrocyty Struktura bikonkvn tvar

Metabolismus erytrocytů Alice Skoumalová

Erytrocyty Ø Struktura: bikonkávní tvar (7, 7 μm) nemají nitrobuněčné organely (membrána obklopující roztok hemoglobinu) Ø Funkce: transport - kyslík do tkání - odstraňování oxidu uhličitého a protonů Ø Doba života 120 dní Ø 4, 6 -6, 2 milionů/μl u mužů, 4, 2 -5, 4 milionů/ μl u žen

Membrána erytrocytů 50% lipidová dvojvrstva (fosfolipidy, cholesterol) 50% proteiny SDS-PAGE: rozdělení podle migrace (proužek 1 -7) isolace a analysa (10 hlavních bílkovin) Integrální: Protein vyměňující anionty, glykoforiny A, B, C Periferní: Spektrin, Ankyrin, Aktin

2 -D mapa membránových proteinů lidských erytrocytů
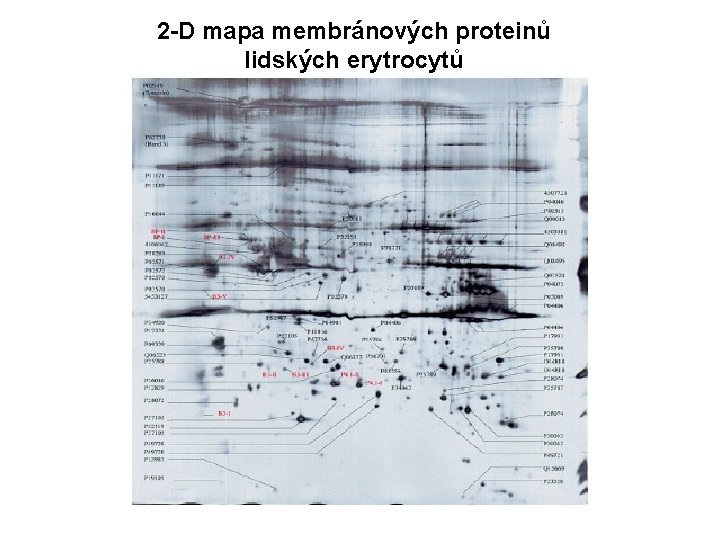
Dědičná sferocytóza (AD) Ødeficit v množství spektrinu nebo jeho abnormality Øpřítomnost sferocytů v periferní krvi Ødestrukce při průchodu slezinou
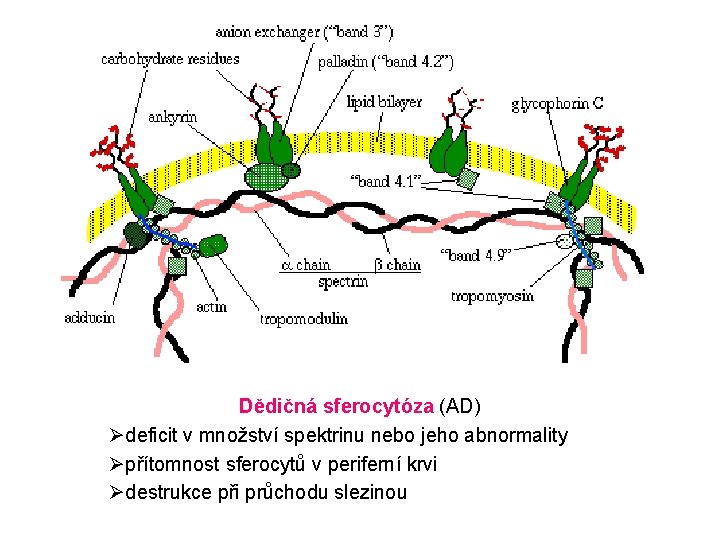
Hemoglobin 4 polypeptidové řetězce + 4 hemové skupiny O 2 se váže na Fe 2+ Hem - Fe 2+- O 2 Hem - Fe 3+ - O 2 • - Methemoglobin (Fe 3+) není schopen vázat O 2 (methemoglobinreduktáza)

Specifika erytrocytů Nemají organely Ø produkce ATP oxidativní fosforylací Ø opravovat poškozené proteiny a lipidy Jsou vystaveny působení volných radikálů Ø autooxidace hemoglobinu (uvolňování O 2 • -) Ø PUFA v membráně (peroxidace lipidů) Ø deformace v kapilárách, uvolnění katalytických iontů (peroxidace lipidů)

Metabolismus erytrocytů Ø Glukóza: energie Ø Glykolýza: ATP a 2, 3 -bisfosfoglycerát Ø Pentosafosfátová dráha: NADPH Ø Syntéza glutathionu (antioxidant) Ø Zánik: globin, Fe 2+, tetrapyrol


Glukóza je zdroj energie Přenašeč pro glukosu 12 transmembránových helikálních úseků kanál pro průchod glukózy nezávislý na inzulínu Glykolýza 1. zdroj ATP laktát 90% energetických požadavků 2. dodavatel 2, 3 -bisfosfoglycerátu (2, 3 -BPG) odklonění glykolýzy (nevzniká ATP) vazba na deoxyhemoglobin, stabilizace, usnadnění uvolňování kyslíku v tkáních


2, 3 -bisfosfoglycerát Allosterický efektor hemoglobinu: Ø stabilizuje deoxyhemoglobin Ø snižuje afinitu hemoglobinu ke kyslíku Klinické aspekty: Ø zvýšená produkce u lidí žijících ve vysoké nadmořské výšce a u kuřáků Ø neváže se na fetální hemoglobin (Hb. F α 2γ 2), větší afinita ke kyslíku, předávání kyslíku plodu přes placentu

Pentosafosfátová dráha Ø NADPH: redukce oxidovaného glutathionu na redukovaný Ø Glutathion: odstraňuje H 2 O 2 z erytrocytů (za katalýzy glutathionperoxidázy obsahující selen) Mutace glukosa-6 -fosfátdehydrogenázy Hemolytická anémie: snížená tvorba NADPH oxidace hemoglobinu, Heinzova tělíska peroxidace lipidů, rozpad erytrocytů Klinika: požití bobů či různých léčiv (primachin, sulfonamidy) 100 milionů lidí deficit aktivity tohoto enzymu (nejčastější enzymopatie)

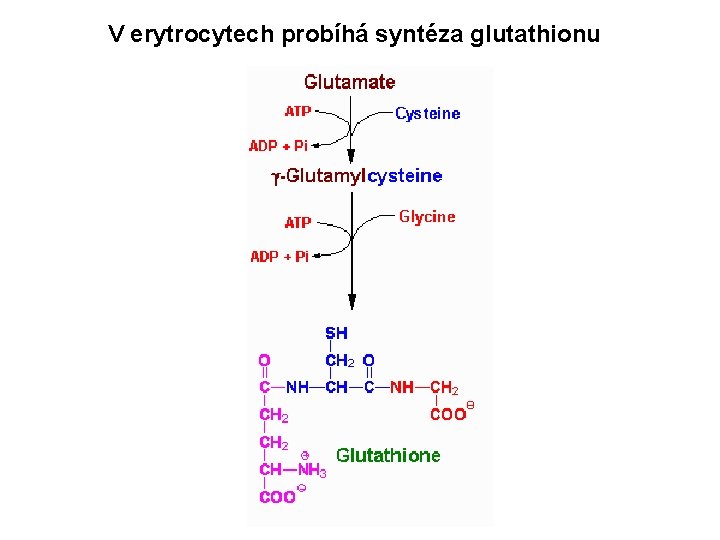
V erytrocytech probíhá syntéza glutathionu
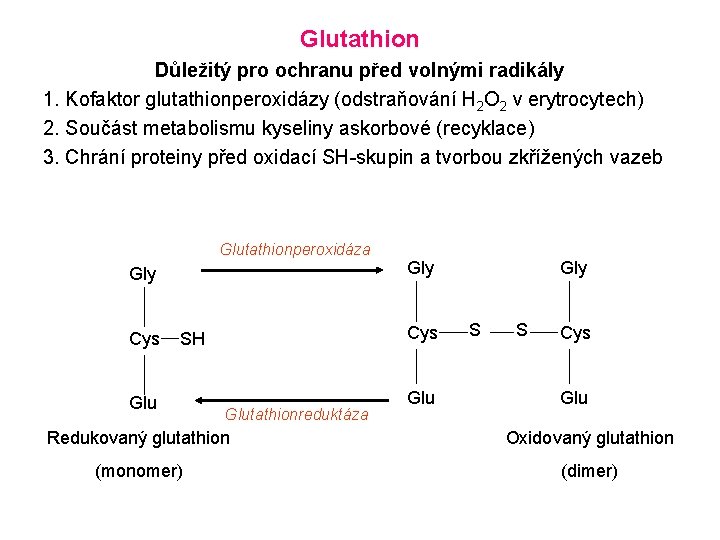
Glutathion Důležitý pro ochranu před volnými radikály 1. Kofaktor glutathionperoxidázy (odstraňování H 2 O 2 v erytrocytech) 2. Součást metabolismu kyseliny askorbové (recyklace) 3. Chrání proteiny před oxidací SH-skupin a tvorbou zkřížených vazeb Glutathionperoxidáza Gly Cys SH Glu Gly Glutathionreduktáza Glu Gly S S Cys Glu Redukovaný glutathion Oxidovaný glutathion (monomer) (dimer)
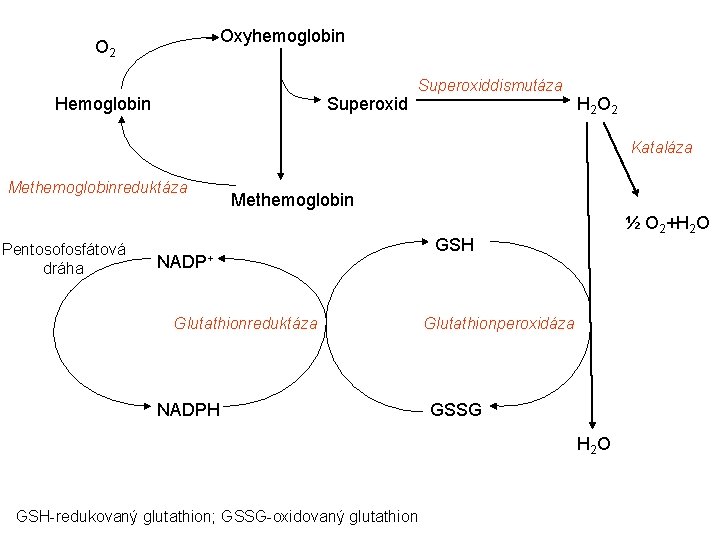
Oxyhemoglobin O 2 Hemoglobin Superoxiddismutáza H 2 O 2 Kataláza Methemoglobinreduktáza Pentosofosfátová dráha Methemoglobin NADP+ Glutathionreduktáza NADPH ½ O 2+H 2 O GSH Glutathionperoxidáza GSSG H 2 O GSH-redukovaný glutathion; GSSG-oxidovaný glutathion

Autooxidace hemoglobinu 3% hemoglobinu každý den se oxiduje Konstantní uvolňování O 2 • Hem - Fe 2+- O 2 Hem - Fe 3+ - O 2 • Hem – Fe 2+- O 2 Hem - Fe 3+ + O 2 • Methemoglobinreduktáza Redukce methemoglobinu FAD, cytochrom b 5 a NADH (z glykolýzy) Methemoglobinemie 1. Dědičná: deficit methemoglobinreduktázy (AR) 2. Abnormální hemoglobin Hb. M (mutace hemoglobinu, náchylný k oxidaci) 3. Vyvolaná požitím léčiv či chemikálií (sulfonamidy, anilin) Klinika: cyanóza (10% Hb ve formě met. Hb) léčba podání redukčních činidel (methylenová modř, kyselina askorbová)

Superoxiddismutáza (SOD) Konvertuje O 2 • - na H 2 O 2 Cu. Zn. SOD ve vysoké koncentraci v erytrocytech Odstranění H 2 O 2: 1. Kataláza hemová skupina s Fe 3+ katalyzuje dekompozici H 2 O 2 na vodu a kyslík: 2 H 2 O 2 2 H 2 O+O 2 2. Glutathionperoxidáza redukuje H 2 O 2 na vodu a zároveň oxiduje glutathion H 2 O 2+2 GSH GSSG+2 H 2 O Glutathionreduktáza GSSG+NADPH+H+ 2 GSH+NADP+ NADPH z pentosafosfátové dráhy (glukóza-6 -fosfátdehydrogenáza)

Spolupráce katalázy a glutathionperoxidázy Kataláza důležitá při vyšších koncentracích H 2 O 2 (vysoké Km pro H 2 O 2) Erytrocyty odstraňují H 2 O 2 a O 2 • - vznikající i v plazmě a jiných tkáních (H 2 O 2 volně difunduje membránou, O 2 • prochází kanálem pro anionty)
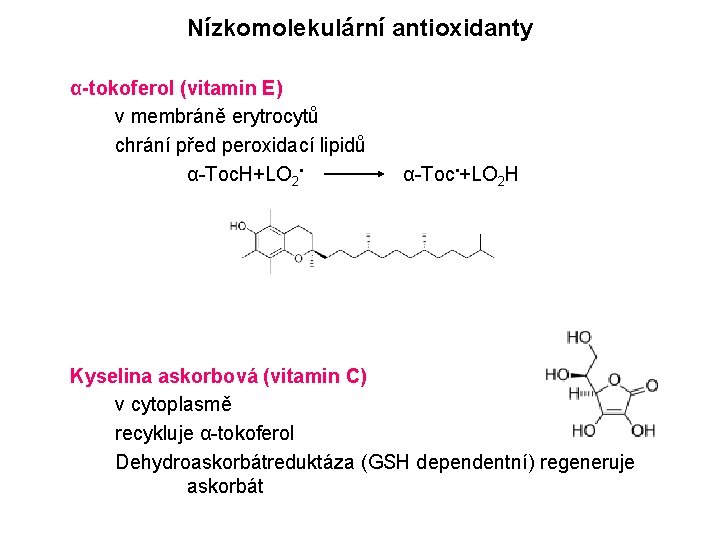
Nízkomolekulární antioxidanty α-tokoferol (vitamin E) v membráně erytrocytů chrání před peroxidací lipidů α-Toc. H+LO 2 • α-Toc • +LO 2 H Kyselina askorbová (vitamin C) v cytoplasmě recykluje α-tokoferol Dehydroaskorbátreduktáza (GSH dependentní) regeneruje askorbát

Hemoglobinopatie Mutace - abnormální struktury hemoglobinu V důsledku mutací dochází k tvorbě srpků, změně afinity ke kyslíku, ztrátě hemu či disociaci tetrameru Nejznámější jsou hemoglobin M a S, dále thalasemie Hemoglobin M Náhrada His (E 8 nebo. F 7) v podjednotce α nebo β Tyr Silná iontová vazba s Tyr stabilizuje železo ve formě Fe 3+ (methemoglobin) Methemoglobin neváže kyslík Thalasemie V důsledku genetických poruch je snížená či chybí tvorba α či β -řetězců (α či β-thalasemie)
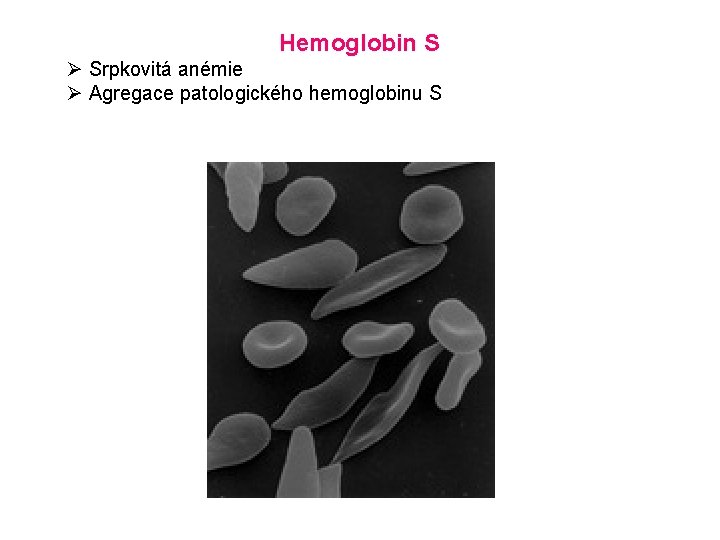
Hemoglobin S Ø Srpkovitá anémie Ø Agregace patologického hemoglobinu S
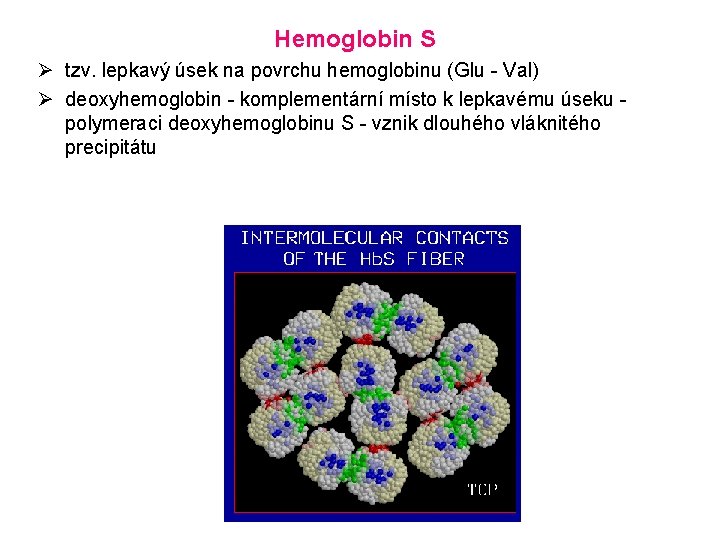
Hemoglobin S Ø tzv. lepkavý úsek na povrchu hemoglobinu (Glu - Val) Ø deoxyhemoglobin - komplementární místo k lepkavému úseku polymeraci deoxyhemoglobinu S - vznik dlouhého vláknitého precipitátu
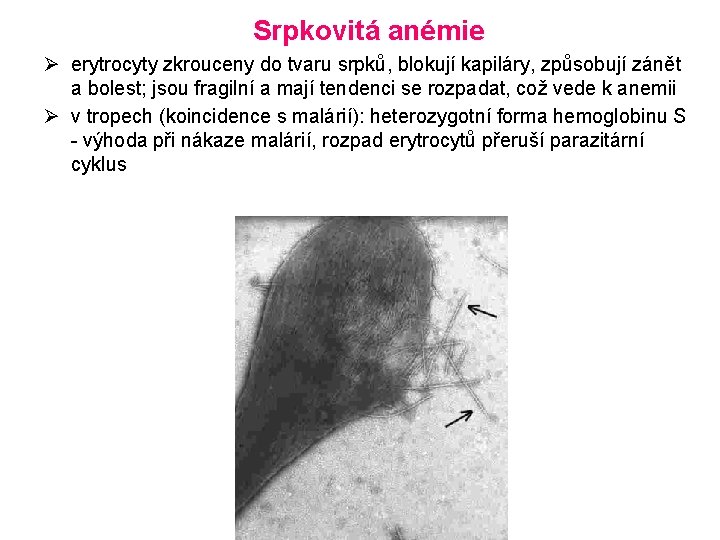
Srpkovitá anémie Ø erytrocyty zkrouceny do tvaru srpků, blokují kapiláry, způsobují zánět a bolest; jsou fragilní a mají tendenci se rozpadat, což vede k anemii Ø v tropech (koincidence s malárií): heterozygotní forma hemoglobinu S - výhoda při nákaze malárií, rozpad erytrocytů přeruší parazitární cyklus
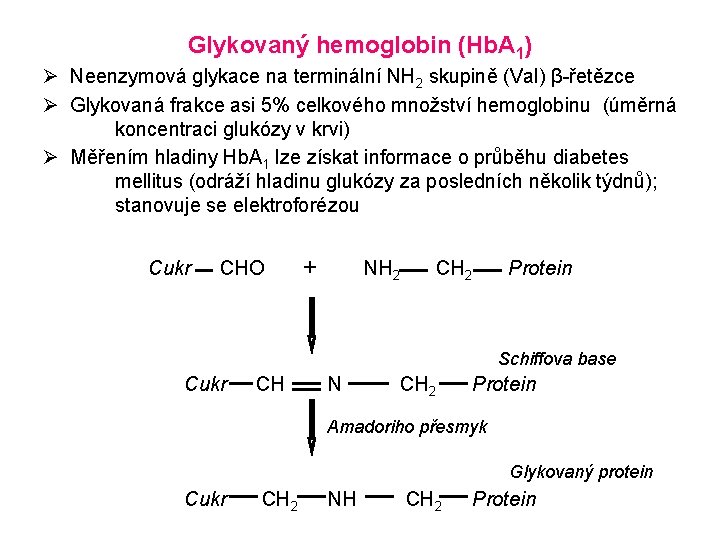
Glykovaný hemoglobin (Hb. A 1) Ø Neenzymová glykace na terminální NH 2 skupině (Val) β-řetězce Ø Glykovaná frakce asi 5% celkového množství hemoglobinu (úměrná koncentraci glukózy v krvi) Ø Měřením hladiny Hb. A 1 lze získat informace o průběhu diabetes mellitus (odráží hladinu glukózy za posledních několik týdnů); stanovuje se elektroforézou Cukr CHO + NH 2 CH 2 Protein Schiffova base Cukr CH N CH 2 Protein Amadoriho přesmyk Glykovaný protein Cukr CH 2 NH CH 2 Protein
- Slides: 27